Діуретична терапія: у пошуках оптимальних шляхів
У статті представлено стислий огляд дослідження, проведеного польськими колегами K. Ozieranski et al., щодо аналізу віддалених наслідків застосування діуретиків, а саме торасеміду і фуросеміду в осіб із серцевою недостатністю (СН). Результати цієї роботи дозволять лікарю-практику обрати оптимальну діуретичну терапію для когорти пацієнтів із такою тяжкою патологією, як хронічна серцева недостатність (ХСН). Дані матеріали були опубліковані у виданні Cardiovascular Drugs and Therapy (2019).
Близько 50% пацієнтів із СН потребують повторного стаціонарного лікування протягом 6 місяців після первинної госпіталізації через погіршення стану, пов’язаного із основним захворюванням. Така статистика вказує на необхідність покращання, зокрема, симптоматичного лікування СН (Ponikowski P. et al., 2016).
Одним із важливих факторів ефективного менеджменту хворих на СН є діуретична терапія (Mueller T.M. et al., 2002). Як свідчать сучасні європейські реєстри, сечогінні препарати призначають при виписці зі стаціонара і амбулаторно приблизно 83% усіх пацієнтів із ХСН (Komajda M. et al., 2016; Maggioni A.P. et al., 2013). Слід зазначити, що поточні клінічні рекомендації Європейського товариства кардіологів (ESC) не підкреслюють переваг будь-яких діуретиків. Проте за останніми даними доведено, що торасемід чинить сприятливий вплив на довгострокові результати у пацієнтів із ХСН, особливо молодих, або тих, які мають дилатаційну кардіоміопатію (Cosin J. et al., 2002; Murray M.D. et al., 2001).
Метою дослідження була оцінка якості життя і клініко-функціонального статусу хворих на СН залежно від включення до терапії петлевих діуретиків, а також надання порівняльної характеристики ефекту фуросеміду і торасеміду в складі комбінованої терапії на віддалені результати лікування (протягом року). Крім того, автори намагались ідентифікувати клінічні фактори, що впливали на вибір діуретика (торасеміду чи фуросеміду) під час виписки.
Первинною кінцевою точкою дослідження було визначено показники загальної смертності та госпіталізації з приводу погіршення СН протягом 30 днів після виписки; вторинні кінцеві точки включали загальну летальність і частоту госпіталізації упродовж 30 днів та загальну смертність за 180 днів після виписки.
Дане клінічне випробування проходило у два етапи – пілотний та довгостроковий. Пілотне дослідження тривало з жовтня 2009 по травень 2010 рр. Довгостроковий етап проводили із травня 2011 по квітень 2013 рр. У дослідження були залучені 1440 учасників із 2019 хворих, зареєстрованих у польських частинах реєстру із СН ESC. Реєстри включали амбулаторних і стаціонарних пацієнтів із хронічною, ускладненою або вперше виявленою СН. Під спостереженням перебували особи, які досягли 18-річного віку та відповідали діагностичним критеріям для СН. Під час проведення порівняльного дослідження збирали та враховували дані хворих щодо анамнезу захворювання, демографії, клінічного стану, результатів діагностичних тестів, фармакотерапії, зокрема частоти використання петлевих діуретиків протягом одного року. Крім того, для кожного з пацієнтів, що отримували як фуросемід, так і торасемід, було визначено функціональний клас (ФК) СН за класифікацією Нью-Йоркської асоціації серця (NYHA).
Пацієнтів було розділено на три групи:
- ті, що отримували фуросемід;
- хворі, яким було призначено торасемід;
- учасники, які отримували обидва петлеві діуретики.
Аналіз здійснювали за допомогою псевдорандомізації – ефективного статистичного методу усунення впливу супутніх факторів, які можуть спотворювати результати обсерваційних досліджень при порівнянні груп спостереження. Дозу фуросеміду 40 мг вважали еквівалентною дозі торасеміду 10 мг.
Результати дослідження показали, що петлеві діуретики є ефективними для полегшення клінічних ознак і симптомів СН. Проте слід зважати на комбінування та дозування вказаних препаратів. У дослідженні було показано, що пацієнти, які отримували одночасно торасемід і фуросемід, мали гірший прогноз, ніж групи, що приймали по одному сечогінному засобу. Комбіноване лікування обома діуретиками відзначалося найвищою частотою первинної (23,8%) та вторинної (59,2%) кінцевих точок. Це було зумовлено, швидше за все, гіршим клінічним станом хворих на початку спостереження.
У цілому достеменно не визначено, чи є залежність між погіршенням довгострокового прогнозу для пацієнтів із СН і одночасним застосуванням двох петлевих діуретиків. Проте виявлено, що ризик смертності залежить від дози діуретичного препарату і зростає з її підвищенням. Примітно, що 50 мг фуросеміду на день (порогове значення) було визначено як один із найвагоміших предикторів смерті протягом 3 років (Dini F.L. et al., 2013; Ozieranski K. et al., 2018). Подібні ефекти порогової дози для торасеміду не досліджувалися.
Своєю чергою, наявні дані свідчать, що торасемід може надавати додаткові переваги з огляду на частоту госпіталізацій пацієнтів із приводу СН, поліпшення функціонального стану, якості життя і навіть знижувати рівень смертності порівняно з фуросемідом та іншими діуретиками. Так, ще в одному відкритому рандомізованому дослідженні (Murray M.D. et al., 2001) у 234 осіб із ХСН показане значне зниження частоти госпіталізацій щодо СН та інших серцево-судинних захворювань у пацієнтів, які отримували лікування торасемідом порівняно з фуросемідом.
Слід зазначити, що торасемід, поза його чистим діуретичним ефектом, може також забезпечити додаткові переваги у хворих на СН.
Як відомо, діуретики, особливо фуросемід, провокують активацію ренін-ангіотензин-альдостеронової системи (РААС). Торасемід, на противагу, разом із діуретичною активністю поєднує в собі ефекти спіронолактону, а саме блокаду РААС. Це може послаблювати ремоделювання міокарда та кардіальний фіброз.
Аналіз даних дослідження щодо активації РААС і, зокрема, гіперсекреції альдостерону на ремоделювання лівого шлуночка (ЛШ) дозволив припустити, що сприятливі кардіальні ефекти торасеміду при ХСН пов’язані з його здатністю гальмувати альдостеронові рецептори не тільки в ниркових канальцях, але й у міокарді. Це приводить до покращання наповнення ЛШ та сповільнення його гіпертрофії, зниження рівня натрійуретичного пептиду. Таким чином, антиальдостеронова дія торасеміду може пояснити його здатність покращувати прогноз у хворих на СН.
Додатковою перевагою торасеміду над фуросемідом є зменшення втрати калію із сечею, що знижує ризик розвитку аритмій.
При тривалому прийомі торасемід, на відміну від фуросеміду, у хворих на СН не тільки поліпшує її ФК, але й зменшує необхідність госпіталізації через декомпенсацію СН. Також він знижує загальну летальність і смертність від серцево-судинних причин (Mamcarz A. et al., 2015; Buggey J. et al., 2015).
Таким чином, можна дійти висновку, що торасемід має більш передбачувану фармакокінетику/фармакодинаміку, менший вплив на концентрацію електролітів і, отже, кращу переносимість пацієнтами порівняно з фуросемідом.
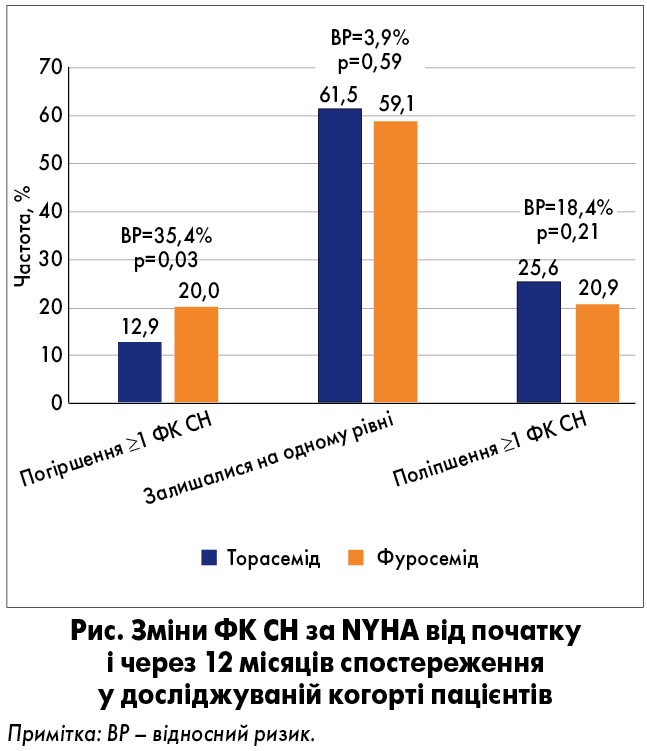 За результатами дослідження, найбільш істотне зниження загальної смертності у групі пацієнтів, що отримували торасемід, спостерігалося в осіб віком <65 років та із дилатаційною кардіоміопатією. На початку випробування групи торасеміду та фуросеміду не відрізнялися щодо ФК СН за NYHA; через 12 місяців лікування середній ФК NYHA був значно нижчим у хворих, які отримували торасемід. Крім того, протягом спостереження застосування торасеміду асоціювалося із нижчим ризиком прогресування СН, ніж при прийомі фуросеміду (12,9% на противагу 20,0%; відповідає ≥1 ФК СН за NYHA). Крім того, у групі торасеміду пацієнти значно прихильніше ставилися до призначеного лікування завдяки меншій частоті застосування препарату, а також через рідші випадки ургентних позивів до сечовипускання (рис.).
За результатами дослідження, найбільш істотне зниження загальної смертності у групі пацієнтів, що отримували торасемід, спостерігалося в осіб віком <65 років та із дилатаційною кардіоміопатією. На початку випробування групи торасеміду та фуросеміду не відрізнялися щодо ФК СН за NYHA; через 12 місяців лікування середній ФК NYHA був значно нижчим у хворих, які отримували торасемід. Крім того, протягом спостереження застосування торасеміду асоціювалося із нижчим ризиком прогресування СН, ніж при прийомі фуросеміду (12,9% на противагу 20,0%; відповідає ≥1 ФК СН за NYHA). Крім того, у групі торасеміду пацієнти значно прихильніше ставилися до призначеного лікування завдяки меншій частоті застосування препарату, а також через рідші випадки ургентних позивів до сечовипускання (рис.).
Загалом до цього часу групи експертів, спираючись на наявні клінічні випробування та економічну рентабельність, декларували перевагу застосування торасеміду над фуросемідом у хворих на СН. Дане дослідження підтверджує попередні звіти, які свідчать про те, що лікування торасемідом порівняно з фуросемідом може зумовити поліпшення ФК CН за класифікацією NYHA, сприяти більш оптимістичному прогнозу в пацієнтів із ХСН та покращанню їхньої якості життя.
Підготувала Наталія Поваляшко
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» №1 (62), березень 2019 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....




