Новітні досягнення у персоналізації реанімаційних заходів при зупинці серця
Зупинка серця (ЗС) залишається важливою причиною смерті та втрати працездатності в усьому світі.
Зокрема, в США щороку трапляється близько 395 тис. випадків ЗС поза лікарнею (ЗСПЛ) та 200 тис. випадків у стаціонарі (ЗСС) (Daya M. et al., 2015; Merchant R. et al., 2011). За будь-яких обставин ЗС значно підвищує ризик захворюваності та смерті, проте при виникненні ЗСПЛ прогноз гірший, що, імовірно, зумовлено пізнішим початком серцево-легеневої реанімації (СЛР). Відтак, підви щується ризик виникнення аритмій, стійких до дефібриляції (ДФ), що спричиняє тривалі періоди відсутньої або низької циркуляції крові і системне ураження органів. Тривалі періоди ЗС без спонтанного відновлення циркуляції (СВЦ) негативно впливають на клінічні наслідки та різко знижують ефективність СЛР (Kuschner C., Becker L., 2019).
Прогрес щодо клінічних наслідків після ЗС. Показники виживання при ЗСПЛ у США за період 1982-2012 рр. становили близько 5,5% (Sasson С. et al., 2012). Останнім часом ці цифри дещо збільшилися внаслідок частішої ініціації СРЛ очевидцями подій вдома або в громадських місцях, а також успішного застосування ДФ до госпіталізації (Girotra S. et al., 2016; Fordyce C. et al., 2017).
Для покращення клінічних наслідків ЗС вивчено багато різних методів реанімації. Деякі з них відносно прості та потребують лише певних змін існуючих основних рятівних заходів, натомість інші пов’язані зі значними витратами часу та ресурсів. Кожне із цих втручань дозволяє надалі персоналізувати реанімаційні заходи, однак стан пацієнтів із ЗС буває різного ступеня складності. Так, засвідчена ЗСС із чутливим до ДФ ритмом характеризується зовсім іншою патофізіологією, ніж ЗСПЛ, що виникла за невідомих обставин зі спробами реанімації впродовж 25 хв. Тому створити уніфікований протокол для простих і складних випадків з урахуванням усіх нових методів реанімації досить проблематично.
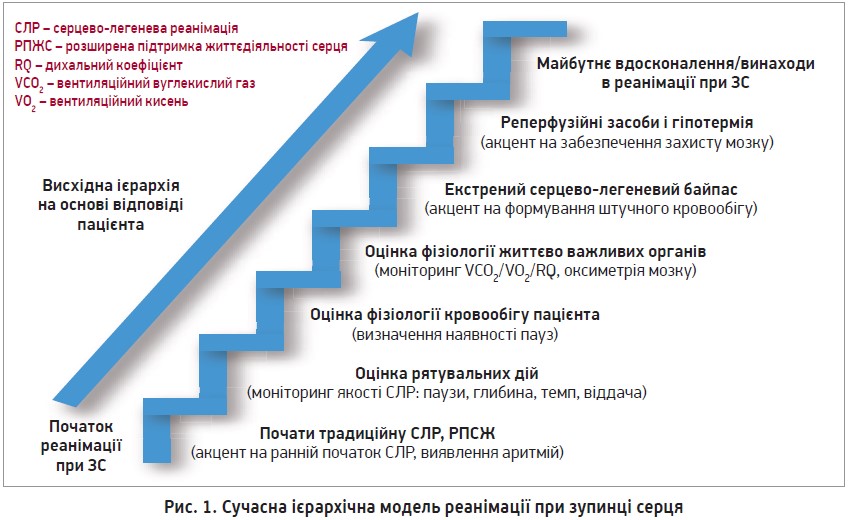
Персоналізація реанімації ЗС через ієрархічну модель. Нові технології, які з’явились унаслідок вивчення патогенезу ЗС, дозволяють покращити виживання і модернізувати підхід до реанімації за допомогою ієрархічної моделі, яка передбачає логічне та поетапне застосування більш прогресивних технологій реанімації залежно від стану пацієнта (рис. 1).
Реанімація починається з найпростіших загальноприйнятих методів, як-от ручна СЛР. Надалі пропонується моніторинг дотримання протоколу рятувальником, тобто оцінка якості дій – компресії, вентиляції, застосування лікарських засобів тощо. Ще вище в ієрархії стоїть моніторинг прямого впливу реанімаційних дій на фізіологію пацієнта, що здійснюється шляхом моніторингу утворення CO2, споживання O2, кровотоку артеріальної і венозної крові та церебральної перфузії. Можливі подальші вдосконалення варіантів реанімації на основі фізіологічних потреб. Отже, ієрархічна модель поступово вдосконалює початкові універсальні дії рятувальника, ускладнюючи їх відповідно до потреб конкретного пацієнта (Kuschner C., Becker L., 2019).
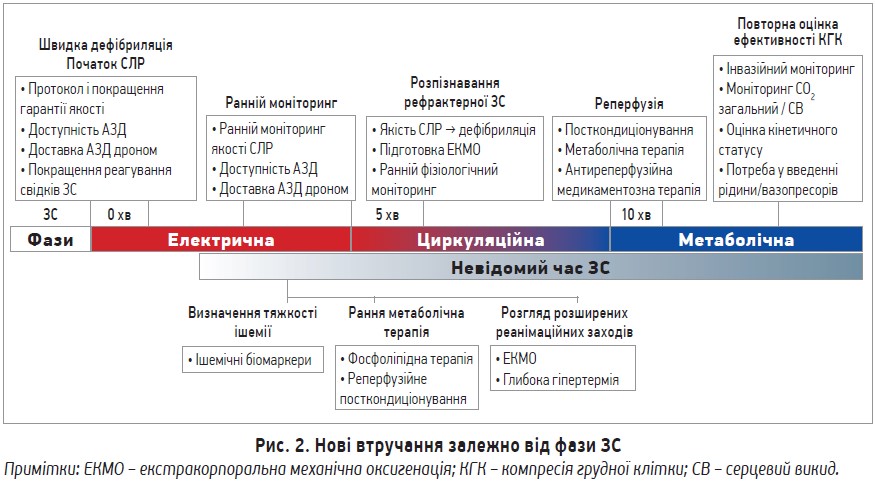
Важливість фактору часу при ЗС. Після виникнення ЗС треба якомога швидше розпочати СЛР та провести ДФ при будь-якій потенційній аритмії (рис. 2). У США для скорочення часу до СВЦ запропоновано такі заходи: зменшення часу реагування екстреної медичної допомоги (ЕМД), навчання населення СЛР та застосування автоматизованих зовнішніх дефібриляторів (АЗД), збільшення їх кількості і доступності. Швидка ініціація СЛР підвищує виживаність при ЗСПЛ, але не впливає на загальну виживаність і неврологічні наслідки (Abrams H. et al., 2013). Дуже важливими для покращення результатів є раннє виявлення та лікування аритмій (рис. 2).
Нещодавно з’явилося повідомлення про використання безпілотних дронів для доставки АЗД у випадках повідомлень про ЗСПЛ. Це підвищило швидкість доставки АЗД протягом 1 хв на 76,5% порівняно з традиційною доставкою засобів ЕМД (Pulver et al., 2016). Іншим новим інструментом контакту людей, тренованих проводити СЛР, є мобільний додаток, який повідомляє членів спільноти про випадки ЗСПЛ у зоні їх перебування. Використання таких програм, як PulsePoint (США), Heart Runner (Швеція) або GoodSAM (Велика Британія), може скоротити час до ініціації СЛР; утім, для оцінки їх впливу на результати необхідні подальші дослідження (Smith C. et al., 2017).
Оцінка та забезпечення якісної СЛР. Незважаючи на налагоджені протоколи, надання послідовної СЛР залишається складним. За даними літератури, на початку ХХІ ст. мали місце значні розбіжності між встановленими рекомендаціями щодо СЛР та практикою її проведення як при ЗСПЛ, так і в разі ЗСС (Wik L. et al., 2005; Abella B. et al., 2005). Попри оновлення настанов у 2013 р. та 2015 р. у літературі є повідомлення, що підтримувати їх послідовність дотепер важко (Sutton R. et al., 2013; Blewer A. et al., 2015). Зрештою, можливі розбіжності в темпі компресії, її глибині та тривалості пауз, а також у швидкості вентиляції (Idris A. et al., 2015; Vadeboncoeur T. et al., 2014; Aufderheide T. et al., 2004). Ці маркери поганої якості СЛР часто трапляються після виснаження рятувальників, що призводить до поступового зниження якості реперфузії та вентиляції. Механізми зворотного зв’язку пропонують рятувальникам новий механізм для забезпечення контролю якості в режимі реального часу (рис. 1, 2). Як формат зворотного зв’язку запропоновано моніторинг різних факторів, як-от характеристики компресії або викид кінцево-припливного вуглекислого газу (EtCO2). Це дозволяє рятувальникам інтуїтивно зрозуміти та виправити невдалі методи реанімації (Weston B. et al., 2017).
Оптимізація СЛР, еволюція ідеальної форми хвилі. Так само, як орієнтований на рятувальників зворотний зв’язок у реальному часі покращує їх здатність підтримувати послідовність дотримання протоколу, зворотний зв’язок, орієнтований на фізіологію пацієнта із ЗС, дозволяє гнучко змінювати протокол відповідно до індивідуальних потреб (рис. 1).
Протокол СЛР шляхом компресій грудної клітки (КГК) фокусується на використанні такого виду КГК, що забезпечує штучний кровообіг, а в поєднанні з вентиляцією робить можливою реоксигенацію шляхом газообміну. Відтак, головним завданням КГК є досягнення виштовхування крові із серця. Тому КГК можна охарактеризувати як форму хвилі з певними характеристиками – частота стиснення, швидкість, глибина та час їх утримання, а також швидкість вивільнення від компресії, час і довжина паузи. Сучасний протокол описує ідеальну форму хвилі як стиснення на глибину не менш ніж 2 дюйми, але не більш ніж 2,4 дюйма зі швидкістю принаймні 100 компресій за хвилину, але не більш, ніж 120 за хвилину, що забезпечує повне вивільнення від стиснення (Neumar R. et al., 2015). Хоча це забезпечує клінічно відповідний протокол, який можна справді виконати вручну, виключення інших характеристик форми хвилі може змінити продуктивність СЛР. Наприклад, у двох нещодавніх публікаціях висвітлено різні погляди на клінічну значущість параметрів вивільнення від стиснення за умов використання моніторів прискорення дефібрилятора (Cheskes S. et al., 2015; Kovacs A. et al., 2015). У першому повідомленні швидкість вивільнення не впливала на виживання, у другому – більш швидкий час вивільнення покращував виживання.
На тваринній моделі шляхом моніторингу судинного потоку під час механічної КГК встановлено, що тривалість часу вивільнення 300 мс порушує забезпечення кровотоку; різниці в гемодинамічних характеристиках між періодами вивільнення 200 та 100 мс не було, але час вивільнення 100 мс асоціювався зі збільшенням утворення ендотрахеального СО2 (Lampe J. et al., 2015). Це свідчить про те, що час вивільнення при КГК може бути більш значимим показником для забезпечення ефективної вентиляції, ніж кровоток.
Чи існує єдина ідеальна форма хвилі? Сучасний протокол КГК розроблений для оптимізації кровотоку на основі припущення, що одна форма хвилі стиснення може однаково підтримувати перфузію в усіх пацієнтів протягом усього періоду СЛР. Однак упродовж реанімації анатомія та фізіологія пацієнтів змінюються. Зламані ребра змінюють вплив КГК на індукцію кровотоку, серце перестає бути помпою, стаючи системою, керованою зворотним тиском, виникає перерозподіл об’єму плазми до інтерстицію внаслідок набряку, депонування крові в мезентеріальних судинах і венозний застій через втрату тонусу артеріол. Такий багатосистемний перерозподіл викликає гіпотензивний стан, що знижує заповнення правого передсердя (Lampe J. et al., 2018).
Чи може одна форма хвилі КГК забезпечувати сталу ефективність, незважаючи на динамічні зміни фізіології ЗС? У тваринній імітаційній моделі ЗС унаслідок фібриляції шлуночків (ФШ) вивчали вплив різноманітних циклічних 2-хвилинних форм хвиль СЛР шляхом програмованого механічного пристрою КГК упродовж 50 хв компресії. Для оцінки змін фізіологічних параметрів та ефективності впливу різних форм хвилі на оптимізацію кровотоку під час реанімаційних заходів використовували фізіологічний моніторинг й артеріальні (загальна сонна, грудна і черевна аорта) і венозні (зовнішня яремна та нижня порожниста вена, праве передсердя) зонди. За 5 циклів СЛР середній артеріальний тиск (АТ) і тиск у правому передсерді зменшилися з 30 і 17 мм рт. ст. до 14 мм рт. ст. відповідно (Lampe J. et al., 2018). Такий розвиток гіпотонії зумовлений депонуванням внутрішньосудинного об’єму в третьому просторі, а ідеальна форма хвилі змінювалася як часова функція з кращим ефектом від моделі КГК з меншою швидкістю та меншим робочим циклом. Отже, основним чинником, який впливає на АТ при ЗС, є час наповнення, що вказує на більшу ефективність повільнішої форми хвилі. Відтак, результати останніх досліджень не надають єдину сталу оптимальну форму хвилі, яка могла б підтримувати кровоток і вентиляцію впродовж усього періоду реанімації. Теоретично цю часову залежність гемодинаміки можна було б покращити шляхом динамічного підходу до реанімації. Зокрема, для поліпшення гіпоперфузії та боротьби з наслідками депонування в третьому просторі можна застосовувати введення рідини та вазопресори на пізніх стадіях реанімації. Аналогічно початкова частота КГК >100/хв з подальшим зменшенням могла б сприяти забезпеченню достатнього часу наповнення впродовж усього періоду реанімаційних заходів. Однак гемодинаміка пацієнта із ЗС змінюється після початку будь-якого втручання. Тому в ідеалі для оцінки впливу реанімаційних заходів потрібно проводити динамічний контроль АТ. Це можна реалізувати шляхом інвазивного моніторингу (встановлення А‑лінії або центрального катетера для оцінки центрального венозного тиску) або менш інвазивними методами, як-от моніторинг периферичного АТ на кінцівках, визначення EtCO2 для оцінки вентиляції та трансезофагеальна ехокардіографія для вимірювання серцевого викиду (Fair J. et al., 2018; Long B. et al., 2018). Використовуючи ці показники, можна розпізнати мінливий кінетичний профіль та адаптувати медикаментозну терапію або форму хвилі КГК відповідно до існуючих потреб. З іншого боку, важко динамічно змінювати форму хвилі КГК, коли реанімаційні заходи проводяться вручну. Це відкриває подальший потенціал для електронних пристроїв КГК, які можна було б програмувати на зміну характеристик форми хвилі у відповідь на задані параметри.
Покращення якості ДФ. Сучасні настанови рекомендують проводити ДФ після 2 хв СЛР за наявності ритму, який піддається дефібриляції, вимагаючи паузи в реанімаційних заходах для його оцінки. Імовірність того, що ДФ зупинить ФШ, переважно відповідає тривалості нелікованої ФШ, як і ступінь коронарної перфузії, підвищений за рахунок СЛР, оскільки серце потребує повернення до фізіологічних умов з поліпшенням метаболічної дисфункції, перш ніж це зробить електричний імпульс. Використовуючи аналіз амплітудно-спектральної площі для прогнозування ймовірності СВЦ, недавнє дослідження продемонструвало, що така прогностична модель може значно зменшити кількість невдалих ДФ, а відтак і тривалість часу припинення СЛР для оцінки ритму (Aiello S. et al., 2017). Інші напрями включають використання подвійної послідовної ДФ, хоча ефективність такого підходу при ЗС не визначена (Simon E. M., Tanaka K., 2018). Подальша робота над покращенням якості ДФ може знизити периреанімаційну захворюваність.
Нові підходи до реанімації ЗС. Якщо традиційна СЛР не забезпечує СВЦ, просування вгору по ієрархічній моделі орієнтується на більш технологічно досконалі методи відновлення перфузії. Зокрема, нові перспективи при ЗС вносить поява вено-артеріальної екстракорпоральної механічної оксигенації (ЕКМО). Результати нещодавнього метааналізу вказують на те, що сучасні публікації про ЕКМО при ЗС включають переважно одноцентрові нерандомізовані дослідження з різними критеріями включення та варіабельними показниками тяжкості або відновлення після ЗС (Holmberg M. et al., 2018). Інший метааналіз, що включав 9 когорт пацієнтів, свідчить, що використання ЕКМО при ЗС покращує довгострокову виживаність і неврологічні наслідки на 15% та 11% відповідно в порівнянні зі стандартною CЛР (Ouweneel et al., 2016). Нещодавнє дослідження CHEER також підтверджує потенціал EКMO у разі ЗС, оскільки 54% пацієнтів вижили і були виписані з повним неврологічним відновленням (Stub D. et al., 2015). Цікаво, що виживаність суттєво залежала від скорочення часу від виникнення колапсу до початку ЕКМО (40 проти 78 хв; р=0,02) та часу від прибуття перфузійної команди до початку ЕКМО (16 проти 30 хв; р=0,01). Це підтверджує думку, що EКMO найбільш ефективна, коли її проводять через 10-15 хв від початку СЛР (Fagnoul D. et al., 2014). Зазначене підкреслює важливість зменшення ішемічного навантаження до початку ЕКМО, оскільки пацієнтів з ішемічним навантаженням >15 хв можна віднести до складної популяції із серйозним ризиком.
Висока летальність у метаболічній фазі ЗС. Відповідно до концепції, запропонованої Вайсфельдтом і Беккером, після періодів тривалої ішемії пацієнти переходять від початкових електричної та циркуляторної фаз ЗС до метаболічної фази (Weisfeldt M., Becker L., 2002). У цей момент рятувальник потрапляє в складну ситуацію, бо негайні СЛР та ЕКМО повторно вводять метаболічно ушкоджене тіло в стан з майже фізіологічним забезпеченням кисню, спричиняючи реперфузійну травму.
Важливо, що швидкий початок СЛР, яка дає СВЦ в електричній фазі ішемічного ушкодження, суттєво покращує виживаність. Це підкреслює важливість підвищення обізнаності населення та швидкого початку реанімації, навіть такої, що базується виключно на КГК. Утім, частіше трапляються випадки реанімації після тривалої ішемії, що суттєво збільшує ризик реперфузійної травми. Це зумовлено складними змінами метаболічної активності клітин через брак кисню (Sekhon M., Griesdale D., 2017). Відсутність утворення АТФ через ішемію індукує внутрішньоклітинний окислювально-відновний зсув, який внаслідок дефіциту кисню унеможливлює перетворення комплексу IV, спричиняючи реакцію електронів із залишковим киснем, унаслідок чого утворюються реактивні часточки кисню (РЧК). Водночас зниження утворення АТФ не дає клітині можливості утримувати електроліти, призводячи до зміщення кальцію, натрію та калію і вторинного осмотичного набряку мітохондрій. Початок СЛР забезпечує 25-40% нормальної циркуляції організму та наближений до фізіологічного рівень кисню, що стимулює утворення РЧК, переважно за рахунок протеїнів окисного фосфорилювання мітохондрій. Тож теоретично ідеальна реанімація має бути орієнтована на стадію метаболічної дисфункції в кожного пацієнта. Незважаючи на те що останні дослідження забезпечують нові можливості для персоналізованого догляду, цей феномен потребує подальшого інтенсивного вивчення.
Лікування метаболічної фази ЗС. Один із підходів, що обмежує вплив реперфузійної травми при вираженій ішемії, – використання посткондиціонування (ПК), тобто коротких пауз у СЛР, унаслідок чого в тканини потрапляє менша кількість кисню. Зменшуючи споживання кисню тканинами, які перебувають у стані метаболічного шоку, ПК пристосовує їх до нормальної здатності споживання кисню, обмежуючи реперфузійну травму та зводячи до мінімуму утворення РЧК.
При порівнянні впливу 15 хв нелікованої ФШ з подальшою CЛР проти CЛР із 4 20-секундними паузами впродовж перших 3 хв (СЛР + ПК) на тваринній моделі встановлено, що використання останньої методики супроводжувалося значно кращими показниками фракції викиду лівого шлуночка через 1 і 4 год та неврологічної функції, оціненої за сумою балів мозкової ефективності за 24 год (Segal et al., 2012). Це підтверджується результатами недавнього дослідження, проведеного з метою з’ясувати, чи спричиняє різка реперфузія дисфункцію мітохондрій головного мозку та серця після реанімації і чи може ПК зменшити цей шкідливий вплив. Дослідження використовувало тваринну модель ЗС унаслідок ФШ та включало 4 групи: неішемічну, 19-хвилинну ЗС унаслідок ФШ без СЛР, 15-хвилинну ФШ з 4-хвилинною СЛР та 15-хвилинну ЗС унаслідок ФШ і СЛР з 4-хвилинним ішемічним ПК. Встановлено, що СЛР + ПК значно покращували дихальну здатність мітохондрій серця, але не впливали на мітохондріальну функцію мозку (Matsuura et al., 2017). Отже, виключно усунення реперфузійної травми не спроможне ефективно покращити неврологічні наслідки ЗС, тому ця складна проблема потребує подальшого вивчення.
Декілька паралельних рішень для пацієнтів зі складними порушеннями метаболізму. Переважно в пацієнтів із ЗСПЛ без свідків спостерігаються несприятливі неврологічні наслідки, оскільки мозок винятково чутливий до тривалої ішемії. Обмеження реперфузійної травми сприяє зменшенню поліорганних ушкоджень, але не здатне забезпечити нормальну фізіологію сильно ушкодженого мозку. Останні публікації підтримують теорію про те, що в цьому процесі значну роль відіграє постішемічна дисфункція фосфоліпідів (ПДФ) (Drgová A. et al., 2004; Hamazaki K., Kim H., 2013; Kim J. et al., 2015). Запропоновано декілька патогенетичних механізмів цього процесу, як-от пряме пошкодження цілісності мембрани, шкідливий вплив підвищених рівнів лізофосфоліпідів (ЛФЛ) і вільних жирних кислот, виснаження запасів фосфоліпідів, необхідних для нормального метаболізму. Розуміння патофізіології метаболічної дисрегуляції в тканинах мозку може суттєво зменшити неврологічні наслідки.
Зміни ліпідів мозку під час ЗС. Пошкодження ліпідів у головному мозку є критичною подією для пацієнта із ЗС. Профіль фосфоліпідів мозкової тканини включає фосфатидилетаноламін (58,3%), фосфатидилхолін (27,6%), фосфатидилсерин (17,3%), фосфатидилінозитол (2,9%), кардіоліпін (0,5%) та фосфатидилгліцерол (0,05%) (Kuschner C. et al., 2018). Значний інтерес представляють ЛФЛ, оскільки вони є основним компонентом клітинних мембран і сприяють широкому спектру фізіологічних функцій, включно з клітинною сигналізацією, транспортом і метаболізмом. Ішемія й утворення РЧК порушують нормальну функцію ЛФЛ, підвищуючи концентрацію поліненасичених жирних кислот (ПНЖК) та розщеплення ЛФЛ, що призводить до підвищення концентрації останніх. Унаслідок таких порушень підвищується концентрація ПНЖК, зокрема арахідонової кислоти, яка запускає прозапальні сигнальні шляхи.
Щодо ролі ПДФ у патофізіології нейронів при ЗС, то у фізіологічних умовах мозок містить унікальний склад фосфоліпідів як у клітинах в цілому, так і в мітохондріях (Kuschner C. et al., 2018). Використовуючи тваринну модель тяжкої ішемії з асфіксією впродовж 30 хв та подальшим 60-хвилинним серцево-легеневим байпасом через EКMO, вивчили склад фосфоліпідів у 4 основних органах – мозку, серці, нирках та печінці. У цілому в усіх зазначених органах рівні ЛФЛ були значно підвищеними, що вказує на збільшення похідних фосфоліпідів, спричинене ПДФ. Однак, незважаючи на те, що після 60-хвилинного серцево-легеневого байпасу внутрішньоклітинні концентрації ЛФЛ у серці, печінці та нирках повернулися до фізіологічних рівнів, концентрації ЛФЛ у мозку не нормалізувалися після реперфузії (Kim J. et al., 2015). Треба ще з’ясувати, із чим саме це пов’язано – з порушенням метаболізму нейронів через зменшення запасів фосфоліпідів чи з чутливістю до прозапальних ефектів ЛФЛ. Нещодавні публікації продемонстрували ключову роль метаболічної дисфункції нейронів у патофізіології ЗС. Після ішемії/реперфузії в головному мозку зменшується рівень кардіоліпіну, який відіграє основну роль у нормальній фізіології мітохондрій. Як наслідок, послаблюється активність комплексу I/III у транспортних ланцюгах електронів у нейронах (Tam J. et al., 2018). Крім того, на тваринній моделі продемонстровано, що застосування кардіоліпінової терапії з використанням SS‑31 покращує виживання та зменшує порушення метаболізму (Zhang W. et al., 2019).
Яке це має практичне значення для покращення неврологічних функцій? Якщо після ішемії мозок не в змозі поповнити фосфоліпідні компоненти через порушення метаболізму, можна спробувати пряме введення їх попередників або інших мітохондріальних стабілізуючих агентів, таких як SS‑31. Крім того, оскільки тканини головного мозку не здатні пом’якшити прозапальні ефекти ЛФЛ після реперфузії, призначення протизапальних препаратів або гіпотермія можуть бути корисними для зменшення запального ураження нейронів (Tahsili-Fahadan P. et al., 2018). Додаткову користь можна очікувати від призначення сполук, здатних нейтралізувати чи виводити вільні радикали, оскільки мозок дуже чутливий до пошкодження РЧК.
Забезпечення нервово-судинної підтримки після реанімації. Після успішної реанімації ЗС дуже важливо забезпечити нормокапнію, оскільки внутрішньочерепний тиск і церебральний кровоток часто змінені внаслідок тривалих періодів гіповентиляції під час ЗС. У пацієнтів після ЗС часто виявляються як гіпо-, так і гіперкапнія, безпосередньо пов’язані з несприятливими неврологічними наслідками (Roberts B. et al., 2013). Натомість забезпечення нормокапнії після реанімації асоціюється зі значним покращенням неврологічних наслідків (Roberts B. et al., 2014).
Поряд із цим важливо контролювати температуру тіла під час і після реанімації. У пацієнтів із ЗС часто виникає гіпертермія, що пов’язано з поганими наслідками. Хоча ідеальна температура, яку слід підтримувати в пацієнта, досі не визначена, сучасна література обстоює концепцію легкої гіпотермії від 33 до 36 °C. Отже, клініцистам важливо вживати заходів для запобігання гіпертермії. Оскільки глибока гіпотермія досліджувалася тільки при гіповолемічній ЗС, її ефективність варто оцінити і при ЗС, зумовленій іншими причинами (Tisherman S. et al., 2017).
Персоналізація реанімації ЗС. Для ілюстрації потенційного клінічного значення персоналізованих реанімаційних заходів при ЗС використано 3 клінічні випадки, кожен з яких демонструє важливість ініціації базового протоколу життєзабезпечення з використанням додаткових фізіологічних параметрів для адаптації ескалації методів реанімації на основі їх чутливості до втручань (рис. 1, 2).
1. У 60-річного чоловіка спостерігається ритм без пульсу. Через дві хв після початку СЛР виникає ФШ. Проведення ДФ забезпечує СВЦ.
2. Чоловік 60 років доставлений до лікарні ЕМД. Очевидці події розпочали СЛР, яку продовжила ЕМД. Не перериваючи КГК, встановлюється артеріальний доступ, що демонструє низький діастолічний АТ. Для його підвищення змінюється форма хвилі шляхом підвищення частоти КГК, що тимчасово підвищує діастолічний АТ. Незважаючи на постійну СЛР, у пацієнта падає тиск. Вводиться адреналін, що забезпечує підвищення АТ і чутливий до шоку ритм. Отже, пацієнт чутливий до адреналіну.
3. Чоловік 60 років доставлений до лікарні ЕМД. Свідками події розпочато СЛР, яку продовжено ЕМД. Поки тривала КГК, встановлюється артеріальний доступ, що демонструє низький діастолічний АТ. Для зміни форми хвилі частота КГК збільшується, що тимчасово підвищує діастолічний АТ. Незважаючи на постійну СЛР, у пацієнта АТ знову знижується. Багаторазове введення адреналіну не забезпечує сталої перфузії, що є показанням для застосування ЕКМО.
Нещодавні досягнення в розумінні патогенезу та лікуванні ЗС надають практикуючим лікарям широкий спектр варіантів втручання. Вони варіюють від підвищення швидкості початкових основних заходів життєзабезпечення до мультидисциплінарних інвазійних втручань, як-от EКМО, оскільки різні пацієнти потребують різних за складністю методів реанімації. Використовуючи ієрархічну модель, лікар може орієнтуватися на нові методи реанімації, щоб підтримувати стійку якість, незважаючи на різну тяжкість хвороби в різних пацієнтів. Це персоналізує підхід до реанімації ЗС, а моніторинг фізіології пацієнта адаптує втручання до конкретних патофізіологічних змін і покращує виживаність.
Kuschner C. E., Becker L. B. Recent advances
in personalizing cardiac arrest resuscitation.
F1000 Research 8: 915; June 2019.
DOI: 10.12688/f1000research.17554.1
Переклала з англ. Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 15-16 (460-461), серпень 2019 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....