Мієлома легких ланцюгів: клінічний випадок та огляд літератури
 Множинна мієлома (ММ) – В-клітинна злоякісна неоплазія, яка характеризується збільшенням кількості монотипних плазматичних клітин у кістковому мозку (КМ), що асоціюється з наявністю моноклонального парапротеїну у сироватці крові або сечі, зниженням рівня нормальних імуноглобулінів і деструктивними змінами у кістках. Частка ММ складає близько 1% у структурі усіх злоякісних новоутворень та 10-15% – гемобластозів. Найчастіше захворювання діагностують в осіб віком 65-74 роки. За підрахунками Американського товариства раку, у 2019 р. лише у США могло бути діагностовано 32 110 нових випадків ММ та 12 960 випадків смерті від цього захворювання. Основними факторами ризику розвитку ММ є похилий вік, генетична схильність, ожиріння, вплив іонізуючого випромінювання та деяких хімічних речовин. При ММ можуть уражатися різні органи, тому симптоми захворювання можуть значно варіювати. Лікування ММ швидко модифікується із впровадженням препаратів нових класів і новішого покоління: імуномодулювальних засобів, інгібіторів протеасом, моноклональних антитіл та інгібіторів гістондеацетилази.
Множинна мієлома (ММ) – В-клітинна злоякісна неоплазія, яка характеризується збільшенням кількості монотипних плазматичних клітин у кістковому мозку (КМ), що асоціюється з наявністю моноклонального парапротеїну у сироватці крові або сечі, зниженням рівня нормальних імуноглобулінів і деструктивними змінами у кістках. Частка ММ складає близько 1% у структурі усіх злоякісних новоутворень та 10-15% – гемобластозів. Найчастіше захворювання діагностують в осіб віком 65-74 роки. За підрахунками Американського товариства раку, у 2019 р. лише у США могло бути діагностовано 32 110 нових випадків ММ та 12 960 випадків смерті від цього захворювання. Основними факторами ризику розвитку ММ є похилий вік, генетична схильність, ожиріння, вплив іонізуючого випромінювання та деяких хімічних речовин. При ММ можуть уражатися різні органи, тому симптоми захворювання можуть значно варіювати. Лікування ММ швидко модифікується із впровадженням препаратів нових класів і новішого покоління: імуномодулювальних засобів, інгібіторів протеасом, моноклональних антитіл та інгібіторів гістондеацетилази.
Пропонуємо читачам розгляд клінічного випадку й огляд міжнародних рекомендацій щодо діагностики, стадіювання та лікувальної тактики при множинній мієломі, розроблених на підставі результатів рандомізованих досліджень і клінічних рекомендацій Європейського товариства медичної онкології, інструкцій Національної онкологічної мережі США (NCCN), з використанням пошукового ресурсу PubMed.
Діагностика
Відповідно до рекомендацій NCCN [1], початкове діагностичне обстеження в усіх пацієнтів включає вивчення анамнезу та фізикальний огляд, а також загальний аналіз периферичної крові, аспіраційну біопсію і трепанобіопсію КМ.
Оцінювання стану кісткового мозку. З метою оцінювання рівня інфільтрації плазматичних клітин рекомендується проведення пункції кісткового мозку та біопсії для визначення кількісних та/або якісних аномалій плазматичних клітин КМ.
Цитогенетичні дослідження. Дослідження кісткового мозку при початковій діагностиці має включати хромосомний аналіз методом флуоресцентної гібридизації in situ (FISH), що виконується на плазматичних клітинах, отриманих шляхом пункції КМ.
На думку членів Групи спеціалістів з питань множинної мієломи NCCN, FISH-дослідження з метою прогностичного визначення плазматичних клітин має проводитися, як мінімум, на виявлення транслокацій t(4;14), t(14;16), делеції 17p13 і ампліфікації хромосоми (для ММ характерні del 13, del 17p13, t(4;14), t(14;16), ампліфікація 1q21); електрофорез з імунофіксацією сироватки (SIFE) – з метою отримання більш конкретної інформації про наявний тип М-протеїну. Оцінювання змін рівнів різних білків, зокрема М-протеїну, допомагає відстежити прогресування хвороби та відповідь на лікування. Імунофіксацію сироватки крові та сечі проводять для виявлення важких ланцюгів імуноглобуліну (Ig)G, IgA, IgM і легких ланцюгів каппа та лямбда. Виконують також візуалізаційні дослідження кісток, молекулярно-генетичне й інші дослідження.
У таблиці наведені критерії діагностики ММ відповідно до рекомендацій Міжнародної робочої групи з мієломи (IMWG).
Стадію хвороби в осіб із активною мієломою визначають за допомогою Міжнародної системи стадіювання (ISS) або системи стадіювання Дьюрі – Салмона. Система ISS ґрунтується на лабораторних показниках, які легко встановити (бета‑2-мікроглобулін і альбумін сироватки)
Радіологічні обстеження. З метою оцінювання остеолітичних уражень рекомендується проведення оглядового радіологічного дослідження скелета або низькодозової комп’ютерної томографії (КТ) усього тіла. Остання більш чутлива при ідентифікації уражень кісток і є преференційним методом.
Множинна мієлома легких ланцюгів
Множинна мієлома легких ланцюгів, або мієлома Бенс-Джонса – це тип ММ, який зустрічається у 15-20% пацієнтів, характеризується продукцією тільки легких ланцюгів каппа та лямбда. Легкі ланцюги мають менший розмір та вагу порівняно з тяжкими, завдяки чому можуть циркулювати в дрібних капілярах і таким чином відкладатися в нирках, нервових закінченнях або інших органах. Залежно від показників відкладення легких ланцюгів цей стан називається або амілоїдозом легких ланцюгів (AL-амілоїдозом), або хворобою відкладення легких ланцюгів.
Лікування при множинній мієломі
Тактика лікування пацієнтів з діагнозом множинна мієлома залежить від того, є пацієнт кандидатом на трансплантацію аутологічних стовбурових клітин (аутоТСК) чи ні. Кандидатами на аутоТСК є пацієнти з діагнозом активна множинна мієлома віком до 65 років з відсутністю протипоказань (тяжка супутня патологія).
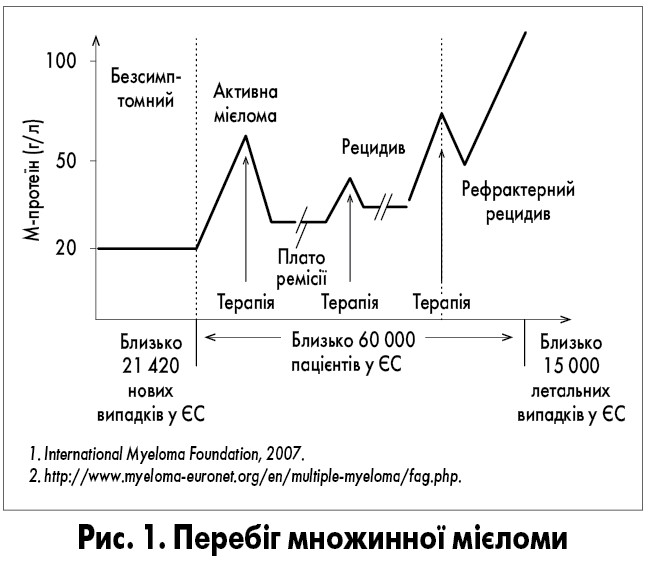 Лікування хворих на ММ, які не є кандидатами на аутоТСК, розпочинається з терапії індукції (3 курси хіміотерапії), після чого оцінюють її ефективність. При отриманні мінімальної відповіді, стабілізації захворювання чи прогресуванні відбувається зміна режиму хіміотерапії (ХТ) або рекомендується участь у клінічних дослідженнях. При отриманні повної відповіді, часткової відповіді чи дуже доброї часткової відповіді курси ХТ продовжують до 6, після чого повторно оцінюють ефективність терапії з подальшим проведенням підтримувальної терапії та/або спостереженням.
Лікування хворих на ММ, які не є кандидатами на аутоТСК, розпочинається з терапії індукції (3 курси хіміотерапії), після чого оцінюють її ефективність. При отриманні мінімальної відповіді, стабілізації захворювання чи прогресуванні відбувається зміна режиму хіміотерапії (ХТ) або рекомендується участь у клінічних дослідженнях. При отриманні повної відповіді, часткової відповіді чи дуже доброї часткової відповіді курси ХТ продовжують до 6, після чого повторно оцінюють ефективність терапії з подальшим проведенням підтримувальної терапії та/або спостереженням.
Поліхіміотерапія (ПХТ) при ММ є основним методом лікування. Найпоширенішими та найбільш ефективними є схеми VRD (бортезоміб + леналідомід + дексаметазон), VMP (ботезоміб + мелфалан + преднізолон), VTD (бортезоміб + дексаметазон + талідомід), VCD (бортезоміб + циклофосфамід + дексаметазон).
Клінічний випадок
Пацієнт О., 60 років, погіршення стану протягом 1 міс, коли з’явилися скарги на слабкість, нудоту, відразу до їжі, схуднення на 4 кг за 3 тижні. Під час лабораторного дослідження виявлено високий рівень креатиніну – 1059 мкмоль/л (норма не вище 106 мкмоль/л), калій – 5,6 ммоль/л (норма 5,1 ммоль/л), гемоглобін – 108 г/л (норма 140г/л), швидкість осідання еритроцитів – 36 мм/год (норма 15 мм/год), B2-MG мікроглобулін – 5,82 мг/л. За даними ультразвукового дослідження органів черевної порожнини та нирок патології не виявлено. За даними КТ скелета вогнищевої патології не виявлено. Проведено трепанобіопсію КМ.
Патогістологічний висновок та результати імуногістохімічного дослідження: гістологічна картина може відповідати плазмоцитомі.
Імуногістохімічне дослідження: Кі‑67(SP6) – експресія позитивна 50%. CD20 (CD20 Ab‑1; L26) – експресія до 10%. CD3 – експресія до 5%. CD68 (Macrophage Marker) Ab‑3 (Clone KP1) – експресія негативна. CD138 Ab‑2 (Clone Ml 15) – експресія дифузно позитивна 50%. MUM1/IRF4(MUM1p) – експресія дифузно позитивна 40%. Плазматичні клітини Ab‑1 (Clone LIV3G11) – експресія позитивна в плазмоциті. CD38 Ab‑3 (Clone 38C03; same as SPC32) – експресія позитивна 30%. Легкі ланцюги каппа Ab‑2 – експресія позитивна. Легкі ланцюги лямбда Ab‑2 – експресія фонова. Амілоїд бета (BAM01) – експресія вогнищево позитивна. Антиген до епітеліальної мембрани EMA Ab‑3 (Clone E29) – експресія вогнищево позитивна. CD45/T200/LCA Ab‑2 (Clone PD7/26/16+2B11) – експресія позитивна 30%. Фарбування конго червоним – позитивна в плазмоцитах.
Цитохімічне та морфологічне дослідження мазків периферичної крові та КМ: за даними цитоморфологічного та цитохімічного дослідження – множинна мієлома. Імунофіксація білків сироватки крові та сечі – моноклональні парапротеїни в сироватці крові не виявлені. Виявлено ВJ-протеїн класу лямбда у сечі в концентрації 0,347 (1,040 г/добу).
Аналіз крові на легкі ланцюги (каппа та лямбда): вільні ланцюги Ig в сироватці крові: каппа – 17,1 (норма 3,3‑19,4), лямбда – 3970 (норма 5,71-26,30), коефіцієнт каппа/лямбда – 0 (0,26-1,65).
Аналіз стернального пунктату: плазматичні клітини – 24,2%.
Діагноз: імуногістохімічна картина відповідає плазмоклітинній мієломі (плазмоцитомі) із переважанням ланцюгів лямбда.
Терапія: з метою циторедукції протягом 5 днів проведено 2 курси дексаметазону в дозі 20-40-40-40-4 мг без позитивної динаміки щодо зниження рівня креатиніну. У зв’язку з наростанням рівня креатиніну, сечовини та калію призначено нирково-замісну терапію – 7 сеансів гемодіалізу. При рівні креатиніну 290 мкмоль/л, сечовини 11 ммоль/л розпочато ПХТ за схемою RVd (бортезоміб у дозі 1,3 мг/м2 площі поверхні тіла в/в у 1‑й, 4, 8 та 11‑й дні, леналідомід 25 мг/день перорально з 1‑го по 14‑й день і дексаметазон 20 мг/день перорально у 1‑й, 2, 4, 5, 8, 9, 11 та 12‑й дні циклу). Після проведення 2 курсів ПХТ за схемою RVd результати дослідження вільних ланцюгів сироватки крові були такими: ланцюги каппа – 24,6 мг/л, лямбда – 446 мг/л, каппа/лямбда – 0,06. На сьогодні пацієнт продовжує лікування, після отримання повної відповіді на лікування планується проведення аутоТСК.
Згідно з протоколами NССN (2020), у пацієнтів зі вперше виявленою ММ RVd є схемою вибору для первинної терапії та єдиною схемою, застосування якої подовжує загальну виживаність (ЗВ).
У рандомізованому дослідженні ІІІ фази SWOG 0777 порівнювали схеми RVd та Rd (леналідомід/дексаметазон) як первинне лікування пацієнтів із ММ. У дослідженні взяли участь 525 пацієнтів, які були рандомізовані на дві групи. Пацієнти 1-ї групи (n=242) отримували лікування за схемою RVd, пацієнти
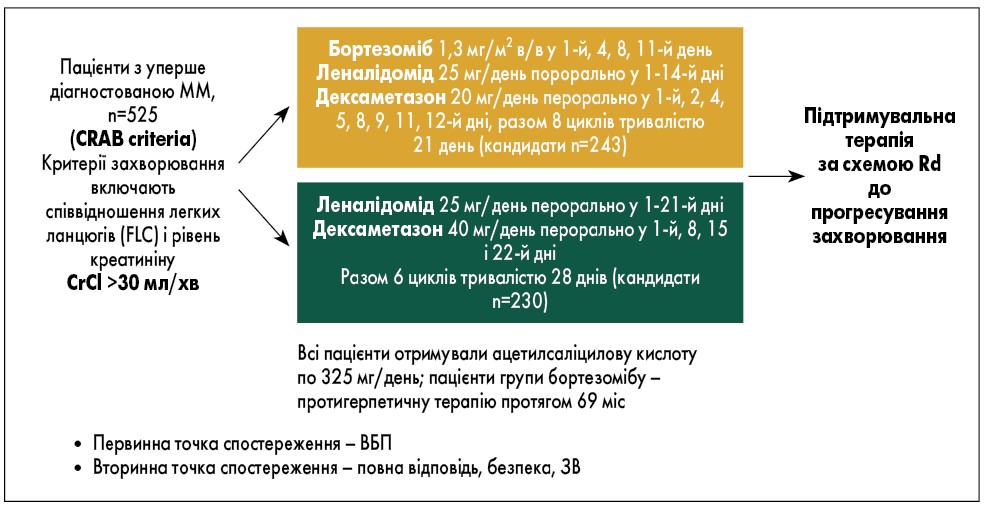 Рис. 2. Дизайн дослідження SWOG 0777
Рис. 2. Дизайн дослідження SWOG 0777
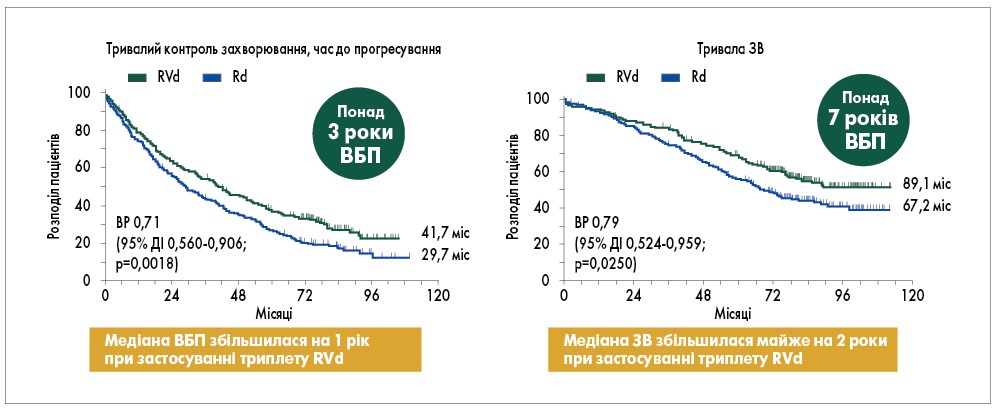 Рис. 3. Схема RVd у порівнянні з Rd для терапії вперше виявленої ММ
Рис. 3. Схема RVd у порівнянні з Rd для терапії вперше виявленої ММ
Висновки
Таким чином, ММ – доволі поширена патологія серед усіх лімфопроліферативних захворювань. Здебільшого захворювання має типову симптоматику, лабораторну, морфологічну й імуногістохімічну картину, однак при деяких формах, таких як мієлома легких ланцюгів, що складає до 20% усіх випадків ММ, встановлення діагнозу та диференційна діагностика викликають труднощі. Одним із перших проявів мієломи легких ланцюгів є симптоми гострої ниркової недостатності, у зв’язку з чим пацієнт звертається до сімейного лікаря, лікаря-нефролога, тому обізнаність лікарів первинної ланки та суміжних спеціалістів дозволяє запідозрити патологію та вчасно направити на консультацію до гематолога. На цьому етапі вчасна діагностика, дотримання затверджених методик первинного обстеження та стандартів лікування дають хороші результати, дозволяють зменшити частоту прогресування захворювання та підвищують шанси досягнення тривалої ремісії.
Література
- Multiple Myeloma. NCCN Clinical Practical Guidelines in Oncology. Версія 4.2020 від 8 травня 2020 р.
- Gerecke C., Fuhrmann S., Strifler S., Schmidt-Hieber M., Einsele H., Knop S. The Diagnosis and Treatment of Multiple Myeloma. Dtsch Arztebl Int. 2016 Jul 11; 113(27-28): 470-476. doi: 10.3238/arztebl.2016.0470.
- Chavda S.J., Yong K. Multiple myeloma. Br J Hosp Med (Lond). 2017 Feb 2; 78(2): C21-C27. doi: 10.12968/hmed.2017.78.2.C21.
- Rajkumar S.V., Dimopoulos M.A., Palumbo A. et al. International Myeloma Working Group updated criteria for the diagnosis of multiple myeloma. Lancet Oncol. 2014; 15: e538-e548.
- Palumbo A., Avet-Loiseau H., Oliva S., Lokhorst H.M., Goldschmidt H., Rosinol L. et al. Revised international staging system for multiple myeloma: a report from international myeloma working group. J Clin Oncol. 2015; 33: 2863-2869.
- Avet-Loiseau H., Durie B.G., Cavo M. et al. International Myeloma Working Group. Combining fluorescent in situ hybridization data with ISS staging improves risk assessment in myeloma: an International Myeloma Working Group collaborative project. Leukemia. 2013; 27(3): 711-717.
- Costa L.J., Zhang M.J., Zhong X. et al. Trends in utilization and outcomes of autologous transplantation as early therapy for multiple myeloma. Biol Blood Marrow Transplant. 2013; 19(11): 1615-1624.
- Scott K., Hayden P.J., Will A., Wheatley K., Coyne I. Bortezomib for the treatment of multiple myeloma. Cochrane Database Syst Rev. 2016. Apr 20; 4: CD010816. doi: 10.1002/14651858.CD010816.pub2.
- Moreau P., San Miguel J., Sonneveld P., Mateos M.V., Zamagni E. et al. ESMO Guidelines Committee. Multiple myeloma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2017 Jul 1; 28(suppl. 4): iv52-iv61. doi: 10.1093/annonc/mdx096.
- Richardson P.G. et al. Lenalidomide, bortezomib, and dexamethasone combination therapy in patients with newly diagnosed multiple myeloma. Blood. 2010 Aug 5; 116(5): 679-686.
- Attal M. et al. Lenalidomide, Bortezomib, and Dexamethasone with Transplantation in Myeloma. N Engl J Med. 2017 Apr 6; 376(14): 1311-1320.
- McCarthy P.L. et al. Lenalidomide after Stem-Cell Transplantation for Multiple Myeloma. N Engl J Med. 2012; 366: 1770-1781.
- Durie B.G. et al. Bortezomib with lenalidomide and dexamethasone versus lenalidomide and dexamethasone alone in patients with newly diagnosed myeloma without intent for immediate autologous stem-cell transplant (SWOG S0777): a randomised, open-label, phase 3 trial. Lancet. 2017 Feb 4; 389(10068): 519-527.
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 3 (64) 2020 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...





