П’ятирічна загальна виживаність у пацієнтів із прогресуючим недрібноклітинним раком легені, які отримували лікування пембролізумабом
Результати дослідження I фази KEYNOTE-001
Для пацієнтів з недрібноклітинним раком легені (НДРЛ) характерна низька медіана загальної виживаності (ЗВ) та 5-річної виживаності. Так, у США з 2008 по 2014 р. 5-річна виживаність усіх пацієнтів з НДРЛ складала 24%, а пацієнтів з віддаленими метастазами – лише 5,5% [1]. Впровадження інноваційних протипухлинних препаратів і використання прогностичних біомаркерів забезпечили покращення результатів лікування пацієнтів з прогресуючим/метастатичним НДРЛ [2, 3]; однак ступінь змін на краще довгострокової виживаності залишився невизначеним.
Важливим досягненням у лікуванні НДРЛ стало нещодавнє впровадження в клінічну практику препаратів, які стимулюють розпізнавання клітин пухлини імунною системою шляхом інгібування передачі сигналів між рецептором програмованої клітинної смерті 1 (PD‑1) та двома лігандами білка програмованої клітинної смерті – PD-L1 і PD-L2 [4, 5]. Пембролізумаб є препаратом моноклональних антитіл, які зв’язуються з рецептором PD‑1 та блокують його взаємодію з PD‑L1 і PD‑L2 [5, 6]. Протипухлинна активність і прийнятна токсичність монотерапії пембролізумабом у пацієнтів з прогресуючим НДРЛ (незалежно від того, отримували вони попереднє лікування чи ні) були вперше продемонстровані у дослідженні Ib фази KEYNOTE‑001 [7]. Слід зазначити, що пацієнти з оціненим за показником Шкали пропорції пухлини (tumor proportion score – TPS) високим рівнем експресії PD-L1, котрий становив 50% або більше, досягали вищої частоти об’єктивної відповіді на лікування та більшої медіани ЗВ порівняно з пацієнтами з низькою/відсутньою експресією PD-L1 у клітинах пухлини. Результати дослідження KEYNOTE‑001 сприяли прискореному схваленню застосування пембролізумабу у пацієнтів з TPS PD-L1 ≥50%, схваленню тесту для оцінки експресії PD‑L1 та включенню пембролізумабу до рекомендацій з лікування при НДРЛ [2, 3].
Ці результати згодом були підтверджені у дослідженні KEYNOTE‑010, що продемонструвало покращення ЗВ на тлі лікування пембролізумабом порівняно з доцетакселом у пацієнтів з прогресуючим НДРЛ, які раніше вже отримували лікування та мали TPS PD-L1 ≥1% [8]. При застосуванні як першої лінії терапії пембролізумаб покращував ЗВ порівняно з хіміотерапією на основі препарату платини у пацієнтів з НДРЛ без молекулярних мутацій EGFR/ALK та з TPS PD-L1 ≥50% (KEYNOTE‑024) [9], а також у пацієнтів з TPS PD-L1 ≥1% (KEYNOTE‑042) [10].
Застосування пембролізумабу у комбінації з подвійною хіміотерапією на основі препарату платини зараз розглядається як стандарт першої лінії терапії, оскільки таке лікування покращує ЗВ пацієнтів з НДРЛ порівняно із застосуванням хіміотерапії на основі препарату платини у поєднанні з плацебо. Це було продемонстровано у дослідженнях KEYNOTE‑189 (пацієнти з неплоскоклітинним раком) [11] та KEYNOTE‑407 (хворі на плоскоклітинний рак) [12]. Однак у пацієнтів з TPS PD‑L1 ≥50% частіше застосовується монотерапія пембролізумабом, ніж пембролізумаб у комбінації з хіміотерапією, Така тактика базується на аналогічних результатах, отриманих при перехресних порівняннях [13]. Оскільки KEYNOTE‑001 було першим дослідженням з оцінки застосування пембролізумабу у пацієнтів з прогресуючим НДРЛ, воно надає інформацію про результати найдовшого на сьогодні подальшого спостереження за пацієнтами з цим діагнозом, які отримували монотерапію пембролізумабом. У цій публікації розглянуті результати 5-річної оцінки ефективності та безпеки терапії пембролізумабом.
Пацієнти та методи
Пацієнти
Повна інформація про дизайн дослідження KEYNOTE‑001 у когортах пацієнтів з НДРЛ вже оприлюднювалася раніше [7, 14]. Вік пацієнтів, які могли бути включені до когорт з НДРЛ, становив ≥18 років; вони мали локально-прогресуючий/метастатичний НДРЛ, вимірювані прояви хвороби за імунозалежними критеріями відповіді (irRC) [15], функціональний статус за шкалою Східної об’єднаної онкологічної групи рівний 1 балу або менше, а також своєчасно взятий при біопсії зразок пухлинної тканини.
Пацієнти, які могли бути включені до когорти без попереднього лікування, раніше не повинні були отримувати системну терапію з приводу прогресуючого захворювання або ад’ювантне лікування протягом попереднього року; також вони не повинні були мати мутації EGFR та/або транслокації ALK (за винятком 11 осіб, які були включені до внесення коректив у протокол дослідження 28 березня 2013 р.) та TPS PD-L1 ≥1%. Пацієнти, придатні до включення у когорти, які вже отримували лікування, мали в анамнезі зафіксований факт його неефективності на фоні прийому одного або двох і більше засобів системної терапії, призначених з приводу прогресування захворювання (залежно від когорти).
Дизайн дослідження та лікування
У ході дослідження KEYNOTE‑001 пацієнти з НДРЛ отримували пембролізумаб внутрішньовенно в дозі 2 мг/кг маси тіла через кожні 3 тижні або в дозі 10 мг/кг через кожні 2 чи 3 тижні. Лікування продовжували до прогресування захворювання, появи непереносимих проявів токсичності, прийняття дослідником рішення про припинення терапії або до моменту вибуття пацієнта з дослідження. Після внесення змін до протоколу у квітні 2016 р. всі пацієнти були переведені з початково призначеного їм режиму лікування на введення пембролізумабу у дозі 200 мг через кожні 3 тижні, а пацієнти, які досягли часткової відповіді або стабілізації захворювання та вже отримали 24-місячний курс лікування, могли його припинити (лікування могло бути відновлене при прогресуванні/рецидиві захворювання).
Кінцеві точки й оцінки
Первинною кінцевою точкою ефективності була частота об’єктивної відповіді (ЧОВ) на лікування. Візуалізаційні дослідження виконувалися пацієнтам через кожні 9 тижнів у перші 2 роки участі у дослідженні, через кожні 16 тижнів – протягом 3-го року, та через кожні 6 міс згодом. Відповідь на лікування оцінювали шляхом незалежного централізованого експертного розгляду згідно з Критеріями оцінки відповіді при солідних пухлинах (RECIST) версії 1.1 [16]; також дослідники проводили оцінку відповіді згідно з irRC [15], про яку і повідомляється в цьому аналізі.
Вторинними кінцевими точками оцінки ефективності були ЗВ і тривалість відповіді (ТВ; час від першої підтвердженої відповіді до першої документальної реєстрації прогресування захворювання). Виживаність оцінювали через кожні 2 міс після припинення лікування пембролізумабом. Реєстрацію небажаних явищ (НЯ) та ступеня їх вираженості проводили згідно з Загальними термінологічними критеріями НЯ Національного інституту раку США (National Cancer Institute Common Terminology Criteria for Adverse Events, версія 4.0).
Експресію PD-L1 у зразках, взятих при біопсії пухлин, оцінювали за допомогою імуногістохімічного аналізу з використанням клону антитіл 22C3 [17]. Позитивний статус експресії PD-L1 визначався як зафарбовування мембран ≥1% пухлинних клітин або характерний патерн зафарбовування, зумовлений запальними інфільтратами з мононуклеарів [7, 17].
Результати
Пацієнти та лікування
Загалом з 9 травня 2012 по 13 липня 2014 р. у дослідження було включено 550 пацієнтів (101 пацієнт, який раніше не отримував лікування, та 449 пацієнтів, яким вже проводили попередню терапію). Станом на дату завершення збору даних (5 листопада 2018 р.) медіана періоду подальшого спостереження склала 60,6 міс (діапазон від 51,8 до 77,9 міс). Медіана тривалості лікування становила 3,3 міс (діапазон від 1 дня до 75,9 міс). На момент проведення аналізу 100 пацієнтів ще залишалися живими. Шістдесят пацієнтів (14 (14%) зі 101 пацієнта, які раніше не отримували лікування, та 46 (10%) із 449 пацієнтів, котрі вже лікувалися раніше) отримали терапію пембролізумабом протягом 2 років чи більше. Один пацієнт з групи, яка отримувала попереднє лікування, припинив терапію через 44,4 міс, а після констатації прогресування захворювання через 47,2 міс розпочав другий курс терапії пембролізумабом (згідно з протоколом дослідження). Під час другого курсу лікування у пацієнта відзначалася часткова відповідь, яка зберігалася до прогресування захворювання, що відбулося через 53,7 міс.
Ефективність
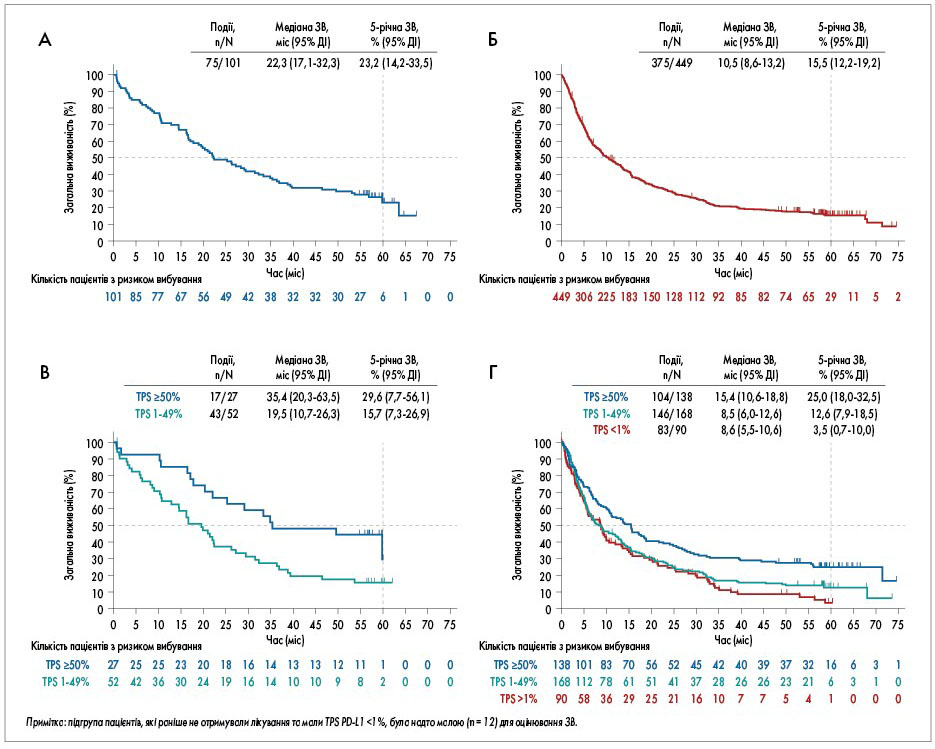
Померли 75 (74,3%) пацієнтів, які раніше не отримували лікування, та 375 (83,5%) пацієнтів, яким уже проводилася попередня терапія. Медіана ЗВ склала 22,3 міс (95% довірчий інтервал – ДІ – 17,1‑32,3) у пацієнтів, що раніше не отримували лікування, та 10,5 міс (95% ДІ 8,6‑13,2) – у пацієнтів, яким проводилася попередня терапія (рис. A та Б).
Через 5 років оцінена за методом Каплана – Меєра ЗВ становила 23,2% у пацієнтів, що раніше не отримували лікування, та 15,5% у пацієнтів, яким проводилася попередня терапія. Серед хворих, які раніше не отримували лікування, ЗВ через 2; 3 та 4 роки становила 49; 37 та 31% відповідно. У пацієнтів, яким раніше проводилася терапія, ЗВ через 2; 3 та 4 роки становила 30,1; 20,9 та 18,2% відповідно.
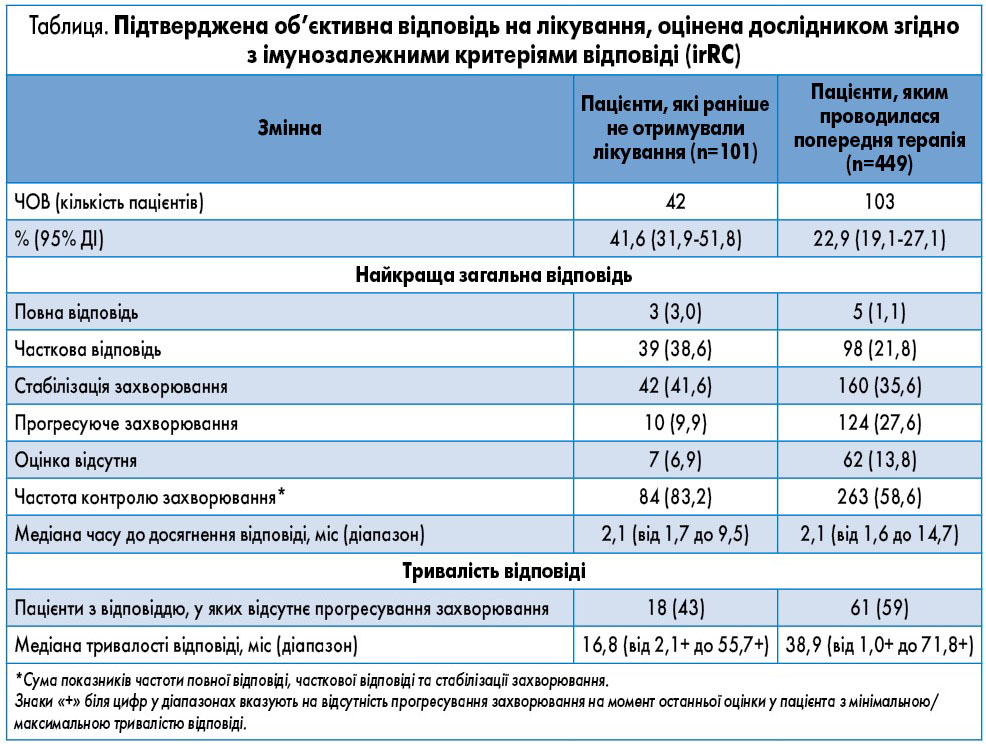
Підтверджена об’єктивна відповідь згідно з оцінкою дослідника за irRC отримана у 42 пацієнтів (41,6%; 95% ДІ 31,9-51,8) у групі, що раніше не отримувала лікування, та у 103 пацієнтів (22,9%; 95% ДІ 19,1-27,1), яким проводилася попередня терапія (таблиця).
Слід зазначити, що ЧОВ, оцінена дослідником за критеріями irRC, була вищою за визначену під час процедури централізованого розгляду результатів згідно з критеріями RECIST у версії 1.1 [7], особливо серед пацієнтів, які раніше не отримували лікування. Повна відповідь була досягнута у 3 пацієнтів, що раніше не отримували лікування, та у 5 пацієнтів, яким проводилася попередня терапія. Більшість відповідей спостерігалася незабаром після початку терапії. Серед 145 пацієнтів з відповіддю на лікування її вдалося досягти протягом 3 та 6 міс у 105 (72%) та 133 (92%) хворих відповідно. Медіана часу до настання відповіді склала 2,1 міс – як у пацієнтів, які раніше не отримували лікування (діапазон 1,7‑9,5 міс), так і у хворих, що отримували попередню терапію (діапазон 1,6‑14,7 міс). Постійна відповідь відзначалася у 18 (43%) хворих, що раніше не отримували лікування, та у 61 (59%) пацієнта, якому проводилася попередня терапія. Серед пацієнтів з об’єктивною відповіддю медіана її тривалості складала 16,8 міс (діапазон від 2,1+ до 55,7+ міс) в осіб, що раніше не отримували лікування, та 38,9 міс (діапазон від 1,0+ до 71,8+ міс) – у пацієнтів, котрим проводилася попередня терапія (таблиця; знаки «+» біля цифр у діапазонах вказують на відсутність прогресування захворювання на момент останньої оцінки у пацієнта з мінімальною/максимальною тривалістю відповіді).
TPS PD-L1 ≥50% асоціювався з тривалішою ЗВ [7]. У групі пацієнтів, які раніше не отримували лікування, медіана ЗВ склала 35,4 міс (95% ДІ 20,3‑63,5), а 5-річна ЗВ – 29,6% серед пацієнтів з TPS PD-L1 ≥50%. У групі пацієнтів, що раніше не отримували лікування, було дуже мало осіб з TPS PD-L1 <1% (n=12), щоб оцінювати частоту ЗВ; однак медіана ЗВ становила 19,5 міс (95% ДІ 10,7‑26,3) при 5-річній ЗВ, рівній 15,7%, у пацієнтів з TPS PD-L1 у межах від 1 до 49% (рис. В). Серед пацієнтів, які раніше отримували лікування та мали TPS PD-L1 ≥50%, медіана ЗВ склала 15,4 міс (95% ДІ 10,6‑18,8), а 5-річна ЗВ – 25%; у пацієнтів з TPS PD-L1 від 1 до 49% ці ж показники становили 8,5 міс (95% ДІ 6,0‑12,6) та 12,6% відповідно; у пацієнтів з TPS PD‑L1 ≤1% – 8,6 міс (95% ДІ 5,5-10,6) та 3,5% відповідно (рис. Г). Коли ЗВ та ЧОВ оцінювали в квартилях, визначених залежно від початкової експресії PD‑L1 (у всіх пролікованих пацієнтів), вищий рівень експресії PD-L1 був асоційований з більшою медіаною ЗВ, 5-річною виживаністю та ЧОВ.
Рис. Оцінка 5-річної ЗВ за методом Каплана – Меєра. A – пацієнти, які раніше не отримували лікування. Б – пацієнти, яким раніше проводилася терапія. В – розподіл пацієнтів, які раніше не отримували лікування, залежно від рівня експресії PD-L1, оціненого за TPS. Г – розподіл пацієнтів, яким раніше проводилася терапія, залежно від рівня експресії PD-L1, оціненого за TPS
Серед 100 пацієнтів, які залишалися живими на момент припинення збору даних, 78 (78%) мали об’єктивну відповідь (20 (77%) з 26 пацієнтів, які раніше не отримували лікування, та 58 (78%) із 74 пацієнтів, які вже отримували попередню терапію). Серед пацієнтів, котрі залишалися живими, повна відповідь на лікування була констатована у 1 хворого, який раніше не отримував лікування, та у 5 пацієнтів, що отримували попередню терапію.
Із 60 пацієнтів, які отримали 2-річний або більш тривалий курс лікування пембролізумабом, 46 залишалися живими на момент припинення збору даних. Оцінена 5-річна ЗВ склала 78,6% в групі, яка раніше не отримувала лікування (n=14), та 75,8% – у групі, яка отримувала попередню терапію (n=46). Серед пацієнтів, які завершили курс терапії пембролізумабом тривалістю 2 роки або довше, об’єктивна відповідь була зареєстрована у 12 (86%) з 14 пацієнтів, які раніше не отримували лікування, та у 42 (91%) із 46 пацієнтів, котрим проводили попередню терапію. Медіана ТВ склала 52 міс (діапазон від 10,2 до 55,7+ міс) і не була досягнута (діапазон від 12,5 до 71,8+ міс) відповідно. На момент припинення збору даних постійна відповідь спостерігалася у 7 (58%) пацієнтів, які раніше не отримували лікування, та у 30 (71%) пацієнтів, що отримували попередню терапію.
Безпека
Пов’язані з лікуванням НЯ виникали загалом у 388 (71%) із 550 пацієнтів. Асоційовані з лікуванням НЯ 3-5 ступеня розвинулися у 69 (13%) пацієнтів. Тільки три додаткових пов’язаних з лікуванням НЯ 3-5 ступеня виникли в період подальшого спостереження після аналізу через 3 роки [14]: гіпертензія, порушення толерантності до глюкози та реакція гіперчутливості – всі вони були оцінені як НЯ 3 ступеня та згодом минули. Серйозні НЯ виникли у 228 (42%) пацієнтів, включаючи 50 (9%) осіб, що мали пов’язані з лікуванням серйозні НЯ. Асоційовані з лікуванням НЯ призвели до припинення лікування у 31 (6%) пацієнта, з яких 9 ще живі, а 7 – мають відповідь на лікування, що триває.
Загалом 92 (17%) пацієнти перенесли імуноопосередковані НЯ. Найчастішим імуноопосередкованим НЯ (всі ступені) були гіпотиреоз (9%), пневмоніт (5%) і гіпертиреоз (2%). У 21 (4%) пацієнта були зафіксовані імуноопосередковані НЯ 3-5 ступеня.
Обговорення
П’ятирічні результати дослідження KEYNOTE‑001 відображають дані найдовшого на сьогодні періоду спостереження за пацієнтами з прогресуючим/метастатичним НДРЛ, які отримували пембролізумаб. Вони очевидно вказують на клінічно значуще покращення порівняно з 5-річною ЗВ 5,5%, яка була досягнута при призначенні стандартної цитотоксичної хіміотерапії безпосередньо перед початком застосування імунотерапії для лікування прогресуючого/метастатичного НДРЛ [1]. Результати оцінки ефективності пембролізумабу, отримані у цьому дослідженні, та виявлена асоціація між експресією пухлиною PD-L1 і ЗВ узгоджуються з даними попередніх рандомізованих контрольованих досліджень з більш обмеженим періодом подальшого спостереження, включаючи KEYNOTE‑010, KEYNOTE‑024 та KEYNOTE‑042 [8, 19, 20]. У сукупності ці дані підтверджують наявність зв’язку між TPS PD-L1, оціненим методом імуногістохімічного аналізу, та довгостроковими наслідками у пацієнтів, які отримували монотерапію пембролізумабом з приводу прогресуючого НДРЛ. Вони підкреслюють потенціал довгострокової користі, який може бути реалізований шляхом індивідуального підбору лікування.
Стійкість та тривалість відповіді, досягнутої під час лікування пембролізумабом, видається важливим фактором, який робить вагомий внесок у покращення ЗВ. Підгрупа пацієнтів не лише залишалася живими через 5 років, а й досягла стійкої відповіді; при цьому деякі пацієнти (як ті, що раніше не отримували лікування, так і ті, котрим проводилася попередня терапія) мали тривалість відповіді ≥4 роки. Серед 60 пацієнтів, які отримували лікування пембролізумабом протягом ≥2 років, більш ніж у 85% була констатована об’єктивна відповідь, а 5-річна виживаність перевищила 75%. Слід зазначити, що на тлі лікування пембролізумабом медіана ТВ склала 52 міс у пацієнтів, котрі раніше не отримували лікування, та на момент аналізу не була досягнута у пацієнтів, яким вже проводилася попередня терапія. Ці результати узгоджуються з даними досліження KEYNOTE‑010, у якому ЧОВ (95%) та 3-річна ЗВ (98,7%) були вищими у пацієнтів, які завершили 2-річне лікування [20]. Важливість досягнення об’єктивної відповіді додатково підкреслюється висновком про те, що більшість пацієнтів, які залишалися живими, її досягли: серед 100 пацієнтів, які були живі на момент проведення аналізу (з них 46 отримали курс терапії пембролізумабом тривалістю 2 роки та більше), 78% мали об’єктивну відповідь.
Довготривалі аналізи рандомізованих контрольованих досліджень (хоча із меншим періодом подальшого спостереження, ніж у представленому аналізі результатів дослідження KEYNOTE- 001) незмінно демонструють покращення ЗВ на тлі лікування пембролізумабом порівняно з цитотоксичною хіміотерапією. У оновленому аналізі результатів дослідження KEYNOTE‑010 у пацієнтів, які вже отримували попереднє лікування з приводу НДРЛ, в осіб з TPS PD-L1 ≥50% 3-річна ЗВ склала 35% при застосуванні пембролізумабу порівняно з 13% у пацієнтів, які отримували доцетаксел (медіана ЗВ 16,9 порівняно з 8,2 міс), тоді як серед осіб з TPS PD-L1 ≥1% 3-річна ЗВ склала 23 та 11% відповідно (медіана ЗВ 11,8 порівняно з 8,4 міс) [20]. Оновлений аналіз результатів дослідження KEYNOTE‑024 продемонстрував, що при застосуванні пембролізумабу як першої лінії терапії у пацієнтів з TPS PD-L1 ≥50% 2-річна ЗВ склала 51,5% порівняно з 34,5% в групі хіміотерапії на основі препарату платини (медіана ЗВ 30,0 порівняно з 14,2 міс) [22]. Таким чином, результати рандомізованих досліджень зіставні з такими непорівняльного дослідження KEYNOTE‑001 в аналогічні моменти часу. Це свідчить про те, що пацієнти з TPS PD-L1 ≥50% можуть отримати більшу абсолютну користь від призначення пембролізумабу як препарату саме першої, а не другої лінії.
П’ятирічна ЗВ була високою, а медіана ЗВ – тривалою в усіх оцінених підгрупах, хоча оцінка цих результатів має інтерпретуватися з обережністю, враховуючи обмежену кількість пацієнтів у різних підгрупах. Згідно з результатами дослідження KEYNOTE‑001, повідомленими через 1 та 3 роки подальшого спостереження [7, 14], гістологічна картина неплоскоклітинного раку була асоційована з вищою 5-річною ЗВ у пацієнтів, які раніше не отримували лікування, тоді як у групі пацієнтів, яким проводилася попередня терапія, виявлено протилежні дані.
Оновлені дані про безпеку, отримані при проведенні поточного аналізу, узгоджуються з відомим профілем безпеки пембролізумабу та підтверджують довготривалу переносимість лікування пацієнтів з прогресуючим НДРЛ цим препаратом. Загальна частота пов’язаних із лікуванням НЯ у цьому аналізі була аналогічною тій, про яку повідомлялося у попередніх аналізах [7, 14]. Частота пов’язаних із лікуванням та імуноопосередкованих НЯ була вищою у пацієнтів, у яких зафіксована відповідь на лікування, порівняно з тими хворими, у яких вона була відсутня.
П’ятирічна виживаність на тлі лікування пембролізумабом (пацієнти, котрі раніше не отримували лікування – 23,2%; хворі, яким проводили попередню терапію – 15,5%) узгоджується з показниками, про які повідомлялося при використанні інших блокаторів PD-(L)1.
Таким чином, отримані у дослідженні KEYNOTE‑001 результати демонструють, що пембролізумаб забезпечує довготривалу перевагу в плані ЗВ і стійку відповідь з прийнятним профілем переносимості та безпеки у пацієнтів з прогресуючим НДРЛ та ескпресією PD-L1 (незалежно від того, чи отримував пацієнт попереднє лікування). У контексті історично низької 5-річної виживаності пацієнтів з прогресуючим НДРЛ ці дані свідчать про можливість значного покращення результатів лікування цієї категорії хворих при застосуванні пембролізумабу.
Стаття друкується у скороченні.
Повний список літератури, що включає 27 джерел, знаходиться в редакції.
J Clin Oncol. 2019 Oct 1; 37(28): 2518-2527. doi: 10.1200/JCO.19.00934.
Переклала з англ. Інга Боброва
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 4 (65) 2020 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...