Місце кардіопротекторної метаболічної терапії в пацієнтів з артеріальною гіпертензією й ішемічною хворобою серця
6 квітня відбулася науково-практична конференція «Серце та судини», під час якої були розглянуті найважливіші аспекти ведення хворих кардіоваскулярного профілю. Доповідь старшого наукового співробітника відділу симптоматичних гіпертензій ДУ «ННЦ «Інститут кардіології ім. М. Д. Стражеска» НАМН України» (м. Київ), кандидата медичних наук Оксани Леонідівни Рековець стосувалася місця кардіопротекторної метаболічної терапії у хворих з артеріальною гіпертензією (АГ) й ішемічною хворобою серця (ІХС).
 Серцево-судинні захворювання (ССЗ) продовжують посідати провідні місця в структурі захворюваності та смертності. За статистичними даними, в Україні зареєстровано 12 млн хворих на АГ, але про наявність гіпертензії знає лише 81%, антигіпертензивні препарати приймає 48%, а досягає нормалізації артеріального тиску (АТ) лише 12% пацієнтів. Проблема досягнення цільових показників АТ є нагальною в усьому світі. Для осіб віком до 65 років цільовий АТ становить <140/90 мм рт. ст., а за умови хорошої переносимості лікування – <130/80 мм рт. ст.
Серцево-судинні захворювання (ССЗ) продовжують посідати провідні місця в структурі захворюваності та смертності. За статистичними даними, в Україні зареєстровано 12 млн хворих на АГ, але про наявність гіпертензії знає лише 81%, антигіпертензивні препарати приймає 48%, а досягає нормалізації артеріального тиску (АТ) лише 12% пацієнтів. Проблема досягнення цільових показників АТ є нагальною в усьому світі. Для осіб віком до 65 років цільовий АТ становить <140/90 мм рт. ст., а за умови хорошої переносимості лікування – <130/80 мм рт. ст.
Зниження систолічного АТ лише на 10 мм рт. ст. дає змогу суттєво зменшити ризик великих серцево-судинних подій і загальну серцево-судинну смертність. АГ й ІХС посідають перше та третє місця відповідно в структурі коморбідних захворювань пацієнтів, які померли від коронавірусної хвороби (COVID‑19), а наявність АГ удвічі підвищує ймовірність госпіталізації до реанімаційного відділення. Це додатково обґрунтовує необхідність належного лікування цих патологічних станів.
Окрім контролю АТ, пацієнтам з АГ та ІХС рекомендована модифікація способу життя (відмова від куріння, здорове харчування, фізичні навантаження), ліпідознижувальна терапія та вторинна профілактика ацетилсаліциловою кислотою.
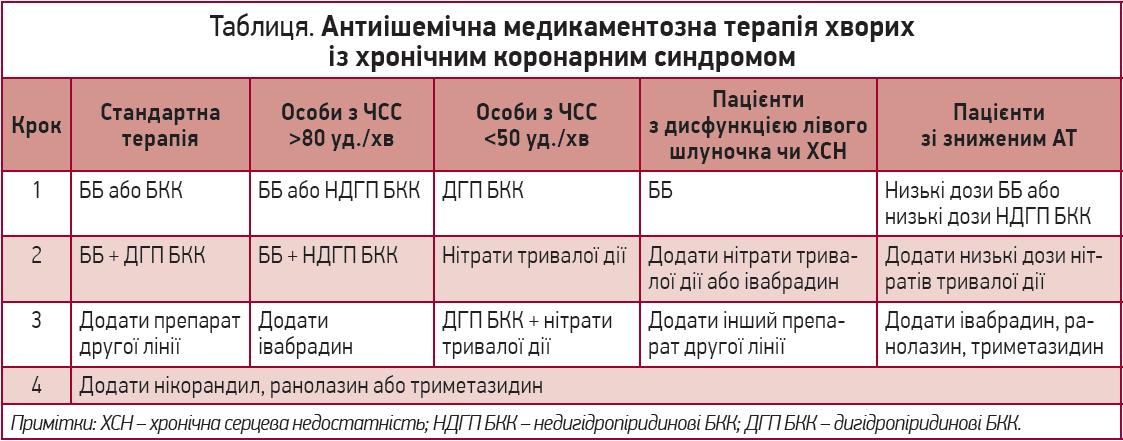
Тривала антиішемічна медикаментозна терапія хворих із хронічним коронарним синдромом, стенокардією та/або задишкою передбачає застосування β-блокаторів (ББ) і блокаторів кальцієвих каналів (БКК). При низькій частоті серцевих скорочень (ЧСС) застосовуються дигідропіридинові БКК, а при високій – недигідропіридинові (табл.). У разі неефективності монотерапії призначаються комбінації цих класів препаратів, згодом додаються нітрати тривалої дії, івабрадин, ранолазин або триметазидин. Рекомендації Європейського товариства кардіологів із діагностики та лікування хронічних коронарних синдромів (2019) вказують, що нікорандил, ранолазин, івабрадин і триметазидин необхідно розглядати як лікування другої лінії для зниження частоти стенокардії та покращення переносимості фізичних навантажень у пацієнтів із непереносимістю лікування ББ, БКК і нітратами тривалої дії чи протипоказаннями до їх застосування, а також у хворих, у яких не вдається контролювати симптоми за допомогою зазначених препаратів.
Дані наукових робіт вказують на те, що довготривалі результати адекватно підібраної медикаментозної терапії ІХС мало відрізняються від результатів хірургічної реваскуляризації. Найпоказовішим є дослідження СОURAGE, в якому порівнювали ефективність двох сучасних стратегій терапії пацієнтів зі стабільною ІХС – агресивне медикаментозне лікування та черезшкірне коронарне втручання (ЧКВ). Пацієнти були рандомізовані на дві групи лікування: ЧКВ з імплантацією стентів у поєднанні з медикаментозною терапією (n=1149); лише медикаментозна терапія (n=1138). За 4,6 року спостереження частота первинних подій становила 19,0% у групі ЧКВ і 18,5% у групі медикаментозної терапії (р=0,62). Отже, ЧКВ як початкова стратегія у хворих на стабільну ІХС не зменшує ризику смерті, інфаркту міокарда чи серцево-судинних подій у порівнянні з медикаментозною терапією.
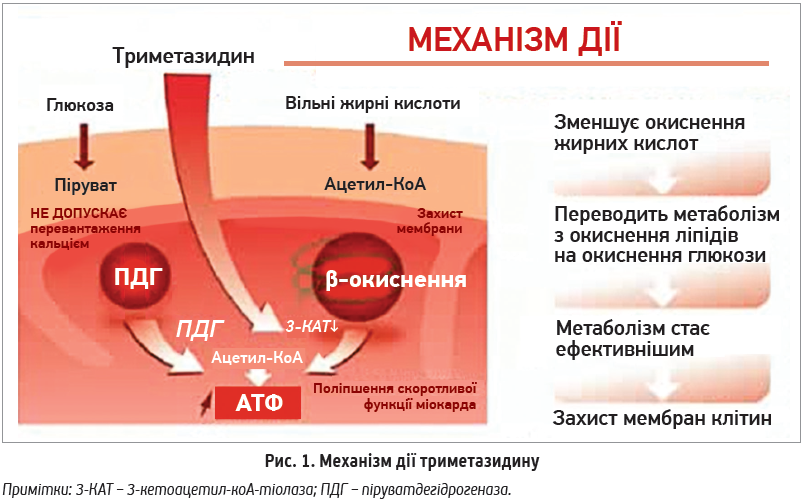
Триметазидин (Карметадин) вказаний як препарат другої лінії терапії стабільної стенокардії в рекомендаціях Товариства кардіологів України та є єдиним цитопротектором, рекомендованим вітчизняним протоколом лікування ІХС, стабільної стенокардії напруження І-ІІ функціональних класів. Триметазидин інгібує 3-кетоацетил-коА-тіолазу – ключовий фермент β-окиснення жирних кислот, а також підвищує активність піруватдегідрогенази – ключового ферменту окиснення глюкози. У результаті цих процесів відбувається своєрідне метаболічне перемикання, що полягає в зниженні використання ліпідних субстратів для вироблення АТФ і збільшенні утилізації глюкози. У зв’язку з пригніченням метаболізму жирних кислот триметазидин підвищує толерантність клітин до ішемії (рис. 1). Ефекти триметазидину в кардіоміоцитах включають зниження апоптозу, модуляцію автофагії та підтримання належного енергетичного балансу (Shu H. et al., 2021).
Триметазидин добре вивчений у різних клінічних дослідженнях. У метааналізі 11 досліджень за участю 1611 пацієнтів, проведеному А.Н. Behzadi та співавт., навіть показано, що прийом триметазидину після реваскуляризації зменшує ризик контраст-індукованої нефропатії у пацієнтів із нирковою недостатністю, яким проводяться коронарна ангіографія й ангіопластика. На тлі вживання триметазидину нефропатія розвивалася лише в 6,6% пацієнтів, а на тлі стандартної терапії – у 20% (Behzadi A. H. et al., 2021).
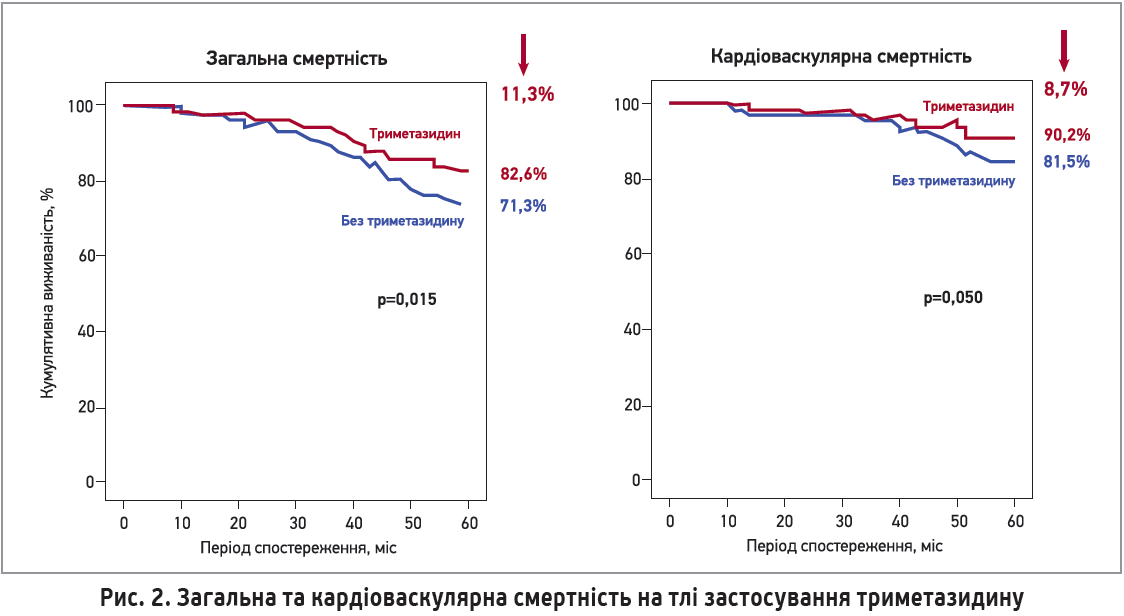
Міжнародне багатоцентрове ретроспективне дослідження G. Fragasso та співавт. (2013), яке включало дані 669 пацієнтів, виявило, що часткове пригнічення окиснення жирних кислот за допомогою триметазидину дозволяє достовірно зменшити загальну та кардіоваскулярну смертність у хворих із серцевою недостатністю: на 11,3 та 8,7% відповідно (рис. 2). Частота госпіталізацій із приводу ССЗ на тлі призначення триметазидину знизилася на 10,4% за 5 років, а період виживаності без стаціонарного лікування зріс до 7,8 міс.
Метааналіз S. Peng і співавт. (2014), який включав 13 досліджень за участю 1628 пацієнтів, встановив, що застосування триметазидину дозволяє достовірно зменшити кількість нападів стенокардії на тиждень, скоротити потребу в нітрогліцерині, подовжити час навантаження до розвитку депресії сегмента ST на 1 мм і збільшити сумарну толерантність до фізичних навантажень порівняно зі стандартною терапією.
За даними експериментальних досліджень, призначення триметазидину зменшує прояви діабетичної кардіоміопатії за рахунок зменшення фіброзу й апоптозу та підсилення автофагії. Ці сприятливі наслідки супроводжувалися покращенням діастолічної функції лівого шлуночка (Zhang L. et al., 2016). Триметазидин сприятливо впливає на життєздатність клітини та запобігає ушкодженню й гіпертрофії кардіоміоцитів у моделі ішемії в щурів, модулюючи гомеостаз кальцію (Wei J. et al., 2015).
Триметазидин чинить сприятливий вплив і при неалкогольній жировій хворобі печінки за рахунок впливу на ліпогенез і зменшення стеатозу (Zhang Y. et al., 2018). Отже, триметазидин є не лише кардіопротектором, а й гепатопротектором. На фармацевтичному ринку України триметазидин представлений, зокрема, препаратом Карметадин (World Medicine, Туреччина), який зарекомендував себе як якісний, ефективний і безпечний лікарський засіб.
Загалом клінічні ефекти Карметадину включають:
- зменшення кількості нападів стенокардії;
- посилення ефективності антиангінальних препаратів гемодинамічного ряду;
- поліпшення скоротливості міокарда в умовах його ішемічної дисфункції;
- зменшення вираженості клінічних проявів серцевої недостатності;
- збільшення толерантності до фізичного навантаження;
- відновлення скоротливості гібернованих ділянок міокарда;
- підвищення якості життя пацієнтів.
Додатковою перевагою є відсутність впливу на центральну гемодинаміку (ЧСС, перед- і постнавантаження, коронарний кровоток).
Рекомендована доза Карметадину становить 35 мг (1 таблетка) 2 р/добу вранці та ввечері під час їжі. Для пацієнтів із помірною нирковою недостатністю рекомендована доза становить 1 таблетку 1 р/добу вранці під час сніданку.
Підготувала Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 8 (501), 2021 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....