Значення скринінгових програм та раннього початку патогенетичної терапії в забезпеченні кращого прогнозу для пацієнтів зі спінальною м’язовою атрофією
 Спінальна м’язова атрофія (СМА) – це рідкісне (орфанне) захворювання, пов’язане з дегенерацією мотонейронів переднього рогу спинного мозку, що призводить до атрофії та слабкості м’язів тулуба і кінцівок. На жаль, сьогодні скринінг СМА не проводиться у багатьох країнах світу, що зумовлює відтермінування початку патогенетичного лікування і зростання ризику інвалідизації та ранньої смертності серед новонароджених і дітей раннього віку. Несвоєчасне виявлення захворювання призводить до його прогресування та збільшення кількості тяжких випадків, які гірше піддаються лікуванню. Ранній скринінг та початок терапії в рамках спеціалізованих референтних центрів за участю команди мультидисциплінарних фахівців є однією з важливих умов продовження тривалості та покращення якості життя хворих на СМА.
Спінальна м’язова атрофія (СМА) – це рідкісне (орфанне) захворювання, пов’язане з дегенерацією мотонейронів переднього рогу спинного мозку, що призводить до атрофії та слабкості м’язів тулуба і кінцівок. На жаль, сьогодні скринінг СМА не проводиться у багатьох країнах світу, що зумовлює відтермінування початку патогенетичного лікування і зростання ризику інвалідизації та ранньої смертності серед новонароджених і дітей раннього віку. Несвоєчасне виявлення захворювання призводить до його прогресування та збільшення кількості тяжких випадків, які гірше піддаються лікуванню. Ранній скринінг та початок терапії в рамках спеціалізованих референтних центрів за участю команди мультидисциплінарних фахівців є однією з важливих умов продовження тривалості та покращення якості життя хворих на СМА.
СМА – це хвороба з аутосомно-рецесивним типом успадкування. Ураження моторного нейрона переднього рогу спинного мозку виникає через зниження синтезу протеїну виживання мотонейронів (survival of motor neuron, SMN) через мутації в гені SMN, внаслідок чого у дітей може розвиватися тяжка гіпотонія м’язів та сколіоз, що призводить до інвалідизації та ранньої смерті (U.R. Monani et al., 2000; T.W. Prior et al., 2016).
Ведення хворих на СМА потребує належної співпраці між батьками дитини та лікарями, розроблення чіткого маршруту пацієнта в умовах референтного центру задля полегшення роботи медичного персоналу при прийомі хворих, особливо у критичному стані, які потребують невідкладної медичної допомоги. Крім того, в референтному центрі зберігається база даних пацієнтів із СМА, що дозволяє лікарям швидко обрати правильну тактику лікування у критичних ситуаціях, беручи до уваги дані анамнезу захворювання, результати лабораторних та інструментальних досліджень, які були проведені раніше. При перебуванні у референтному центрі дитина знаходиться під пильним наглядом спеціалістів, які за необхідності можуть залучати мультидисциплінарну команду для спільного обговорення спірних питань тактики ведення пацієнтів. Необхідна корекція лікування та відповідні рекомендації надаються лікарями після виписки хворого з центру. Крім того, фахівці клініки можуть запропонувати пацієнтам участь у клінічних дослідженнях, що може сприяти полегшенню загального стану хворого, продовженню тривалості ремісії без потреби у додаткових фінансових витратах з боку пацієнта та його сім’ї.
Перед стартом лікування лікарі повинні розповісти хворому чи батькам пацієнта про захворювання СМА та його наслідки, про методи та цілі терапії, про необхідність проведення люмбальної пункції для подальшого інтратекального введення сучасного хворобомодифікуючого лікарського засобу, що дозволить забезпечити кращий ефект лікування, ніж при його внутрішньовенному введенні, а також про можливі ускладнення під час лікування. Підвищення обізнаності батьків (опікунів) пацієнта щодо хвороби сприятиме налагодженню контакту між лікарем та пацієнтом, формуванню довіри до медичного персоналу референтного центру.
СМА – захворювання невиліковне, тому основною метою терапії є сповільнення прогресування хвороби, зменшення вираженості рухових функціональних обмежень та запобігання розвитку ускладнень, які негативно впливають на повсякденну життєдіяльність пацієнта. З цією метою було розроблено сучасний хворобомодифікуючий лікарський засіб Спінраза (діюча речовина – нусінерсен), вводити який потрібно інтратекально, що вимагає попереднього забору спинномозкової рідини шляхом люмбальної пункції в об’ємі, еквівалентному об’єму препарату, що вводиться. Перед проведенням люмбальної пункції слід забезпечити належну гідратацію пацієнта з подальшою премедикацію. Для локальної анестезії застосовують лідокаїн, щоб зменшити біль та його вплив як стресового фактора на діяльність наднирників, що може призвести до виділення катехоламінів та появи небажаних ефектів під час лікування. Згодом вводять мідазолам у дозі 0,3 мг/кг болюсно (максимальна доза 10 мг) та ескетамін по 0,1 (0,1-0,3) мг/кг болюсно (з можливим підвищенням дози лікарського засобу до 50 мг за потреби). При поєднаному застосуванні мідазоламу та ескетаміну можна досягти більш контрольованого знеболення, ніж при використанні лише ескетаміну. Перед початком введення рідини у спинномозковий канал варто провести забір ліквору, а потім повільно вводити той же об’єм лікарського засобу, який було забрано раніше. Струминне введення рідини у спинномозковий канал протипоказане. Вищезазначена особливість введення лікарського засобу у спинномозковий канал зумовлена високою ймовірністю швидкого виникнення гіпертензії у лікворній системі, що може призвести до небажаних наслідків.
Часто проведення люмбальної пункції у хворих на СМА ускладнюється через виражений сколіоз та зміщення анатомічних орієнтирів пункції. Таким пацієнтам (і дорослим, і дітям) проводять відповідні заміри та визначають місце пункції, яке відмічають позначками на тілі. Іншим важливим моментом, який слід враховувати при проведенні люмбальної пункції, є панічні атаки, що можуть виникнути перед початком маніпуляції, тому важливо забезпечити хворому відповідний психологічний комфорт.
Після проведення люмбальної пункції хворий повинен лежати на животі. Йому призначають аналгетики (парацетамол, ібупрофен, метамізол), внутрішньовенне введення NaCl та глюкози і відпочинок до кінця поточного дня.
Перед проведенням лікування варто також провести психологічну підготовку пацієнта, пояснивши хворому чи батькам дитини те, що ефект від лікування може стати помітним не одразу, а через певний проміжок часу.
Одним із досягнень у лікуванні СМА стала поява на фармацевтичному ринку України препарату Спінраза фармацевтичної компанії «Янссен», дія якого спрямована на збільшення продукції білка SMN. Застосування цього лікарського засобу полегшує перебіг СМА та уповільнює прогресування захворювання завдяки забезпеченню захисту мотонейронів переднього рогу від подальшого руйнування та атрофії, що дозволяє продовжити тривалість періоду ремісії (C.A. Chiriboga et al., 2016).
Ефективність та безпеку нусінерсену вивчали в одному з проспективних досліджень, що проводилося в Словенії та Чехії за участю 61 пацієнта віком від 2 місяців до 19 років. За станом усіх учасників спостерігали протягом 14 місяців, при цьому контрольна оцінка проводилася перед початком лікування, через 6 міс (після 5-го інтратекального введення препарату) та 14 міс (після введення 7 доз лікарського засобу). Результати дослідження свідчать про те, що лікування нусінерсеном було ефективним незалежно від типу СМА. Після 14-місячного лікування у пацієнтів із СМА типу I (p=0,002) та типу II (p=0,002) відмічалося достовірне покращення моторних функцій, у той час як у пацієнтів із СМА III типу спостерігалася тенденція до позитивних змін (p=0,051). У дітей загальний бал за моторною шкалою був вищим у хворих на СМА II типу, ніж I типу, що свідчить про дещо вищу ефективність лікування хворих із СМА I типу.
Кращі результати лікування відмічалися у пацієнтів молодшого віку. Було встановлено наявність взаємозв’язку між раннім початком лікування та покращенням моторних функцій після 14-місячного лікування при СМА I типу, в той час як при II та III типах такої тенденції не виявлено (рис.).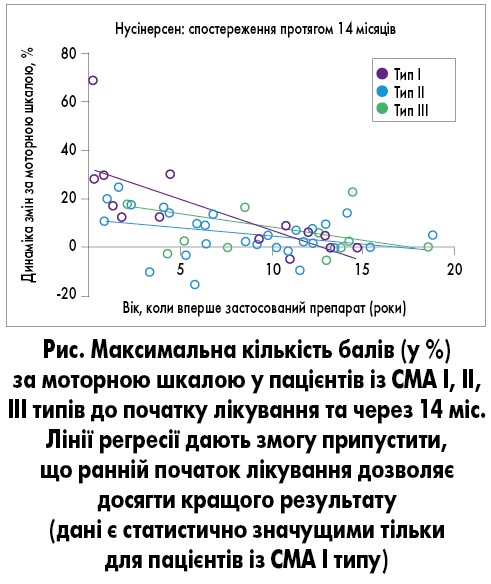
Крім того, дослідження показано, що при наявності більшої кількості копій SMN2 відмічалося більш виражене покращення моторних функцій. Проте в окремих хворих старшого віку на пізній стадії захворювання теж спостерігалися переваги від проведеного лікування.
У дослідженні також вивчалася безпека застосування нусінерсену. Мінімальні побічні ефекти були присутні у 24 пацієнтів з 61 (приблизно у 40%) та були пов’язані з такими скаргами: 10 хворих скаржилися на біль у поперековому відділі хребта, 8 – на головний біль, 4 – на витік цереброспінальної рідини, 4 – блювання, 2 – підвищену дратівливість, 1 – висип у місці пункції та 1 – на парестезію ніг. Варто зазначити, що після люмбальної пункції хворі з витоком спинномозкової рідини не могли лежати на животі через сколіоз, тому їм підкладали під хребет подушку. В цілому не спостерігалося серйозних побічних реакцій, які б змусили хворих припинити лікування (D. Osredkar et al., 2020).
Під час лікування необхідно проводити монітинг загального стану пацієнта, оцінку моторних функцій з належною фото- та відеореєстрацією для кращого розуміння динаміки (прогресування чи регресування) симптомів захворювання.
Невід’ємною складовою покращення лікування хворих на СМА є співпраця з іншими референтними центрами та участь у клінічних дослідженнях, що у майбутньому дозволить підвищити ефективність лікування цієї групи пацієнтів. Сьогодні скринінг СМА та його лікування доступні не в усіх країнах, тому слід розширювати діяльність референтних центрів задля ранньої діагностики захворювання, що дозволить швидше розпочати лікування та досягти більш вираженого покращення моторних функцій, ніж при зверненні на пізніх стадіях.
Розвиток медицини відбувається досить стрімко, завдяки чому у лікарів з’явилася можливість застосовувати сучасні лікарські засоби для лікування пацієнтів із СМА, що сприяє стабілізації та покращенню клінічного перебігу хвороби. Однак варто пам’ятати про значення своєчасної діагностики захворювання, що дозволить почати терапію препаратом Спінраза на ранніх термінах, у той час як відтермінування лікування дає гірші результати. СМА є невиліковним захворюванням, однак з розвитком науки та ретельним вивченням нових лікарських засобів у серії клінічних досліджень, можливо, з часом вдасться забезпечити хворим належну якість життя та подовжити його тривалість.
 Пам’ятка для лікаря
Пам’ятка для лікаря
Ознаки СМА: на що звертати увагу
Захворювання починається з м’язової слабкості та загальної втрати сил.
Де (ким) може бути виявлений пацієнт із підозрою на СМА?
- Новонароджені: під наглядом неонатолога у пологовому відділенні.
- Немовлята: під наглядом педіатра, сімейного лікаря у Центрі надання первинної медико-санітарної допомоги (поліклініці).
- Діти до 18 років та дорослі: у ЦПМСД (поліклініці), консультативній поліклініці спеціалізованого науково-дослідного інституту, на прийомі у сімейного лікаря.
Дії спеціаліста, що встановив можливі ознаки СМА
(рекомендовані для захисту інтересів пацієнта)
Організувати відправку зразка крові пацієнта до діагностичної ДНК-лабораторії (або надати батькам інформацію, де це можна зробити).
У випадку підтвердження діагнозу СМА
- Направити пацієнта на консультацію до експерта зі СМА.
- Направити пацієнта на лікарську кваліфікаційну комісію у ЦПМСД для оформлення документів, що пов’язані з соціальним захистом осіб з інвалідністю.
- Надати інформацію про пацієнтські, громадські організації для самостійної реєстрації в реєстрі пацієнтів із СМА.
CP-249227
Тематичний номер «Педіатрія» № 3 (59) 2021 р.
СТАТТІ ЗА ТЕМОЮ Педіатрія
Вроджена дисфункція кори надниркових залоз (ВДКНЗ) – це захворювання з автосомно-рецесивним типом успадкування, в основі якого лежить дефект чи дефіцит ферментів або транспортних білків, що беруть участь у біосинтезі кортизолу. Рання діагностика і початок лікування пацієнтів з ВДКНЗ сприяє покращенню показників виживаності та якості життя пацієнтів....
Алергічний риніт (АР) є поширеним запальним захворюванням верхніх дихальних шляхів (ВДШ), особливо серед педіатричних пацієнтів. Ця патологія може знижувати якість життя, погіршувати сон та щоденну продуктивність. Метою наведеного огляду є надання оновленої інформації щодо епідеміології АР та його діагностики, з урахуванням зв’язку з бронхіальною астмою (БА). ...
Американська академія педіатрії (AAP) оновила рекомендації щодо контролю грипу серед дитячого населення під час сезону 2023-2024 рр. Згідно з оновленим керівництвом, для профілактики та лікування грипу в дітей необхідно проводити планову вакцинацію з 6-місячного віку, а також своєчасно застосовувати противірусні препарати за наявності показань. ...
Поширеність і вплив алергічних захворювань часто недооцінюють [1]. Ключовим фактором алергічної відповіді є імуноглобулін (Ig) Е, присутній на поверхні тучних клітин і базофілів. Взаємодія алергену з IgЕ та його рецепторним комплексом призводить до активації цих клітин і вивільнення речовин, у тому числі гістаміну, які викликають симптоми алергії [2]. Враховуючи ключову роль гістаміну в розвитку алергічних реакцій, при багатьох алергічних станах, включаючи алергічний риніт і кропив’янку, пацієнту призначають антигістамінні препарати [3, 4]....




