Стратегія персоніфікованої терапії для пацієнтів із ревматичними захворюваннями
Ревматичні хвороби займають вагоме місце у структурі соматичних патологій у пацієнтів різного віку та є однією з найбільш значущих медичних проблем. Тривалий перебіг і високий ступінь інвалідизації суттєво знижують якість життя хворих. Стрімкий розвиток медицини вимагає від клініциста тримати руку на пульсі новітніх технологій діагностики й терапії ревматичних захворювань. У межах VIII Національного конгресу ревматологів України, що відбувся цьогоріч у жовтні, фахівці Всеукраїнської асоціації ревматологів України сумісно із представниками Європейського альянсу асоціацій ревматологів (EULAR) обговорювали актуальні новини ревматології та шляхи імплементації досягнень світової науки у практику вітчизняних лікарів.
Оптимальний вибір підходу до лікування ревматичних захворювань
Про оптимальний вибір стратегії терапії для осіб із ревматичними захворюваннями та місце інгібіторів фактора некрозу пухлин α (ФНП-α) у практиці ревматолога розповіли лікар-ревматолог вищої категорії, керівник Клініки сучасної ревматології (м. Запоріжжя), д. мед. н., професор Дмитро Геннадійович Рекалов та головна позаштатна ревматологиня КНП ХОР «Обласна клінічна лікарня» (м. Харків), к. мед. н., доцентка Світлана Анатоліївна Трипілка.
та головна позаштатна ревматологиня КНП ХОР «Обласна клінічна лікарня» (м. Харків), к. мед. н., доцентка Світлана Анатоліївна Трипілка.
За словами Д.Г. Рекалова, розвиток імунології, впровадження нових технологій та імунобіологічних підходів терапії спонукає до появи нового погляду на лікування ревматичних патологій.
Згідно із класифікаційною оцінкою Міжнародного товариства з дослідження спондилоартриту (ASAS), критеріями для встановлення діагнозу аксіального спондилоартриту (СпА) є скарги на хронічний біль у спині впродовж більш ніж трьох місяців у пацієнтів віком ≤45 років із наявним сакроілеїтом при візуалізації та ≥1 ознакою СпА або ж позитивним результатом дослідження на ген HLA-B27 і ≥2 ознаками СпА.
До ознак СпА відносять наступні:
- запальний біль у спині;
- периферичний артрит;
- дактиліт;
- ентезит;
- сімейний анамнез СпА;
- позитивна відповідь на терапію нестероїдними протизапальними препаратами (НПЗП);
- увеїт;
- псоріаз;
- неспецифічні захворювання кишечника (хвороба Крона, неспецифічний виразковий коліт);
- підтвердження гена HLA-B27;
- підвищення рівня С-реактивного білка.
Наявний сакроілеїт визначають як достовірне рентгенографічне підтвердження відповідно до модифікованих нью-йоркських діагностичних критеріїв або ознак активного сакроілеїту на магнітно-резонансній томографії (Rudwaleit et al., 2009).
Незважаючи на наявні рекомендації для клініцистів, шлях хворого на аксіальний СпА від сімейного лікаря до ревматолога часто суттєво затримується, і діагноз встановлюється із запізненням. Зокрема, у США відстрочення становить близько 14 років, Німеччині – 6 років (Danve, Redeker, 2019). Тому кожен молодий дорослий із хронічним болем у спині та ознаками запалення має прицільно розглядатися лікарем будь-якого фаху як пацієнт із підозрою на аксіальний СпА.
Головна мета лікування осіб зі СпА – це зниження запальної активності, що відображається у зменшенні клінічної симптоматики та позитивній динаміці лабораторних показників, і запобігання ураженню аксіального скелета. Терапевтичними мішенями вважаються неактивна хвороба, що відповідає індексу активності СпА (ASDAS) <1,3, або низький ступінь активності за ASDAS <2,1 (Smolen et al., 2020). При ранньому початку лікування 35% хворих, що мали симптоми довше ніж три роки, досягають часткової ремісії (Poddubnyy, 2020).
Пацієнти з нерентгенологічним та рентгенологічним аксіальним СпА мають подібні характеристики, як-от:
- Якість життя, пов’язана зі здоров’ям, за опитувальником якості життя щодо психічного здоров’я (SF‑36 MCS).
- Виявлення екстра-артикулярних симптомів та периферичних проявів.
- Подібність змін оцінки відповідно до батського індексу активності анкілозивного СпА (BASDAI) та рівня болю за шкалою загальної оцінки пацієнта (PGA).
В обох випадках призначення ефективної протизапальної терапії впливає на швидку нормалізацію об’єктивних показників та симптомів (Lopez-Medina et al., 2019).
За оновленою настановою Американської колегії ревматологів (ACR, 2019), при активній хворобі у разі неефективності НПЗП та фізіотерапії необхідно розглянути можливість призначення біологічної терапії: інгібіторів ФНП-α або інтерлейкіну‑17 (ІЛ‑17).
Для використання у країнах Європи схвалені наступні біологічні агенти для лікування рентгенологічного аксіального СпА:
- із групи інгібіторів ФНП-α – етанерцепт, інфліксимаб, адалімумаб, голімумаб;
- із групи інгібіторів ІЛ‑17 – секукінумаб, іксекізумаб.
Зазначені препарати, крім інфліксимабу, також затверджені для терапії нерентгенологічного аксілярного СпА (Poddubnyy, 2020).
Доцільно зазначити, що лікування біологічними препаратами дозволяє досягти короткострокового контролю над симптоматикою та запаленням, що у довготривалій перспективі приводить до запобігання структурного ушкодження хребта, іліосакральних суглобів та обмеження функцій. При рентгенологічному й нерентгенологічному аксілярному СпА застосування інгібіторів ФНП-α та ІЛ‑17 дозволяє досягти 40% поліпшення симптомів (згідно з ASAS).
У дослідженні ESTER оцінювали довгострокову клінічну ефективність етанерцепту, який почали застосовувати на ранніх етапах аксілярного СпА. Протягом 10 років спостереження було відзначено стійку клінічну відповідь у пацієнтів із рентгенологічним та нерентгенологічним аксіальним СпА. Етанерцепт добре переносився протягом усього періоду лікування і демонстрував хороший профіль безпеки без нових несприятливих явищ (Proft et al., 2021).
На фармацевтичному ринку України етанерцепт доступний у вигляді препарату Енбрел® виробництва компанії «Пфайзер».
Широке впровадження BASDAI та ASDAS обґрунтовує для лікарів-практиків передумови щодо заміни НПЗП на імунобіологічні препарати. Перехід на біологічні засоби необхідний, якщо у хворого підтверджено HLA-B27, і не було досягнуто мети лікування (відсутність клінічних симптомів, неактивне захворювання або низька активність). Парціальне дозування НПЗП не здатне контролювати хворобу чи симптоматику. Призначення НПЗП у повній дозі може бути ефективнішим, але асоційоване з побічними реакціями, тому доцільно застосовувати комбінацію останніх із біологічним препаратом (Poddubnyy, 2020).
Для підтвердження практичної ефективності рекомендацій пропонуємо до уваги читачів клінічний кейс із доповіді Дмитра Геннадійовича.
Клінічний випадок
Пацієнт, 25 років, протягом останніх трьох років відзначає біль у сідницях вночі, що триває більш ніж шість тижнів; вправи та фізична активність вагомо не впливають на симптоматику.
Перебіг хвороби. На ранніх етапах захворювання приймання НПЗП дозволяло полегшити біль на 90‑100%. Пацієнт був оглянутий сімейним лікарем, ортопедом, неврологом, фізіотерапевтом. За результатами рентгенографії кульшових суглобів, змін не виявлено. Отримував терапію НПЗП та ін’єкцію в ахіллове сухожилля.
Обстеження. За результатами лабораторного обстеження виявлене підвищення запальних показників: індекси ASDAS – 2,1 та BASDAI – 5,5, підтверджений HLA-B27. Після консультації ревматолога було проведено магнітно-резонансну томографію кульшових суглобів – зафіксовано білатеральний набряк кісткового мозку, порушення кортикального шару із субхондральними ерозіями; підозра на двобічний сакроілеїт. Враховуючи клінічні ознаки та результати обстежень, підтверджено діагноз нерентгенологічного аксіального СпА.
Терапія. Призначено НПЗП у повній дозі (75 мг диклофенаку двічі на добу), що на початку було пов’язано із хорошою відповіддю хворого. Перебіг захворювання ускладнився абдомінальним болем та прогресувальною втратою ваги, що лікарі розцінили як прояв побічних явищ при використанні НПЗП.
Стратегію лікування було змінено: призначено етанерцепт у дозі 50 мг/тиждень. У динаміці пацієнт відзначає поліпшення симптоматики, згідно з даними обстеження – зменшення запального стану, оцінки за ASDAS – 1,2 і BASDAI – 2.
***
Модифікацію поглядів на терапію ревматичних захворювань через власний клінічний досвід спостерігала Світлана Анатоліївна. За її словами, починаючи від 30-х рр. минулого століття і дотепер відбулися (р)еволюційні зміни у підходах до лікування ревматичних патологій. Новим етапом стало використання імунобіологічної терапії, зокрема, етанерцепт був першим препаратом, що увійшов у практику лікарів.
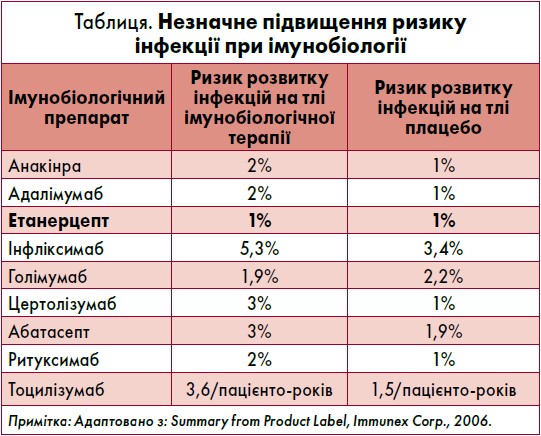
За даними ACR, ефективність імунобіологічних препаратів відзначено у лікуванні ревматоїдного (РА), псоріатичного (ПсА) та ювенільного ідіопатичного артриту, аксілярного СпА, псоріазу, хвороби Крона, виразкового коліту, системного червоного вовчака та інших захворювань (Burmester, 2020). Загальними протипоказаннями для призначення біологічних хворобомодифікувальних антиревматичних препаратів (бХМАРП) є індивідуальна непереносимість, активний інфекційний процес, поточна онкологічна або демієлінізувальна патологія, інтерстиційне захворювання легень, виразна серцева недостатність, вагітність і лактація, вікові обмеження. Слід зауважити, що існує дещо підвищений інфекційний ризик при застосуванні імунобіологічної терапії. Важливо, що цей показник не відрізняється порівняно із плацебо тільки для етанерцепту (1% на 100 пацієнто-років) (таблиця).
На сьогодні актуальною для України є проблема туберкульозу (ТБ) як опортуністичної інфекції у пацієнтів із ревматичною патологією. Перед лікарем постає питання вибору оптимальної стратегії терапії. В цьому контексті необхідно пам’ятати про важливу роль ФНП у патогенезі формування гранульоми. Слід зазначити, що застосування інгібітора ФНП-α етанерцепту супроводжується нижчим ризиком виникнення туберкульозу порівняно з іншими імунобіологічними препаратами, зокрема адалімумабом та інфліксимабом (Scott, 2014; Desai et al., 2018; van Dartel et al., 2013).
Як зауважила С.А. Трипілка, практичним алгоритмом обстеження пацієнтів перед призначенням імуносупресивної терапії та лікування латентної форми ТБ є затверджений МОЗ наказ від 04.04.2014 р. № 620. Для хворих, у яких підтверджено латентний ТБ, застосування біологічних засобів може бути розпочате або відновлене через один місяць лікування ТБ за допомогою протитуберкульозних препаратів за схемою: приймання ізоніазиду протягом дев’яти місяців, або ізоніазиду в комбінації з рифампіцином три місяці, або монотерапія рифампіцином упродовж чотирьох місяців. Особи із латентним ТБ, які мають позитивні показники на початку лікування, можуть залишатися «позитивними» до цих тестів навіть після успішної профілактичної терапії ТБ. Для цієї групи хворих необхідний ретельний моніторинг клінічних ознак і симптомів активного ТБ, оскільки повторення шкірної проби або КВФ-тест не допоможуть при діагностиці реактивації ТБ.
Як було зазначено, лідером з інфекційної безпеки серед біологічних препаратів є етанерцепт, тому Енбрел® може бути варіантом вибору при лікуванні ревматологічного захворювання на тлі латентного ТБ. Для порівняння: моноклональні антитіла проти ФНП викликають реактивацію ТБ у 3‑4 рази частіше, ніж етанерцепт.
Іншими проблемами, що можуть спіткати лікаря, є втрата ефективності лікування та вторинна імуногенність. Необхідно пам’ятати про можливий регрес протягом 2‑6 місяців від початку терапії та для попередження цього призначати комбінації біологічних і синтетичних ХМАРП (Grith et al., 2015).
Також важливим для хворих є питання відміни інгібіторів ФНП-α після досягнення ремісії. Вибір стратегії лікування має бути персоніфікованим.
Енбрел® доступний у лікарській формі розчину для ін’єкцій: 1 попередньо наповнений шприц містить 25 або 50 мг етанерцепту; 1 попередньо наповнена ручка містить 50 мг етанерцепту. Такі форми випуску є зручними як для хворих, так і лікарів.
Енбрел® рекомендований для лікування активного РА від помірного до тяжкого ступеня в комбінації з метотрексатом або у вигляді монотерапії, ювенільного ідіопатичного артриту в дітей та підлітків віком від 2 років, прогресуючого ПсА в дорослих у разі недостатньої відповіді на базові протиревматичні засоби, аксіального СпА. Крім того, препарат застосовують у дорослих пацієнтів із тяжким активним анкілозивним спондилітом за недостатньої ефективності традиційного лікування, дорослих із тяжкою стадією нерентгенологічного аксіального СпА з об’єктивними симптомами запалення, на що вказує підвищений рівень С-реактивного білка та/або результати МРТ, які мають недостатню відповідь на нестероїдні протизапальні препарати (НПЗП), а також для терапії бляшкового псоріазу в дорослих і дітей із 6 років.
Клінічний досвід ведення молодої пацієнтки з РА та застосування імунобіологічної терапії при ревматичних патологіях під час пандемії COVID‑19
Завідувачка ревматологічного відділення № 2 КНП «Олександрівська клінічна лікарня м. Києва», к. мед. н. Тетяна Олександрівна Меффорд зазначила, що прийняття рішень при лікуванні РА потребує зваження його переваг і ризиків. Терапія має сповільнювати рентгенографічну прогресію, зменшувати симптоми, зберігати можливість планування сім’ї, підвищувати фізичну функцію та якість життя хворого. При виборі оптимального препарату необхідно звертати увагу на можливі побічні явища, коморбідність, режим уведення, вплив на спосіб життя, вартість терапії тощо. Тактика вибору лікування повинна базуватися на алгоритмах, рекомендованих АСR спільно з EULAR (2019).
зазначила, що прийняття рішень при лікуванні РА потребує зваження його переваг і ризиків. Терапія має сповільнювати рентгенографічну прогресію, зменшувати симптоми, зберігати можливість планування сім’ї, підвищувати фізичну функцію та якість життя хворого. При виборі оптимального препарату необхідно звертати увагу на можливі побічні явища, коморбідність, режим уведення, вплив на спосіб життя, вартість терапії тощо. Тактика вибору лікування повинна базуватися на алгоритмах, рекомендованих АСR спільно з EULAR (2019).
Для жінок із РА порівняно з такими без РА характерний коротший репродуктивний вік, вони частіше потребують лікування від безпліддя, довшого часу для настання вагітності та мають триваліші інтервали між вагітностями. Мультифакторна проблема з фертильністю зумовлена високою активністю захворювання і супутнім запаленням, наявним хронічним больовим синдромом, що сприяє інвалідизації, прийманням препаратів для лікування основного ревматичного захворювання, зниженням сексуальної активності, психологічними проблемами, віковими особливостями (Jawaheer et al., 2011; Wallenius et al., 2011).
Т.О. Меффорд поділилася клінічним досвідом ведення пацієнтки репродуктивного віку із РА.
Клінічний випадок
Пацієнтка, 31 рік, хворіє на РА протягом двох років, отримує метотрексат у дозі 15 мг/тиждень, планує вагітність.
Перебіг хвороби. За даними лабораторного обстеження, зберігаються високі показники ревматоїдного фактора, антитіл до циклічного цитрулінового пептиду і шкали активності РА (DAS28).
Терапія. Після консультації згідно з алгоритмом EULAR (2019) рекомендовано продовжити приймання 15 мг/тиждень метотрексату та почати терапію етанерцептом у дозі 50 мг/тиждень підшкірно із подальшим контролем через три місяці.
Згідно з результатами обстеження, через три місяці відзначене зниження показників за DAS28, що дозволило відмінити метотрексат і залишити монотерапію етанерцептом. Через 6 і 9 місяців від початку лікування рівень за DAS28 стабільний у межах показників, що відповідають ремісії. Пацієнтка продовжує отримувати етанерцепт по 50 мг/тиждень підшкірно.
***
На етапі планування вагітності необхідно визначити активність артриту та, зокрема, чи можливе використання поточної терапії під час вагітності, якщо ж ні – перевести на інше лікування. Під час вагітності терапію слід продовжувати, бажано з адаптацією до клінічної ситуації. Для лікування запальних артритів рекомендовані гідроксихлорохін, сульфасалазин, азатіоприн, інгібітори ФНП-α. Використання преднізолону можливе у дозі до 20 мг/добу. З обережністю застосовують ритуксимаб та НПЗП (обмежити у 3-му триместрі). Протипоказаний метотрексат через тератогений ефект.
У післяпологовому періоді рекомендовано повернутися до терапії, що була до вагітності. Пацієнтка не повинна робити вибір між власним комфортом та грудним вигодовуванням. Під час лактації можливе застосування гідроксихлорохіну, сульфасалазину, азатіоприну, колхіцину, НПЗП (ібупрофену), інгібіторів ФНП-α, ритуксимабу, тоцилізумабу, секукімумабу, циклоспорину, такролімусу, преднізолону в дозі не більш як 20 мг, у разі приймання преднізолону ˃20 мг необхідно відтермінувати годування на 4 год. Протипоказано призначати лефлуномід, циклофосфамід, мофетилу мікофенолат, метотрексат (Sammaritano et al., 2020).
В умовах пандемії COVID‑19 постає важливе питання співвідношення потенційної користі терапії ревматичного захворювання та ризику інфікування / тяжкого перебігу інфекції через імуносупресивний влив ліків. Необхідно обговорювати з кожним пацієнтом доцільність внесення змін у терапевтичний режим (доза, шлях, частота введення), що могло б зменшити кількість візитів до лікувальних закладів. Варто віддавати перевагу таким аспектам, як:
- використання засобів із коротшим періодом напіввиведення, як-от сульфасалазин, гідроксихлорохін, етанерцепт, інгібітори JAK;
- підшкірний шлях уведення для проведення терапії в домашніх умовах.
Лікар повинен оцінити доцільність початку біологічної терапії (ступінь активності захворювання, прогноз) та за можливості відтермінувати початок на 2‑3 місяці, адже ризик інфекційних ускладнень максимальний у перші 4‑6 місяців від початку лікування (NICE, BSR, 2020).
Розрахунок ризику серйозних інфекцій у пацієнтів із РА проводять з урахуванням таких факторів: віку (˃60 років), функціонального статусу, коморбідних станів (як-то хронічні захворювання нирок або легень), лікування глюкокортикоїдами, кількості ХМАРП, які були неефективними, попередніх серйозних інфекцій, терапії на момент обстеження інгібіторами ФНП-α або небіологічними ХМАРП (Strangfeld et al. 2011).
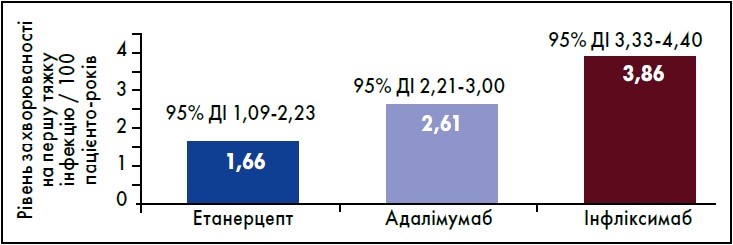
За даними біологічного реєстру DREAM, кількість хворих на РА, за якими велося спостереження протягом п’яти років, становила 2356 осіб. Рівень захворюваності на першу тяжку інфекцію був найнижчий на тлі приймання етанерцепту (1,66 на 100 пацієнто-років) порівняно з адалімумабом (2,61) та інфліксимабом (3,86) (рис. 1) (van Dartel et al., 2013).
Рис. 1. Ризик розвитку тяжких інфекцій та випадків припинення терапії через побічні явища за результатами реєстру DREAM
Адаптовано за van Dartel et al., 2013.
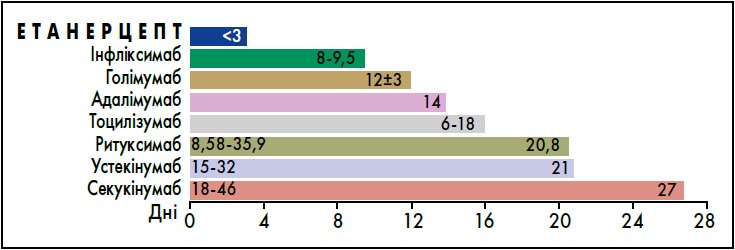
Завдяки короткому періоду напіввиведення (<3 днів), етанерцепт забезпечує швидке виведення препарату та, як наслідок, керованість терапії, що робить її гнучкою до індивідуальних потреб пацієнтів із ревматичними захворюваннями (Kerrigan, 2019). Тож Енбрел® посідає найвигіднішу позицію серед інших бХМАРП (рис. 2).
Рис. 2. Період напівиведення різних ХМАРП
Адаптовано за N. Kerrigan, 2019.
За словами лекторки, швидкий клінічний ефект на активність захворювання, функціональний статус та покращення рентгенологічних ознак є перевагами терапії інгібіторами ФНП-α. Серед інших можливостей – високодієва комбінація з метотрексатом, опція зменшення дози НПЗП і глюкокортикоїдів, ефективність при ранньому РА й довготривалому перебігу для пацієнтів без терапії ХМАРП або за неефективності/непереносимості багатьох ХМАРП, швидка відповідь на терапію, можливість використання при плануванні, під час вагітності та протягом періоду лактації, задовільна переносимість, але необхідність контролю інфекційних побічних реакцій (скринінг на туберкульоз, вакцинація, навчання пацієнта щодо можливого розвитку інфекційних явищ).
Особи з ревматичними захворюваннями, які отримують лікування інгібіторами ФНП-α, сульфасалазином, лефлуномідом, азатіоприном, циклофосфамідом, белімумабом, препаратами ІЛ, преднізолоном у дозі ˃20 мг/добу, не потребують зміни режиму дозування ліків або термінів проведення вакцинації проти COVID‑19 (ACR, 2021).
Стратегії персоніфікованого вибору лікування РА
Цікавим клінічним досвідом ведення пацієнтки із РА та стратегією персоніфікованого вибору терапії для хворих, які страждають на РА, поділилася старша наукова співробітниця відділу некоронарних хвороб серця, ревматології та терапії ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України (м. Київ), к. мед. н. Олена Олексіївна Гарміш.
Клінічний випадок
Пацієнтка, 32 роки, із 16 років страждає на РА. У лікуванні були використані всі можливості терапії синтетичними ХМАРП: хвора отримувала метотрексат, лефлуномід, сульфасалазин, метилпреднізолон.
В анамнезі. Гастродуоденальні ускладнення від терапії НПЗП. Пацієнтка 10 років тому за призначенням приймала ритуксимаб у загальній дозі 4500 мг протягом двох років, що сприяло ремісії патології та дозволило відмінити метилпреднізолон. У 2015 р. пацієнтка завагітніла і народила здорову дитину, період вагітності та лактації безмедикаментозний.
Терапія. У 2017 р. через загострення захворювання було призначено ритуксимаб, однак у зв’язку з інфузійною побічною реакцією на тлі лікування препарат відмінили та призначили метилпреднізолон. Після цього дві спроби введення ритуксимабу в дозі 1000 мг № 2 зі швидкістю 75 мл/год супроводжувалися інфузійною реакцією, що не дозволяло продовжувати його використання.
Подальший перебіг хвороби. У пацієнтки зберігається суглобовий синдром, переважно колінних та плечових суглобів, ранкова скутість упродовж 2 год. Варто зауважити, що після терапії ритуксимабом серед перших ознак повторного загострення процесу може бути підвищення запальних показників крові. За даними лабораторного обстеження, у хворої підвищені рівні швидкості осідання еритроцитів і С-реактивного білка.
Подальша тактика лікування. Враховуючи тривалий анамнез захворювання та неефективність терапії, перед лікарем постає питання вибору подальшої стратегії ведення пацієнтки. Серед індивідуальних вимог до препарату – можливість застосування монотерапії та відміни глюкокортикоїдів, швидкий/стабільний ефект лікування, досягнення ремісії та можливість майбутньої вагітності. Для виключення ймовірності повторної імунної реакції хворій було призначено інший клас препаратів, інгібітор JAK тофацитиніб.
***
На фармацевтичному ринку України тофацитиніб представлений препаратом Ксельянз виробництва компанії «Пфайзер». Результати численних досліджень клінічної ефективності тофацитинібу дозволяють виділити популяцію хворих, яким показане призначення препарату Ксельянз. Так, необхідна наявність таких критеріїв, як:
- дорослі пацієнти із РА, що характеризується середнім і тяжким ступенем активності;
- наявність непереносимості або недостатньої відповіді на метотрексат.
Важлива перевага тофацитинібу – швидкий протизапальний ефект (впродовж трьох діб із розвитком максимального ефекту до 3-го місяця), що зберігається до 96 місяців лікування. Клінічна ефективність тофацитинібу не залежить від попередньої терапії РА. За даними реєстрів HUMAN-TOR і HIRA Registry, через шість місяців від початку лікування пацієнтів, які раніше не отримували біологічні ХМАРП або не мали відповіді на їх застосування, клінічна ефективність тофацитинібу була в межах 94‑100% (Kim et al., 2019).
Як зауважила Олена Олексіївна, згідно з настановою ACR/EULAR (2019), інгібітори ФНП-α і JAK-інгібітори є однаково рекомендованими препаратами для лікування РА. Але JAK-інгібітори мають низку переваг при застосуванні (Strand, 2021):
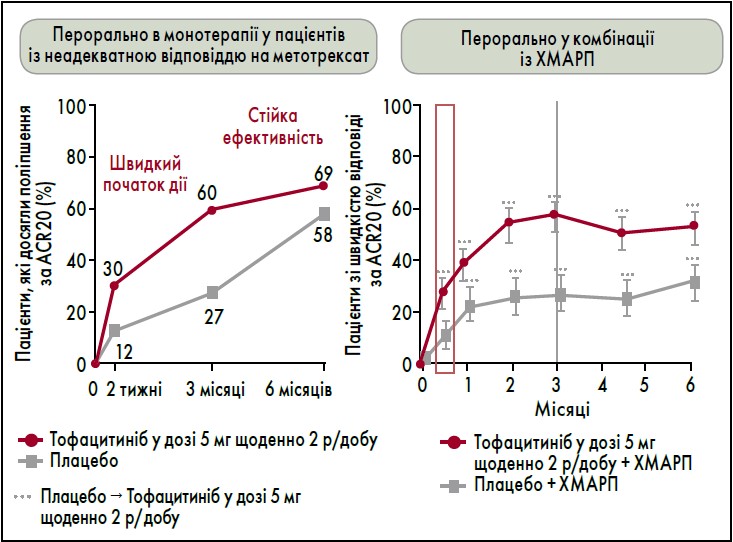
- Швидкий початок дії (рис. 3).
- Краща прихильність до терапії (78% пацієнтів продовжують терапію тофацитинібом через два роки від призначення і 51% – через п’ять років).
- Зручність застосування (Ксельянз представлений у таблетованій формі, застосування не залежить від приймання їжі).
Рис. 3. Швидкий протизапальний ефект тофацитинібу
Примітка: Адаптовано за V. Strand et al., 2015.
Завдяки тому, що період напіввиведення препарату Ксельянз становить приблизно 3 год, є можливість швидкого покращення стану хворих без побічних ефектів. Частота серйозних інфекцій при використанні JAK-інгібіторів становить 2,93 на 100 пацієнто-років, що є найнижчим показником серед ХМАРП і підтверджує прийнятний рівень безпеки їх застосування (Strand et al., 2015).
Підготувала Ольга Загора
Повний список літератури знаходиться в редакції
За підтримки представництва компанії
«Пфайзер Експорт Бі. Ві.» в Україні
PP-ENB-UKR-0025
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 1-2 (80-81) 2022 р.
СТАТТІ ЗА ТЕМОЮ Ревматологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....
Зв’язок між рівнем сироваткової сечової кислоти (ССК) і ризиком серцево-судинних захворювань (ССЗ) упродовж багатьох років є предметом вивчення дослідників. Установлено, що рівень ССК – незалежний предиктор смерті від усіх причин і серцево-судинної смерті, зокрема від гострого коронарного синдрому, інсульту та серцевої недостатності (СН). Також опубліковано багато робіт про зв’язок між ССК і функцією нирок. Попри значну кількість публікацій, деякі моменти, а саме: яким є оптимальний поріг ССК для визначення ризику ССЗ, чи необхідна корекція значень ССК для функції нирок, чи є ССК ключовим патологічним елементом метаболічної дисрегуляції, потребують прояснення....