Патофізіологія та класифікація нейрогенних дисфункцій нижніх сечових шляхів
У статті представлено фізіологічні основи акту сечовипускання; розглянуто причини іннервації нижніх сечових шляхів, включно із класифікацією та патофізіологією нейрогенних дисфункцій нижніх сечових шляхів; описано основні урологічні синдроми в нейроурології та неврологічні захворювання, які проявляються урологічними симптомами.
Ключові слова: нижні сечові шляхи; іннервація; класифікація та патофізіологія нейрогенних дисфункцій нижніх сечових шляхів; урологічні синдроми в нейроурології.
Основними функціями нижніх сечових шляхів (НСШ), а саме сечового міхура (СМ) й уретри, які забезпечують акт сечовипускання, є накопичення та виділення сечі. Ці функції регулюються нервовою системою (центральною й периферичною), яка координує активність СМ (детрузора) та сфінктерного апарату сечівника (уретри). СМ – унікальний орган, непосмуговані волокна якого у процесі еволюції потрапили під вольовий контроль (набули здатності контролюватися ЦНС). Тому будь-яке порушення іннервації міхура на різних рівнях призводить до порушення акту сечовипускання, функцій наповнення та спорожнення із відповідною симптоматикою.
Фізіологічні основи акту сечовипускання
При поступовому заповненні СМ сечею внутрішньоміхуровий тиск залишається низьким і становить 5-10 см вод. ст. у горизонтальному положенні людини. Збереження сталого низького внутрішньоміхурового тиску у фазу наповнення забезпечується за рахунок еластичності та розтяжності стінок міхура (у зарубіжній літературі — «compliance»), а також одночасної активізації невральних механізмів, які стримують скорочення детрузора. Нейроанатомія СМ була представлена у попередніх роботах [1, 2, 8].
Еластичність та розтяжність стінок СМ пов’язана з наявністю в ній постійного рівня колагену, еластину та ретикулярних волокон, що дозволяє збільшувати об’єм міхура у 2-3 рази без підвищення внутрішньоміхурового тиску. Умовами фази наповнення є акомодація (пристосування) СМ до збільшення об’єму сечі при низькому внутрішньоміхуровому тиску із відповідними суб’єктивними відчуттями, закритий внутрішній отвір уретри (шийка міхура) у спокої та у період підвищення внутрішньочеревного тиску, а також відсутність мимовільних скорочень детрузора [7, 11, 14]. Симпатична нервова система забезпечує фазу наповнення СМ за рахунок збудження β-адренорецепторів тіла міхура (виникає розслаблення детрузора) та збудження α-адренорецепторів дна СМ та проксимального відділу уретри (зростає опір шийки СМ та проксимального відділу уретри). Під час переміщення тіла із горизонтального положенння у вертикальне тиск у СМ підвищується до 50-60 см вод. ст. за рахунок ваги органів черевної порожнини та трансмісії (передачі) внутрішньочеревного тиску на міхур. Сміх, кашель, фізичні навантаження сприяють підвищенню внутрішньоміхурового тиску до 100-200 см вод. ст.
Механізм утримання сечі у СМ складний і включає центральну та периферичну нервові системи, а також скелетну (посмуговану) та гладеньку (непосмуговану) мускулатуру уретри. У нормі внутрішньоуретральний тиск постійно перевищує тиск у СМ, тому нетримання сечі не спостерігають. Різниця між тиском в уретрі (Pur) та СМ (Pves) називається затульним тиском (Pclos). З віком Pclos знижується (особливо у жінок у постклімактеричному періоді) і його можна визначити за формулою Pclos = 100 – вік хворого (хворої) у роках [30]. Згідно з даними уродинаміки, при цистометрії наповнення перше відчуття наповнення СМ (FS) виникає, коли міхур наповнений до 40% його ємності, перший позив до сечовипускання (FD) – коли міхур наповнений до 60%, сильний позив до сечовипускання (SD) – коли міхур наповнений до 90% (рис. 1) [20]. Сильний позив до сечовипускання (SD) у здорових людей відрізняється від ургентних позивів (скарга на раптове бажання до спорожнення СМ, яке важко стримати) при гіперактивному СМ [2, 25]. Сильний позив до сечовипускання (SD) можливо відкласти до зручного для сечовипускання моменту (завдяки гальмівному впливу кори головного мозку на рефлекс сечовипускання), і цей позив характеризується відсутністю страху нетримання сечі та підвищення детрузорного тиску. Натомість ургентність при гіперактивному СМ характеризується невідкладністю, страхом нетримання сечі та підвищенням детрузорного тиску.
Рис. 1. Схематичне зображення фаз наповнення та спорожнення СМ [7]
Акт сечовипускання здійснюється наступним чином. Перший позив до сечовипускання виникає при заповненні СМ 150-250 мл сечі за рахунок надходження аферентних імпульсів від баро- та механорецепторів у спінальні центри сечовипускання (симпатичний – T10-L2, парасимпатичний – S2-4), а потім послідовно у супраспінальні відділи центральної нервової системи. По мірі наповнення СМ частота аферентних імпульсів збільшується, що викликає позив та рефлекс сечовипускання. Рефлекс може бути подавлений імпульсами з кори головного мозку. Якщо цього не відбувається – еферентні парасимпатичні моторні імпульси, що надходять до детрузора, призводять до його скорочення. Нормальний акт сечовипускання починається раптовим та повним розслабленням поперечно-смугастого сфінктера уретри з відсутністю скорочень його за даними електроміографії [1, 2, 7, 14, 15, 22] (рис. 2, 3). Після цього майже одразу підвищується внутрішньоміхуровий тиск та знижується внутрішньоуретральний. Тиск у СМ та у проксимальному відділі уретри стають однаковими (ізобаричними). Початок сечовипускання залежить як від подачі сенсорних (аферентних) сигналів, так і від зворотного зв’язку, який включає механізми зниження внутрішньоуретрального тиску й активності мускулатури тазового дна. Виникає значна парасимпатична стимуляція скорочення детрузора та вольове здійснення акту сечовипускання. Потрапляння сечі у проксимальний відділ уретри призводить до скорочення детрузора (уретро-міхуровий рефлекс). Умовами спорожнення СМ є скоординовані скорочення гладенької мускулатури детрузора одночасно зі зниженням опору на рівні внутрішнього та зовнішнього сфінктерів уретри (відсутність детрузорно-сфінктерної дисинергії [ДСД]), а також відсутність анатомічної обструкції уретри. Внутрішньоміхуровий тиск у фазу скорочення СМ залежить від внутрішньоуретрального тиску, останній у нормі складає від 30 до 50 см вод. ст. Вольове переривання акту сечовипускання пов’язане з раптовим скороченням поперечно-смугастого сфінктера уретри та мускулатури тазового дна, що через рефлекторний механізм перериває скорочення детрузора та виділення сечі. Рефлекс сечовипускання знаходиться під вольовим контролем і центр його розташований у стовбурі головного мозку (понтинний мікційний центр Barrington). Існують чотири нервові структури, які відповідають за активацію та координацію рефлексу сечовипускання: кора головного мозку (передлобна кора, поясна кора, острівець), стовбурова частина мозку (навколоводопровідна сіра речовина середнього мозку, понтинний мікційний центр), сакральний центр сечовипускання та периферичні ганглії СМ (рис. 4-6). У фазу наповнення СМ виникає збудження рецепторів розтягнення, що, з одного боку, веде до низькочастотної стимуляції аферентних нервів, а з іншого – активує центри сечовипускання у центральній нервовій системі. Від них еферентні імпульси передаються на β-адренорецептори стінки СМ, які викликають розслаблення детрузора, а також на α-адренорецептори, які призводять до скорочення шийки міхура та уретри (рис. 7). СМ та уретра отримують різнобічну, але достатньо збалансовану й скоординовану іннервацію із парасимпатичної, симпатичної та соматичної нервових систем. Симпатична нервова система (медіатор – норадреналін, рецептори – адренергічні) гальмує скорочення детрузора й сприяє утриманню сечі у СМ, парасимпатична (медіатор – ацетилхолін, рецептори – мускаринові) сприяє скороченню детрузора та виведенню сечі з міхура. Соматична нервова система за рахунок скорочення зовнішнього посмугованого сфінктера уретри (медіатор – ацетилхолін, рецептори – нікотинові) сприяє утриманню сечі у СМ (рис. 8, 9). Скоординоване синергічне скорочення детрузора та розслаблення посмугованого сфінктера уретри характеризує нормальний акт сечовипускання (табл. 1). Після закінчення виділення сечі (акту сечовипускання) виникає закриття шийки СМ за рахунок скорочення мускулатури тазового дна та сфінктерного апарату уретри, підвищується внутрішньоуретральний тиск і знижується внутрішньоміхуровий, і фаза наповнення міхура починається знову.
Рис. 2. Фізіологія акту сечовипускання за даними відеоуродинаміки [7, 15]
Рис. 3. Схематичне зображення фаз наповнення та спорожнення СМ [7]
PMC — понтинний мікційний центр; PAG — навколоводопровідна сіра речовина середнього мозку; ACG — передня поясна кора; PFC — передлобна кора; RI — острівець
Рис. 4. Іннервація НСШ та вищі центри контролю акту сечовипускання:
а — структури головного мозку, відповідальні за утримання сечі (позитронно-емісійна томографія у поєднанні із функціональною МРТ);
б — спрощена модель структур супраспінального контролю рефлексу сечовипускання;
в — структури головного та спинного мозку, відповідальні за рефлекс сечовипускання (схематичне зображення) [7, 21]
Рис. 5. Структури головного та спинного мозку, відповідальні за функції наповнення та спорожнення СМ (схематичне зображення) [7, 22]
Рис. 6. Аферентна й еферентна іннервація НСШ, співвідношення структур головного й спинного мозку, відповідальних за функції наповнення та спорожнення СМ (схематичне зображення) [7, 29]
Рис. 7. Локалізація рецепторів у СМ та уретрі, вплив симпатичної й парасимпатичної нервових систем на функцію СМ та уретри [8]
Рис. 8. Симпатична, парасимпатична та соматична іннервація НСШ [2, 7]
Рис. 9. Іннервація НСШ, їх рецептори та медіатори [7, 24]
|
Таблиця 1. Іннервація НСШ, рецептори, нейротрансмітери та механізм їх дії на стінку СМ і уретри [7, 29] |
||||||
|
Іннервація |
Локалізація |
Нерв |
Нейротрансмітер |
Рецептор |
Механізм дії |
Результат |
|
Парасимпатична |
S2-S4 |
Тазовий |
Ацетилхолін |
Мускариновий |
Скорочення детрузора |
Спорожнення СМ |
|
Релаксація шийки СМ |
Спорожнення СМ |
|||||
|
Симпатична |
Т10-Т12 |
Підчеревний |
Норадреналін |
β |
Релаксація детрузора |
Затримка (утримання) сечі |
|
α |
Скорочення шийки СМ |
Затримка (утримання) сечі |
||||
|
Соматична |
Аферентні та еферентні S2-S4 |
Статевий |
Ацетилхолін |
Нікотиновий |
Скорочення зовнішнього сфінктера уретри |
Затримка (утримання) сечі |
Класифікація нейрогенних дисфункцій нижніх сечових шляхів
Умовно виділяють наступні рівні регуляції СМ: кірково-підкірковий (лобні частки кори, гіпоталамус, таламус), стовбуровий або понтинний, спінальний (крижовий парасимпатичний та грудо-поперековий симпатичний вегетативні центри) та периферичний (інтрамуральні нервові структури, тазове сплетення, паравертебральні симпатичні ганглії) [4, 5, 7, 16-18]. Нейрогенний сечовий міхур – це дисфункція СМ внаслідок порушення його іннервації. Сьогодні замість терміну «нейрогенний сечовий міхур» використовують термін «нейрогенна дисфункція нижніх сечових шляхів (НДНСШ)» з огляду на те, що при порушенні іннервації СМ має місце і порушення іннервації та функції сфінктерного апарату уретри. НДНСШ включає стани, зумовлені вродженими або набутими ураженнями різних рівнів нервових шляхів, що забезпечують функцію довільного сечовипускання та утримання сечі. НДНСШ супроводжується порушенням функції детрузора (гіперактивність, гіпоактивність, відсутність активності – аконтрактильність), сфінктерного апарату уретри (гіперактивність, гіпоактивність), а також ДСД. Вид НДНСШ при неврологічних захворюваннях визначається локалізацією та характером патології. На рис. 10-12 представлено класифікацію НДНСШ Європейської асоціації урологів (EAU, 2022), що базується на класифікації H. Madersbacher (1990) [18, 23], яка дозволяє орієнтовно, без виконання уродинамічних досліджень встановити вид НДНСШ та вибрати відповідне початкове лікування. Класифікація є універсальною (застосовна до будь-якого неврологічного захворювання та травми), хоча й не на 100% дозволяє визначити дисфункцію системи «детрузор – сфінктерний апарат уретри». Це пов’язано з політопністю ураження нервових структур при деяких захворюваннях (наприклад, при розсіяному склерозі) та нейропластичністю нейронів із відновленням функції (частковою або повною) детрузора і сфінктерного апарату уретри (наприклад, при спинномозковій травмі).
Рис. 10. Характер дисфункцій НСШ та їх симптоматика при неврологічних захворюваннях і травмах залежно від локалізації патології [7]
Рис. 11. Характер дисфункцій НСШ (детрузор, сфінктер) при неврологічних захворюваннях і травмах залежно від локалізації патології [7, 18]
Рис. 12. Характер дисфункцій НСШ при неврологічних захворюваннях та травмах залежно від локалізації патології. Справа схематично представлено очікувальний стан НСШ (детрузор — сфінктер) [2, 7, 8, 18, 22]
При НДНСШ нейроурологи виділяють: нейрогенну гіперактивність детрузора, нейрогенну гіпо- та аконтрактильність детрузора, ДСД та нейрогенну сфінктерну недостатність [5, 7, 22, 24, 29]. Характер та локалізація неврологічного ураження, симптоматика НДНСШ, дані цистометрії представлені у табл. 2.
|
Таблиця 2. Характер та локалізація неврологічного ураження, симптоматика НДНСШ, дані цистометрії [7, 29] |
|||
|
Локалізація ураження |
Симптоми |
Захворювання |
Дані цистометрії |
|
Супрапонтинні |
Часті імперативні позиви, полакіурія, ноктурія, імперативне нетримання сечі |
Інсульт Паркінсонізм Деменція Гідроцефалія Церебральний параліч Пухлини та травматичні ушкодження головного мозку Розсіяний склероз |
Детрузорна гіперактивність |
|
Спінальні (субпонтинні-супра- сакральні) |
Часті імперативні позивки, полакіурія, ноктурія, імперативне нетримання сечі, утруднене та переривчасте сечовипускання, затримка сечі |
Розсіяний склероз Травми та пухлини спинного мозку Спинномозкова грижа (spina bifida) Мієлодисплазія Патологія міжхребцевих дисків Поперечний мієліт |
Детрузорна гіперактивність, детрузорно-сфінктерна дисинергія |
|
Субсакральні |
Утруднене та переривчасте сечовипускання, затримка сечі |
Синдром «кінського хвоста» (cauda equine) Ятрогенне ушкодження тазових нервів (при хірургічних та акушерсько-гінекологічних операціях на тазових органах, променевій терапії) Периферична нейропатія (цукровий діабет, зловживання алкоголем, генітальний герпес) |
Детрузорна гіпоактивність, сфінктерна недостатність |
Анатомічна класифікація нейрогенних дисфункцій НСШ виділяє наступні нейроанатомічні ураження: супрапонтинні, інфрапонтинні-супрасакральні, сакральні, «кінський хвіст» та тазові нерви (рис. 13). При супрапонтинних ураженнях має місце втрата гальмівного контролю вищих центрів сечовипускання над понтинним мікційним центром та крижовим центром сечовипускання. При супрапонтинних ураженнях у хворих виникає часте денне (полакіурія) та нічне (ноктурія) сечовипускання, імперативні позиви до сечовипускання (ургентність) із можливим імперативним нетриманням сечі. При інфрапонтинних-супрасакральних ураженнях має місце активація рефлексу сечовипускання через втрату над ним контролю понтинного мікційного центру. Виникає нейрогенна гіперактивність детрузора та ДСД. При сакральних ураженнях спостерігають різну картину: гіпер- та гіпоактивність детрузора (аж до арефлексії), зниження контрактильності сфінктерного апарату уретри, може мати місце і ДСД [22]. При ураженні типу «кінського хвоста» та тазових периферичних нервів (інфрасакральні ураження) виникає гіпо- та арефлексія детрузора; денервація (зниження активності) зовнішнього сфінктера уретри, хоча можлива і його спастичність (гіперактивність).
Рис. 13. Нейроанатомічна класифікація нейрогенних дисфункцій НСШ [7, 29]
Уродинамічна класифікація функцій та дисфункцій НСШ Міжнародного товариства з утримання сечі (ICS) [21] представлена у табл. 3, характер дисфункцій НСШ (детрузор, уретральний сфінктер) при неврологічних захворюваннях та травмах залежно від локалізації патології – на рис. 14, 15, а етіологія НДНСШ залежно від рівня ураження – у табл. 4.
Рис. 14. Характер дисфункцій НСШ (детрузор, сфінктер уретри) при неврологічних захворюваннях та травмах залежно від локалізації патології [7]
Рис. 15. Функція детрузора та сфінктерного апарату уретри при неврологічних захворюваннях та травмах залежно від локалізації ураження (а-в) [15]
|
Таблиця 3. Уродинамічна класифікація функцій та дисфункцій НСШ ICS [21] |
||
|
|
Фаза наповнення СМ |
Фаза спорожнення СМ |
|
Сечовий міхур Норма Патологія |
Релаксація детрузора Гіперактивність детрузора: • ідіопатична • нейрогенна |
Скорочення детрузора Гіпо-/аконтрактильність детрузора |
|
Уретра Норма Патологія |
Скорочення сфінктерного апарату уретри Сфінктерна недостатність уретри (через гіпермобільність уретри у жінок або ураження її нервово-м’язових структур у чоловіків та жінок) |
Релаксація сфінктерного апарату уретри Обструкція уретри, дисфункціональне сечовипускання, детрузорно-сфінктерна дисинергія |
|
Таблиця 4. Етіологія нейрогенних дисфункцій НСШ залежно від рівня ураження [7, 29] |
||||
|
Причини |
Медичні |
Хірургічні |
Дегенеративні |
Вроджені |
|
Рівень ураження |
||||
|
Супрапонтинні |
Порушення мозкового кровообігу (інсульт) Розсіяний склероз |
Пухлини Травма |
Хвороба Паркінсона |
Церебральний параліч Гідроцефалія |
|
Інфрапонтинні – супрасакральні |
Розсіяний склероз Інфекція Інсульт |
Травма |
Пролапс дисків Стеноз хребтового каналу Спинна сухотка |
Спинномозкова грижа |
|
Інфрасакральні |
Оперізуючий лишай |
Пухлини Травма |
Спинна сухотка |
Агенезія крижової кістки |
|
Периферичні |
Цукровий діабет Медикаментозна нейропатія |
Операції на товстому кишечнику, прямій кишці та внутрішніх статевих органах |
|
Менінгомієлоцеле |
ДСД – спорожнення СМ (детрузора) виникає одночасно із мимовільними скороченнями сфінктерного апарату уретри. Термін «детрузорно-сфінктерна дисинергія» використовують, коли виявляють у пацієнта неврологічну патологію. У разі відсутності неврологічної патології говорять про дисфункціональне сечовипускання.
Патофізіологія основних урологічних синдромів у нейроурології
Урологічні прояви нейрогенної дисфункції НСШ характеризуються затримкою сечі, гіперактивністю детрузора (із/без імперативного нетримання сечі), нетриманням сечі та ДСД. До неурологічних проявів спинномозкової травми відносять вегетативну дисрефлексію.
Нейрогенна затримка сечі. Затримку поділяють на гостру та хронічну, остання може бути повною та неповною. Гостра затримка сечі (ішурія) характеризується повним раптовим припиненням виділення сечі із переповненого СМ за наявності болісних позивів до сечовипускання. У неврологічних хворих гостра затримка сечі може не проявлятися больовим синдромом. Гостра затримка сечі є порушенням спорожнюючої (евакуаторної) функції СМ. Повна затримка сечі – неможливість спорожнити СМ (виділити будь-яку кількість сечі із СМ). Неповна затримка сечі – порушення спорожнення СМ, при якому об’єм виділеної сечі не перевищує об’єм залишкової. Зумовлена анатомічною (функціональною) обструкцією СМ, детрузорною гіпоактивністю або обома цими факторами. Залишкова сеча – об’єм сечі у СМ після сечовипускання. Хронічна повна затримка сечі може проявлятись парадоксальною ішурією, коли пацієнт відмічає неможливість спорожнити СМ, при цьому у нього одночасно має місце мимовільне виділення декількох крапель сечі. Парадоксальна ішурія (парадоксальне нетримання сечі) – нетримання сечі одночасно із її затримкою (нетримання через переповнення СМ).
Нейрогенна затримка сечі виникає зазвичай при ураженні попереково-крижового відділу хребта, де знаходиться крижовий центр сечовипускання з парасимпатичною моторною іннервацією СМ (рис. 16). При цьому виникає гіпоактивність детрузора з нормо- або гіперактивністю сфінктерного апарату уретри. Нейрогенну затримку сечі спостерігають і при гіперактивності сфінктерного апарату уретри за наявності нормальної активності детрузора. Механічна обструкція НСШ у 80-90% випадків є причиною виникнення гострої затримки сечі, переважно (99%) у чоловіків – через наявність у них доброякісної гіперплазії простати, раку простати, стриктури уретри та іншої інфравезикальної обструкції (рис. 17). Нейрогенна затримка сечі складає всього 2-3% серед усіх випадків гострої затримки сечі і, як правило, зумовлена гіпоактивністю детрузора [6, 13, 26]. Нейрогенна затримка сечі може бути виявлена і у хворих із доброякісною гіперплазією простати. Необхідно пам’ятати про медикаментозну гіпоактивність детрузора через вживання протипаркінсонічних препаратів. Нейрогенні причини затримки сечі представлені у табл. 5. При ішемічному інсульті нейрогенна затримка сечі (частота – 20%) зумовлена ураженням центрів сечовипускання, розташованих у лобних частках кори, гіпоталамусі та середньому мозку [24].
Рис. 16. Патофізіологія нейрогенної затримки сечі [29]
Рис. 17. Причини затримки сечі [7, 24]
|
Таблиця 5. Нейрогенні причини затримки сечі [29] |
|
|
Локалізація ураження |
Причини |
|
Головний мозок |
Захворювання судин головного мозку, струс мозку, розсіяний склероз, пухлина, паркінсонізм, гідроцефалія |
|
Спинний мозок |
Розсіяний склероз, менінгоміелоцеле, патологія міжхребцевих дисків, гематома або абсцес спинного мозку, патологія судин спинного мозку, поперечний мієліт, пухлини conus medullaris або cauda equine, spina bifida |
|
Автономний або периферичний нерв |
Нейропатія автономної нервової системи, цукровий діабет, вірус оперізуючого герпесу, поліомієліт, радикальні хірургічні втручання на органах таза, сакральна (перидуральна) анестезія, травма спинного мозку, злоякісна анемія, спинна сухотка |
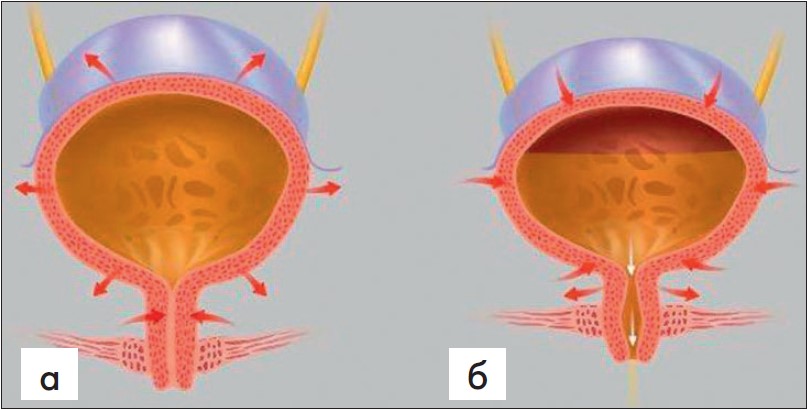
Нейрогенне нетримання сечі. Фізіологія утримання сечі у СМ та патофізіологія нетримання сечі представлена на рис. 18. У чоловіків та жінок основними видами нетримання сечі є стресове, імперативне та змішане (90-95% всіх видів нетримання сечі) (рис. 19). У хворих із нейрогенною дисфункцією сечових шляхів нетримання сечі зумовлене гіперактивністю детрузора (нейрогенне імперативне нетримання сечі), ДСД, гіпо- та аконтрактильністю детрузора з переповненням СМ (парадоксальне нетримання сечі), недостатністю функції сфінктерного апарату уретри (нейрогенне стресове нетримання сечі) (рис. 20). Функціональний стан детрузора та сфінктерного апарату уретри при нейрогенній дисфункції сечових шляхів встановлюють за допомогою уродинамічних та відеоуродинамічних досліджень. При супрапонтинних ураженнях імперативне нетримання сечі спричинене нейрогенною гіперактивністю детрузора через втрату контролю кортикальних центрів над рефлексом сечовипускання. При спінальних ураженнях нетримання сечі зумовлене нейрогенною гіперактивністю детрузора, а також ДСД. При субсакральних ураженнях нетримання сечі зумовлене підвищенням тиску у переповненому СМ із розтягненням шийки міхура, виникненням парадоксальної ішурії (парадоксального нетримання сечі); також мають місце випадки нейрогенного стресового нетримання сечі через гіпоактивність сфінктерного апарату уретри.
Рис. 18. У нормі утримання сечі в наповненому СМ відбувається за рахунок збереженої сфінктерної функції уретри та відсутності спонтанних або спровокованих скорочень детрузора (а); при гіперактивності детрузора (ідіопатичній чи нейрогенній) імперативне (ургентне) нетримання сечі відбувається за рахунок спонтанних або спровокованих скорочень детрузора (б), при цьому внутрішньоміхуровий тиск перевищує нормальний внутрішньоуретральний тиск або знижений (при поєднаному порушенні й сфінктерної функції уретри — так зване змішане нетримання сечі)
Рис. 19. Етіологія основних видів нетримання сечі [8, 28]
Рис. 20. Патофізіологія нейрогенного нетримання сечі [29]
Детрузорно-сфінктерна дисинергія – cкорочення детрузора одночасно із мимовільним скороченням сфінктерного апарату уретри. Саме гіперактивність детрузора та ДСД сприяють підвищенню внутрішньоміхурового тиску, виникненню міхурово-сечовідного рефлюксу, уретерогідронефрозу, висхідного рецидивуючого пієлонефриту та ниркової недостатності (рис. 21, 22). Мимовільне сечовипускання характерне для немовлят та дітей раннього віку до досягнення 3-5 років, у яких цей процес контролює лише автономна частина нервової системи, а далі, із віком, акт сечовипускання стає контрольованим [27]. У нормі внутрішньоміхуровий тиск становить 10-15 см вод. ст. СМ вважають «небезпечним», коли внутрішньоміхуровий тиск становить більше 40 см вод. ст. або коли виявляють ДСД. ДСД спостерігають при спінальних (супрасакральних-інфрапонтинних) ураженнях (травмах та неврологічних захворюваннях).
Рис. 21. Детрузорно-сфінктерна дисинергія при спінальних (супрасакральних-інфрапонтинних) ураженнях (травмах та неврологічних захворюваннях) [29]
Рис. 22. Детрузорно-сфінктерна дисинергія при нейрогенних дисфункціях НСШ із виникненням міхурово-сечовідного рефлюксу сечі, розширенням верхніх сечових шляхів, розвитком пієлонефриту та ниркової недостатності [27]
J. G. Blaivas та співавт. (1981) [14, 29] при уродинамічних дослідженнях у хворих із ДСД запровадили три типи цього стану (рис. 23):
І тип – підвищення детрузорного тиску супроводжується підвищенням активності зовнішнього сфінктера уретри, на піку детрузорного тиску відмічають різке зниження активності зовнішнього сфінктера уретри, що клінічно проявляється нейрогенним імперативним нетриманням сечі;
ІІ тип – підвищення детрузорного тиску супроводжується переривчастим підвищенням активності зовнішнього сфінктера уретри, що клінічно проявляється переривчастим струменем сечі;
ІІІ тип – підвищення детрузорного тиску супроводжується постійним підвищенням активності зовнішнього сфінктера уретри, що клінічно проявляється обструкцією уретри та затримкою сечі, а також неможливістю розпочати акт сечовипускання.
ДСД І типу має місце при неповному ураженні спинного мозку, ДСД ІІ та ІІІ типу спостерігається при повному ураженні спинного мозку. ДСД поділяють на постійну та періодичну [29]. При постійній ДСД частіше виникають урологічні ускладнення у зв’язку із підвищеним внутрішньоміхуровим тиском, що супроводжується міхурово-сечовідним рефлюксом сечі, двобічним уретерогідронефрозом, нирковою недостатністю, а також інфекціями сечових шліхів.
Міхурово-сечовідний рефлюкс зустрічається у 10-30% хворих із НДНСШ, особливо в дітей. Причиною їх є втрата затульної функції міхурово-сечовідного сегмента через підвищений внутрішньоміхуровий (детрузорний) тиск у результаті нейрогенної гіперактивності детрузора, гіперактивності сфінктерного апарату уретри, ДСД. Це призводить до розширення верхніх сечових шляхів, їх інфікування та втрати функції нирок при двобічному ураженні. Діагностика міхурово-сечовідного рефлюксу базується на виконанні висхідної та мікційної цистографії, а також відеоуродинамічних досліджень (рис. 24). Класифікація міхурово-сечовідного рефлюксу представлена на рис. 25. І ступінь – потрапляння сечі у нерозширений сечовід; ІІ ступінь – потрапляння сечі у нерозширений сечовід, миску та чашечки; ІІІ ступінь – незначне розширення сечоводу, миски та чашечок; ІV ступінь – покручення сечоводу та значне розширення чашково-мискової системи; V ступінь – виражене покручення сечоводу та значне розширення чашково-мискової системи із відсутністю сосочків нирки.
Рис. 23. Типи ДСД за J. G. Blaivas та співавт. (1981) [14, 29]
Рис. 24. Висхідна цистограма у хворої із НДНСШ: відмічається двобічний міхурово-сечовідний рефлюкс V ст. [7]
Рис. 25. Класифікація міхурово-сечовідного рефлюксу [7, 22]
Автономна дисрефлексія – раптова та посилена реакція вегетативної нервової системи на різні стимули у хворих із ураженням спинного мозку або порушенням функції спинного мозку на рівні сегмента Т6 та вище. Вона визначається як підвищення систолічного артеріального тиску (АТ) >20 мм рт. ст. від початкового рівня. Автономна дисрефлексія є потенційно небезпечним станом у таких хворих і характеризується гіперактивацією симпатичної нервової системи у відповідь на аферентний сигнал із різким підвищенням АТ та високим ризиком виникнення геморагічного інсульту. Можливе підвищення АТ при автономній дисрефлексії до 200-300 мм рт. ст. Підняття АТ супроводжується симптомами (головний біль, нечіткий зір, закладеність носа, гіперемія обличчя, підвищена пітливість, бліда та холодна шкіра), можливий безсимптомний перебіг гіпертензії (у 35-50% хворих) [12, 16, 22]. Автономна дисрефлексія у 90% хворих зумовлена ушкодженням шийного відділу спинного мозку і може виникати до 40 разів на день. Травма спинного мозку вище шостого грудного хребця проявляється автономною дисрефлексією у 48-80% хворих. У хворих із повним ушкодженням спинного мозку автономна дисрефлексія виникає у 3 рази частіше, ніж у хворих із неповним. Автономна дисрефлексія, як правило, не виникає у період спінального шоку, а лише після його закінчення; у перший рік після спинномозкової травми її відмічають у 92% хворих. Аферентні стимули, які викликають автономну дисрефлексію, представлені у табл. 6. До 85% всіх аферентних стимулів мають урологічну причину. Патогенез та клініка автономної дисрефлексії у хворих із спинномозковою травмою представлені на рис. 26. Підвищення АТ та церебральна вазодилатація є причиною виникнення геморагічного інсульту. У першу чергу необхідно перевірити й виключити перетиснення та закупорку катетера Фолі слизово-сольовими масами із перерозтягненням СМ. При закупорці катетера виконують його заміну на новий, при цьому в уретру необхідно ввести лубрикант із лідокаїном та антисептиком (катеджель). При нормальній роботі уретрального катетера необхідно перевірити кишечник на предмет калового завалу та після місцевого знеболення прямої кишки лідокаїном (катеджель) видалити калові маси. При підвищенні АТ >150 мм рт. ст. використовують антигіпертензивні препарати з короткою дією (каптоприл – 25 мг, ніфедипін – 10 мг). АТ контролюють протягом 2 год після усунення причини автономної дисрефлексії.
Рис. 26. Етапи (1-5) патогенезу та симптомів автономної дисрефлексії у хворих із спинномозковою травмою [7, 16]
|
Таблиця 6. Причини автономної дисрефлексії у хворих із спинномозковою травмою [7, 16] |
|
|
Сечостатеві |
Перерозтягнення СМ Інфекції сечових шляхів, епідидимоорхіт Детрузорно-сфінктерна дисинергія Статевий акт Камені нирок Перекрут яєчка |
|
Гастроінтестинальні |
Перерозтягнення кишечника, каловий завал Анальні стриктури Гастродуоденальні виразки Камені жовчних шляхів, холецистит Гастроезофагеальний рефлюкс |
|
Шкірні |
Пролежні Опіки (у т.ч. сонячні) Укуси комах Врослі нігті |
|
М‘язово-скелетні |
Стискаючий одяг Зміна положення тіла Спастичність м’язів Травми та переломи кісток Тромбоз глибоких вен Фізичні вправи |
|
Діагностичні процедури |
Цистоскопія Уродинамічні (відеоуродинамічні) дослідження із цистометрією Екстракорпоральна дистанційна літотрипсія Хірургія, анестезія |
|
Інші |
Введення препаратів Стиснення калитки Вагітність, пологи, менструальні спазми Холод Зловживання алкоголем |
Лікування основних урологічних синдромів у нейроурології буде представлено в наступних публікаціях.
Література
- Горовий В. І. Анатомія синдрому гіперактивного сечового міхура у жінок // Медичні аспекти здоров’я жінки. – 2022. – № 1 (142). – С. 1-19.
- Гіперактивний сечовий міхур у жінок / За ред. В.І. Горового та ін. – Вінниця: «Твори», 2022. – 368 с.
- Дубенко Е. Г. Нарушения мочеиспускания при заболеваниях нервной системы и методы их патогенетического лечения // Журнал неврології ім. Б. М. Маньковського. – 2015. – Т. 3, № 1. – С. 86-89.
- Клиническая нейроанатомия и неврология по Фицжеральду / Э. Мтуи и др.; пер. с англ. – М.; Изд-во Панфилова, 2018. – 400 с.
- Крупин В.Н., Белова А. Н. Нейроурология: руководство для врачей. – М.: Антидор, 2005. – 464 с.
- Невідкладна урологія в практиці лікарів хірургічного профілю / Горовий В. І. та ін. – Вінниця: «Твори», 2018. – 824 с.
- Нейроурологія / За ред. Горового В. І. та ін. – Вінниця: «Твори», 2023. – 520 с.
- Нетримання сечі у жінок: навчальний посібник / За ред. Горового В. І., Яцини О. І. – Вінниця: ТОВ «Твори», 2020. – 472 с.
- Переверзев А.С., Козлюк В. А. Симптомы нижних мочевых путей. – Харьков: Факт, 2009. – 431 с.
- Пушкарь Д.Ю., Касян Г. Р. Функциональная урология и уродинамика. – М.: ГЭОТАР – Медиа, 2013. – 376 с.
- Синдром гиперактивного мочевого пузыря в клинической практике врача-уролога / Касян Г. Р. и др. // Метод. рекомендации № 2. – М., 2016. – 36 с.
- Стандартизація в нейрохірургії / За ред. Є. Г. Педаченка. – К., 2019. – 152 с.
- Шварц П.Г., Попов С. В. Нейрогенная задержка мочи. – М.: Изд-во «Прес-Бюро», 2011. – 224 с.
- Abrams P. Urodynamics. – 3rd ed. – Springer –Verlag London Limited, 2006. – 340 p.
- Campbell-Walsh Urology / Wein A. J. et al. – 11th ed. – Philadelphia: Elsevier, 2016. – 4904 p.
- Consultation in neurourology / Corcos J., Przydacz M. – Springer, 2018. – 310 p.
- De Groat W., Graffiths D., Yoshimura N. Neural control of the Lower urinary tract // Compr. Physiol. – 2015. – Vol. 5. – P. 327-396.
- EAU Guidelines on neuro-urology / Blok В. et al. – EAU, 2022. – 44 p.
- Female urology / Raz S., Rodriguez L. V. – 3rd ed. – Elsevier Saunders, 2008. – 1038 p.
- Fowler C., Griffiths D., de Groat W. C. The neural control of micturation // Nat. Rev. Neurosci. – 2008. – Vol. 9. – P. 433-466.
- Incontinence / Albrams P. et al. – 6th ed. – ICS – ICUD, 2017. – 2336 p.
- Liao L., Madersbacher H. Neurourology. Theory and practice. – Springer, 2019. – 548 p.
- Madersbacher H. Іntravesical electrical stimulation for the rehabilitation of the neuropatic bladder // Paraplegia. – 1990. – Vol. 28. – P. 349-352.
- Neuro-Urology / Dmochowski R., Heesakkers J. — Springer, 2018. – 454 p.
- Overactive bladder syndrome and urinary incontinence // Hashim H., Abrams P. – Oxford University Press, 2012. – 84 p.
- Serlin D.C., Heideebaugh J. J., Stoffet J. T. Urinary retention in adults: evaluation and initial management // Am. Fam. Physician. 2018. – Vol. 98. – P. 494-503.
- Staffel J. T. Detrusor sphincter dyssynergia: a rewiev of physiology, diagnosis, and treatment strategies // Trans. Androl. Urol. – 2016. – Vol. 5. – P. 127-135.
- Textbook of female urology and urogynaecology / Cardozo L., Staskin D. – 2nd ed. – Informa Healthcare, 2006. – 1384 p.
- Textbook of the neurogenic bladder // Corcos J. et al. – 3rd ed. – CRC Press, 2016. – 800 p.
- Urogynecology and reconstructive pelvic surgery / Walters M. D., Karram M. M. – 3rd ed. – Philadelphia: Mosby Elsevier, 2015. – 600 р.
Тематичний номер «Урологія. Нефрологія. Андрологія» № 3 (30), 2023 р.
СТАТТІ ЗА ТЕМОЮ Урологія та андрологія
У лютому відбулася щорічна Всеукраїнська науково-практична конференція «Малоінвазивні технології в урології», присвячена актуальним проблемам сучасної урології. Пропонуємо огляд найцікавіших доповідей, що прозвучали в рамках заходу....
Інфекції сечовивідних шляхів (ІСШ) у всьому світі посідають провідне місце серед інфекційних захворювань дорослого населення. Поряд із тим серед фахівців зростає занепокоєння щодо триваючого зростання стійкості бактерій до більшості антибіотиків. Експерти провідних міжнародних товариств наголошують на необхідності розсудливого і виваженого призначення антимікробних препаратів. Про основні принципи раціональної антибіотикотерапії в урології, зокрема при проведенні діагностичних і хірургічних втручань, ми попросили розповісти завідувача відділу відновної урології та новітніх технологій ДУ «Інститут урології ім. акад. О.Ф. Возіанова НАМН України», доктора медичних наук, професора В’ячеслава Миколайовича Григоренка. ...
Процедура трансректальної біопсії простати супроводжується високим ризиком інфекційних ускладнень, тому проведення антимікробної профілактики при цьому втручанні є обов’язковим. Однак зростання антибіотикорезистентності, а також нещодавні рекомендації щодо обмеження призначень фторхінолонів значно звужують спектр можливих варіантів такої профілактики. Міжнародною мультидисциплінарною групою експертів на основі літературних джерел та клінічного досвіду було розроблено ряд настанов стосовно запобігання інфекційним ускладненням при біопсії простати та обґрунтовано доцільність і переваги призначення з цією метою фосфоміцину ...
Кількість людей, які страждають і помирають від вірусного гепатиту В (ВГВ), можна порівняти з кількістю хворих на коронавірусну хворобу 2019 року (COVID‑19), яка наразі викликає велике занепокоєння в усьому світі. Тому вкрай важливим залишається питання передачі вірусу, у тому числі через статеві клітини. Попередніми дослідженнями встановлено, що гени ВГВ, інтегровані в людські сперматозоїди, здатні до реплікації та експресії після передачі ембріонам. Однак досі це явище не було підтверджено клінічними дослідженнями у пацієнтів. Автори вивчали особливості інтеграції ВГВ у геном сперматозоїдів пацієнтів та аналізували можливі клінічні наслідки для потомства ...





![Рис. 1. Схематичне зображення фаз наповнення та спорожнення СМ [7]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic1.jpg)
![Рис. 2. Фізіологія акту сечовипускання за даними відеоуродинаміки [7, 15]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic2.jpg)
![Рис. 3. Схематичне зображення фаз наповнення та спорожнення СМ [7]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic3.jpg)
![Рис. 4. Іннервація НСШ та вищі центри контролю акту сечовипускання: а — структури головного мозку, відповідальні за утримання сечі (позитронно-емісійна томографія у поєднанні із функціональною МРТ); б — спрощена модель структур супраспінального контролю рефлексу сечовипускання; в — структури головного та спинного мозку, відповідальні за рефлекс сечовипускання (схематичне зображення) [7, 21]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic4_1.jpg)
![Рис. 4. Іннервація НСШ та вищі центри контролю акту сечовипускання: а — структури головного мозку, відповідальні за утримання сечі (позитронно-емісійна томографія у поєднанні із функціональною МРТ); б — спрощена модель структур супраспінального контролю рефлексу сечовипускання; в — структури головного та спинного мозку, відповідальні за рефлекс сечовипускання (схематичне зображення) [7, 21]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic4_2.jpg)
![Рис. 5. Структури головного та спинного мозку, відповідальні за функції наповнення та спорожнення СМ (схематичне зображення) [7, 22]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic5.jpg)
![Рис. 6. Аферентна й еферентна іннервація НСШ, співвідношення структур головного й спинного мозку, відповідальних за функції наповнення та спорожнення СМ (схематичне зображення) [7, 29]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic6.jpg)
![Рис. 7. Локалізація рецепторів у СМ та уретрі, вплив симпатичної й парасимпатичної нервових систем на функцію СМ та уретри [8]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic7.jpg)
![Рис. 8. Симпатична, парасимпатична та соматична іннервація НСШ [2, 7]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic8.jpg)
![Рис. 9. Іннервація НСШ, їх рецептори та медіатори [7, 24]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic9.jpg)
![Рис. 10. Характер дисфункцій НСШ та їх симптоматика при неврологічних захворюваннях і травмах залежно від локалізації патології [7]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic10.jpg)
![Рис. 11. Характер дисфункцій НСШ (детрузор, сфінктер) при неврологічних захворюваннях і травмах залежно від локалізації патології [7, 18]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic11.jpg)
![Рис. 12. Характер дисфункцій НСШ при неврологічних захворюваннях та травмах залежно від локалізації патології. Справа схематично представлено очікувальний стан НСШ (детрузор — сфінктер) [2, 7, 8, 18, 22]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic12.jpg)
![Рис. 13. Нейроанатомічна класифікація нейрогенних дисфункцій НСШ [7, 29]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic13.jpg)
![Рис. 14. Характер дисфункцій НСШ (детрузор, сфінктер уретри) при неврологічних захворюваннях та травмах залежно від локалізації патології [7]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic14.jpg)
![Рис. 15. Функція детрузора та сфінктерного апарату уретри при неврологічних захворюваннях та травмах залежно від локалізації ураження (а-в) [15]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic15.jpg)
![Рис. 16. Патофізіологія нейрогенної затримки сечі [29]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic16.jpg)
![Рис. 17. Причини затримки сечі [7, 24]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic17.jpg)
![Рис. 19. Етіологія основних видів нетримання сечі [8, 28]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic19.jpg)
![Рис. 20. Патофізіологія нейрогенного нетримання сечі [29]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic20.jpg)
![Рис. 21. Детрузорно-сфінктерна дисинергія при спінальних (супрасакральних-інфрапонтинних) ураженнях (травмах та неврологічних захворюваннях) [29]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic21.jpg)
![Рис. 22. Детрузорно-сфінктерна дисинергія при нейрогенних дисфункціях НСШ із виникненням міхурово-сечовідного рефлюксу сечі, розширенням верхніх сечових шляхів, розвитком пієлонефриту та ниркової недостатності [27]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic22.jpg)
![Рис. 23. Типи ДСД за J. G. Blaivas та співавт. (1981) [14, 29]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic23.jpg)
![Рис. 24. Висхідна цистограма у хворої із НДНСШ: відмічається двобічний міхурово-сечовідний рефлюкс V ст. [7]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic24.jpg)
![Рис. 25. Класифікація міхурово-сечовідного рефлюксу [7, 22]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic25.jpg)
![Рис. 26. Етапи (1-5) патогенезу та симптомів автономної дисрефлексії у хворих із спинномозковою травмою [7, 16]](/multimedia/userfiles/images/2023/Uro_3_2023/Urol_3_2023_st12-18_pic26.jpg)