Можливості контролю серцево-судинних ризиків при подагрі та гіперурикемії. Роль уратзнижувальної терапії
 Сечова кислота (СК) – кінцевий продукт метаболізму пуринів, який здебільшого синтезується в печінці та виводиться нирками і кишечником [1, 2]. Гіперурикемія – підвищений рівень СК у сироватці крові – є метаболічною основою подагри, одного з найпоширеніших запальних артритів. У середні віки подагра вважалася хворобою надмірності аристократії, нині її поширеність зростає у всьому світі через зміни в харчуванні, переважання в дієті оброблених продуктів, фруктози та збільшення поширеності ожиріння [3].
Сечова кислота (СК) – кінцевий продукт метаболізму пуринів, який здебільшого синтезується в печінці та виводиться нирками і кишечником [1, 2]. Гіперурикемія – підвищений рівень СК у сироватці крові – є метаболічною основою подагри, одного з найпоширеніших запальних артритів. У середні віки подагра вважалася хворобою надмірності аристократії, нині її поширеність зростає у всьому світі через зміни в харчуванні, переважання в дієті оброблених продуктів, фруктози та збільшення поширеності ожиріння [3].
Безсимптомна гіперурикемія є поширеним станом, що сприяє розвитку багатьох коморбідних станів. Масштабне дослідження в популяції США показало, що в 2015-2016 рр. поширеність гіперурикемії становила 20,2%, тоді як подагри – 3,9% [4]. Сьогодні відомо, що як подагра, так і безсимптомна гіперурикемія асоціюються з підвищеним ризиком розвитку метаболічного синдрому, цукрового діабету та серцево-судинних захворювань (ССЗ), включаючи артеріальну гіпертензію, ішемічну хворобу серця (ІХС), серцеву недостатність (СН).
Гіперурикемія та подагра. Ризик розвитку СН і віддалена смертність: нові дані дослідження NHANES
Попередні дослідження свідчать про те, що гіперурикемія і подагра асоційовані з підвищеним ризиком СН. Це пов’язують з посиленим розпадом пуринів та окислювальним стресом [5, 6]. З іншого боку, окислювальний стрес, ендотеліальна дисфункція, запалення та інсулінорезистентність можуть частково пояснити збільшення частоти СН у популяції людей з гіперурикемією і подагрою [7, 8].
У 2001-2018 рр. у США проводилося масштабне Національне опитування здоров’я та харчування (NHANES). Зокрема, вивчалися метаболічні чинники ССЗ. Нещодавно китайські автори провели новий аналіз даних дослідження NHANES, застосовуючи сучасні методи статистичної обробки даних, для вивчення зв’язку між гіперурикемією, подагрою та СН [9]. Гіперурикемія визначалася як рівень СК ≥420 мкмоль/л (7 мг/дл) у чоловіків і ≥360 мкмоль/л (6 мг/дл) у жінок. Також досліджували вплив гіперурикемії та подагри на віддалену смертність пацієнтів із СН.
До аналізу залучили дві когорти учасників дослідження NHANES за 2001-2018 (204 179 060 учасників) і за 2007-2018 рр. (223 702 171 учасник), з яких 40 044 228 (19,6%) мали гіперурикемію, 9 158 600 (4,1%) – подагру. Літній вік, діабет, інсульт, ІХС виявилися факторами ризику розвитку СН у пацієнтів із гіперурикемією та подагрою. Було показано, що пацієнти з гіперурикемією або подагрою мали вищу ймовірність розвитку СН: у 2,46 і 2,35 раза відповідно. Також наявність підвищеного рівня СК або подагри збільшувала ризики розвитку ІХС (у 1,33 та 1,85 раза відповідно), інсульту (в 1,43 та 1,63 раза відповідно) з урахуванням поправок на вік, стать, расу, індекс маси тіла.
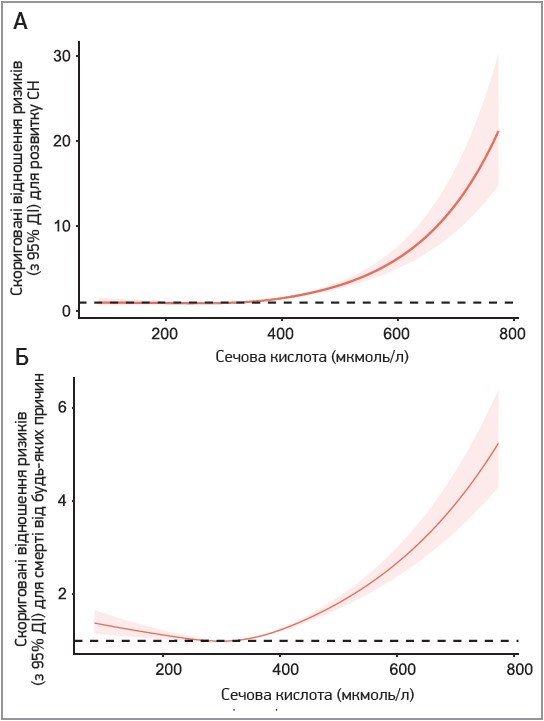
Співвідношення між рівнем СК і ризиком розвитку СН представлено на рисунку 1A. Було встановлено, що рівні СК позитивно асоціювалися з ризиком СН у людей віком ≥20 років і показали нелінійну кореляцію (p<0,001). Співвідношення між рівнем СК і ризиком смертності від усіх причин представлено на рисунку 1Б. Виявлено J-подібний зв’язок між рівнем СК і смертністю від усіх причин (p<0,001).
Рис. 1. Залежність між рівнем СК (мкмоль/л) і ризиком СН, виявлена за допомогою моделі обмеженого кубічного сплайну (А); залежність між рівнем СК (мкмоль/л) і смертністю від усіх причин, виявлена за допомогою обмеженої моделі кубічного сплайну (Б)
Примітка: модель була скоригована з урахуванням віку, статі, раси й індексу маси тіла; ДІ – довірчий інтервал.
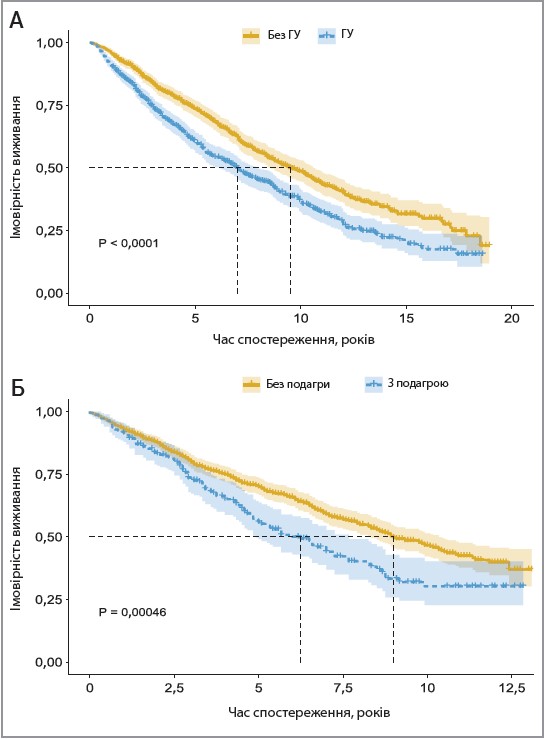
Криві виживаності Каплана – Мейєра для пацієнтів із СН наведено на рисунку 2. Показник 5-річної виживаності становив 59,9% у групі хворих із СН і гіперурикемією, а також 55,9% у групі СН + подагра. Середня виживаність складала 7 років і 6,25 року відповідно. У групах СН + гіперурикемія та СН + подагра було зареєстровано статистично вищу смертність від усіх причин порівняно з групами учасників із СН без гіперурикемії або подагри.
Рис. 2. Криві виживаності Каплана – Мейєра, які демонструють смертність від усіх причин у пацієнтів із СН, ускладненою гіперурикемією (А) або подагрою (Б)
Отже, в межах масштабного дослідження NHANES [9] було отримано важливі для охорони здоров’я результати щодо зв’язків гіперурикемії та подагри з розвитком СН і смертністю. В амбулаторних пацієнтів із гіперурикемією чи подагрою в 2,46 та 2,35 раза частіше виникала СН. У хворих із СН і гіперурикемією або подагрою в 1,37 та 1,45 раза спостерігалася більша ймовірність смерті від усіх причин у довгостроковому періоді спостереження порівняно з тими, хто не мав гіперурикемії або подагри. Таким чином, у клінічній практиці слід звертати увагу на рівні СК і суглобові симптоми в пацієнтів із СН. З іншого боку, в разі встановлення діагнозу подагри необхідно оцінити серцево-судинні ризики та розглянути питання про початок уратзнижувальної терапії (УЗТ).
Лікування до цілі. Принципи та можливості сучасної УЗТ
Згідно із сучасними експертними настановами, основа лікування подагри – довготривала УЗТ, спрямована на досягнення та підтримання цільового рівня СК у сироватці крові <357 мкмоль/л (або <6,0 мг/дл). Ця стратегія отримала назву «лікування до цілі» та наразі є загальновизнаною. Європейською протиревматичною лігою (EULAR) та Американською колегією ревматології (ACR) УЗТ рекомендовано хворим із діагностованою подагрою, котрі перенесли щонайменше 2 напади гострого артриту на рік, а також за наявності тофусів, хронічної подагричної артропатії, нефролітіазу, коморбідних станів, наприклад ССЗ, хронічної хвороби нирок [10, 11]. Важливо пояснити хворому, що після досягнення цільового сироваткового рівня уратів УЗТ слід продовжити, лікування зазвичай є пожиттєвим.
Що стосується безсимптомної гіперурикемії, то єдиний підхід відсутній. EULAR та ACR не рекомендують розпочинати УЗТ таким пацієнтам. Однак, за даними епідеміологічних досліджень, гіперурикемія визнається незалежним фактором серцево-судинного ризику. Зокрема, опубліковане в 2021 р. дослідження CARDIA показало, що чоловіки та жінки, в яких рівень СК був підвищеним на початку спостереження та зростав найвищими темпами протягом наступних 20 років життя (від 7,57 і 5,60 мг/дл у перший рік до 8,38 і 6,95 мг/дл відповідно в чоловіків і жінок), мали 2,89-кратне збільшення ризику розвитку серцевих захворювань, СН або цереброваскулярних подій порівняно з тими, чий рівень СК залишався в межах норми (до 6 мг/дл) [12]. Паралельно накопичуються експериментальні докази того, що гіперурикемія сприяє прогресуванню ССЗ, оскільки відкладення уратів у тканинах і внутрішньоклітинне накопичення СК спричиняють хронічне запалення [13, 14]. З іншого боку, встановлено, що УЗТ покращує функції артеріального ендотелію та знижує рівень системного запалення, наявного у хворих на подагру навіть у періоди між загостреннями [15]. Таким чином, ранній початок УЗТ може бути корисним як із погляду контролю загострень подагри, так і з метою профілактики майбутніх ускладнень з боку серцево-судинної системи, нирок [16]. З урахуванням цього деякі національні експертні асоціації, наприклад у Японії, уже пропонують лікувати безсимптомну гіперурикемію, коли рівень СК ≥536 мкмоль/л (9 мг/дл) [17].
Вибір інгібітора ксантиноксидази
Згідно з експертними рекомендаціями, УЗТ слід розпочинати із препаратів, які блокують фермент ксантиноксидазу, перешкоджаючи в такий спосіб продукуванню СК [10, 11]. До інгібіторів ксантиноксидази належать алопуринол і фебуксостат. Алопуринол тривалий час залишався найзастосовуванішим препаратом для проведення УЗТ через цінову доступність і добре вивчені профілі ефективності й безпеки. До недоліків алопуринолу належать підвищений ризик побічних реакцій з боку шкіри, тривалий процес титрування для досягнення ефективної дози, неефективність у пацієнтів зі зниженою функцією нирок.
Сучасним засобом для довготривалої УЗТ є селективний інгібітор ксантиноксидази фебуксостат. Підвищена вибірковість дії на фермент ксантиноксидазу та відмінна від пуринів структура фебуксостату пояснюють нижчу частоту побічних явищ і можливість його застосування навіть після реакцій гіперчутливості до алопуринолу [18].
Дані численних клінічних досліджень демонструють ключові переваги фебуксостату:
- простий підбір дози (80 мг для всіх пацієнтів, 120 мг – у разі недостатньої ефективності початкової дози);
- швидше досягнення та краще утримання цільових рівнів СК у пацієнтів із подагрою порівняно з алопуринолом [19, 20];
- збереження ефективності щодо зниження СК при зниженій функції нирок;
- нефропротекторний ефект – здатність стримувати прогресування ниркової дисфункції [21, 22].
У деяких дослідженнях вивчали потенційні кардіопротекторні ефекти фебуксостату. Перші порівняння двох інгібіторів ксантиноксидази в пацієнтів із високим серцево-судинним ризиком – у дослідженнях CARES [23] та FAST [24] – показали, що терапія алопуринолом і фебуксостатом була однаково безпечною для серцево-судинної системи.
У японському дослідженні FREED [25] порівнювали частоту церебральних, серцево-судинних і ниркових подій у хворих із гіперурикемією, які отримували фебуксостат, і тих, хто одержував традиційну терапію алопуринолом з модифікацією способу життя. Загалом у дослідженні взяли участь 1070 пацієнтів літнього віку із СК від >7,0 до ≤9,0 мг/дл і підвищеним ризиком розвитку церебральних, серцево-судинних або ниркових захворювань, що визначався наявністю гіпертензії, цукрового діабету 2 типу, захворюваннями нирок або обтяженим анамнезом. Пацієнтів розподілили до груп лікування фебуксостатом або алопуринолом та спостерігали протягом 36 міс. У результаті досягнутий рівень СК становив 4,50±1,52 мг/дл у групі фебуксостату та 6,76±1,45 мг/дл у групі традиційної терапії алопуринолом (p<0,001). Застосування фебуксостату асоціювалось зі значущим зниженням частоти комбінованої кінцевої точки, яка включала церебральні, серцеві та ниркові події (23,3 проти 28,7%; р=0,02) [25]. Потенційні кардіо- та нефропротекторні властивості фебуксостату заслуговують на подальше вивчення з огляду на зростання поширеності гіперурикемії у популяції та експериментально доведені зв’язки підвищеного рівня СК із розвитком і прогресуванням ССЗ.
Подафеб (АТ «Київський вітамінний завод») – єдиний фебуксостат українського виробництва повного циклу. Одна таблетка Подафебу містить 80 або 120 мг фебуксостату. Подафеб показаний для лікування хронічної гіперурикемії при захворюваннях, що супроводжуються відкладанням кристалів уратів, у т. ч. за наявності тофусів та/або подагричного артриту на цей час або в анамнезі. Рекомендована доза становить 80 мг 1 р/добу перорально (незалежно від прийому їжі). Ефект лікарського засобу спостерігається досить швидко, що робить можливим повторне визначення концентрації СК через 2 тиж. Якщо концентрація СК у сироватці крові перевищує 6 мг/дл (357 мкмоль/л) після 2-4 тиж лікування, слід розглянути підвищення дози до 120 мг 1 р/добу. Метою лікування є зменшення концентрації СК у сироватці крові та підтримання її на рівні <6 мг/дл (357 мкмоль/л). Рекомендована тривалість прийому для профілактики нападів подагри, відповідно до інструкції, становить не менше 6 міс, а згідно з експертними рекомендаціями, УЗТ має бути тривалою та пожиттєвою.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 4 (565), 2024 р
СТАТТІ ЗА ТЕМОЮ Ревматологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Серед препаратів, які мають велику доказову базу щодо лікування пацієнтів із захворюваннями дихальних шляхів з алергічним компонентом, особливий інтерес становлять антагоністи лейкотрієнових рецепторів (АЛТР). Ці препарати мають хорошу переносимість у дорослих та дітей, а також, на відміну від інгаляційних кортикостероїдів (ІКС), характеризуються високим комплаєнсом, тому посідають чільне місце в лікуванні пацієнтів із респіраторною патологією. У лютому відбувся міждисциплінарний конгрес із міжнародною участю «Життя без алергії International» за участю провідних вітчизняних міжнародних експертів. Слово мав президент Асоціації алергологів України, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Зайков із доповіддю «Місце АЛТР у лікуванні пацієнтів із респіраторною патологією». ...
Розбір клінічного випадку...