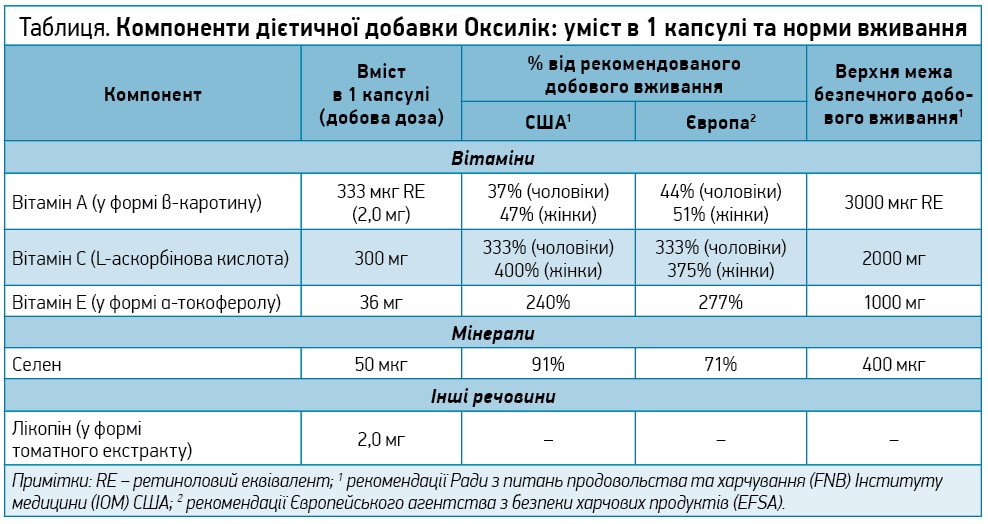
Антиоксидантний захист щитоподібної залози – запорука здоров’я всього тіла
Щитоподібна залоза (ЩЗ) – унікальний ендокринний орган, який впливає на кожну клітину організму. Тиреоїдні гормони підтримують нормальну роботу травної, кардіоваскулярної, нервової, кістково-м’язової, репродуктивної та імунної систем, а в разі зміни рівнів можуть порушувати їх функціонування [1-5]. Особливістю ЩЗ є найвищий серед усіх внутрішніх органів уміст йоду та селену [6], а також високий рівень фізіологічних окислювальних реакцій і водночас висока сприйнятливість до окислювального пошкодження [7]. Зниження рівнів антиоксидантів й окислювальний стрес, які погіршуються за дефіциту селену, можуть пошкоджувати тканину ЩЗ із подальшою появою клінічного гіпер- або гіпотиреозу, розвитком супутніх захворювань і погіршенням якості життя [8-11].
Як окислювальний стрес пошкоджує ЩЗ?
Окислювальні реакції відбуваються в усіх органах і тканинах, але в ЩЗ вони є необхідними для синтезу гормонів [12]. Установлено, що в ЩЗ фізіологічно утворюється величезна кількість активних форм кисню (АФК), особливо перекису водню (H2O2); це пояснює вислів про те, що ЩЗ є органом «окисної природи» [13, 14]. Крім H2O2, в синтезі гормонів ЩЗ беруть участь також інші вільні радикали та реакційно активні речовини, утворені із залишків йоду чи тирозину [15, 16]. У фізіологічних умовах існує баланс між утворенням і детоксикацією вільних радикалів. Для підтримання цього балансу ЩЗ еволюційно виробила ефективні захисні механізми, що включають антиоксидантні молекули та процес компартменталізації потенційно токсичних молекул [17]. Однак за окислювального стресу, спричиненого екзогенними чи ендогенними прооксидантами (іонізуючим випромінюванням, дефіцитом антиоксидантів тощо), відбувається підвищене пошкодження макромолекул ЩЗ, що може зумовити різні захворювання ЩЗ (включно з раком) [18-21].
Окислювальний стрес ЩЗ невід’ємно пов’язаний із запаленням цього органа. АФК й інші вільні радикали чинять прозапальний ефект на ЩЗ, а також, навпаки, запалення внаслідок зміни рівнів тиреоїдних гормонів і цитокінів зумовлює окислювальний стрес, порушує функцію ЩЗ і пригнічує гіпофізарно-тиреоїдну вісь [22, 23]. На тканинному рівні гіпотиреоз підсилює окислювальний стрес, що, своєю чергою, погіршує гіпотиреоз через інгібування дейодинази, тобто утворюється хибне коло (рис. 1) [24].
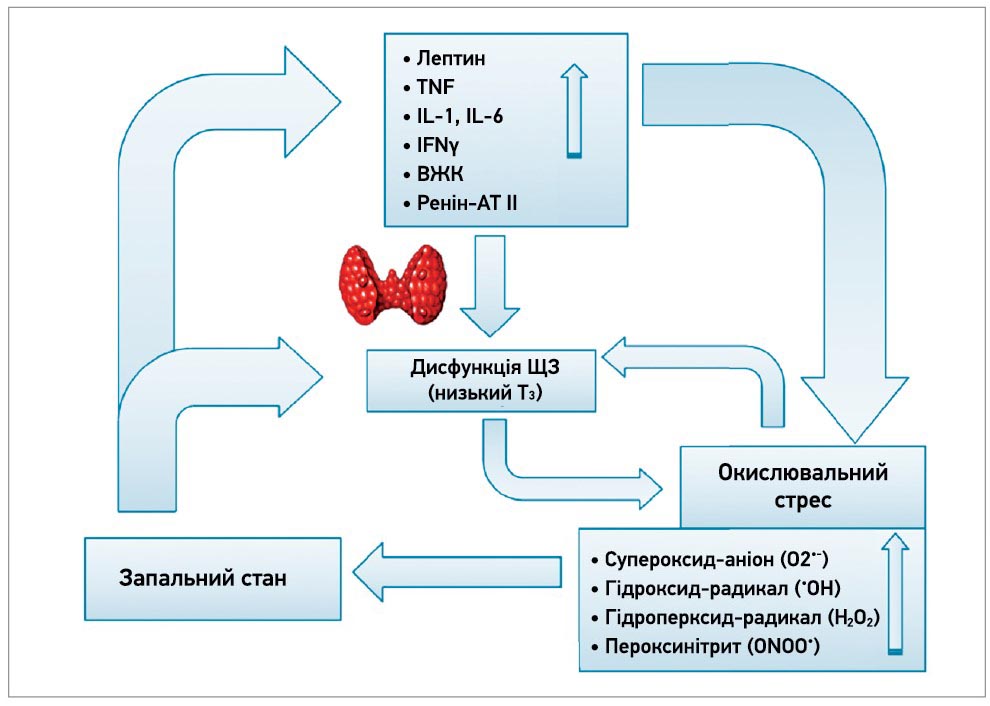 Рис. 1. Модель взаємозв’язку між окислювальним стресом, запаленням і порушенням функції ЩЗ
Рис. 1. Модель взаємозв’язку між окислювальним стресом, запаленням і порушенням функції ЩЗ
Примітки: АТ – ангіотензин; ВЖК – вільні жирні кислоти; IFN – інтерферон; IL – інтерлейкін; TNF – фактор некрозу пухлини.
Дефіцит селену
Окремим фактором окислювального стресу ЩЗ є дефіцит селену (Se) [25-27]. Cеленопротеїни мають вирішальне значення для антиоксидантного захисту ЩЗ, синтезу тиреоїдних гормонів і глобальної цілісності тироцитів, оскільки вони присутні в антиоксидантних ферментах, як-от глутатіонпероксидаза, тіоредоксинредуктаза й дейодиназа. За експериментального виснаження селенопротеїнів у ЩЗ очікувано з’являлося підвищене окислювальне пошкодження мембранних ліпідів, білків і ДНК [28].
Головна причина селенодефіцитних станів – недостатнє надходження цього мікроелемента з їжею через його низький уміст у ґрунті сільськогосподарських угідь [29]. Слід зазначити, що проблема дефіциту селену (як і йоду) характерна для всіх територій нашої планети, віддалених від Світового океану, що пов’язано з вимиванням цих мікроелементів із верхніх шарів ґрунту під час танення льодовиків [30]. Установлено, що в деяких регіонах із тяжким йододефіцитом супутній дефіцит Se підвищує тяжкість гіпотиреозу та спричиняє мікседематозний кретинізм [31, 32]. Водночас показано, що адекватне забезпечення Se захищає ЩЗ від пошкодження на тлі надлишку призначеного йоду в умовах співіснування обох дефіцитів [33, 34].
В Україні недостатнє забезпечення Se зареєстровано практично в усіх регіонах, але найвираженіший дефіцит спостерігають у Волинській, Сумській, Харківській і Київській областях [29, 35]. З огляду на це особливої актуальності набуває проблема забруднення довкілля. Зокрема, доведено, що підвищений вплив деяких токсикантів (свинець, кадмій, ртуть, миш’як, алюміній) спричиняє дефіцит Se через порушення його всмоктування (зокрема, в ланцюгу живлення ґрунт – рослина – тварина) [36]. Останнім часом дефіцит цього мікроелемента пов’язують також зі зміною структури харчування українців, меншим споживанням м’яса, риби й інших морських продуктів, які разом із зерновими є основним джерелом Se [37]. При цьому внаслідок технологічної переробки продуктів дефіцит Se в них посилюється [38].
Дефіцит антиоксидантних вітамінів
Доведено, що за більшості хвороб ЩЗ спостерігають низькі рівні антиоксидантних вітамінів А, С, Е [39].
Вітамін А є потужним антиоксидантом і діє як поглинач вільних радикалів (самостійно, а також у складі великої ферментної системи). Дефіцит вітаміну А чинить негативний вплив на функцію ЩЗ, зокрема може спричиняти розвиток гіпертиреозу – гіперметаболічного стану, що супроводжується збільшенням загального споживання кисню, утворенню АФК, а також інших вільних радикалів [40, 41].
Знижений рівень вітаміну Е при захворюваннях ЩЗ зумовлений його використанням для запобігання пошкодженню вільними радикалами, вираженому в пацієнтів із дисфункцією ЩЗ [42]. Також установлено, що вітамін Е діє як поглинач АФК при дисфункції фолікулярних клітин ЩЗ [43]. Інші дослідження продемонстрували, що АФК пригнічують активність ферменту, відповідального за перетворення Т4 на активний гормон Т3, і що достатній рівень вітаміну Е може пом’якшити цей ефект [44, 45].
Вітамін С – потужний природний антиоксидант, здатний знешкоджувати АФК шляхом їх відновлення до стабільніших сполук [46]. За окислювального стресу (особливо при гіпертиреозі) вітамін С надмірно окислюється та втрачає свої антиоксидантні властивості [40].
Синдром низького Т3
Сьогодні дедалі більшу увагу науковців привертає т. зв. еутиреоїдний хворобливий синдром, або синдром низького Т3 (СНТ3), – стан, який характеризується зниженою периферичною конверсією Т4 у Т3 за нормальної секреції тиреоїдних гормонів [24]. СНТ3 асоціюється з такими станами, як голодування, ожиріння, стресові розлади, синдром хронічної втоми, надмірні фізичні навантаження, депресія тощо [46-50]. СНТ3 також можуть зумовлювати певні лікарські засоби, зокрема кортикостероїди, естрогени, оральні контрацептиви, ацетилсаліцилова кислота тощо [51-53].
Згідно із сучасною концепцією, за своєю суттю СНТ3 є гіпотиреозом на тканинному рівні, спричиненим внутрішньоклітинним і системним окислювальним стресом (рис. 2).
 Рис. 2. Як гіпер-, так і гіпотиреоз можуть зумовлювати оксилювальний стрес із різними механізмами
Рис. 2. Як гіпер-, так і гіпотиреоз можуть зумовлювати оксилювальний стрес із різними механізмами
Примітки: АФК – активні форми кисню; АФА – активні форми азоту; NO – оксид азоту; МДА – малоновий діальдегід; PON‑1 – параоксоназа‑1; ЗАА – загальна антиоксидантна активність.
Оскільки тиреоїдні гормони підвищують продукцію АФК, при гострому окислювальному пошкодженні СНТ3 може бути адаптивним механізмом. Але якщо окислювальний стрес триває, СНТ3 швидко стає дезадаптивним і підтримує дисфункцію ЩЗ. На відміну від справжнього гіпотиреозу при СНТ3 замісна гормональна терапія зазвичай не потрібна, натомість доцільним є застосування вітамінно-мінеральних комплексів із Se [24].
Синергічна дія Se й антиоксидантних вітамінів
Завдяки визнанню ключової ролі окислювального стресу в патології ЩЗ останніми роками в тиреоїдології широко застосовують спеціальні дієтичні добавки – вітамінно-мінеральні комплекси, що містять Se, вітаміни-антиоксиданти (А, С, Е) й інші речовини, для захисту клітин ЩЗ, профілактики автоімунних порушень, гіпо- та гіпертиреозу, онкопатології ЩЗ [54]. Установлено, що за вираженого окислювального стресу Se-вмісні ферменти працюють на межі своїх можливостей; призначення Se не завжди забезпечує подальше підвищення їхньої активності. Водночас додавання до Se антиоксидантних вітамінів створює сприятливий «клімат» на рівні ферментів і в цей спосіб потенціює дію Se [55]. Крім того, вітамін Е разом із Se-вмісним ферментом глутатіонпероксидазою підтримує цілісність клітинних мембран і бере участь у відновлювальних реакціях із глутатіоном [56].
У нещодавньому дослідженні також було продемонстровано, що комбінація лікопіну (каротиноїд томатів), вітаміну Е, вітаміну С та β-каротину (провітаміну А) має антиоксидантні властивості, котрі перевищують такі арифметичної суми окремих компонентів, тобто досягається виражений синергічний ефект [57].
Додаткові джерела Se – органічні чи неорганічні?
У природі та живих організмах Se присутній в органічній і неорганічний формах; його головними органічними формами є селенометіонін і селеноцистеїн [58]. Неорганічні форми представлені селенітом, селенідом, селенатом і елементарним Se.
Серед харчових продуктів найбільше Se містять бразильські горіхи (6-8 горіхів = 989% добової норми), морепродукти (тунець, сардина, устриці), м’ясні субпродукти та яйця; менша кількість Se також присутня в інших горіхах, м’ясі (свинина, яловичина, курятина), цільнозернових і молочних продуктах, бобових [59-63]. Питна вода не є значущим джерелом Se в більшості регіонів світу [64, 65].
У західних країнах дуже популярними є дієтичні добавки із Se; наприклад, у США їх уживають 18-19% дорослих і дітей [66]. Ці добавки можуть містити органічний Se (часто у формі селенометіоніну чи збагачених Se дріжджів) або неорганічні солі Se – селенат або селеніт натрію. Вважають, що органічні форми Se всмоктуються краще, ніж неорганічні, проте наукові дані щодо порівняльної біодоступності різних форм Se в людини досить обмежені [67]. За даними Ради з питань продовольства та харчування Інституту медицини США (FNB), біодоступність селенометіоніну становить >90%, селеніту натрію – >50%, селенату натрію – близько 100% [68]. Водночас селенометіонін і селеніт натрію більшою мірою утримуються в організмі, а селенат натрію легше виводиться із сечею.
Se є мікроелементом із вузьким «терапевтичним вікном», що може нести як користь (за вживання в адекватних кількостях), так і шкоду (в разі перевищення дози чи накопичення в організмі) [69]. З огляду на це органічні форми Se можуть бути менш безпечними через ризик кумуляції. Ще однією проблемою є те, що зазвичай джерело селенометіоніну в дієтичних добавках – дріжджі, котрі вирощують у збагаченому Se середовищі [70]. У нещодавньому дослідженні в селенових дріжджах, окрім селенометіоніну, було виявлено додатково понад 60 різних Se-вмісних сполук, зокрема >20 метаболітів, про котрі раніше не повідомлялося [71]. Невідомо, які біологічні ефекти матимуть ці сполуки при вживанні людиною. Крім того, характер накопичення Se в різних штамах дріжджів дуже різний, тому продукти на їхній основі можуть значно відрізнятися за низкою параметрів, як-от термін зберігання, біодоступність і токсичність, і їх практично неможливо стандартизувати [70]. Загалом регуляторні органи, зокрема FNB [72] та EFSA (Європейський Союз) [73], у рекомендаціях щодо вживання Se не зазначають переваг певної форми, але з огляду на вищенаведені дані неорганічні форми (особливо селенат натрію) можна вважати безпечнішими. Між іншим, дитячі молочні суміші в більшості країн містять саме неорганічні форми Se [74].
Оксилік – антиоксидантна формула для захисту ЩЗ і всього організму
Дієтична добавка Оксилік – унікальний продукт німецької компанії Woerwag Pharma, спеціально розроблений для захисту клітин організму від окислювального стресу [75]. Оксилік містить Se (у формі селенату натрію), посилений іншими потужними антиоксидантами – вітамінами А, С, Е й лікопіном, завдяки чому захищає від окислювального стресу ЩЗ, підтримує природну захисну систему та сприяє здоров’ю всього тіла.
Дози компонентів Оксиліку підібрані для максимальної безпеки й за умови застосування відповідно до інструкції є значно нижчими від верхньої межі безпечного добового вживання (табл.). Форма Se (селенат натрію) характеризується високою біодоступністю й низьким ризиком кумуляції, а стандартизована доза цього мінералу (50 мкг, 71-91% від добової потреби) підібрана так, щоби забезпечувати організм Se з урахуванням Se, що надходить з їжею. Підвищені дози вітамінів С та Е узгоджуються з даними досліджень [76-79], у яких було продемонстровано позитивний вплив таких доз на функцію ЩЗ, і при цьому є цілком безпечними. Формула Оксиліку посилена лікопіном – найпотужнішим серед відомих каротиноїдів антиоксидантом із нейропротекторними, протипухлинними, протизапальними, гіпохолестеринемічними та прокогнітивними властивостями [80].
Оксилік рекомендовано вживати дорослим по 1 капсулі 1 р/добу під час прийому їжі, тривалість курсу становить 1-3 міс або за порадою лікаря.
Список літератури знаходиться в редакції.
Підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 2 (495), 2021 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
21 березня в рамках II Міжнародної школи «Сучасний лікар: від теорії до практики» професор кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, лікар-ендокринолог вищої категорії, доктор медичних наук Вікторія Олександрівна Сергієнко представила доповідь, присвячену хронічним ускладненням цукрового діабету (ЦД). Зокрема, було акцентовано увагу на причинах розвитку діабетичної полінейропатії (ДП), розглянуто клінічні варіанти цього ускладнення, діагностичні підходи та основні принципи лікування. Пропонуємо огляд цієї доповіді у форматі «запитання – відповідь»....
Останніми десятиліттями в усьому світі спостерігалося значне зростання поширеності цукрового діабету (ЦД), що зумовило серйозні наслідки стосовно якості життя населення, а також спричинило певний тягар для системи охорони здоров’я та економічні витрати [1]. За даними Діабетичного атласу Міжнародної діабетичної федерації (International Diabetes Federation Diabetes Atlas), у 2021 р. ≈537 млн людей мали ЦД і, за прогнозами, до 2045 р. цей показник досягне 783 млн [2]. Значна захворюваність і підвищена смертність асоційовані з пов’язаними із ЦД макросудинними (інфаркт міокарда, інсульт) і мікросудинними (сліпота, ниркова недостатність, ампутації) ускладненнями [3]....
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....