Ехокардіографія (частина 2)
Частина 1 Частина 2
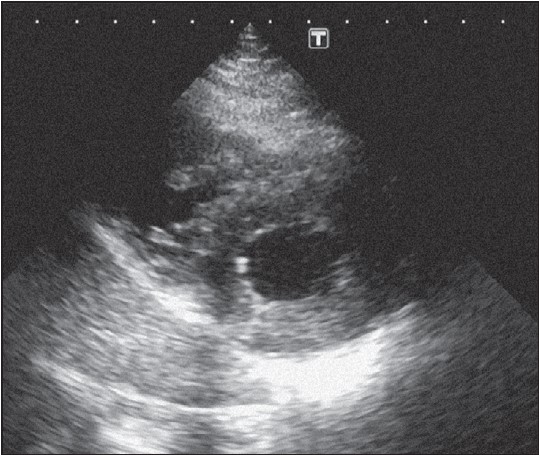
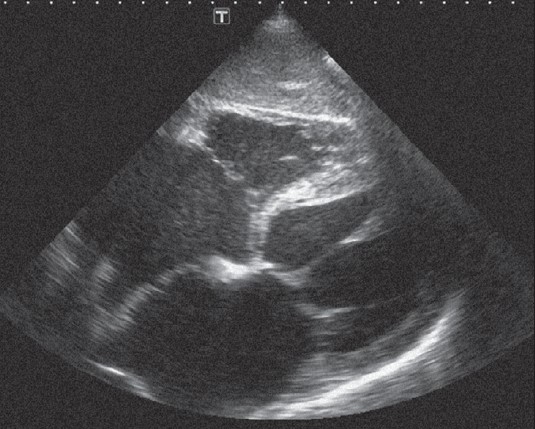
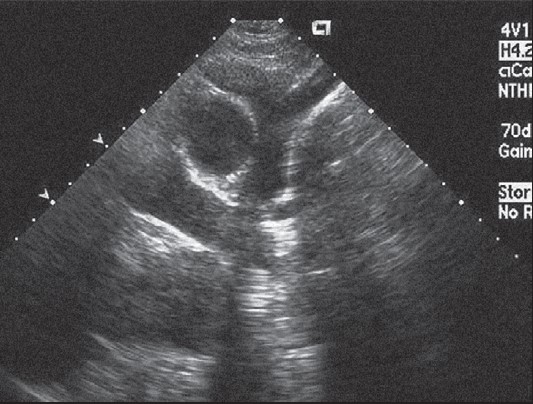
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9).
Рис. 22.9. Парастернальне зображення по короткій осі на рівні верхівки
Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи.
Верхівкові зображення
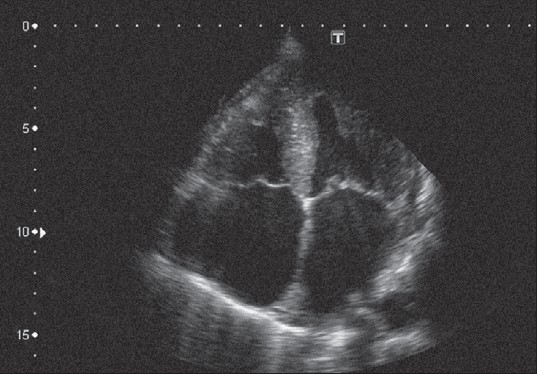
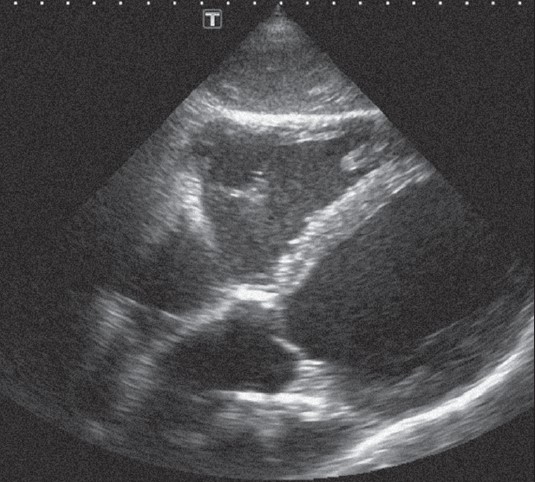
Продовжують двовимірне ультразвукове дослідження серця, перемістивши датчик на верхівку і зорієнтувавши площину скенування так, щоб отримати переріз через усі чотири камери (рис. 22.10). Пацієнт лежить на лівому боці, а датчик прикладають над верхівковим поштовхом і «націлюють» його на праву лопатку.
Рис. 22.10. Верхівкове чотирикамерне зображення серця (угорі - шлуночки серця, внизу — передсердя; справа - ліві відділи, зліва - праві відділи серця)
Хоча технічні можливості сучасної ультразвукової апаратури дозволяють розміщувати зображення на екрані в різний спосіб, традиційним є положення верхівкою серця догори (що ближче структура до датчика, то вище її зображення на екрані). На цьому зображенні правий шлуночок вдається відрізнити від лівого за такими ознаками:
- Перегородкова (септальна) стулка тристулкового клапана прикріплюється до стінки серця трохи глибше, тобто ближче до верхівки, ніж передня стулка мітрального клапана.
- У порожнині правого шлуночка видно так званий надшлуночковий гребінь (модераторний пучок), якого немає в лівому шлуночку.
- У правому шлуночку набагато виразніша трабекулярність.
Нижче на зображенні за лівим передсердям можна побачити низхідний відділ аорти (переріз по короткій осі), а також нижні легеневі вени, що впадають у ліве передсердя (Otto, 2013).
За такого положення датчика ультразвукові промені йдуть паралельно до міжшлуночкової та міжпередсердної перегородок. Остання є досить тонкою, особливо в центральній частині – ділянці овальної ямки. Чітка візуалізація будь-якої структури при УЗ-дослідженні досягається тоді, коли вона розміщена перпендикулярно до ходу променів. Коли ж структура розміщена паралельно, то її зображення буде менш чітким, а при незначній товщині – його взагалі не буде. Тому з верхівкового доступу на чотирикамерному зображенні часто здається, що немає центральної частини міжпередсердної перегородки. Щоб достовірно діагностувати дефект міжпередсердної перегородки, необхідно використовувати ще й інші підходи, зокрема підреберний (Lancellotti and Cosyns, 2016).
На верхівковому чотирикамерному зображенні отримуємо переріз нижньої частини МШП. Базальний сегмент цієї частини перегородки дістає кров з домінантної вінцевої артерії, що дає гілки до нижньої поверхні серця (це або права вінцева артерія, або обвідна гілка лівої вінцевої артерії). Верхівковий та середній сегменти перегородки дістають кров з іншої артерії, а саме з передньої низхідної гілки лівої вінцевої артерії. Бічна стінка лівого шлуночка, яку видно на цьому зображенні, кровопостачається обвідною гілкою. Якщо коронарний кровоплин порушено, то видно погіршення функції власне того сегмента, який живиться критично звуженою або перекритою вінцевою артерією. Тому при значному стенозі низхідної гілки лівої вінцевої артерії скоротливість базального сегмента перегородки не буде погіршуватися, тоді як верхівковий і середній сегменти стануть гіпокінетичними (Lancellotti and Cosyns, 2016).
При дослідженні з верхівкового підходу в реальному часі потрібно звернути увагу насамперед на рівномірність скорочення усіх стінок, а також на те, як рухаються стулки мітрального і тристулкового клапанів (Танасічук та співавт., 2015).
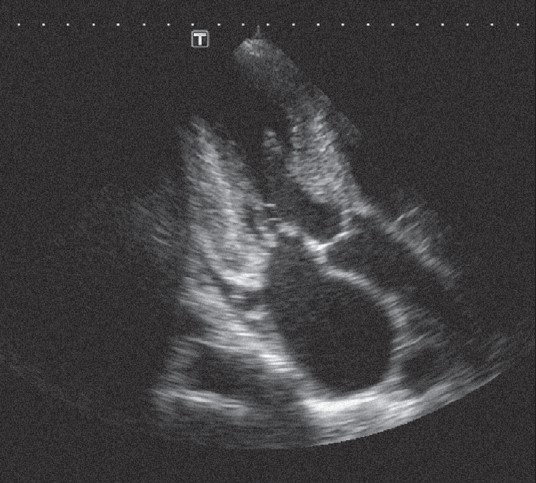
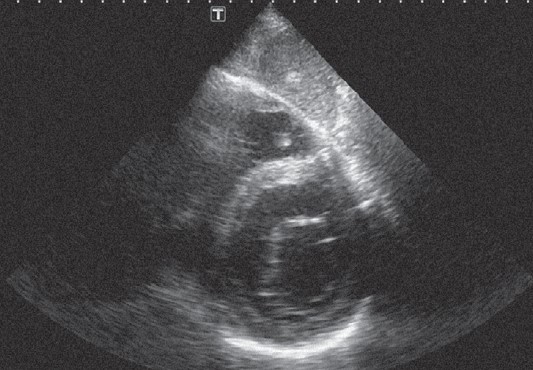
Якщо датчик залишити в цьому ж місці і повернути його за годинниковою стрілкою, то можна дістати верхівкове зображення лівого шлуночка по довгій осі (рис. 22.11).
Рисунок 22.11. Верхівкове зображення лівого шлуночка серця по довгій осі
Це зображення можна отримати ще й іншим способом: спочатку дістають парастернальне зображення лівого шлуночка по довгій осі, а потім пересувають датчик на верхівку серця, не змінюючи його нахил.
На екрані при такому зображенні верхівка лівого шлуночка розташована вгорі. У реальному часі можна оцінити роботу мітрального й аортального клапанів. Добре видно вихідний тракт лівого шлуночка, а також безпосереднє продовження нижньої стінки аорти в передню мітральну стулку, а верхньої стінки аорти – в МШП. За такої орієнтації площини скенування бачимо переріз передньої частини МШП, яка постачається кров’ю гілками від передньої міжшлуночкової артерії. Задня бічна стінка лівого шлуночка, яку видно на цьому перерізі, дістає кров або від обвідної гілки лівої вінцевої артерії, або від правої вінцевої артерії. Знову ж таки, в реальному часі звертаємо увагу на рівномірність скорочення всіх сегментів, як вони рівномірно потовщуються, рівномірно наближаються (Флакскампф, 2013).
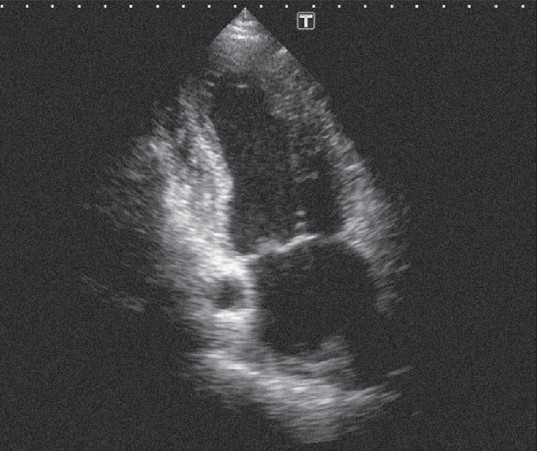
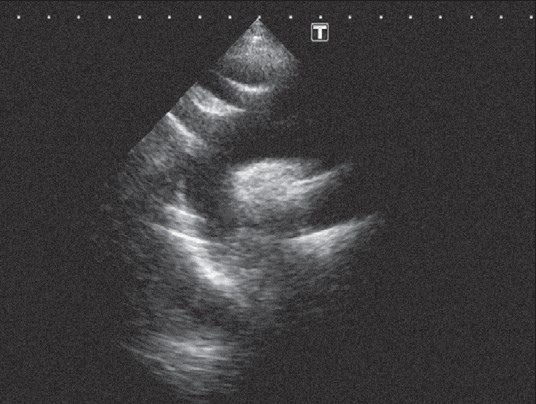
Якщо зберігати положення датчика в попередній позиції і далі повертати його за годинниковою стрілкою, нахиляючи при цьому площину скенування латеральніше, то можна отримати верхівкове двокамерне зображення (рис. 22.12). Угорі – лівий шлуночок, його відділяють від передсердя обидві мітральні стулки. Стінка шлуночка, що праворуч на екрані, є передньою, а та, що ліворуч, є нижньою (задньою діафрагмальною). Знову ж таки при дослідженні в реальному часі звертаємо увагу на рівномірність скорочення стінок.
Рис. 22.12. Верхівкове двокамерне зображення лівих відділів серця
Верхівкові ехокардіографічні зображення мають таке діагностичне значення:
- Розпізнавання вроджених вад серця в дітей та дорослих.
- Оцінювання сегментарної скоротливості міокарда за ішемічної хвороби.
- Визначення стану мітрального, аортального та тристулкового клапанів.
- Оцінка окремих сегментів стулок мітрального клапана.
Крім анатомічної оцінки цих клапанів, саме на верхівкових зображеннях найліпше проводити доплерівське визначення швидкостей кровоплину через них. Адже за такого скенування потоки крові будуть паралельними (або майже паралельними) до напрямку ультразвукових променів, що забезпечує високу точність доплерівських вимірювань. Тому, власне, при верхівковому розташуванні датчика виконують вимірювання швидкостей кровоплину і градієнтів тиску при мітральному стенозі, аортальному стенозі або тристулковій недостатності (Lancellotti and Cosyns, 2016).
Субкостальні зображення
Датчик ставлять в епігастральній ділянці, а площину скенування скеровують то вгору, щоб отримати зображення структур серця, то вниз, щоб візуалізувати великі судини, розташовані нижче: черевну аорту і нижню порожнисту вену з печінковими венами, що впадають у неї.
Насамперед з підреберного підходу отримують чотирикамерне зображення. Для цього площину скенування розміщують спочатку перпендикулярно до поверхні тіла, а потім нахиляють вгору.
Коли кут між датчиком і фронтальною площиною досягне 30‑40°, на екрані з’явиться зображення чотирьох камер серця. Вгорі екрана, вище від зображення серця, буде зображення паренхіми печінки (рис. 22.13). Верхівку серця із цього доступу зазвичай не видно (Feigenbaum et al., 2010).
Нахиляючи площину скенування ще вперед, отримують зображення аорти (рис. 22.14). Чіткої візуалізації аортального клапана із субкостального доступу часто досягають у хворих, у яких не вдавалося цього зробити з парастернального підходу. Особливо це стосується пацієнтів з емфіземою легень, вузькими міжреберними проміжками або ожирінням (Поташев, 2011). При обстеженні з підреберного підходу ультразвукові промені вже не йдуть паралельно до міжпередсердної перегородки, як при верхівковому підході.
На субкостальному чотирикамерному зображенні положення міжпередсердної перегородки щодо променів стає майже перпендикулярним. І тому саме із цього підходу найліпше видно міжпередсердну перегородку і дефекти в ній (Lancellotti and Cosyns, 2016).
Повернувши датчик так, щоб площина скенування стала перпендикулярно до положення, при якому отримано субкостальне чотирикамерне зображення, дістають перерізи серця по короткій осі (рис. 22.15). Вони аналогічні до зображень по короткій осі, отриманих із парастернального підходу.
Рис. 22.13. Субкостальне чотирикамерне зображення серця
Рис. 22.14. Субкостальне зображення чотирьох камер і аорти
Рис. 22.15. Субкостальне зображення по короткій осі на рівні морального клапана
Основні субкостальні зображення по короткій осі:
- Рівень папілярних м’язів.
- Рівень мітрального клапана.
- Рівень основи серця.
Субкостальний підхід дає змогу візуалізувати нижню порожнисту вену по її довгій осі. Для цього датчик ставлять в епі- гастральну ямку, а площину скенування орієнтують сагітально по серединній лінії, злегка нахиливши вправо. Тоді нижню порожнисту вену видно позаду від печінки. Також вдається побачити її місце злиття з правим передсердям, де іноді можна виявити так званий євстахієвий клапан.
На вдиху нижня порожниста вена частково спадається, а на видиху, коли зростає внутрішньогрудний тиск, вона стає ширшою. Обов’язково звертають увагу на ці нормальні респіраторні зміни ширини просвіту нижньої порожнистої вени. У випадку високого тиску в правому передсерді і високого діастолічного тиску в правому шлуночку (наприклад, констриктивний перикардит) діаметр нижньої порожнистої вени на вдиху і на видиху не змінюється (Otto, 2013).
Повертаючи і нахиляючи датчик так, ніби хочуть заглянути під праву лопатку, дістають зображення місця, де печінкові вени зливаються з нижньою порожнистою веною. Одночасно побачити всі три печінкові вени не вдається, бо вони не лежать в одній площині.
Якщо залишити датчик в епігастральній ямці, а площину скенування знову зорієнтувати сагітально, тільки дещо нахилити ліворуч, то можна отримати зображення черевного відділу аорти по її довгій осі. Завжди видно характерну пульсацію. Попереду від аорти легко візуалізувати верхню брижову артерію, яка відразу повертає донизу і йде майже паралельно з аортою. Повернувши площину скенування поперечно, можна дістати переріз обох цих судин по короткій осі. Нижня порожниста вена лежить праворуч від хребта, має форму, близьку до трикутника, на вдиху частково спадається. Аорта розташована ліворуч від хребта, виглядає як вузьке кільце і пульсує.
Супрастернальні зображення
Щоб отримати супрастернальні зображення серця і судин, датчик розміщують в яремній ямці, а площину скенування спочатку орієнтують так, як розташована дуга аорти: праворуч спереду – ліворуч назад. Ліворуч на екрані буде зображення висхідного відділу грудної аорти, а праворуч – початкова частина низхідного відділу. Під горизонтальною частиною грудної аорти (поперечний відділ дуги аорти) бачимо праву гілку легеневої артерії у перерізі по її короткій осі. У багатьох осіб вдається добре вивести відгалуження артеріальних гілок дуги аорти: плечоголовного стовбура, лівих сонної та підключичної артерій (Флакскампф, 2013).
Щоб краще розглянути весь висхідний відділ грудної аорти (включно з аортальним клапаном і частково лівим шлуночком), нахиляють площину скенування трохи вперед і вправо (рис. 22.16).
Рис. 22.16. Зображення дуги аорти, отримане із супрастернального підходу
Якщо площину скенування повертати за годинниковою стрілкою від тієї позиції, при якій розглядаємо дугу аорти, то можна отримати зображення, на якому буде видно поперечний переріз дуги аорти, тобто зображення по короткій осі. На цьому зображенні горизонтальний відділ дуги аорти має вигляд кільця. Праворуч від нього видно верхню порожнисту вену. Трубчаста структура під аортою – права гілка легеневої артерії по довгій осі, глибше – ліве передсердя (рис. 22.17). Часом вдається побачити місця впадіння всіх чотирьох легеневих вен у ліве передсердя.
Рис. 22.17. Супрастернальне зображення поперечного відділу дуги аорти по короткій осі
Поставивши датчик у правій надключичній ямці і скерувавши площину скенування вниз, можна візуалізувати всю верхню порожнисту вену: від злиття обох брахіоцефальних вен аж до впадіння у праве передсердя.
Отже, застосовуючи різні підходи і позиції датчика, можна отримати багато різних ультразвукових перерізів, що дають змогу дослідити анатомічну будову серця, розміри камер, взаємне розташування судин, які впадають у серце чи виходять із нього. Крім того, вдається оцінити, як працюють клапани і як скорочуються шлуночки.
Однак далеко не завжди вдається отримати якісні зображення при всіх ультразвукових перерізах з різних підходів. Якщо серце прикрите легенями, міжреберні проміжки вузькі, живіт великий з грубим шаром підшкірного жиру, а шия коротка і товста, то проведення ехокардіогра- фічного дослідження майже неможливе. Але з часом, як багатшає досвід і зростає вправність, кількість «ехо-непридатних» пацієнтів значно зменшується.
23. Одновимірна ехокардіографія
Одновимірна ехокардіографія, або М-спосіб (М-mode) – історично перший спосіб ультразвукового скенування. На серце посилають лише один промінь, який відбивається від його структур, поглинається ними або розсіюється. Датчик приймає відбитий промінь, передає сигнал в апарат, де відбувається аналіз.
Оброблену інформацію подають на екран у вигляді графіка, на якому по горизонталі зазначають час, а по вертикалі – відстань.
Тобто одновимірна ехокардіограма – це розгорнений у часі графік руху структур серця щодо одного променя, який скенує. Як самостійний метод одновимірне скенування нині не застосовують (Otto, 2013).
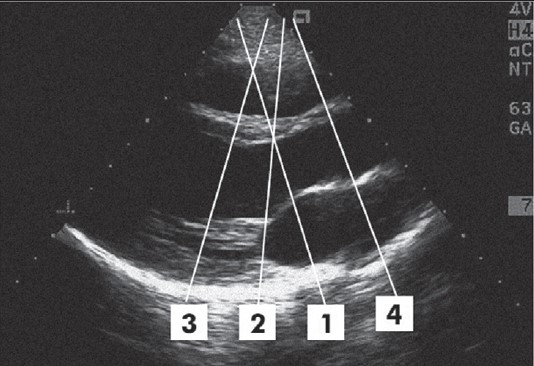
Основні зображення в одновимірному режимі легко вивести, показавши хід променя, що скенує, на двовимірному зображенні по довгій осі лівого шлуночка з парастернального підходу (рис. 23.1).
Рис. 23.1. Стандартні напрямки ходу променя у випадку одновимірного скенування
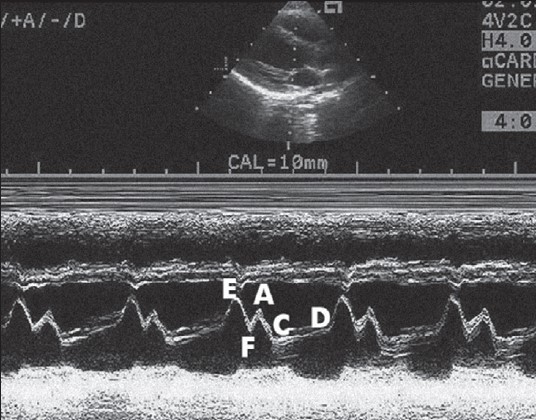
Якщо промінь при скенуванні проникає в серце по лінії 1, як це показано на рис. 23.1, то на графіку вгорі отримують зображення руху стінки правого шлуночка, нижче – міжшлуночкової перегородки, ще нижче видно характерний рух передньої стулки мітрального клапана, а найнижче – стінки лівого передсердя (рис. 23.2).
Рис. 23.2. Одновимірна ехокардіограма в першій позиції променя при одновимірному скенуванні. На лінії руху передньої стулки мітрального клапана буквами позначають точки: Е — пік ранньодіастолічного відкриття; F — середньодіастолічне прикриття; А — пізньодіастолічне відкриття, зумовлене систолою передсердя; С — точка систолічного змикання стулок мітрального клапана; D — початок діастолічного відкриття (закінчення систолічного змикання) стулок мітрального клапана. Відрізок CD — період систолічного змикання мітрального клапана
Передня мітральна стулка під час діастоли виписує М-подібну криву (відкриття – прикриття – відкриття), а під час систоли – косовисхідну лінію.
Коли ж, скенуючи, промінь посилають по лінії 2, то на відміну від попереднього зображення, нижче від передньої стулки мітрального клапана реєструється рух задньої мітральної стулки, що має вигляд букви W (рис. 23.3).
Рис. 23.3. Одновимірна ехокардіограма в 2-й позиції променя при одновимірному скенуванні. Стрілкою вказано рух задньої стулки МК у вигляді літери W
Під ним – зображення руху задньої стінки лівого шлуночка. Амплітуда руху (розмах) задньої стулки менша, ніж передньої (Feigenbaum et al., 2010].
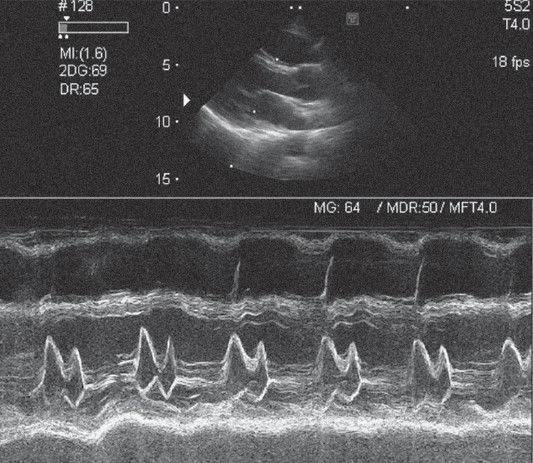
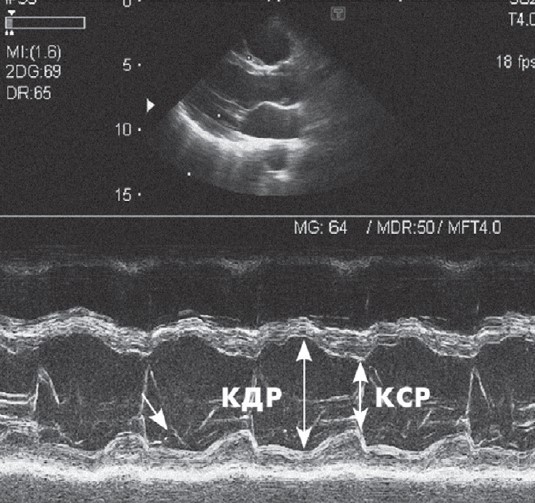
Третя позиція променя при скенуванні дозволяє отримати зображення (рис. 23.4), яке використовують для визначення розмірів шлуночків і розрахунку показників скоротливої здатності серця (Коваленко та співавт., 2012). Промінь для цього посилають через шлуночки таким чином, щоб він ішов перпендикулярно до міжшлуночкової перегородки і нижче від країв мітральних стулок, але вище від верхівок папілярних м’язів (Lang et al., 2015).
Рисунок 23.4. Одновимірна ехокар- діограма в третій позиції променя при одновимірному скенуванні. На цьому зображенні проводять визначення кінцевого систолічного і кінцевого діастолічного розмірів лівого шлуночка для розрахунків за формулою L. Teicholtz
Знаючи кінцевий діастолічний (КДР) та кінцевий систолічний (КСР) розміри лівого шлуночка, обчислюють його кінцевий діастолічний та кінцевий систолічний об’єми за формулою L. Teicholtz:
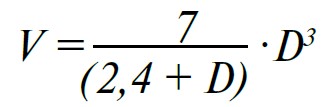
де V – об’єм, D – розмір (КДР чи КСР).
Показники скоротливої здатності лівого шлуночка
1. Фракційне вкорочення (fractional shortening, FS):
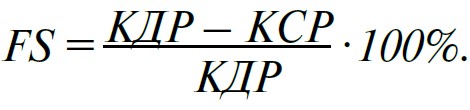
Норма – 28‑44%, у середньому – 36%.
2. Фракція викиду (ejection fraction, EF):
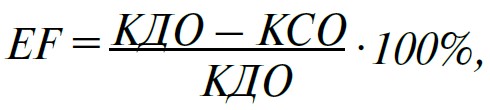
де КДО – кінцевий діастолічний об’єм, КСО – кінцевий систолічний об’єм.
Норма – 48‑78%, у середньому – 65%.
3. Швидкість циркулярного вкорочення волокон (circumferencial
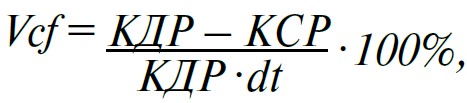
де dt – період вигнання крові з лівого шлуночка (відповідає часові, протягом якого аортальний клапан відкритий, і вимірюється за одновимірною ехокардіограмою при четвертій позиції променя, який скенує).
Норма становить 1,02‑1,94 с‑1, у середньому – 1,3 с‑1.
Значення норми ехокардіографічних параметрів для дорослих:
- Діастолічний розмір правого шлуночка – 0,9‑2,6 см (у середньому 1,8 см).
- Кінцевий діастолічний розмір лівого шлуночка – 3,5‑5,7 см (у середньому 4,7 см).
- Товщина задньої стінки лівого шлуночка – 0,6‑1,1 см (у середньому 0,9 см).
- Товщина міжшлуночкової перегородки – 0,6‑1,1 см (у середньому 9 см).
- Розмір лівого передсердя –1,94,0 см (у середньому 2,9 см).
- Діаметр кореня аорти – 2,03,7 см (у середньому 2,7 см).
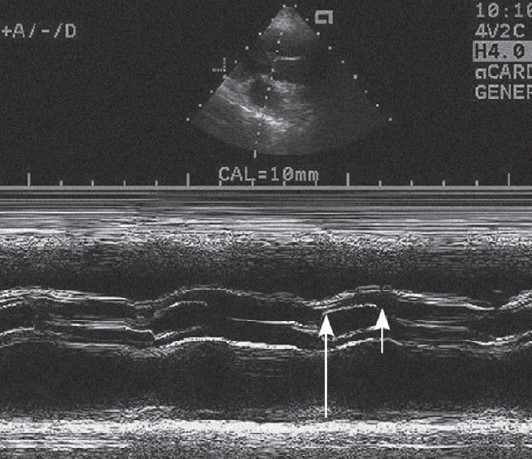
За четвертої позиції промінь, який скенує, скеровують через вихідний відділ правого шлуночка, корінь аорти і ліве передсердя (рис. 23.5). На цьому зображенні оцінюють рух стулок аортального клапана, а також визначають розмір кореня аорти і лівого передсердя.
Рис. 23.5. Одновимірна ехокардіо- грама в четвертій позиції променя при одновимірному скенуванні. Чітко видно момент відкриття аортального клапана (довга стрілка) і момент закриття (коротка стрілка). Часовий проміжок між стрілками відображає час вигнання крові з лівого шлуночка
Стулки аортального клапана в нормі виписують характерні криві руху («скринька і змійка»). На початку систоли стулки різко відходять до стінок аорти і в такому положенні перебувають протягом усього періоду вигнання крові з лівого шлуночка («скринька»). Закрившись на початку діастоли, вони змикаються в центрі просвіту аорти і дають зображення у вигляді хвилястої лінії («змійка») (Lancellotti and Cosyns, 2016).
Нині одновимірну ехокардіографію як самостійний метод обстеження серця не застосовують. Крім того, розрахунки розмірів та об’ємів лівого шлуночка, а також його фракції викиду переважно проводять, використовуючи двовимірне зображення. Однак у багатьох ситуаціях М-спосіб доповнює уявлення про рух серцевих структур і дає важливу для діагностики інформацію. Зокрема цим методом оцінюють тривалість і часове розміщення пролапсу мітрального клапана, виявляють систолічне прогинання стулок мітрального клапана вперед до міжшлуночкової перегородки і середньосистолічне прикриття стулок аортального клапана в пацієнтів з гіпертрофічною кардіоміопатією, оцінюють скоротливу здатність правого шлуночка за величиною систолічної екскурсії фіброзного кільця тристулкового клапана.
Додатковою ознакою зниження скоротливої здатності лівого шлуночка за одновимірною ехокардіограмою може слугувати збільшення відстані між точкою Е руху передньої стулки мітрального клапана та лівою поверхнею міжшлуночкової перегородки понад 20 мм (що відповідає зниженню фракції викиду лівого шлуночка менше 30%).
ДОПЛЕРІВСЬКА ЕХОКАРДІОГРАФІЯ
Фізичні засади
Принцип доплерографії полягає в тому, що відбитий від рухомого об’єкта ультразвуковий промінь змінює свою частоту пропорційно до швидкості руху об’єкта. При цьому, якщо об’єкт рухається в одному з ультразвуковим променем напрямку, то частота відбитого ультразвуку буде меншою, ніж частота ультразвуку, випроміненого датчиком. Якщо ж об’єкт рухається до датчика (тобто назустріч випроміненому ультразвуку), то частота ультразвуку у відбитому промені буде більшою, ніж вихідна (Feigenbaum et al., 2010).
Аналізуючи зміну частоти ультразвуку, відбитого від рухомого об’єкта, можна визначити:
1) швидкість об’єкта – вона тим більша, чим більшою є різниця частоти ультразвуку;
2) напрямок руху об’єкта – якщо об’єкт наближається до датчика, то частота відбитого ультразвуку стає більшою, ніж вихідна, а якщо об’єкт віддаляється, то частота стає меншою.
Крім швидкості, із якою рухається об’єкт, на зміну частоти відбитого ультразвуку впливає кут між напрямком руху об’єкта і напрямком посланого ультразвукового променя. За інших однакових умов зміна частоти буде найбільшою тоді, коли цей кут становить 0°, тобто обидва напрямки збігаються. Коли ж випромінений ультразвук іде перпендикулярно до напрямку руху об’єкта, змін частоти відбитого ультразвуку не буде взагалі. Іншими словами, для підвищення точності вимірювання треба посилати ультразвуковий промінь якомога паралельніше до напрямку руху об’єкта, швидкість якого визначають. Якщо ж це не вдається, то необхідно враховувати кут і вносити поправку до розрахунків за рівнянням Доплера:
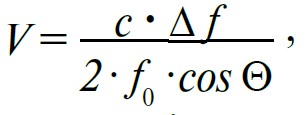
де V – швидкість потоку крові (відповідає швидкості руху еритроцитів); с – швидкість поширення ультразвуку в тканинах (1560 м/с); Δf – зміна частоти відбитого ультразвуку (доплерівський зсув частоти); f0 – частота випроміненого ультразвуку; Q— кут між напрямком потоку крові та напрямком випроміненого ультразвукового променя.
Коли визначають швидкість потоку крові в серці та судинах, то рухомими об’єктами виступають еритроцити. Електронна частина доплерівського ультразвукового апарата аналізує зміну частоти відбитого від еритроцитів і вловленого датчиком ультразвуку, а швидкість проходження ультразвуку через м’які тканини (с) і частота випромінюваного ультразвуку (f0) відомі. Якщо ж хід скенувального променя та напрямок потоку крові не є паралельними, то враховують кут 0 (проводять кутову корекцію).
Типи кровоплину
Виділяють два типи потоку крові в серці та судинах: ламінарний (пошаровий) та турбулентний (завихрений). Ламінарний потік крові характерний тим, що еритроцити рухаються паралельно до стінок з майже однаковою швидкістю (Otto, 2013).
Проте шари крові, які розташовані ближче до стінок, внаслідок тертя все ж таки рухаються дещо повільніше, ніж ті шари, що розташовані ближче до центру просвіту. Тому такий потік і називається пошаровим (ламінарним). У серці та всіх великих судинах у нормі течія крові має власний ламінарний характер, а її швидкість рідко перевищує 1,5 м/с.
Інший тип кровоплину виникає відразу за місцем звуження і характеризується різноманітністю швидкостей і напрямків руху окремих еритроцитів. Це турбулентний або завихрений потік. Зазвичай такий потік вказує на патологію: стеноз, регургітацію на клапанах чи сполучення між камерами серця або судинами з великою різницею тиску між ними.
Крім того, потік крові в серці та артеріальних судинах має пульсуючий характер, зумовлений систолічним викидом крові до аорти і легеневої артерії та одночасним припиненням потоку через мітральний і тристулковий клапани. Під час діастоли в артеріях потік крові сповільнюється, а в серці відбувається заповнення шлуночків через атріовентрикулярні отвори. У великих венах також змінюється швидкість кровоплину, що зумовлено зміною внутрішньогрудного тиску залежно від фаз дихання.
Види доплерівського ультразвукового дослідження:
- Дослідження безперервною хвилею (Continuous Wave Doppler – CW Doppler – постійний або безперервний доплер).
- Дослідження імпульсною хвилею (Pulsed Wave Doppler – PW Doppler – імпульсний доплер).
- Кольорове доплерівське дослідження (Colour Doppler – кольоровий доплер).
- Енергетичне доплерівське дослідження (Colour Doppler Energy – Ultrasound Angio).
- Тканинне доплерівське дослідження (Tissue Doppler – тканинний доплер).
Терміни «постійний доплер», «імпульсний доплер» і «кольоровий доплер» широко застосовують у щоденній практиці, а саме слово «доплер» у цих словосполученнях є еквівалентом терміна «метод ультразвукового дослідження з використанням ефекту Доплера».
Доплерівське дослідження безперервною хвилею (постійний доплер)
Особливістю такого дослідження є те, що в датчику, яким його проводять, задіяні одночасно два п’єзоелектричні елементи. Один із них безперервно надсилає ультразвуковий промінь, а другий безперервно приймає відбиті сигнали, які виникли на всьому шляху цього променя через серце або тканини, і передає їх до аналізувального пристрою. Постійний доплер дає можливість визначати як низькі, так і дуже високі швидкості, але не дає змоги встановити, де саме (в якій точці) за ходом променя трапився потік із максимально зареєстрованою швидкістю.
Іншими словами, постійний доплер не дозволяє оцінити швидкість і напрямок потоку в якійсь певній точці, а вловлює і одночасно реєструє всі швидкості рухомих об’єктів, які трапилися на шляху променя при скенуванні (Feigenbaum et al., 2010).
Провести доплерівське дослідження безперервною хвилею можна двома типами датчиків. Перші дозволяють дістати двовимірне зображення в реальному часі і по ньому «націлити» постійний доплерівський промінь на важливі для діагностики місця. Однак ці датчики мають досить велику поверхню, що не дає змоги використати вузькі «ультразвукові віконечка» і скерувати промінь максимально паралельно до потоку. Датчики другого типу (pencil probe – non-imagine probe – пальчиковий датчик) мають маленьку поверхню, проте дозволяють проводити лише постійне доплерівське дослідження без двовимірного зображення перерізу серця або судини. Вони забезпечують високу чутливість постійного доплерівського дослідження, але вимагають певного досвіду від оператора, бо націлювати промінь на потрібні місця доводиться наосліп (Otto, 2013).
Отримана при доплерівському дослідженні інформація доступна для аналізу в двох формах:
- Акустичний сигнал. За характером звуку оцінюють приблизно швидкість потоку і його тип (ламінарний чи турбулентний).
- Візуальне зображення. За допомогою графіка, де по горизонтальній осі – час, а по вертикальній – швидкість потоку, а тому можна оцінити, як змінюється швидкість за певний проміжок часу.
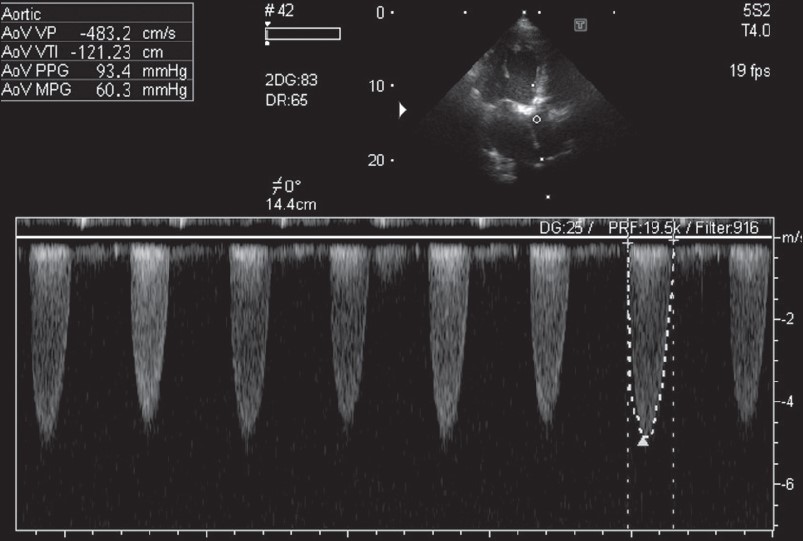
Існує чіткий зв’язок між швидкістю потоку крові через вузьке місце та перепадом тиску на звуженні: чим більша різниця тиску над і під стенозом, тим вища швидкість у місці звуження (і навпаки). Отже, визначивши швидкість потоку крові в місці стенозування, можна розрахувати градієнт (перепад) тиску на ньому (рис. 24.1).
Рис. 24.1. Реєстрація швидкості потоку через звужений отвір аортального клапана безперервним доплерівським методом (CW Doppler). Увімкнувши на діагностичному апараті режим розрахунків, ставлять курсор на вершину параболічного зображення, зазначаючи у такий спосіб максимальну (пікову) швидкість (у цьому випадку — 483 см/с). За цією швидкістю апарат розраховує максимальний (піковий) систолічний градієнт тиску на клапані, який у цьому випадку становить 93 мм рт. ст. Обвівши зовнішню рамку графіка потоку, визначаємо інтеграл швидкості в часі (VTI) і середній систолічний градієнт тиску (60 мм рт. ст.). Отримані цифри висвітлено в лівому верхньому кутку зображення
Цей розрахунок виконують за простою формулою:
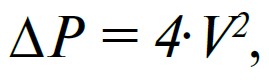
де АР – градієнт тиску (мм рт. ст.), а V – визначена швидкість потоку (м/с).
У випадку оцінювання клапанних стенозів аорти або легеневої артерії можна визначити пікову (найвищу) швидкість і за нею розрахувати піковий (максимальний) систолічний градієнт тиску між шлуночком та великою артерією (Флакскампф, 2013).
Коли ж характеризують тяжкість мітрального стенозу, то переважно використовують середній діастолічний градієнт тиску на мітральному клапані, розрахувавши його по середній швидкості діастолічного потоку через мітральний отвір. А середню швидкість, своєю чергою, обчислюють автоматично після обведення рамки на постійному доплерівському графіку трансмітрального потоку (за умови, що ввімкнено відповідну програму розрахунків).
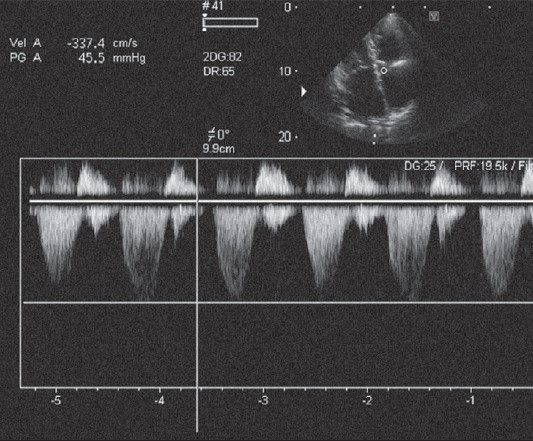
Для того щоб оцінити величину систолічного тиску в правому шлуночку, достатньо «спіймати» зворотний потік на тристулковому клапані й визначити його пікову швидкість. За величиною пікової швидкості струменя регургітації обчислюють піковий градієнт тиску між правим шлуночком і правим передсердям під час систоли (рис. 24.2). Якщо до цієї величини додати 10 мм рт. ст. (це приблизний тиск у правому передсерді за умови, що немає явищ застою по великому колу кровообігу), то можна дістати величину тиску в правому шлуночку (Otto, 2013).
Рис. 24.2. Безперервнохвильова доплерографія зворотного потоку на тристулковому клапані. Максимальна швидкість потоку в цьому випадку — 3,37 м/с, що відповідає систолічному градієнту тиску на клапані — 45 мм рт. ст. (цифрові дані — у верхньому лівому кутку)
Величину діастолічного тиску в легеневій артерії можна визначити, якщо зареєструвати потік регургітації на клапані легеневої артерії і поміряти його швидкість (пікову та/або середню). У зв’язку з тим, що діастолічний тиск у правому шлуночку близький до 0 мм рт. ст., то величина діастолічного градієнта тиску на легеневому клапані відповідає величині діастолічного тиску в легеневій артерії (Коваленко та співавт., 2009).
Прогностично і тактично важливу інформацію несе величина градієнта систолічного тиску між лівим і правим шлуночками у хворих із дефектом міжшлуночкової перегородки. Щоб цей градієнт розрахувати, потрібно, знову ж таки, визначити швидкість струменя крові, який б’є через дефект з одного шлуночка в другий. А це зробити нескладно навіть пальчиковим датчиком, скерувавши промінь через дефект максимально паралельно до потоку. Значення систолічного тиску в правому шлуночку в таких випадках легко обчислити, віднявши величину градієнта систолічного тиску між шлуночками, визначену за максимальною швидкістю потоку крові через дефект, від величини систолічного артеріального тиску, виміряного звичайним тонометром на плечовій артерії.
Адже систолічний тиск у плечовій артерії є таким самим, як і в аорті та лівому шлуночку, якщо аортальний клапан не стенозований.
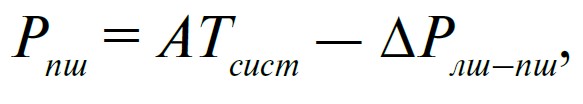
де Рпш – тиск у правому шлуночку;
АТсист – систолічний артеріальний тиск;
ΔРлш-гш – градієнт систолічного тиску між лівим і правим шлуночками.
Практично можна розрахувати градієнт (різницю) тиску між будь-якими порожнинами (камерами серця, судинами), якщо вдається зареєструвати потік крові з однієї порожнини в іншу і поміряти його швидкість за допомогою доплерівського дослідження. Цей метод дає можливість «безкровного зондування серця», а цифрові значення, які дістають описаним вище способом, знаходять чітке підтвердження при катетерному зондуванні серця (Флакскампф, 2013).
Доплерівське дослідження імпульсною хвилею (пульсовий доплер)
Цей метод має істотну перевагу над доплерівським дослідженням безперервною хвилею: він дозволяє визначити швидкість і напрямок потоку крові у певній точці – так званому «пробному об’ємі» (sample volume – пробний об’єм), яку можна вибрати на двовимірному зображенні в реальному часі. Тобто, отримавши потрібне двовимірне зображення, оператор має можливість визначити швидкість, напрямок і характер потоку крові у вибраній ним точці, тобто саме в тому місці, яке його цікавить. Серйозним недоліком методу є те, що він не дає можливості вимірювати високі швидкості потоку, що зумовлено технічними особливостями (Feigenbaum et al., 2010].
Принцип згаданого методу полягає в тому, що випромінює ультразвуковий промінь і приймає його відображення один і той самий п’єзоелектричний елемент. Випромінення не відбувається постійно, а окремими імпульсами (pulsed wave – імпульсна хвиля). Крім того, черговий імпульс датчик надсилає лише тоді, коли отримав відбиття попереднього імпульсу. Отже, в будь-який момент через досліджувані тканини проходить лише один ультразвуковий сигнал (Lancellotti and Cosyns, 2016).
Оцінювання параметрів потоку саме у визначеному місці досягається тим, що виконується аналіз відбитого ультразвуку, який повернувся лише через певний часовий інтервал. Усі інші відбиті рухомими еритроцитами ехосигнали, які повертаються до датчика поза визначеним часовим інтервалом, ігноруються і не аналізуються. Цей часовий інтервал розраховується таким чином, що його власне вистачає для проходження ультразвукової хвилі від датчика через тканини до заданої точки, а потім назад до датчика. Швидкість проходження ультразвуку через м’які тканини і кров відома – 1560 м/с. Усі відбиті рухомими частинками ехосигнали, які приходять назад раніше (тобто з меншої глибини) або пізніше (тобто з більшої глибини), ніж заданий часовий інтервал, не беруться до уваги. Тут і заховане технічне обмеження методу: максимальний доплерівський зсув частоти (Δfmax), який може бути визначений, становить половину від частоти повторення імпульсу (pulse repetition frequency – PRF).
Δfmax = PRF/2.
Як уже було згадано вище, за доплерівським зсувом частоти обчислюють швидкість руху еритроцитів (рівняння Доплера). Тобто, максимально можлива швидкість, яку можна виміряти методом імпульсної хвилі (пульсовим доплером), визначається частотою повторення імпульсу, а та своєю чергою залежить від того, на якій глибині від поверхні датчика розташована точка, де потрібно провести вимірювання швидкості. Чим глибше лежить потрібна точка, тим меншою має бути частота повторення імпульсу і тим меншу швидкість можна виміряти. Це явище називається обмеженням Найквіста (Nyquist limit).
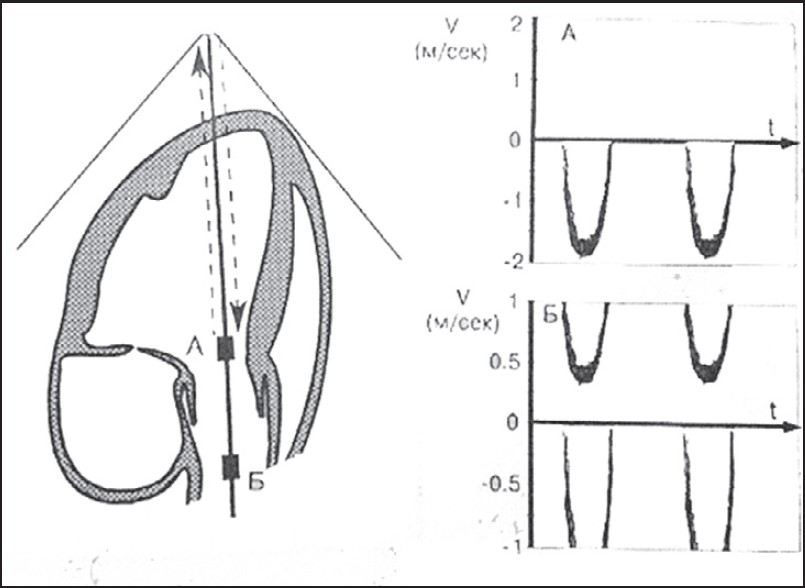
На рис. 24.3 схематично зображено, яке практичне значення має обмеження Найквіста. Якщо пробний об’єм розміщено у точці А (вихідний відділ лівого шлуночка), то кожен наступний імпульс може бути посланий не раніше, ніж тоді, коли попередній встигне дійти до точки А, а його відлуння – повернутися до датчика. Власне цим визначається максимально можлива частота повторення імпульсу (PRF) і, відповідно, максимальна швидкість потоку, яку можна виміряти. Точка Б розташована далі від поверхні датчика, а тому частота повторення імпульсу при визначенні швидкості потоку в цьому місці мусить бути нижчою. Для точки Б обмеження Найквіста має меншу величину, ніж для точки А. Хоча швидкість потоку в точках А і Б практично однакова, в точці А її вдалося зареєструвати і поміряти (верхня схема), а в точці Б – ні. На нижній схемі показано феномен хибного відображення (aliasing): якщо вимірювана швидкість перевищує обмеження Найквіста для цієї точки, то на графіку зміни швидкості в часі та частина кривої, яка більша, ніж допустима величина, опиняється з протилежного боку, що унеможливлює кількісне вимірювання.
Рис. 24.3. Обмеження Найквіста
Отже, імпульсний доплер дає можливість оцінити характер потоку і виміряти його швидкість у вибраній оператором точці, але не дозволяє визначати високі швидкості (які перевищують обмеження Найквіста).
У здоровому серці в більшості випадків швидкість потоку крові через клапани вдається визначити методом імпульсного доплера. Але коли йдеться про патологію, коли швидкість потоку дуже висока і її конче потрібно виміряти, доводиться застосовувати постійний доплерівський метод (Lancellotti and Cosyns, 2016).
Обидва описані методи доповнюють один одного: імпульсний доплер дає змогу встановити місце, де є аномальний потік, а постійний доплер дає можливість точно визначити його швидкість. Однак в сучасних ультразвукових діагностичних апаратах завдяки технологічним інноваціям безперервно хвильовий доплерівський метод має можливість точно оцінити швидкість потоку у вибраній оператором потрібній точці, незважаючи на глибину її розміщення. Характер потоку через атріовентрикулярні клапани і швидкість визначають методом імпульсної хвилі. Для цього отримують верхівкове чотирикамерне зображення, а пробний об’єм розміщують між стулками мітрального (або тристулкового) клапана, змістивши від фіброзного кільця до глибини шлуночка.
Основні доплерівські характеристики потоків крові через клапани серця представлено у таблиці 24.2.
|
Таблиця 24.1. Порівняння доплерівських досліджень методом імпульсної хвилі та методом безперервної хвилі |
||
|
|
Метод імпульсної хвилі (PW Doppler) |
Метод безперервної хвилі (CW Doppler) |
|
Переваги |
Можливість оцінити потік у певній точці |
Можливість вимірювання високих швидкостей |
|
Недоліки |
Вимірювання високих швидкостей неможливе |
Оцінювання потоку в певній точці неможливе |
|
Таблиця 24.2. Характеристика нормальних потоків через клапани серця і магістральні судини |
|||||
|
Місце визначення швидкості потоку |
Нормальна швидкість потоку, м/с |
Графіка потоку |
Рекомендовані підходи для виконання вимірювань |
Чинники, які впливають на величину швидкості та графіку потоку |
|
|
Діти |
Дорослі |
||||
|
Мітральний клапан, діастола |
1,0 (0,8-1,3) |
0,9 (0,6-1,3) |
М-подібна |
Верхівкове чотирикамерне зображення Верхівкове зображення по довгій осі лівого шлуночка |
Діастолічні властивості лівого шлуночка. Вік досліджуваного: із віком перша хвиля (Е) стає нижчою, а друга хвиля (А) — вищою. ЧСС: за тахікардії наростає хвиля А |
|
Тристулковий клапан, діастола |
0,6 (0,5-0,8) |
0,5 (0,3-0,7) |
М-подібна |
Верхівкове чотирикамерне зображення |
Діастолічні властивості правого шлуночка. Вік досліджуваного. ЧСС. Фаза дихання: на вдиху потік прискорюється |
|
Вихідний відділ правого шлуночка та легенева артерія, систола |
0,9 (0,7-1,1) |
0,8 (0,6-0,9) |
Параболічна |
Парастернальний підхід, коротка вісь, рівень аортального клапана |
Положення пробного об’єму в просвіті легеневої артерії: чим ближче до центру, тим вища швидкість |
|
Вихідний відділ лівого шлуночка, систола |
1,0 (0,7-1,2) |
0,9 (0,7-1,1) |
Параболічна Можлива реєстрація низькоамплітудних діастолічних потоків, |
Верхівкове п’ятикамерне зображення мітрального отвору |
|
|
Аортальний клапан і висхідний відділ грудної аорти, систола |
1,5 (1,2-1,8) |
1,4 (0,81-1,7) |
Параболічна |
Супрастернальний підхід Права надключична ямка Правий парастернальний підхід з першого-другого міжребер’я Верхівкове зображення по довгій осі лівого шлуночка |
У висхідній аорті вища швидкість реєструється при розміщенні пробного об’єму ближче до зовнішнього вигину. 3 віком людини швидкість стає меншою (внаслідок більшого діаметра висхідного відділу аорти в старших людей) |
Продовження у наст. Номерах
Тематичний номер «Кардіологія. Ревматологія. Кардіохірургія» № 1 (92) 2024 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Серед препаратів, які мають велику доказову базу щодо лікування пацієнтів із захворюваннями дихальних шляхів з алергічним компонентом, особливий інтерес становлять антагоністи лейкотрієнових рецепторів (АЛТР). Ці препарати мають хорошу переносимість у дорослих та дітей, а також, на відміну від інгаляційних кортикостероїдів (ІКС), характеризуються високим комплаєнсом, тому посідають чільне місце в лікуванні пацієнтів із респіраторною патологією. У лютому відбувся міждисциплінарний конгрес із міжнародною участю «Життя без алергії International» за участю провідних вітчизняних міжнародних експертів. Слово мав президент Асоціації алергологів України, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Зайков із доповіддю «Місце АЛТР у лікуванні пацієнтів із респіраторною патологією». ...
Розбір клінічного випадку...