Жовтяниця новонароджених дітей
Уніфікований клінічний протокол спеціалізованої медичної допомоги
Жовтяниця новонароджених (ЖН) є одним із найпоширеніших неонатальних клінічних станів. Її виявляють приблизно у 60 % доношених й у 80 % передчасно народжених дітей. У більшості новонароджених цей стан не потребує лікування. Проте приблизно у 10 % немовлят може розвинутися клінічно значуща жовтяниця, яка може призводити до істотних негативних наслідків (неврологічного ураження і навіть смерті). В інших випадках жовтяниця може бути симптомом серйозного захворювання. Важливо своєчасно виявити всіх таких дітей і надати їм правильну медичну допомогу.
В УКПМД представлені загальні підходи до надання допомоги новонародженим, які мають клінічні ознаки жовтяниці. Надані рекомендації щодо діагностики, диференційної діагностики і лікування новонароджених із різними формами жовтяниць.
І. Паспортна частина
1.4. Мета протоколу
Мета протоколу – забезпечити якість, ефективність та доступність надання медичної допомоги новонародженим дітям із жовтяницею.
1.8. Коротка епідеміологічна інформація
Тимчасове підвищення рівня білірубіну в сироватці крові спостерігається в усіх дітей після народження, але лише приблизно 60% доношених і 80% недоношених дітей на першому тижні життя мають певний ступінь жовтяниці. У більшості новонароджених жовтяниця є фізіологічною, тому важливо своєчасно виявити клінічно значущу жовтяницю і/або захворювання, клінічною ознакою яких є жовте забарвлення шкіри та/або слизових оболонок.
Новонароджені із жовтяницею потребують ретельного спостереження, оскільки приблизно у 10% може виникнути клінічно значуща жовтяниця, яка потенційно може призвести до істотних негативних наслідків (неврологічного ураження і навіть смерті). Важливо своєчасно виявити захворювання, клінічною ознакою яких є жовте забарвлення шкіри та/або слизових оболонок. Причинами появи такої жовтяниці можуть бути: несумісність груп крові матері і дитини (найчастіше несумісність за резус-антигенами або АВ0), інші причини гемолізу, сепсис (інфекція), захворювання печінки, крововиливи, порушення обміну речовин тощо.
Частота розвитку небезпечних випадків гіпербілірубінемії у новонароджених Європи та Північної Америки становить 0,4-2,7 випадка на 100 тис. пологів. У країнах із менш досконалими системами медичної допомоги новонародженим частота таких випадків вища. У розвинених країнах частота гострої білірубінової енцефалопатії (ГБЕ) у дітей із гіпербілірубінемією понад 500 мкмоль/л коливається від 2 до 10%. Частота ядерної жовтяниці (ЯЖ) у розвинених країнах становить 1,2-2,3 на 100 тис. живих новонароджених. Ризик цієї патології може бути вищим у системах охорони здоров’я з обмеженими ресурсами.
II. Загальна частина
У більшості випадків жовтяниця виникає в перші 2-4 доби життя дитини і розцінюється як фізіологічний стан, оскільки найчастіше спричинена особливостями розвитку та метаболізму дитини у цей віковий період. Однак навіть у здорових доношених дітей жовтяниця не завжди є безпечною. Один або декілька чинників (підвищена продукція білірубіну, зниження печінкового захоплення, недостатність процесів кон’югації, порушення екскреції і/або відтоку жовчі, підвищена кишково-печінкова циркуляція тощо) можуть спричинити підвищення рівня загального білірубіну сироватки (ЗБС), що вимагатиме диференційної діагностики та, за потреби, лікування жовтяниці. Призначення додаткового обстеження є доцільним для визначення основної причини жовтяниці у випадках її ранньої появи або високого рівня білірубіну; у разі підвищення концентрації прямого білірубіну (ПБ); якщо жовтяниця триває довше, ніж це характерно для фізіологічної жовтяниці, або за наявності у дитини інших патологічних ознак.
При високому рівні ЗБС крові, незалежно від причини, щоб запобігти ушкодженню мозку, дитину необхідно лікувати. Клінічна діагностика й оцінювання тяжкості жовтяниці можуть бути утрудненими, особливо у передчасно народжених немовлят.
Важливу роль у профілактиці тяжких форм жовтяниці та її наслідків має впровадження уніфікованого підходу до надання медичної допомоги новонародженим з урахуванням існуючих рівнів перинатальної та неонатальної допомоги в Україні.
ІІІ. Основна частина
3.1. Профілактичні заходи
Положення протоколу. Профілактичні заходи щодо клінічно значущої ЖН потрібно спрямовувати на своєчасне виявлення рівнів ЗБС, за наявності яких потрібні додаткові діагностичні заходи та медичні втручання. Ці заходи включають профілактику ЖН, пов’язаної з гемолітичною хворобою новонародженого (ГХН); виявлення немовлят із груп ризику щодо прогресування гіпербілірубінемії та нейротоксичної дії білірубіну; візуальне оцінювання жовтяниці; підтримку грудного вигодовування (годування грудним молоком), а також запобігання значній втраті маси тіла в новонародженої дитини.
Обґрунтування. Профілактика починається під час вагітності з виявлення та лікування жінок, у яких є ризик продукції антитіл до антигенів еритроцитів, що може призвести до ГХН. Усім вагітним жінкам потрібно визначати групову і Rh-належність крові, а також наявність антиеритроцитарних антитіл (АЕА) у крові Rh-негативних жінок (якщо батько дитини має Rh-позитивну кров або його Rh-фактор невідомий) під час першого антенатального візиту і повторно, у 28 тижнів вагітності. Ризик розвитку ГХН існує, якщо матір є Rh-негативною, має групу крові 0 (I) і/або у її крові наявні АЕА до антигенів D, C, c, E, e, K та ін.
Профілактичні дії з виявлення вагітних жінок із групи ризику, спрямовані на уникнення сенсибілізації організму матері Rh-антигенами еритроцитів плода, здійснюють відповідно до чинних галузевих стандартів у сфері охорони здоров’я з акушерства.
Немовлята з чинниками ризику значущої гіпербілірубінемії та нейротоксичної дії білірубіну в анамнезі вимагають ретельнішого спостереження, ніж інші діти (панель 1). Наявність цих чинників ризику вимагає додаткових оглядів немовляти, оцінювання результатів лабораторного обстеження, а також ретельного аналізу даних сімейного анамнезу щодо захворювань системи крові і жовтяниці в період новонародженості у попередньо народжених дітей. Урахування наявності чинників ризику в анамнезі дитини є важливим для профілактики ускладнень ЖН. Оцінювати їх слід відразу після народження дитини, у разі появи жовтяниці, і повторно, якщо стан дитини погіршується.
Усі медичні працівники, а також батьки новонароджених дітей мають знати клінічні ознаки ЖН для її своєчасного виявлення. Спочатку ЖН з’являється на обличчі і зі збільшенням рівня білірубіну в крові поширюється на тулуб і кінцівки дитини. Регресує у зворотному напрямку.
Візуальне оцінювання локалізації ЖН не дозволяє надійно прогнозувати рівень ЗБС у новонароджених дітей. Однак якщо у немовляти візуально зовсім немає ЖН, то малоймовірно, що рівень ЗБС перевищує 205 мкмоль/л.
Батькам рекомендується оглядати дитину на наявність ЖН за будь-якої нагоди (особливо в перші 72 год життя).
У немовлят, які перебувають на грудному вигодовуванні, частіше виявляють ЖН, яка у частині випадків може мати ознаки нефізіологічної. Залежно від віку на момент появи і механізмів виникнення, розрізняють жовтяницю, пов’язану з недостатнім грудним вигодовуванням, і жовтяницю, пов’язану з грудним молоком.
Важливо підтримувати грудне вигодовування, сприяти першому прикладанню дитини до грудей протягом першої години після народження з наступними частими прикладаннями на вимогу дитини (щонайменше 8 разів на добу).
Ознаки ефективного смоктання включають відсутність дискомфорту та збільшення об’єму молока у матері, чутне ковтання дитини, адекватне виділення сечі (не менше 4 мокрих підгузків за першу добу і не менше 6 мокрих підгузків пізніше) та фізіологічну втрату маси тіла (менше 10% маси тіла при народженні в перші 48 год життя) дитини.
Немовлят, які перебувають на грудному вигодовуванні й отримують достатньо ГМ, не слід догодовувати молочними сумішами.
Необхідні дії
Обов’язкові
- Профілактика ЖН, пов’язаної з ГХН.
Дітям, які народилися від Rh-негативних матерів або матерів з 0 (I) групою крові, якомога скоріше після народження визначити групову і Rh-належність крові, використовуючи пуповинну або периферійну кров.
Якщо дитина, народжена такою матір’ю, є відповідно Rh-позитивною або має А (ІІ)/В (ІІІ) групу крові, потрібно провести пряму пробу Кумбса, використовуючи ту саму кров.
- Оцінювання чинників ризику значущої гіпербілірубінемії та нейротоксичної дії білірубіну.
Оцінити наявність чинників ризику значущої гіпербілірубінемії і нейротоксичної дії білірубіну в анамнезі у кожної новонародженої дитини (панель 1).
Панель 1
Оцінювання чинників ризику значущої гіпербілірубінемії та нейротоксичної дії білірубіну
Чинники ризику значущої гіпербілірубінемії та нейротоксичної дії білірубіну:
- ГВ менше 38 тиж, ризик зростає зі зменшенням ГВ;
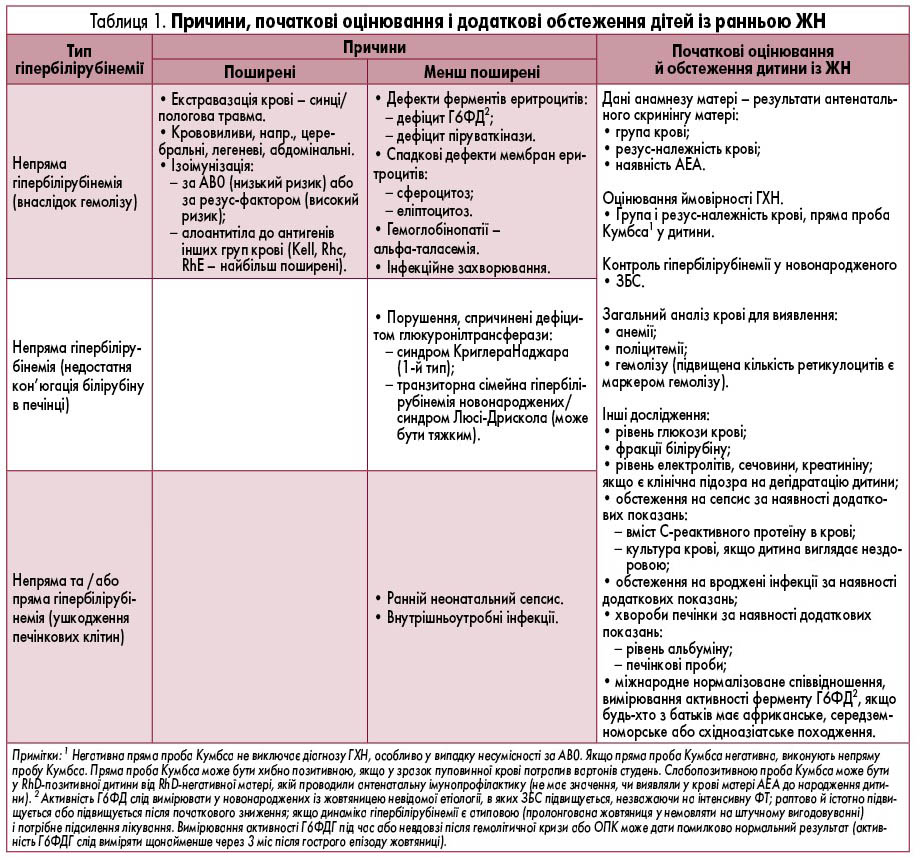
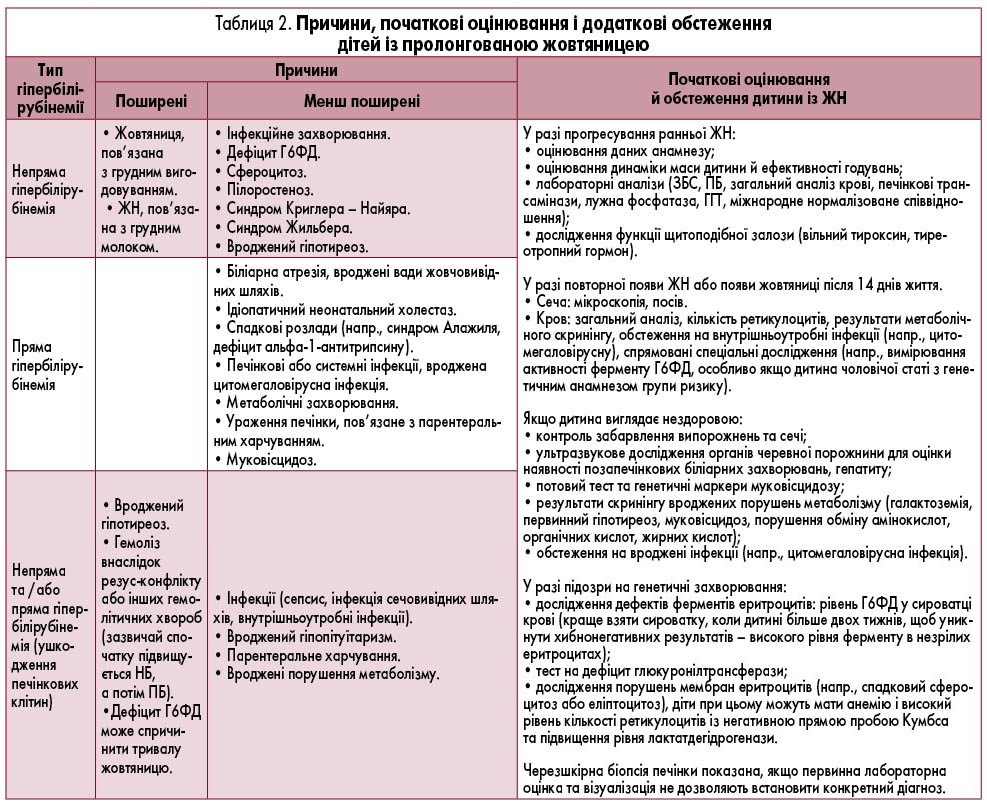
- емоліз з будь-якої причини: ГХН, дефіцит Г6ФД або інші гемолітичні стани (табл. 1, 2).
Чинники ризику значущої гіпербілірубінемії:
- ЖН у перші 24 год після народження;
- батьки, брат або сестра дитини потребували ФТ або ОПК;
- виключно грудне вигодовування дитини з неналежним споживанням ГМ;
- дитина з макросомією від матері, хворої на цукровий діабет;
- гематоми шкіри голови або великі синці у дитини, поліцитемія;
- синдром Дауна.
Чинники ризику нейротоксичної дії білірубіну:
- сепсис;
- асфіксія;
- значна клінічна нестабільність протягом перших 24 год життя.
Наявність чинників ризику значущої гіпербілірубінемії вимагає обов’язкового візуального спостереження за дитиною, щоб виявити появу жовтяниці (кожні 8 год упродовж перших 72 год життя), а у разі виявлення – додаткового обстеження з визначенням рівня транскутанного білірубіну (ТкБ) або ЗБС.
Наявність чинників ризику значущої гіпербілірубінемії і нейротоксичної дії білірубіну знижує рівні ЗБС, які вказують на потребу розпочати ФТ або підсилити лікування.
- Візуальне оцінювання жовтяниці.
Візуально оцінювати колір шкіри і слизових оболонок на наявність жовтяниці в усіх немовлят принаймні кожні 12 год від народження до виписки та безпосередньо перед випискою, якщо дитина перебуває у закладі охорони здоров’я (ЗОЗ) щонайменше упродовж перших 72 год життя.
Оглядати дитину повністю роздягненою в умовах достатнього (оптимально денного) освітлення та забезпечення теплового захисту.
Колір шкіри оцінювати після легкого натискання на неї (до рівня підшкірної основи), а також оглядати склери та слизові оболонки немовляти. Під час оцінювання враховувати особливості анатомічного поширення ЖН.
- Належне грудне вигодовування і запобігання значній втраті маси тіла.
Підтримувати матерів, які мають намір годувати виключно грудьми, для збільшення продукції молока і встановлення належного годування дитини.
Щоденно контролювати кількість спожитого молока, враховуючи кількість повністю мокрих підгузків (не менше 4 мокрих підгузків в першу добу і не менше 6 у наступні доби), для запобігання значній втраті маси тіла дитини (понад 10 % маси тіла при народженні в перші 48 год життя).
Збільшувати кількість годувань грудьми і за потреби зважувати дитину до і після годування, якщо є підозра на недостатнє споживання ГМ.
Після обговорення з батьками догодовувати дитину зцідженим ГМ, донорським ГМ або молочною сумішшю, якщо, незважаючи на вжиті заходи, споживання ГМ під час грудного вигодовування залишається недостатнім, про що свідчать швидке прогресування ЖН на тлі зниженого діурезу і втрати маси тіла понад 10% при народженні.
Не призначати додаткову воду або розчин глюкози ентерально, щоб запобігти гіпербілірубінемії або знизити рівень білірубіну.
3.2. Діагностика жовтяниці
Положення протоколу. В усіх дітей із ЖН потрібно оцінити дані анамнезу відповідно до додатку 1 до цього УКПМД, їм також слід провести повне об’єктивне обстеження і за наявності показань – додаткове обстеження з визначенням рівня білірубіну й інших показників.
Хворі новонароджені (будь-яка дитина з ЖН, стан якої порушений або погіршується, або наявні інші патологічні ознаки), вимагають більш термінового і детальнішого обстеження та лікування (табл. 1, 2), оскільки етіологія ЖН може бути пов’язана з різними патологічними станами. Діагностичні заходи передбачають оцінювання рівня білірубіну та додаткові дослідження за потреби.
Хоча наявність або відсутність видимої ЖН є важливою та визнаною клінічною ознакою, вона не є надійною щодо оцінювання реального рівня ЗБС крові (або тяжкості гіпербілірубінемії). Зокрема, не можна покладатися на результати візуального оцінювання ЖН для виявлення гіпербілірубінемії у надзвичайно недоношених (гестаційний вік (ГВ) <28 тижнів) немовлят і у дітей, в яких рівень білірубіну швидко зростає.
Вирішення щодо спостереження та надання медичної допомоги новонародженим із гіпербілірубінемією передбачає оцінювання результатів вимірювання ТкБ і/або ЗБС за допомогою спеціальних номограм (рис. 1-6) з урахуванням гестаційного і постнатального віку, а також маси тіла дитини при народженні.
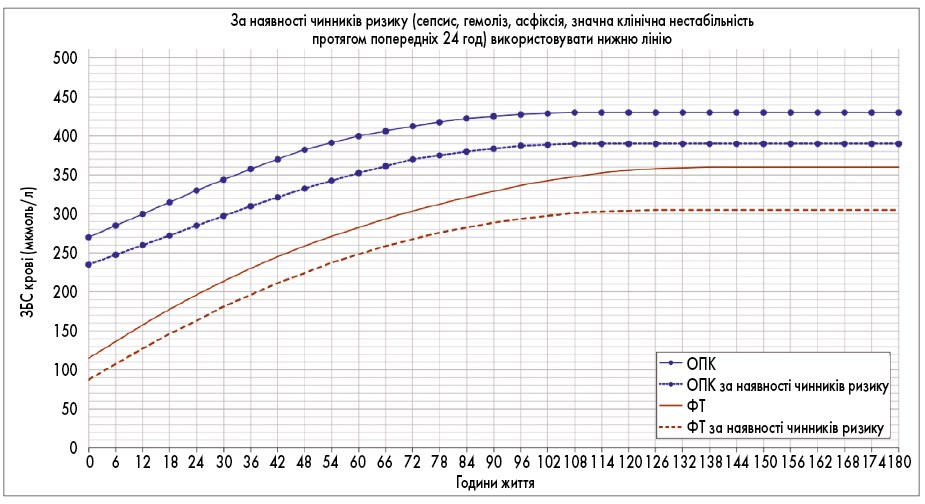 Рис. 1. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ >38 тиж
Рис. 1. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ >38 тиж
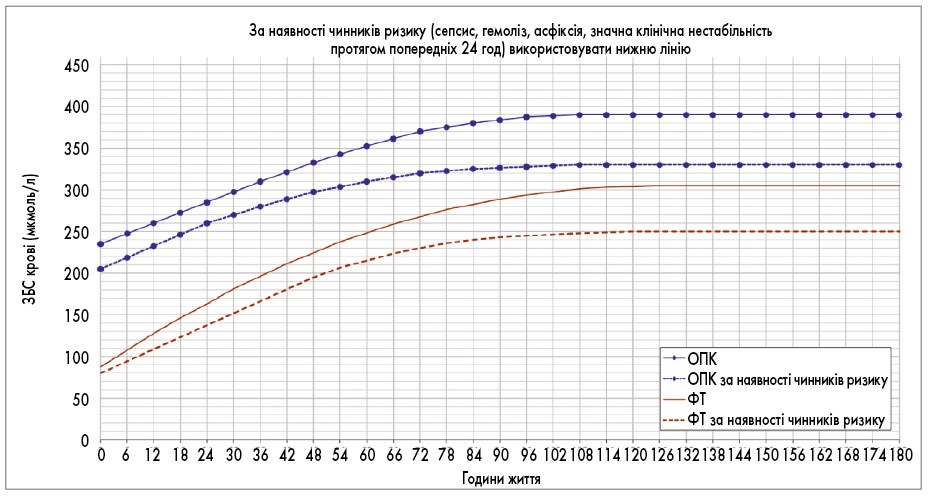 Рис. 2. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ від 35 до 37+6 тиж
Рис. 2. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ від 35 до 37+6 тиж
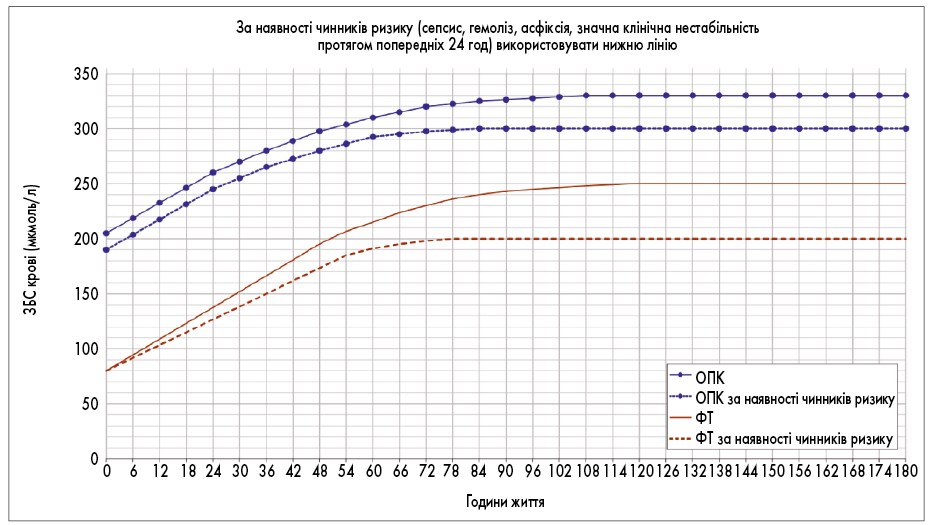 Рис. 3. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ <35 тиж і масою тіла >1999 г
Рис. 3. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ <35 тиж і масою тіла >1999 г
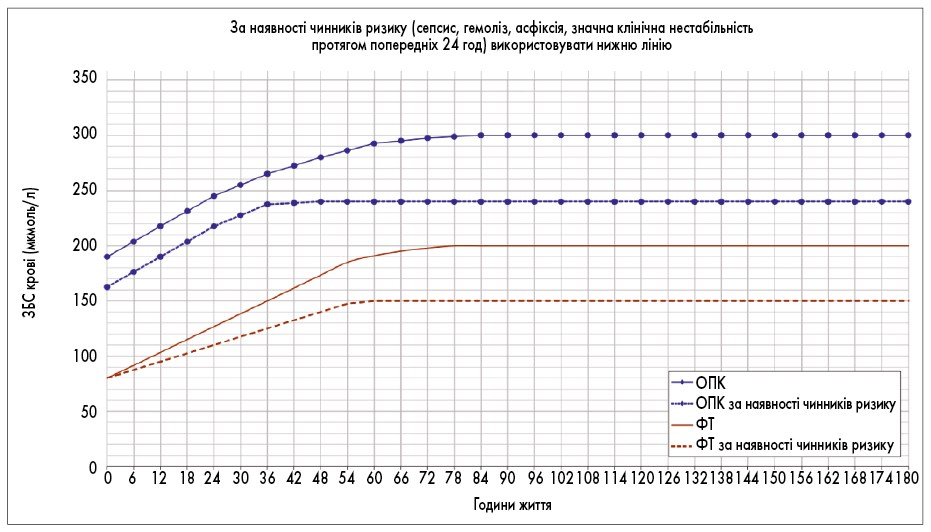 Рис. 4. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ <35 тиж і масою тіла 1500-1999 г
Рис. 4. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ <35 тиж і масою тіла 1500-1999 г
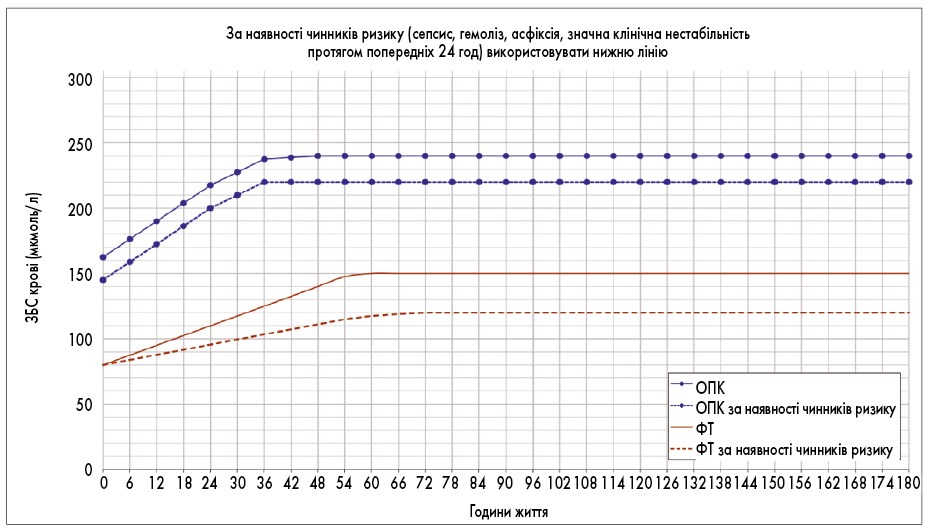 Рис. 5. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ <35 тиж і масою тіла 1000-1499 г
Рис. 5. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ <35 тиж і масою тіла 1000-1499 г
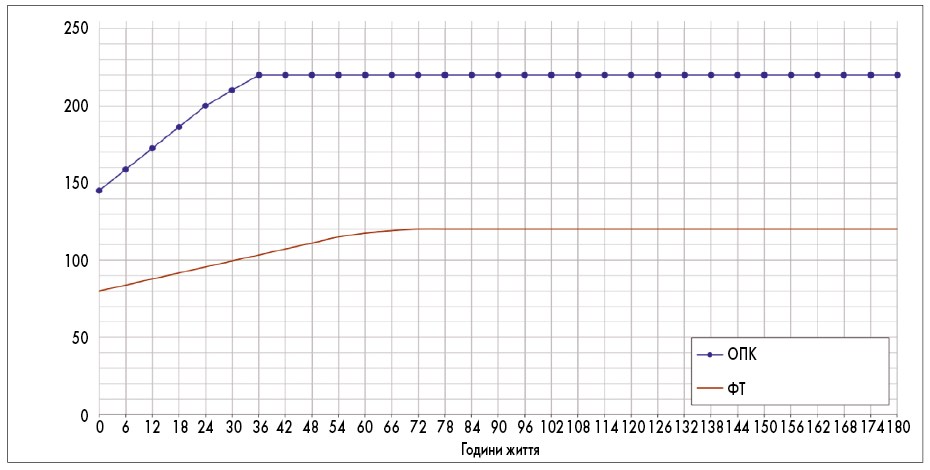 Рис. 6. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ <35 тиж і масою тіла <1000 г
Рис. 6. Номограма визначення потреби ФТ і ОПК у новонароджених із ГВ <35 тиж і масою тіла <1000 г
Обґрунтування. Транскутанний білірубінометр вимірює інтенсивність жовтого забарвлення відбитого від шкіри світла і використовує алгоритм для прогнозування рівня ТкБ на підставі об’єктивного оцінювання кольору шкіри дитини. Хоча вимірювання ТкБ не оцінює безпосередній вміст білірубіну в крові, воно є дійсним і надійним, якщо використовується як скринінговий тест для виявлення немовлят, яким потрібне вимірювання ЗБС. Водночас, транскутанна білірубінометрія зменшує кількість інвазивних досліджень крові та ймовірність зростання ЗБС до небезпечного рівня.
Транскутанні білірубінометри широко застосовують для скринінгу гіпербілірубінемії у доношених і пізніх недоношених дітей та виявлення новонароджених, які потребують фототерапії (ФТ). Однак через обмежену точність вимірювань не рекомендується використовувати їх для оцінювання гіпербілірубінемії у новонароджених із ГВ <35 тижнів.
Транскутанні білірубінометри застосовують згідно з рекомендаціями виробника. Якщо у відділенні наявні різні моделі таких приладів, важливо для окремої дитини використовувати прилад однієї моделі.
Кореляція рівнів ТкБ і ЗБС варіює залежно від ділянки тіла, на якій здійснюють вимірювання, але в більшості випадків ТкБ може замінити ЗБС, якщо рівень останнього є меншим 257 мкмоль/л.
Вимірювання ЗБС, який включає прямий і непрямий білірубін сироватки крові, є золотим стандартом діагностики гіпербілірубінемії в новонароджених. Вимірювання ЗБС – єдиний доступний тест, який використовують для прогнозування ризику виникнення білірубінової енцефалопатії (БЕ).
Для визначення потреби лікування ЖН рівень ЗБС крові порівнюють з відповідним показником на номограмі (рис. 1-6), з урахуванням гестаційного і постнатального віку, а також маси тіла дитини при народженні. Якщо результат первинного вимірювання ЗБС крові новонародженого знаходиться у межах 50 мкмоль/л нижче порогового значення для початку ФТ, слід повторно визначити ЗБС й оцінити результат за номограмою.
У хворих новонароджених й у дітей з пролонгованою жовтяницею можуть бути показання до вимірювання рівня ЗБС і непрямого білірубіну (НБ) для діагностики холестазу.
НБ із більшою ймовірністю, ніж ЗБС, проникає через гематоенцефалічний бар’єр й ушкоджує мозок. У пацієнтів із гіпербілірубінемією здатність альбуміну зв’язувати білірубін може бути недостатньою, що призводить до підвищення рівня НБ та збільшує ризик ГБЕ. Водночас відсутні переконливі дані, які б дозволяли пов’язувати вміст альбуміну в крові новонароджених із ризиком розвитку гіпербілірубінемії й ГБЕ.
Новонароджені зі стійким підвищенням ЗБС у межах 35 мкмоль/л нижче порогового значення для початку обмінного переливання крові (ОПК) можуть мати НБ, причини якої включають ГХН, гіпотиреоз, позасудинний крововилив, синдром Криглера – Найяра тощо.
Підвищення концентрації ПБ свідчить про високу ймовірність холестазу, що визначає необхідність додаткового обстеження дитини. Важливо враховувати причини неонатальної прямої гіпербілірубінемії, крім атрезії жовчних шляхів, за наявності яких потрібно своєчасно призначити лікування: інфекції сечовивідних шляхів, сепсис, деякі вроджені порушення метаболізму тощо (табл. 1-2).
Додаткові обстеження для визначення основної причини гіпербілірубінемії, як правило, потрібні для новонароджених дітей, які мають такі ознаки:
- рання гіпербілірубінемія з високим рівнем білірубіну;
- пролонгована гіпербілірубінемія;
- підвищення рівня ПБ;
- нестабільність клінічного стану і/або наявність інших патологічних клінічних ознак.
Необхідні дії
Обов’язкові
Оцінювання рівня білірубіну включає:
- ТкБ.
Виміряти ТкБ у ділянці грудини або чола дитини, в якої підозрюється наявність ЖН. Якщо рівень TкБ у межах 50 мкмоль/л, нижче або перевищує рівень, для якого рекомендовано розпочати ФТ, слід виміряти ЗБС; те саме потрібно зробити, якщо ТкБ ≥257 мкмоль/л.
Вимірювання TкБ не рекомендується:
- у перші 24 год життя дитини;
- у передчасно народжених дітей із ГВ <35 тижнів;
- у випадках пролонгованої жовтяниці;
- у разі виявлення прямої гіпербілірубінемії;
- якщо дитина отримує або отримувала ФТ;
- якщо дитині проводилося обмінне переливання крові (ОПК).
В усіх цих випадках слід обов’язково визначати ЗБС.
Вимірювання ЗБС крові. Необхідно у таких випадках:
- у будь-якої дитини, в якої ЖН виявлена в перші 24 год життя;
- у новонароджених із жовтяницею та ГВ <35 тижнів;
- у будь-якої дитини старше 24 год, якщо під час первинного огляду ЖН здається значущою (нижче рівня пупка);
- у новонароджених із пролонгованою жовтяницею.
Не потрібно вимірювати ЗБС у дітей, які не мають явної ЖН.
Оцінювати результати вимірювань ЗБС за номограмами, які відповідають гестаційному (з урахуванням маси при народженні) і постнатальному віку дитини (рис. 1-6).
Не віднімати показники ПБ від результатів вимірювання ЗБС, визначаючи потребу лікування гіпербілірубінемії у новонародженого.
Повторно визначати ЗБС, якщо результат попереднього вимірювання у межах 50 мкмоль/л нижче порогового значення, для якого рекомендовано розпочати ФТ:
- у новонароджених у відносно задовільному стані з ГВ ≥38 тиж і постнатальним віком більше 24 год за наявності чинників ризику нейротоксичної дії білірубіну в анамнезі (панель 1), повторно визначити ЗБС через 18 год;
- за відсутності таких чинників ризику – через 24 год;
- в інших категоріях новонароджених старше 12 год повторно визначити ЗБС через 6-24 год.
У новонароджених у задовільному стані з ГВ ≥38 тижнів, постнатальним віком більше 24 год і рівнем ЗБС нижче порогового значення для початку ФТ більше, ніж на 50 мкмоль/л, повторні вимірювання недоцільні.
Якщо доступні результати кількох вимірювань ЗБС (або TкБ) для виявлення немовлят із вищим ризиком значущої гіпербілірубінемії, можна використати показник погодинного приросту білірубіну:
- приріст білірубіну ≥5,1 мкмоль/л/год у перші 24 год життя або ≥3,4 мкмоль/л/год у пізнішому віці свідчить про наявність гемолізу;
- у такому випадку слід виконати пряму пробу Кумбса, якщо цього не було зроблено попередньо.
Якщо зафіксоване не пов’язане з дією ФТ спонтанне зниження ЗБС протягом принаймні 6 год, ризик наступного зростання ЗБС є незначним. У цій ситуації додаткові вимірювання ЗБС не потрібні, якщо немає інших тривожних клінічних ознак (підсилення жовтяниці або погіршення стану дитини).
Рівень ЗБС у пуповинній крові (або периферичній крові відразу після народження) та позитивний результат прямої проби Кумбса з пуповинною кров’ю (або з периферичною кров’ю відразу після народження) не слід використовувати для прогнозування ризику значущої гіпербілірубінемії.
Контроль фракцій білірубіну. Одночасно вимірювати ЗБС крові, НБ і ПБ у новонароджених:
- зі стійким підвищенням ЗБС у межах 35 мкмоль/л нижче порогового значення для початку ОПК;
- із пролонгованою жовтяницею;
- у нестабільному клінічному стані з темною сечею та знебарвленими випорожненнями.
Додаткові обстеження. Призначити додаткові обстеження відповідно до рекомендацій (табл. 1, 2).
3.3. Лікування
Положення протоколу. Лікування призначається, коли гіпербілірубінемія досягає небезпечного рівня, незалежно від причини, щоб запобігти ушкодженню мозку дитини. Вирішення щодо того, коли розпочинати терапію і яким методом, ґрунтуються на оцінці результатів вимірювання ЗБС крові залежно від гестаційного і постнатального віку, маси тіла при народженні та наявності чинників ризику нейротоксичної дії білірубіну (панель 1, рис. 1-6).
Для лікування ЖН використовують такі методи:
- стандартну й інтенсивну ФТ;
- внутрішньовенне введення імуноглобулінів (якщо ЖН спричинена ГХН);
- ОПК;
- забезпечення адекватного харчування.
Гіпербілірубінемія і, відповідно, жовтяниця можуть бути спричинені серйозними або навіть небезпечними для життя хворобами, які вимагають термінової діагностики та лікування.
Немовлята, які потребують підсиленого лікування, мають перебувати у відділенні інтенсивної терапії новонароджених (ВІТН).
Обґрунтування. ФТ – втручання, яке найчастіше використовують для лікування дітей із ЖН. ФТ забезпечує швидке зниження рівня білірубіну і запобігає підвищенню ЗБС до рівня, за наявності якого рекомендується ОПК. Близько 0,5-4% новонароджених із ЖН потребують ФТ.
Клінічна відповідь дитини залежить від ефективності ФТ та балансу між швидкістю продукції білірубіну та його знешкодженням. Ефективність ФТ визначається дозою опромінення, яка, у свою чергу, залежить від типу джерела світла, тривалості експозиції, відстані від поверхні шкіри до лампи, а також від площі поверхні тіла немовляти, яка опромінюється.
Початок ФТ визначається рівнем ЗБС залежно від ГВ і постнатального віку на момент обстеження, маси тіла при народженні та наявності чинників ризику нейротоксичної дії білірубіну (рис. 1-6). У динаміці спостереження потрібно переглядати доцільність призначення ФТ, враховуючи нові показники ЗБС крові. ФТ не показана, якщо рівень ЗБС не перевищує поріг, для якого рекомендується розпочати ФТ (рис. 1-6). Показань для профілактичного застосування ФТ немає.
Момент повторного вимірювання рівня ЗБС після початку ФТ та частота подальшого моніторингу цього показника під час ФТ визначаються віком дитини, наявністю чинників ризику нейротоксичної дії білірубіну і траєкторією рівня ЗБС.
Під час ФТ важливо забезпечувати новонароджену дитину достатньою кількістю рідини та контролювати діурез, оскільки екскреція люмірубіну із сечею є основним механізмом, за допомогою якого ФТ знижує рівень ЗБС.
Ентеральне харчування під час ФТ є необхідним для кращого виведення білірубіну з випорожненнями і зменшення зворотного всмоктування білірубіну за рахунок кишково-печінкової циркуляції. Під час ФТ немовлятам слід продовжувати оральне/ентеральне годування. Стандартну ФТ можна переривати для годування та/або догляду за дитиною, а також забору крові.
Якщо рівень ЗБС знаходиться у межах 35 мкмоль/л нижче порогу, для якого рекомендоване ОПК, необхідним є невідкладне лікування для швидкого усунення підвищених концентрацій білірубіну, запобігання ОПК та ГБЕ. Підсилення лікування за таких умов передбачає використання інтенсивної ФТ, внутрішньовенне введення рідини, а також внутрішньовенне введення імуноглобулінів дітям із ГХН. Кілька клінічних досліджень продемонстрували, що внутрішньовенне введення імуноглобулінів може зменшувати потребу в ОПК у немовлят із ГХН.
Лікування слід підсилити, коли ЗБС новонародженого вперше досягає або перевищує значення у межах 35 мкмоль/л нижче порогу, для якого рекомендується ОПК. Період підсилення лікування закінчується, коли рівень ЗБС стає нижчим за порогове значення, для якого рекомендовано підсилення лікування. Після завершення періоду підсилення лікування слід продовжити стандартну ФТ.
Метою ОПК є швидке зниження рівня ЗБС, запобігання проникненню НБ через гематоенцефалічний бар’єр, видалення еритроцитів, вразливих до материнських антитіл, зниження загального рівня гемолітичних антитіл, коригування анемії, якщо вона є.
Під час ОПК переливають кров у кількості, яка дорівнює двом об’ємам циркулюючої крові дитини – 160 мл/кг у доношеної дитини і 180 мл/кг у передчасно народженої (панель 2).
Панель 2
Техніка виконання ОПК
ОПК виконують у ВІТН ЗОЗ III або ІІ рівня медичної допомоги. Відразу після надходження дитини до ВІТН швидко визначають групу та резус-належність крові, щоб у разі потреби якомога скоріше розпочати ОПК.
ОПК є стерильною процедурою, яку виконують з чітким дотриманням усіх відповідних вимог. Протягом інтервалу часу, необхідного для підготовки до виконання ОПК, немовлятам слід проводити інтенсивну ФТ.
Обмінне переливання подвійним об’ємом крові (160-180 мл/кг) замінює приблизно 85% еритроцитів немовляти. Процедура рутинно передбачає катетеризацію вени пуповини, виведення і введення крові аліквотами, які становлять приблизно 10% або менше об’єму крові немовляти.
Для ОПК потрібно використовувати препарати донорської крові, перевірені на наявність вірусів гепатиту В і С, ВІЛ, цитомегаловірусу і збудника сифілісу, а також опромінені для профілактики синдрому «трансплантат проти хазяїна».
Перед переливанням донорські еритроцити і свіжозаморожену плазму змішують, утворюючи «відновлену» донорську кров. Бажаний гематокрит такої крові – 45-55%.
Підготовка необхідного обладнання
- Джерело променевого тепла або кувез.
- Обладнання для реанімації: реанімаційний мішок, реанімаційні маски, джерело кисню.
- Носошлунковий (ротошлунковий) зонд.
- Набір інструментів і матеріалів для катетеризації судин пуповини: стерильні пелюшки, пупкова лігатура, пупкові катетери, триходові крани, пінцети, затискач, ножиці, скальпель, шлунковий зонд, голки, шовк.
- Розчин антисептика.Стерильні шприци об’ємом 5, 10 і 20 мл.
- Стерильні вата та бинт.
- Термометр.
- Пульсоксиметр та монітори для контролю артеріального тиску і серцевої діяльності.
- Водяна баня з контрольованим підігрівом.
Вибір продуктів крові для ОПК
За наявності ГХН за Rh-несумісністю використовують одногрупну з дитиною Rh-негативну еритромасу або Rh-негативну еритромасу 0 (I) групи, змішану з плазмою AB (IV) групи крові або із плазмою, сумісною з кров’ю дитини.
За наявності ГХН за АВ0-несумісністю використовують еритромасу 0 (I) групи з Rh-фактором дитини, змішану з плазмою AB (IV) групи або плазмою, сумісною з кров’ю дитини.
В ургентних випадках, якщо невідома Rh-належність крові дитини, використовують Rh-негативну еритромасу 0 (I) групи, змішану з плазмою AB (IV) групи.
За наявності одночасної несумісності за Rh-фактором та АВ0-системою використовують Rh-негативну еритромасу 0 (I) групи, змішану з плазмою AB (IV) групи.
Види ОПК
У доношених новонароджених об’єм циркулюючої крові (ОЦК) становить 80 мл/кг, у недоношених – 90 мл/кг.
Розрізняють стандартне й ізоволемічне ОПК. Стандартне ОПК виконують за допомогою одного судинного доступу (вена пуповини) з почерговим введенням і виведенням певного об’єму крові. Ізоволемічне ОПК виконують з одночасним виведенням крові дитини з пуповинної (або іншої) артерії та введенням донорської крові у пуповинну (або іншу) вену (такий вид ОПК краще переноситься недоношеними новонародженими або новонародженими з набряковою формою ГХН). Незалежно від виду ОЦК, його виконують двома об’ємами.
Потрібний для приготування відновленої крові об’єм препаратів донорської крові розраховують за однією з наведених нижче формул.
Формула 1
Кількість еритромаси (мл) = Загальний об’єм крові для ОПК × 0,5 (бажаний Ht) /0,7 (Ht еритромаси)
Формула 2
Кількість плазми = загальний об’єм крові для ОПК - об’єм еритромаси
Формула 3
Якщо неможливо визначити гематокрит, співвідношення між плазмою та еритроцитами орієнтовно становить 1:2,5.
Гематокрит відновленої крові для переливання повинен складати 45-55%.
Температура відновленої крові для переливання повинна бути 37 °С.
Підготовка до виконання ОПК
Перевірити групу і Rh-належність препаратів донорської крові.
Приготувати відновлену донорську кров.
Виконати проби на групову, індивідуальну (крові дитини і матері) та біологічну сумісність.
Зважити дитину.
Практичні аспекти виконання ОПК
Перед початком ОПК аспірувати вміст шлунка і залишити у ньому зонд.
Забезпечити безперервний моніторинг рівня сатурації гемоглобіну киснем і частоти серцевих скорочень дитини, продовжуючи його під час виконання процедури; артеріальний тиск і наявність сечі перевіряти не рідше 1 разу на годину.
Під час ОПК продовжувати ФТ і вимірювати температуру тіла дитини мінімум 1 раз на годину.
Помити й дезінфікувати руки.
Одягнути стерильні халат, шапочку, маску і рукавички.
Обробити залишок пуповини і ділянку шкіри довкола нього антисептиком.
Накласти на ділянку пупкового кільця фенестровану стерильну пелюшку.
Накласти на залишок пуповини (бажано на шкірну частину) стерильну пупкову лігатуру і затягнути її.
Зрізати залишок пуповини відразу під клемою стерильним скальпелем та ідентифікувати судини пуповини.
Утримуючи край вени пінцетом, розширити її просвіт відповідними рухами браншу затискача, видалити тромби (якщо є) й увести у вену катетер на мінімальну глибину, що дозволяє отримати вільний зворотний потік крові, після чого зафіксувати катетер.
Розпочати ОПК, взявши першу порцію крові у дитини.
Кров виводити та вводити рівними об’ємами зі швидкістю 3-4 мл/хв:
- по 20 мл дітям із масою тіла понад 3000 г;
- по 15 мл дітям із масою тіла 2000-3000 г;
- по 10 мл дітям із масою тіла 1000-2000 г;
- по 5 мл дітям із масою тіла 850-1000 г;
- по 3 мл дітям із масою тіла менше 850 г.
У першій та останній порції виведеної крові визначити рівень ЗБС.
У разі використання цитратного консерванту після введення кожних 100 мл відновленої цитратної донорської крові додатково ввести 2 мл 10% розчину кальцію глюконату. За умови використання іншого консерванту додатково вводити розчин кальцію глюконату не потрібно.
Потребу профілактичного введення антибіотика після завершення ОПК визначати індивідуально. Інфекція трапляється нечасто, але є найпоширенішим ускладненням.
Якщо вирішено призначити антибіотик, відразу після завершення процедури внутрішньовенно ввести разову дозу ампіциліну.
У випадку, якщо дитина після ОПК не потребуватиме інфузійної терапії, необхідно витягнути катетер та накласти давлючу пов’язку на пуповинний залишок.
У випадку, якщо дитина після ОПК потребуватиме внутрішньовенного введення рідини, остаточно зафіксувати катетер у вені пуповини.
Після завершення ОПК визначити рівень ЗБС через 1-2 год, гематокрит, вміст глюкози у крові і зробити загальний аналіз сечі через 4-6 год.
Оформлення документації
Заповнити протокол ОПК.
Ускладнення
Виконання ОПК пов’язане з ризиками внаслідок використання препаратів донорської крові та виконанням самої процедури. Можливі ускладнення включають інфекційні захворювання, що передаються через кров, тромбоцитопенію, коагулопатію, хворобу «трансплантат проти хазяїна», некротизуючий ентероколіт, тромбоз воротної вени, електролітні порушення (наприклад, гіпокальціємія та гіперкаліємія), серцева аритмія тощо.
Немовлят з показаннями до підсилення лікування, які можуть потребувати ОПК, слід переводити у ВІТН. Після госпіталізації потрібно швидко визначити групу та резус-належність крові і катетеризувати вену пуповини, забезпечивши периферичне місцезнаходження кінчика катетера, щоб за потреби якомога скоріше розпочати ОПК.
На сьогодні немає науково-доказової бази рутинного застосування медикаментозних препаратів для лікування ЖН.
Недостатнє харчування супроводжується зменшеним споживанням калорій і нутрієнтів, а також призводить до зневоднення дитини, що підвищує ризик гіпербілірубінемії.
Дітей на грудному вигодовуванні, які під час ФТ споживають недостатню кількість грудного молока і мають надмірну втрату маси тіла (>10 % маси тіла при народженні) або ознаки гіповолемії, потрібно догодовувати зцідженим материнським (бажано) або пастеризованим донорським молоком. Можна використовувати молочну суміш, якщо грудне молоко недоступне. Якщо грудне вигодовування перервано, його слід відновити якомога скоріше.
Немає доказів того, що внутрішньовенне введення рідини забезпечує значну додаткову користь. Проте внутрішньовенна інфузія є потенційним варіантом корекції дегідратації, гіповолемії і/або гіпернатріємії у зневоднених немовлят, які споживають недостатню кількість рідини з молоком матері.
Необхідні дії
Обов’язкові
- Фототерапія.
Розпочати стандартну ФТ, якщо рівень ЗБС досягає порогового значення для початку ФТ на номограмі відповідно до ГВ і постнатального віку дитини на момент обстеження, маси тіла при народженні та наявності чинників ризику нейротоксичної дії білірубіну (рис. 1-6).
Переконатися, що відповідне обладнання використовується згідно з інструкціями виробника, зокрема, лампа знаходиться на належній відстані від поверхні тіла дитини.
Перевірити рівномірність опромінення поверхні тіла дитини – потрібно, щоб світло охоплювало максимальну площу поверхні (дитина повністю роздягнена, немає необхідності прикривати хлопчикам калитку світлонепроникною пов’язкою; очі дитини захищені спеціальними окулярами або світлонепроникною пов’язкою).
Доношена дитина під час ФТ може знаходитися у ліжечку, передчасно народжених дітей слід помістити в інкубатор.
Забезпечити постійне спостереження за дитиною, зокрема, моніторинг температури тіла, контроль адекватності харчування за допомогою щоденного зважування дитини й оцінювання кількості мокрих підгузків, виявлення виділень з очей та інших ознак кон’юнктивіту.
Після початку ФТ повторювати вимірювання ЗБС кожні 4-6 год доти, поки не буде досягнуто контролю над рівнем ЗБС; після того як рівень ЗБС стабілізується або почне знижуватися – через кожні 12-24 год.
У немовлят, які були повторно госпіталізовані для лікування за допомогою ФТ, повторити вимірювання ЗБС через 2-3 год після початку ФТ, щоб оцінити її ефективність.
Припинити ФТ, якщо ЗБС знизиться щонайменше на 35 мкмоль/л нижче порогового значення, яке вказувало на потребу початку ФТ. Триваліший період ФТ є обґрунтованим, якщо існує ризик повторного зростання ЗБС (ГВ <38 тижнів, постнатальний вік <48 год на момент початку ФТ, наявність ГХН, рівень ЗБС у межах 35 мкмоль/л нижче порогового значення, що свідчить про потребу ФТ).
Перевірити рівень ЗБС через 6-12 год після припинення ФТ і повторно через 24 год у немовлят із ГХН, які отримували ФТ до 48 год життя; через 18-24 год після припинення ФТ – в усіх інших немовлят.
Довести до відома батьків інформацію про лікування гіпербілірубінемії за допомогою ФТ (зокрема, щодо очікуваної тривалості лікування, можливості сумісного перебування з матір’ю, необхідності продовжувати грудне вигодовування та батьківського догляду за дитиною).
- Підсилення лікування.
Якщо дитина перебуває у ЗОЗ, де немає ВІТН, забезпечити її невідкладне переведення до лікарні, в якій є таке відділення.
Розпочати інтенсивну ФТ і призначити рідину внутрішньовенно (10% розчин глюкози і 0,9% розчин натрію хлориду у співвідношенні 3:1) у кількості 80 мл/кг/добу для новонароджених віком <48 год; від 80 до 100 мл/кг/добу для дітей віком ≥48 год. Подальші коригування базуються на вимірюванні електролітів сироватки крові.
Призначати немовлятам із ГХН внутрішньовенний імуноглобулін (0,5-1,0 г/кг введення протягом 2-4 год). За потреби повторити через 12 год.
Провести термінове лабораторне обстеження дитини (ЗБС, ПБ, ЗАК, групова та резус-належність крові, інші біохімічні показники відповідно до клінічних показань) та замовити продукти крові для запланованого ОПК. ОПК слід робити у ЗОЗ, де є ВІТН.
Рівень ЗБС крові вимірювати принаймні кожні 2 год від початку періоду підсилення лікування до його закінчення.
Не переривати інтенсивну ФТ для годування, продовжувати ентеральне харчування, підтримку лактації/грудного вигодовування. Інтенсивну ФТ можна переривати для догляду за очима дитини та на час забору крові.
- Обмінне переливання крові.
Невідкладно виконати ОПК, якщо:
- є клінічні ознаки ГБЕ (погане смоктання, пронизливий крик або повторне апное, дистонія/гіпертонус, судоми, опістотонус);
- рівень ЗБС дорівнює або перевищує порогове значення для ОПК на відповідній номограмі (рис. 1-6);
- якщо за наявності ГХН погодинний приріст ЗБС (за умови проведення інтенсивної ФТ) ≥7 мкмоль/л (несумісність за Rh-фактором) і ≥ 10 мкмоль/л (несумісність за системою АВ0).
Не використовувати співвідношення альбумін/білірубін для визначення потреби ОПК.
Якщо під час підготовки до ОПК (до початку останнього) концентрація ЗБС стає нижчою від порогового значення, що свідчить про потребу ОПК, й у немовляти немає ознак ГБЕ, втручання можна відкласти; водночас важливо продовжувати виконання інших лікувальних заходів і контролювати концентрацію ЗБС кожні 2 год, поки вона не стане нижче порогового значення для підсилення лікування.
Новонародженим дітям із ГХН і тяжкою анемією, що загрожує життю (водянка плода, шок) для стабілізації стану серцево-судинної системи невідкладно перелити 10 мл/кг 0 (I) резус-негативних еритроцитів. За наявності тяжких дихальних розладів, спричинених плевральним випотом і/або асцитом, зробити торакоцентез і/або парацентез. Після стабілізації стану серцево-судинної системи невідкладно виконати ОПК у ВІТН, використовуючи ізоволемічну техніку (панель 2).
За наявності симптоматичної анемії та стабільного серцево-судинного статусу у новонароджених із ГХН вибір між ОПК та простим переливанням еритроцитарної маси ґрунтується на таких чинниках:
- якщо у дитини є ознаки ГБЕ, робити ОПК;
- якщо у дитини тяжка анемія та гіпербілірубінемія без ознак ГБЕ, робити ОПК за умови, що гематокрит <25% та/або рівень ЗБС дорівнює або перевищує порогове значення для ОПК (рис. 1-6);
- якщо ЗБС не досягає порогового значення для ОПК, а симптоми анемії помірні (гематокрит 25-35%), перелити еритроцитарну масу;
- перелити еритроцитарну масу, якщо є затримка виконання ОПК з будь-якої причини.
Продовжувати ФТ під час ОПК (можна використовувати лише одну лампу ФТ).
Після завершення ОПК відновити ФТ у тому ж режимі, що був перед ОПК. Визначити рівень ЗБС крові через 1-2 год після завершення ОПК.
Під час ОПК не слід зменшувати об’єм перелитої крові (завжди переливати 2 об’єми циркулюючої крові), вводити альбумін і рутинно вводити кальцію глюконат (панель 2).
- Використання лікарських засобів.
Не використовувати для лікування ЖН лікарські засоби, які можуть збільшити ризик розвитку ГБЕ або не мають достатньо доказів ефективності і безпеки.
- Харчування.
Годувати новонароджену дитину грудьми 8-12 разів на день.
Своєчасно виявляти симптоми недостатності харчування і дегідратації.
Не догодовувати рутинно немовлят, які отримують ФТ.
Внутрішньовенне введення додаткової рідини рутинно не показане. Критеріями призначення введення додаткової рідини є:
- передбачення потреби, враховуючи індивідуальні особливості для корекції дегідратації;
- за наявності гіповолемії або гіпернатріємії з гіповолемією;
- якщо пероральне споживання рідини є недостатнім з будь-яких причин;
- під час проведення інтенсивної ФТ.
Бажані
Перевірити потужність джерела світла при ФТ на відповідність рекомендованим параметрам.
3.4. Планування виписки
Положення протоколу. Виписку новонароджених планують і здійснюють відповідно до чинних галузевих стандартів у сфері охорони здоров’я. За наявності візуальних ознак ЖН у дитини перед випискою слід забезпечити необхідні діагностичні кроки для вирішення питання щодо можливості виписки дитини додому для амбулаторного спостереження. Якщо вирішено виписувати новонароджену дитину додому, у виписному епікризі потрібно означити ймовірні ризики та забезпечити передачу інформації лікарю-педіатру або лікарю загальної практики – сімейному лікарю.
Необхідні дії
Обов’язкові
Оцінити клінічні ознаки ЖН перед випискою дитини із ЗОЗ (особливо якщо її вік становить менше 72 год).
Якщо дитина не потребувала лікування ЖН, за умови задовільного клінічного стану, налагодженого грудного вигодовування і поширення жовтяничного забарвлення шкіри на момент виписки не нижче пупкової лінії, дитину можна виписати додому під нагляд дільничного лікаря-педіатра або лікаря загальної практики – сімейного лікаря.
У разі успішної ФТ виписувати дитину не скоріше, ніж через 24 год після завершення ФТ, якщо клінічний стан дитини задовільний, а ознак прогресування ЖН немає.
Усім дітям, яких лікували за допомогою ФТ, перед випискою потрібно оцінити функцію слуху за допомогою аудіометрії. Якщо дитина не потребувала ФТ, але на момент імовірної виписки жовте забарвлення шкіри поширюється нижче пупкової лінії, визначити рівень ЗБС крові.
Якщо рівень ЗБС свідчить про необхідність ФТ (залежно від наявності чинників ризику), відкласти виписку принаймні на 24 год або перевести дитину у відділення новонароджених.
Якщо рівень ЗБС більше, ніж на 50 мкмоль/л нижче від порогового значення для початку ФТ, імовірність наступного зростання рівня ЗБС є мінімальною і дитину можна виписати додому.
Якщо рівень ЗБС знаходиться у межах 50 мкмоль/л нижче порогового значення для початку ФТ, питання виписки вирішувати індивідуально.
Надати лікарю первинної ланки медичної допомоги, який спостерігатиме за немовлям після виписки з акушерського стаціонару, інформацію про стан новонародженого (включно зі встановленим діагнозом, переліком виконаних лікувальних заходів, результатами проби Кумбса, останніми показниками TкБ, ЗБС і віком, в якому вони визначалися).
Організувати спостереження за дітьми з ЖН після виписки лікарем-педіатром або лікарем загальної практики – сімейним лікарем (у випадку виписки на 3 добу життя необхідно оглянути дитину вдома до досягнення віку 5 діб). Якщо відповідні огляд та спостереження є неможливими або сумнівними, виписку слід відкласти.
Перед випискою батькам дитини надати письмову й усну інформацію про ЖН, зазначивши, що повторне медичне консультування потрібно, якщо у дитини з’являться симптоми небезпеки.
IV. Опис етапів медичної допомоги
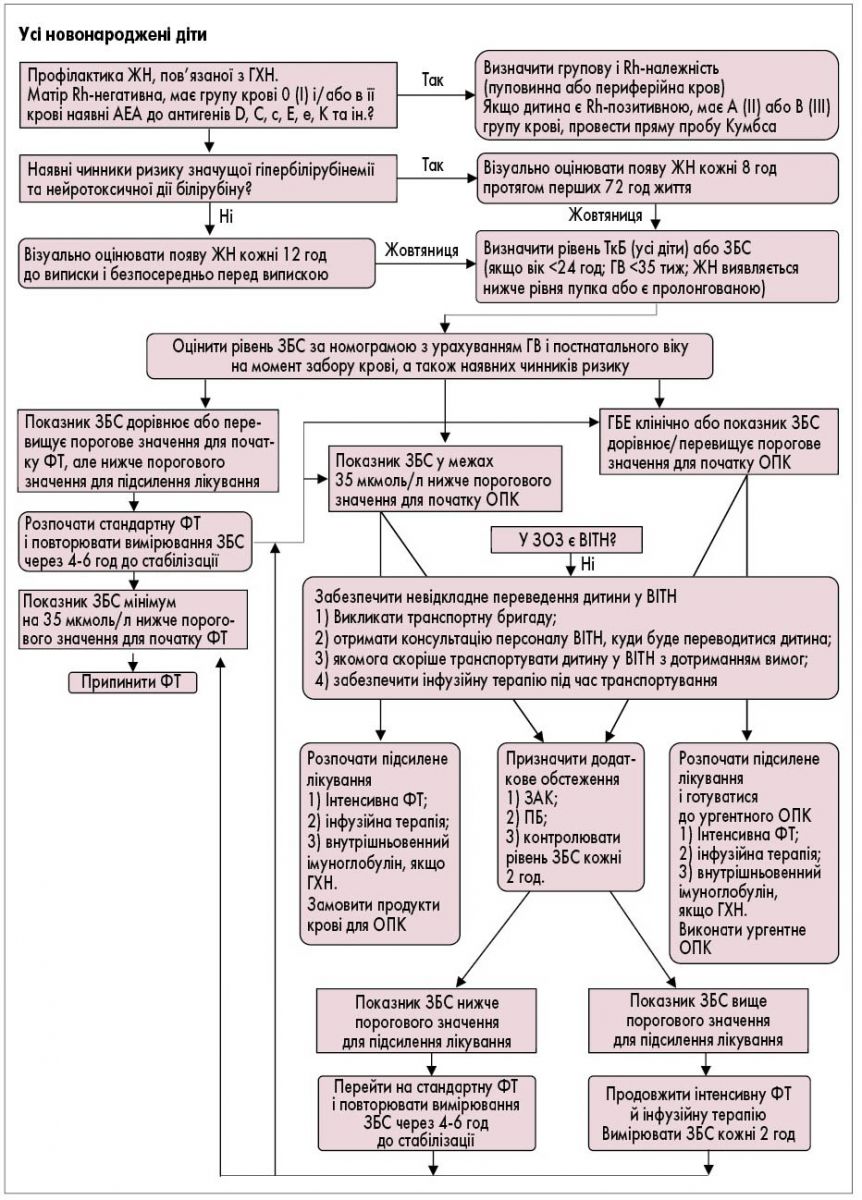
Алгоритм надання медичної допомоги дітям із ЖН
V. Ресурсне забезпечення виконання протоколу
На момент затвердження цього УКПМД засоби матеріально-технічного забезпечення дозволені до застосування в Україні. Під час розробки та застосування внутрішніх документів ЗОЗ/клінічного маршруту пацієнта необхідно перевірити реєстрацію в Україні засобів матеріально-технічного забезпечення, які вносяться до документу, та відповідність призначення лікарських засобів інструкції для медичного застосування лікарського засобу, затвердженої Міністерством охорони здоров’я України. Державний реєстр лікарських засобів України знаходиться за посиланням http://www.drlz.com.ua/
5.1. Кадрові ресурси
Лікарі: педіатр-неонатолог, анестезіолог дитячий, які мають сертифікати післядипломної підготовки та безперервний професійний розвиток (БПР) з неонатології відповідно до чинних вимог; середній медичний персонал, який бере участь у наданні медичної допомоги новонародженим дітям.
5.2. Матеріально-технічне забезпечення
Оснащення: відповідно до табеля оснащення.
Лікарські засоби: розчини глюкози різних концентрацій (40%, 10%, 5%); вода очищена; розчин натрію хлориду 0,9%; розчин кальцію глюконату 10%; імуноглобулін людини нормальний для внутрішньовенного введення.
VI. Індикатори якості медичної допомоги
Для оцінки якості надання медичної допомоги новонародженим дітям із жовтяницею рекомендовано використовувати індикатори, які є інструментами клінічного аудиту та моніторингу якості надання медичної допомоги. Застосування цих індикаторів дозволяє не лише оцінювати якість медичної допомоги у ЗОЗ, що надають спеціалізовану медичну допомогу новонародженим, а також порівнювати якість медичної допомоги між декількома ЗОЗ не тільки у межах однієї області, а також між різними регіонами. Для кожного індикатора існує порогове значення, а також описана методологія його розрахунку. Джерелом для встановлення порогового значення кожного з індикаторів є результати досліджень, вже перевірений існуючий досвід ЗОЗ/регіонів, а також думки фахівців та експертів.
Запропоновані індикатори якості є базовими для всіх ЗОЗ і є складовими процесу надання допомоги новонародженій дитині з жовтяницею. Водночас частину ЗОЗ можуть відрізняти не лише певні особливості надання медичної допомоги новонародженим, але й особливі проблеми, а тому на рівні ЗОЗ/регіону можуть бути розроблені додаткові індикатори якості, які будуть враховувати ці особливості і сприятимуть покращенню якості надання медичної допомоги.
6.2. Паспорти індикаторів якості медичної допомоги
- Наявність у ЗОЗ, що надає спеціалізовану медичну допомогу новонародженим, внутрішніх документів ЗОЗ щодо надання допомоги новонародженим дітям із ЖН.
- Відсоток новонароджених дітей із ЖН, у яких оцінювали наявність чинників ризику значущої гіпербілірубінемії та нейротоксичної дії білірубіну, від усіх немовлят, які потребували такої оцінки.
- Відсоток новонароджених дітей із ЖН, в яких (хоча б одноразово) визначали ТкБ, від усіх немовлят, які потребували такого обстеження.
- Відсоток новонароджених дітей із ЖН, в яких (хоча б одноразово) визначали ЗБС за наявності показань, від усіх немовлят, які потребували такого обстеження.
- Відсоток новонароджених дітей із ЖН, яким розпочато ФТ за наявності показань, від усіх немовлят, які потребували ФТ.
***
УКПМД «Жовтяниця новонароджених дітей» за своєю формою, структурою та методичними підходами щодо використання вимог доказової медицини розроблений відповідно до Методики розробки та впровадження медичних стандартів медичної допомоги на засадах доказової медицини, затвердженою наказом № 751 Міністерства охорони здоров’я України від 28 вересня 2012 року, зареєстрованого в Міністерстві юстиції України 29 листопада 2012 року за № 2001/22313.
УКПМД «Жовтяниця новонароджених дітей» розроблено на підставі адаптованої клінічної настанови «Жовтяниця новонароджених дітей», в якій наведено рекомендації з найкращої клінічної практики щодо спостереження та лікування новонароджених дітей з ЖН. Ознайомитися з клінічною настановою можна за посиланням: https://www.dec.gov.ua/cat_mtd/galuzevi-standarti-ta-klinichni-nastanovi/.
Цей УКПМД не охоплює всіх можливих ситуацій і не описує єдино правильний спосіб надання медичної допомоги новонародженій дитині із жовтяницею. Різноманітні варіанти клінічної практики, які враховують конкретні умови й обставини, а також особливості надання медичної допомоги на місцях можуть бути прийнятними. Остаточне вирішення щодо оптимального варіанту надання медичної допомоги новонародженій дитині із ЖН мають ухвалювати відповідні працівники охорони здоров’я з урахуванням наявних клінічних даних, результатів додаткового обстеження і методів лікування, що застосовувалися.
Текст адаптовано й уніфіковано відповідно до стандартів тематичного випуску медичної газети «Здоров’я України».
Повний текст протоколу на сайті https://moz.gov.ua
Тематичний номер «Педіатрія» № 3 (69) 2023 р.
СТАТТІ ЗА ТЕМОЮ Педіатрія
Вроджена дисфункція кори надниркових залоз (ВДКНЗ) – це захворювання з автосомно-рецесивним типом успадкування, в основі якого лежить дефект чи дефіцит ферментів або транспортних білків, що беруть участь у біосинтезі кортизолу. Рання діагностика і початок лікування пацієнтів з ВДКНЗ сприяє покращенню показників виживаності та якості життя пацієнтів....
Алергічний риніт (АР) є поширеним запальним захворюванням верхніх дихальних шляхів (ВДШ), особливо серед педіатричних пацієнтів. Ця патологія може знижувати якість життя, погіршувати сон та щоденну продуктивність. Метою наведеного огляду є надання оновленої інформації щодо епідеміології АР та його діагностики, з урахуванням зв’язку з бронхіальною астмою (БА). ...
Американська академія педіатрії (AAP) оновила рекомендації щодо контролю грипу серед дитячого населення під час сезону 2023-2024 рр. Згідно з оновленим керівництвом, для профілактики та лікування грипу в дітей необхідно проводити планову вакцинацію з 6-місячного віку, а також своєчасно застосовувати противірусні препарати за наявності показань. ...
Поширеність і вплив алергічних захворювань часто недооцінюють [1]. Ключовим фактором алергічної відповіді є імуноглобулін (Ig) Е, присутній на поверхні тучних клітин і базофілів. Взаємодія алергену з IgЕ та його рецепторним комплексом призводить до активації цих клітин і вивільнення речовин, у тому числі гістаміну, які викликають симптоми алергії [2]. Враховуючи ключову роль гістаміну в розвитку алергічних реакцій, при багатьох алергічних станах, включаючи алергічний риніт і кропив’янку, пацієнту призначають антигістамінні препарати [3, 4]....