Базисні причини психосоматичних розладів і ренесанс полірецепторної фармакотерапії
За прогнозами ВООЗ, до 2020 року нейропсихічні розлади посядуть перше місце серед неінфекційних хвороб і паралізують економічне життя на планеті (WHO, 2006). Особливо актуальною є проблема соматизації – схильності пацієнта переживати психологічний стрес на фізіологічному рівні (Lipowsky J., 1988). Це призводить до формування психосоматичних розладів (ПСР), які виявляються тривогою та депресією, спричиняють погане самопочуття й непрацездатність пацієнтів і часто трапляються в практиці лікарів різних спеціальностей (WHO, 2017).

Основні причини ПСР і сучасні принципи їх лікування розглянув у своїй доповіді професор кафедри пропедевтики внутрішньої медицини № 2 Національного медичного університету ім. О.О. Богомольця, доктор медичних наук Сергій Геннадійович Сова на науково-практичній конференції з міжнародною участю «ХІ Нейросимпозіум» (10-12 вересня 2019 року, м. Одеса).
Акцентуючи на актуальності проблеми, професор навів вислів Сократа: «Великою помилкою є те, що тілесні й душевні хвороби лікують різні лікарі, адже тіло та душа нероздільні». Принаймні половина пацієнтів, які звертаються до лікаря із соматичними скаргами, потребують корекції емоційного стану (Чабан О., 2009), а понад 90% пацієнтів з емоційними розладами звертаються до терапевтів і лікарів загальної практики (Мороз С., 2011).
Визначення. ПСР – це група хворобливих станів, які трапляються через взаємодію психічних і соматичних факторів і виявляються соматизацією психічних порушень, психічними розладами, що відбивають реакцію на соматичну хворобу, чи соматичною патологією під впливом психогенних факторів.
Базисні причини ПСР. Близько 70% ПСР становлять емоційні порушення. У третини пацієнтів вони зумовлені генетичними причинами, ще у чверті – проблемами в ранньому дитинстві, в 30% – проблемами в пізніші періоди життя, в 10% – соціальними чинниками, тоді як на інші причини припадає до 5% випадків (Чабан О., 2017).
До генетичних чинників належать особливості індивіда та психічного реагування, алекситимія, аутизм. Серед патогенетичних механізмів розглядають особливості рецепторів і синтезу нейромедіаторів, інволютивний медіаторний дефіцит і порушення у відділах нервової системи чи в нейрональних зв’язках, які беруть участь у формуванні та модуляції емоцій. Так, дзеркальні нейрони острівкової зони скроневої частки головного мозку відіграють важливу роль у витісненні емоційного конфлікту та проекції сигналу в різні ділянки неокортексу, наслідком чого в пацієнта з’являються найрізноманітніші соматичні скарги. Витіснення у фронтотемпоральні ділянки кори частіше спричиняє тривогу, тоді як конверсія в тім’янопотиличні ділянки переважно супроводжується депресією.
Проблеми, пов’язані з формуванням особистості, формують у дитини основну базальну емоцію (страх), яка згодом виливається в тривожні або інші емоційні розлади, тож і в соматизацію. До цих причин зараховують конфлікти в сім’ї, соціальні умови, дефіцит любові й уваги (особливо у віці до 5 років), насилля, дефіцит логічного пояснення «що можна, а що не можна».
Не менше важать причини, закладені в наступних періодах дитинства й пов’язані з дефектами виховання. Так, зміна принципів заохочення/покарання однакових учинків за різних обставин порушує критичну оцінку ситуації, надмірна опіка погіршує здатність самостійно ухвалювати рішення, тоді як відсутність підтримки й байдужість провокують безпорадність. Неоднакове ставлення до дітей або осуд їх перед друзями породжують злість, образу та заздрощі; погрози й залякування спричиняють дитячу емоцію непевності себе. Несприятливо впливають на дитину батьківська надмірна лояльність або, навпаки, суворість і перфекціонізм.
Серед інших можливих причин ПСР слід зазначити психологічні травми, тривалий стрес, нозогенії, соматогенії, блокування таких потреб, як любов і турбота, соціальне й політичне напруження, метаболізацію (метаболічний синдром і його компоненти, неалкогольна жирова хвороба печінки), адикції та надуживання, дефіцит психологічної допомоги й дефекти терапії.
Принципи терапії. ПСР формуються через неспроможність людини пережити емоційний конфлікт на психологічному рівні, тому найважливішим завданням лікаря є ідентифікація конфлікту, а пацієнт має його усвідомити.
Розрізняють три основні принципи терапії: етіотропний, патогенетичний і симптоматичний. Етіотропний полягає у виключенні «субстратної» хвороби, ідентифікації й усвідомленні причини з наступним впливом на неї шляхом соматичного й неврологічного обстеження та психотерпії. Патогенетичний принцип передбачає психофармакотерапію, метаболічну терапію та методи «зворотного зв’язку».
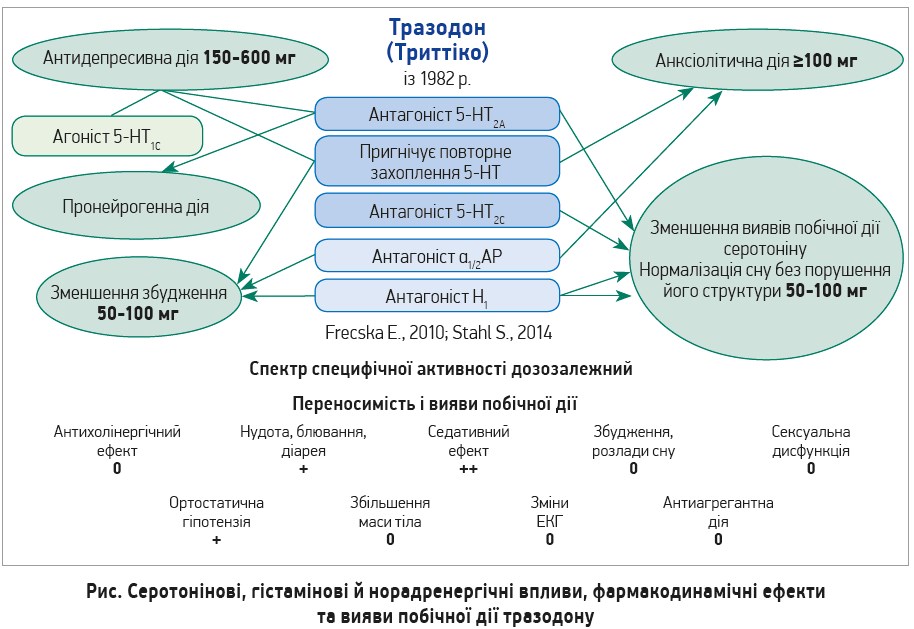
Власне психофармакотерапія на сьогодні є основою патогенетичної терапії ПСР. Слід наголосити: після тривалого періоду панування селективних інгібіторів зворотного захоплення серотоніну (ЗЗС) відбувається ренесанс полірецепторної терапії. Відомий американський психіатр, професор Стефан Стахл стверджує, що сучасна парадигма лікування великих депресивних розладів зміщується від вибіркового пригнічення ЗЗС до поєднання цього механізму з іншими фармакологічними впливами в межах серотонінової системи (Stahl S., 2014). Найкраще це завдання реалізує тразодон – модулятор серотонінової системи з мультимодальною рецепторною дією, котра забезпечує антидепресивний, анксіолітичний, пронейрогенний ефекти, нормалізацію сну та зменшення збудження. Спектр специфічної активності тразодону дозозалежний: у дозах до 75-100 мг переважає гіпноседативний ефект, після 100-150 мг починається протитривожна дія, антидепресивний ефект потребує вищих доз (рис.).
Тразодон застосовують у світі понад 30 років, отож доказова база ефективності та безпеки препарату достатня й переконлива (Fagiolini A. et al., 2012). Результати прямих порівнянь із такими антидепресантами, як іміпрамін, амітриптилін, мапротилін, сертралін, міансерин, міртазалін, флювоксамін, венлафаксин, бупропіон і флуоксетин, показують, що антидепресивний ефект тразодону порівнянний із селективними інгібіторами ЗЗС (Blacker R. et al.,1988; Davey A., 1988; Debus J. et al., 1988; Moon C. et al., 1988; Botros W. et al., 1989; Beasley C. et al., 1991; Cunningham L. et al., 1994; Weisler R. et al., 1994; Van Moffaert M. et al., 1995; Munizza C. et al., 2006).
За рандомізованого подвійного сліпого порівняння впливу тразодону й пароксетину позитивний ефект мали понад 85% пацієнтів із кожної групи, 2/3 пацієнтів мали ремісію. Проте тразодон значно краще усував порушення сну (Kasper S. et al., 2005). Нещодавно проведений систематичний огляд седативної та снодійної ефективності тразодону виявив, що препарат має сприятливий профіль переносимості й безпеки та мінімальний ризик формування залежності. Отже, тразодон є препаратом вибору за наявності безсоння у структурі депресії, особливо в пацієнтів із супутніми серцево-судинними захворюваннями, при соматоформних больових розладах, деменції, алкогольній залежності, психіатричних розладах, безсонні через вагітність і після менопаузи, посттравматичному стресовому розладі та в здорових людей із порушеннями сну, надуживанням кофеїну тощо. У наступних дослідженнях доцільно вивчити ефективність і безпеку тразодону в дітей, у різних вікових групах пацієнтів із вторинним безсонням (апное уві сні, хронічний біль, фіброміалгії), а також дослідити здатність препарату покращувати прогноз інших захворювань шляхом нормалізації сну (Jaffer K. et al., 2017).
Щодо профілю безпеки, то згідно з настановами Національної служби охорони здоров’я Великої Британії тразодон є препаратом першої лінії для лікування пацієнтів із депресивними розладами, порушеннями сну, а також у пацієнтів із підвищеним ризиком кровотеч і серцево-судинною патологією (NHS, 2017). Препарат має мінімум виявів побічної дії (рис.), серед них седативний ефект, який за тривожно-депресивних розладів часто відіграє позитивну роль.
На вітчизняному ринку тразодон представлений препаратом Триттіко (країна-виробник – Італія, постачальник – ТОВ «ДілеоФарма») в кількох формах: таблетки пролонгованої дії по 75 або 150 мг, а також вкриті плівковою оболонкою Триттіко ХR по 300 мг, які мають правильну фармакокінетичну модель без піків зі швидким формуванням плато, що забезпечує абсолютну ефективність при вживанні 1 раз на добу.
Показання та рекомендовані дози: за тривожно-депресивних розладів краще призначати Триттіко XR 150 або 300 мг до прийому їжі. При порушеннях сну, вегетостабілізації, ситуативних соматоформних розладах (СФР) рекомендовано Триттіко в дозі 75 мг за 1-2 год до сну. Якщо СФР персистує понад місяць, призначають Триттіко по 150 мг на добу перед сном. Початкова доза завжди має становити 75-150 мг перед сном із поступовим титруванням (за необхідності) до досягнення добової дози 300 мг за 1-2 прийоми.
Отже, за недостатнього ефекту від етіотропної терапії ПСР препаратом вибору є дієвий і безпечний модулятор серотонінової системи тразодон (Триттіко), мультимодальна рецепторна дія котрого забезпечує дозозалежний гіпноседативний, анксіолітичний та антидепресивний ефекти.
Підготувала Ольга Королюк
Медична газета «Здоров’я України 21 сторіччя» № 5 (474), березень 2020 р.
СТАТТІ ЗА ТЕМОЮ Неврологія
Стрес і тривожність чинять потужний несприятливий вплив і на самопочуття окремих індивідуумів, і на загальний стан здоров’я всієї популяції світу. Цей несприятливий вплив значно підсилили пандемія COVID‑19 та війна в Україні (Celuch M. et al., 2023)....
16-17 лютого в Києві відбувся науково-практичний майстер-клас «Хронічний стрес сьогодення: обрані запитання про здоров’я жінки в різні вікові періоди». Під час заходу виступили фахівці різних спеціальностей, було обговорено важливі аспекти жіночого здоров’я як психологічного, так і фізичного. Доповіді присвячувалися різноманітним питанням, зокрема репродуктивним проблемам, онкологічним захворюванням, психосоматичним розладам. Під час події виступила засновниця Академії довголіття Dr. Skytalinska, віцепрезидент Асоціації дієтологів України, лікар-дієтолог Оксана Василівна Скиталінська. Доповідь Оксани Василівни була присвячена впливу тривалого стресу на харчування та пов’язані з цим наслідки для здоров’я жінок. Окрім пояснення механізмів негативного впливу стресу, під час доповіді лікарка також надала важливі практичні рекомендації стосовно здорового харчування....
Події останніх 5 років є неабияким викликом для психічного стану кожного українця: спочатку – пандемія коронавірусу та запроваджені через неї карантинні обмеження, а далі – повномасштабне російське вторгнення, що триває уже понад 2 роки. Все це спричиняє погіршення психічного здоров’я населення. Такі надзвичайні ситуації, що характеризуються загрозою з невизначеною тривалістю, створюють масивне стресове навантаження, яке підсилюється відчуттям самотності та відчуженості, підвищують тривожність, а також є підґрунтям розвитку психічних розладів. Відомо, що ці стани порушують розумову діяльність, тобто перешкоджають концентрації та аналізу інформації. ...
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....