Роль фіксованої комбінації базального інсуліну та агоніста глюканоподібного пептиду‑1 в інтенсифікації лікування цукрового діабету 2 типу
Клінічний досвід застосування фіксованої комбінації інсуліну гларгін та ліксисенатиду (Соліква)
 5 листопада 2020 року, за підтримки компанії Sanofi, відбулася довгоочікувана зустріч провідних експертів у галузі діабетології. Увазі учасників заходу була репрезентована новітня інформація щодо використання першої представленої в Україні фіксованої комбінації інсуліну гларгін та агоніста рецептора глюканоподібного пептиду‑1 (арГПП‑1) ліксисенатиду. Головним доповідачем виступив один із провідних іспанських ендокринологів – доктор медицини Francisco Javier Ampudia-Blasco (Франциско Хав’єр Ампудія-Бласко). Презентації охопили широкий спектр питань стосовно інновацій у менеджменті пацієнтів із цукровим діабетом (ЦД), зокрема результати недавніх клінічних досліджень та практичні аспекти інтенсифікації лікування ЦД 2 типу в умовах реальної клінічної практики.
5 листопада 2020 року, за підтримки компанії Sanofi, відбулася довгоочікувана зустріч провідних експертів у галузі діабетології. Увазі учасників заходу була репрезентована новітня інформація щодо використання першої представленої в Україні фіксованої комбінації інсуліну гларгін та агоніста рецептора глюканоподібного пептиду‑1 (арГПП‑1) ліксисенатиду. Головним доповідачем виступив один із провідних іспанських ендокринологів – доктор медицини Francisco Javier Ampudia-Blasco (Франциско Хав’єр Ампудія-Бласко). Презентації охопили широкий спектр питань стосовно інновацій у менеджменті пацієнтів із цукровим діабетом (ЦД), зокрема результати недавніх клінічних досліджень та практичні аспекти інтенсифікації лікування ЦД 2 типу в умовах реальної клінічної практики.
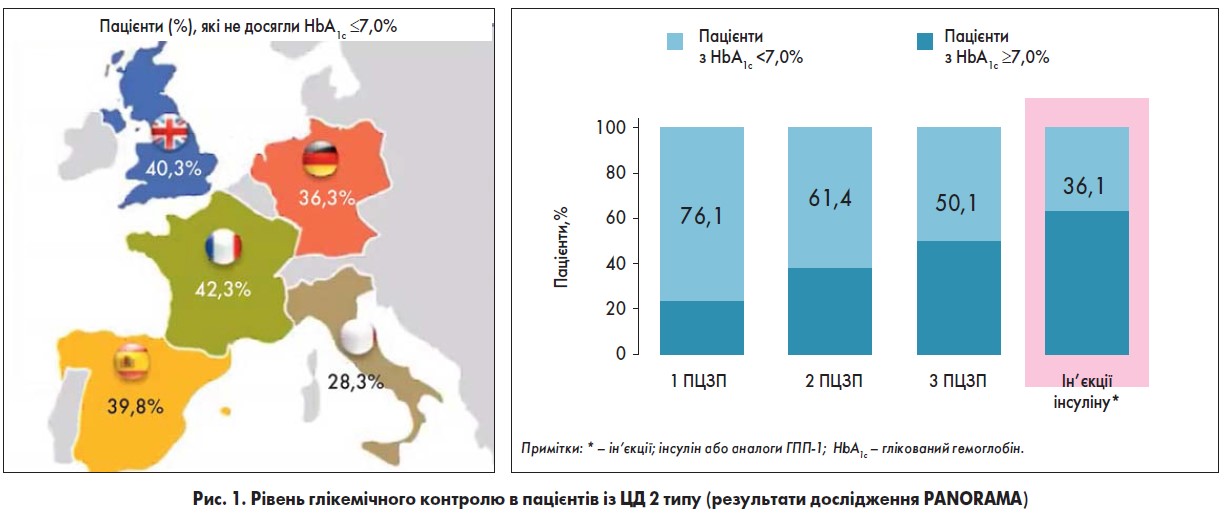
Незважаючи на стрімкий розвиток сучасної ендокринології та діабетології, ефективність лікування ЦД, як мовиться, залишає бажати кращого. За результатами обсерваційного багатоцентрового мультинаціонального крос-секційного дослідження PANORAMA з оцінки показників глікемічного контролю у хворих на ЦД 2 типу (n=5817; вік учасників – ≥40 років), в Європі частка пацієнтів, яким не вдалося досягти глікемічних цілей лікування, коливається від 28,3% у Франції до 40,3% у Великій Британії. Варто звернути увагу на те, що призначення інсуліну дало можливість досягти компенсації лише в 36,1% пацієнтів. Більш детальна інформація щодо глікемічного контролю в пацієнтів із ЦД 2 типу відображена на рисунку 1 (De Pablos-Velasco P. et al., 2014).
Ці показники свідчать про недостатню інтенсифікацію терапії ЦД, що часто пов’язано з певною терапевтичною інерцією, а насправді – зі страхом лікарів призначати інсулін або збільшувати його дозу пацієнтам із ЦД 2 типу. Водночас затримка в інтенсифікації лікування характерна не лише для інсулінотерапії (ІТ), але й для попередніх етапів цукрознижувальної терапії (ЦЗТ). Так, згідно з даними К. Khunti та співавт., додавання ще одного перорального цукрознижувального препарату (ПЦЗП) займає в середньому 1,6-2,9 року, старт ІТ у пацієнта, який отримує 3 ПЦЗП, відстрочується на 6-7,1 року, а додавання арГПП‑1, премікса чи болюсного інсуліну – ще додаткових 3,7 року (Khunti K. et al., 2013; Khunti K. et al., 2016).
Згадана затримка інтенсифікації лікування не тільки підвищує ризик виникнення хронічних ускладнень ЦД, але й зменшує шанси на досягнення контролю глікемії надалі (рис. 2).
Таким чином, вчасна інтенсифікація допоможе якомога раніше вивести пацієнтів на цільові показники глікемії і тим самим уникнути багатьох ускладнень ЦД.
Сучасні настанови з ведення пацієнтів із ЦД, поряд із рекомендаціями щодо модифікації способу життя та призначення метформіну, пропонують більш індивідуалізований підхід до лікування. Для цього необхідно враховувати (ADA, 2019; Garber A.J. et al., 2018; Lipscombe L. et al., 2018; IDF, 2017; Qaseem et al., 2017):
- Наявність супутньої патології: атеросклерозу, серцевої недостатності, хронічної хвороби нирок.
- Потребу в комбінованій терапії відразу після встановлення діагнозу.
- Можливість більш агресивної та ранньої інтенсифікації лікування.
- Фактори, пов’язані з особливостями як препаратів, так і пацієнта, зокрема вартість лікування.
- Поєднання препаратів із різними механізмами дії.
Оптимальним та інноваційним підходом до ЦЗТ, який задовольняє вимогу, викладену в міжнародних регламентуючих документах, є призначення комбінації базального інсуліну (БІ) та арГПП‑1. Перевагою цієї комбінації є вплив як на рівень глюкози плазми натще (ГПН), так і на постпрандіальну глікемію (ППГ). Даний ефект зумовлений механізмом дії кожного з компонентів комбінації. БІ підвищує периферичне засвоєння глюкози та знижує продукцію глюкози в печінці, що дає можливість контролювати рівень ГПН. АрГПП‑1, своєю чергою, підвищує глюкозозалежне виділення ендогенного інсуліну та знижує секрецію глюкагону, унаслідок чого досягається контроль ППГ (Balena R. et al., 2013; Baggio L.L. et al., 2017; Wang Z. et al., 2010; Holst J.J. et al., 2007). Згідно з рекомендаціями Американської діабетичної асоціації (ADA, 2019) комбінація БІ та арГПП‑1 має потужний цукрознижувальний ефект і нижчий ризик набору ваги та гіпоглікемії проти інтенсифікованого режиму ІТ. АрГПП‑1 короткої дії ексенатид 2 р./день або ліксисенетид мають сильніший постпрандіальний влив.
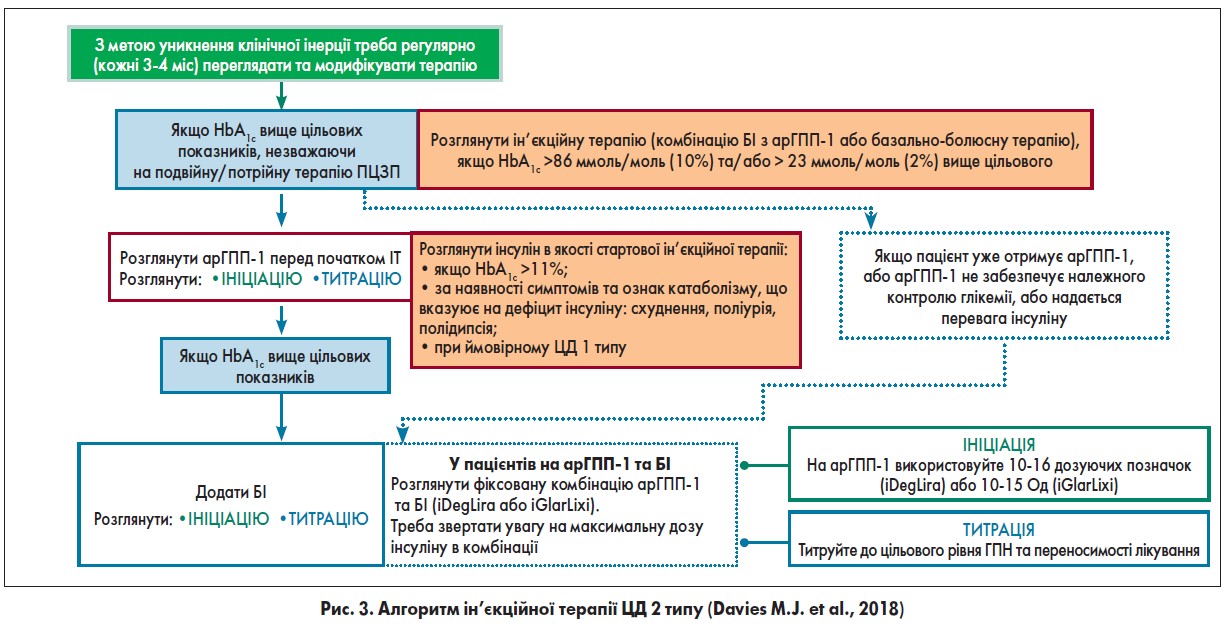
Ключові рекомендації консенсусного звіту ADA та Європейської асоціації з вивчення цукрового діабету (EASD) стосовно ін’єкційної терапії ЦД 2 типу відображені на рисунку 3.
Терапевтичні опції в пацієнтів, які не досягають глікемічних цілей на БІ (ADA, 2018):
1. Додавання однієї ін’єкції інсуліну короткої дії перед найбільшим прийомом їжі, а в разі неефективності такого втручання – перехід на базально-болюсну терапію.
2. Додавання арГПП‑1.
3. Перехід на премікс-інсулін двічі на добу (перед сніданком та вечерею), а за неефективності – тричі на добу.
У разі незадовільного результату від застосування одного із режимів розглядають перехід на альтернативні режими.
При цьому варто пам’ятати, що недоліками інтенсифікації терапії за рахунок інсуліну короткої дії (болюсу) та премікс-інсуліну є підвищений ризик набору ваги та розвитку гіпоглікемії. До того ж зростає кількість ін’єкцій, що завжди негативно впливає на прихильність пацієнтів до лікування.
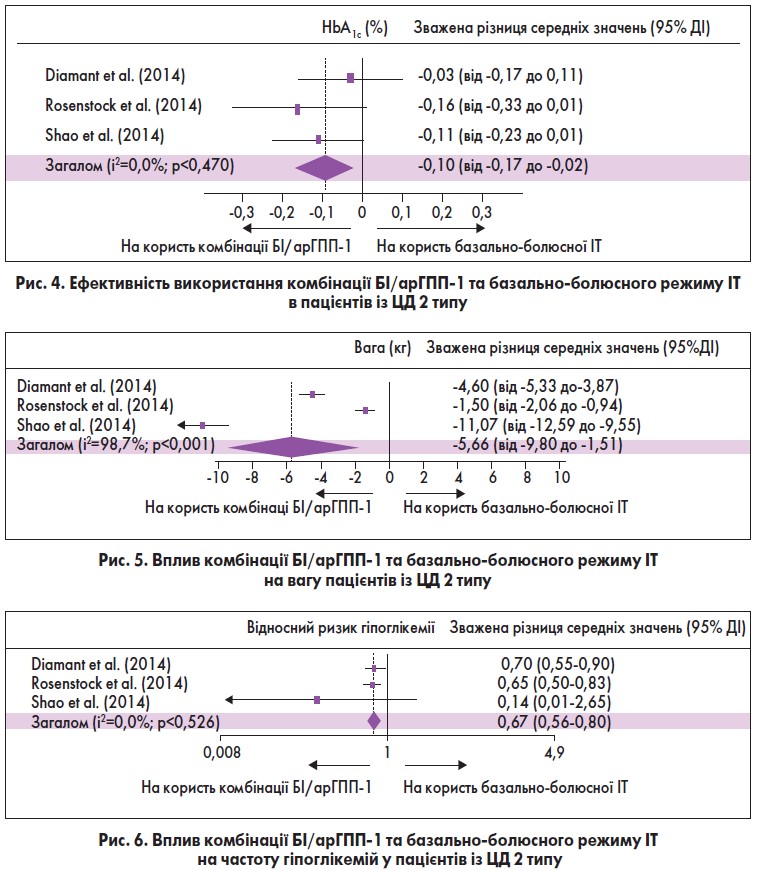
Ефективність і безпечність використання комбінації БІ/арГПП‑1 проти базально-болюсного режиму ІТ оцінювалися в систематичному огляді, який включив дані з 3 рандомізованих клінічних досліджень. Отримані результати відображені на рисунках 4-6 (Eng C. et al., 2014).
Отже, згідно з результатами систематичного огляду, застосування комбінації БІ/арГПП‑1 у пацієнтів із ЦД 2 типу дає можливість успішніше досягтися цілей лікування і при цьому супроводжується нижчим ризиком розвитку гіпоглікемій та набору ваги.
Отримані результати оцінки безпеки використання різних схем ЦЗТ перекликаються з даними дослідження VARIATION (Bajaj H.S. et al., 2017), в якому протягом 6 днів вивчали добову варіабельність глікемії в 160 пацієнтів із ЦД 2 типу віком 18-80 років та рівнем HbA1c ≤7,5. Було виявлено, що використання комбінації БІ/арГПП‑1 супроводжувалося найменшою добовою варіабельністю глікемії та ризиком гіпоглікемій, якщо порівняти з комбінацією БІ + ПЦЗП, премікс-інсуліну та базально-болюсної ІТ.
Утім, варто зазначити, що результати використання комбінації БІ/арГПП‑1 в умовах реальної клінічної практики не повністю відповідали даним, отриманим у ході контрольованих досліджень. Так, у ретроспективному аналізі, проведеному в США, оцінювалася ефективність терапії комбінацією БІ/арГПП‑1 у 7320 пацієнтів із ЦД 2 типу протягом 12 міс (Lin J. et al., 2016). Клінічні первинні та вторинні кінцеві точки відображені в таблиці 1.
Такі результати пояснюються вкрай низьким комплаєнсом, адже понад 80% пацієнтів не виявляли прихильності до лікування протягом періоду дослідження. Причиною цього стали 2 ін’єкції, клінічна інерція та побічні реакції через гіпоглікемію.
Рівень HbA1c залежить як від ПГН, так і від рівня ППГ. У дослідженні Riddle та співавт. було показано, що в пацієнтів на БІ саме ППГ відповідальна за 66% усіх гіперглікемій (Riddle et al., 2011).
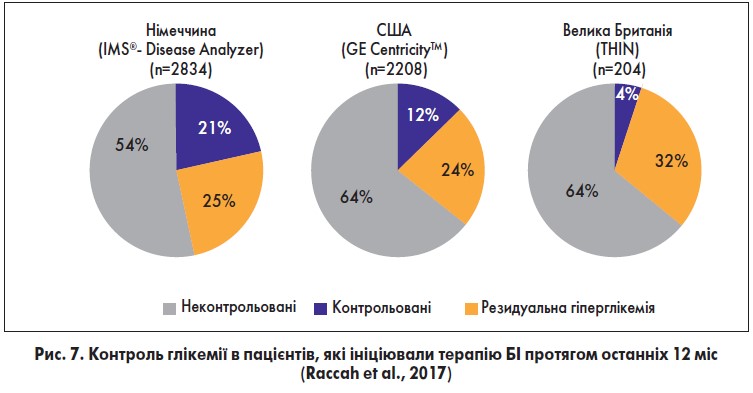
Аналіз результатів із 3 електронних медичних баз даних продемонстрував, що чимало пацієнтів із належними показниками ГПН не досягають при цьому цільового рівня HbA1c. Це явище називають резидуальною, або залишковою, гіперглікемією (рис. 7).
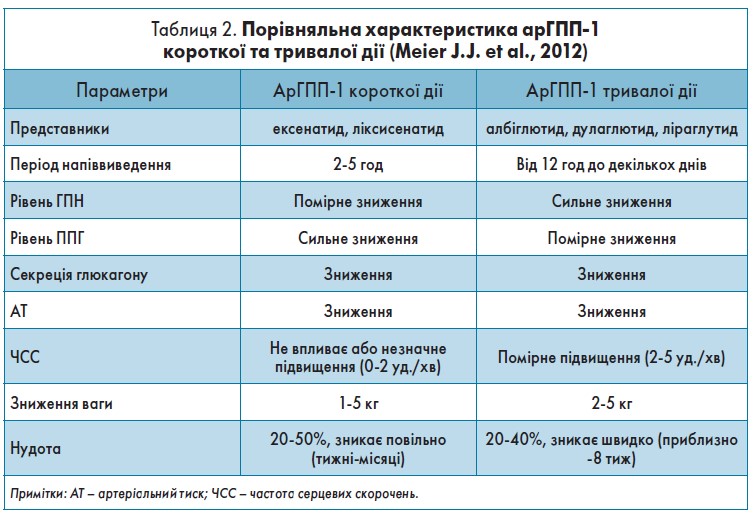
Препаратом, який найбільш оптимально допомагає зменшити частоту епізодів резидуальної гіперглікемії, є арГПП‑1 (основні характеристики арГПП‑1 короткої та тривалої дії відображені в таблиці 2).
Як можна побачити з таблиці, арГПП‑1 короткої дії мають кращий потенціал щодо зниження ППГ, а отже, і частоти резидуальної гіперглікемії.
У рандомізованому відкритому паралельному мультицентровому дослідженні порівнювали ефективність двох арГПП‑1 – ліксисенатиду і ліраглутиду – у 148 дорослих пацієнтів із неконтрольованим ЦД 2 типу, які отримували метформін у дозі 1,5 г/добу. У результаті виявилося, що ліксисенатид достовірно краще знижував рівень ППГ проти арГПП‑1 тривалої дії ліраглутиду (Kapiza C. et al., 2013).
Ліксисенатид та інсулін гларгін входять до складу першої фіксованої комбінації БІ/арГПП-1, яка є надійним та зручним методом контролю глікемії, зокрема резидуальної. Ефективність і безпечність даної комбінації оцінювали в дослідженні LixiLan-L (Aroda V.R. et al., 2016).
Відкрите рандомізоване дослідження охопило 736 пацієнтів із ЦД 2 типу. Критеріями включення була терапія БІ у дозі 15-40 Од/добу протягом ≥6 міс в якості монотерапії або в комбінації з ПЦЗП, рівень HbA1c ≥7,5-10% та ГПН ≤180 мг/дл. Залученим у дослідження пацієнтам було ініційовано та титровано інсулін гларгін протягом 6 тижнів. У подальшому учасники були рандомзовані на 2 групи: одна (n=369) продовжувала лікуватися інсуліном гларгін (iGlar) у комбінації з метформіном, друга (n=367) була переведена на фіксовану комбінацію гларгін + ліксисенатид (iGlarLixi) та метформіну.
Первинною кінцевою точкою було зниження рівня HbA1c на 30-му тиж лікування. Вторинні кінцеві точки включали: відсоток пацієнтів, які досягли цільового рівня HbA1c <7%; 2-годинні показники ППГ; зміна маси тіла на 30-й тиж лікування; зміни 7-точкового глікемічного профілю, отриманого шляхом самостійного вимірювання рівня глюкози крові; комбіновану кінцеву точку. Кінцевими точками безпеки були частота епізодів симптоматичної гіпоглікемії та побічних реакцій з боку шлунково-кишкового тракту (ШКТ) (плюс серцево-судинні події, алергічні реакції, панкреатичні ускладнення, лабораторні та основні показники життєдіяльності, антитіла до інсуліну та ліксисенатиду). Демографічні та вихідні клініко-лабораторні показники були зіставними в обох групах.
Пацієнтам, які отримували БІ у дозі <30 Од/добу, були видані жовті ручки iGlarLixi (10-40 Од); ті ж учасники дослідження, чия доза БІ була вища за 30 Од/добу, розпочали лікування відразу з оливкової ручки (30-60 Од).
У результаті на 30-му тиж терапії в пацієнтів із групи iGlarLixi спостерігалося статистично значуще зниження рівня HbA1c від вихідного рівня проти пацієнтів із групи iGlar (-1,1% проти -0,6% відповідно; р<0,0001): середній кінцевий рівень HbA1c сягнув 6,9% (52 ммоль/моль) проти 7,5% (58 ммоль/моль) відповідно (рис. 8).
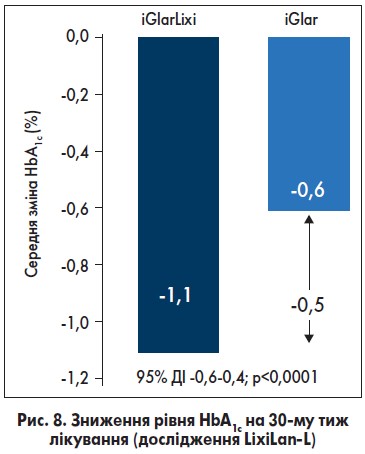 Рівня HbA1c <7,0% (53 ммоль/моль) досягли 55% пацієнтів із групи iGlarLixi проти 30% учасників із групи лікування iGlar. Середня вага тіла зменшилася на 0,7 кг на тлі терапії iGlarLixi та зросла на 0,7 кг при застосуванні iGlar (різниця склала 1,4 кг; р<0,0001). Частота задокументованих симптоматичних гіпоглікемій (≤70 мг/дл) була порівняною між групами. Помірні шлунково-кишкові розлади виникали рідко, але були частішими при застосуванні iGlarLixi (Aroda V.R. et al., 2016).
Рівня HbA1c <7,0% (53 ммоль/моль) досягли 55% пацієнтів із групи iGlarLixi проти 30% учасників із групи лікування iGlar. Середня вага тіла зменшилася на 0,7 кг на тлі терапії iGlarLixi та зросла на 0,7 кг при застосуванні iGlar (різниця склала 1,4 кг; р<0,0001). Частота задокументованих симптоматичних гіпоглікемій (≤70 мг/дл) була порівняною між групами. Помірні шлунково-кишкові розлади виникали рідко, але були частішими при застосуванні iGlarLixi (Aroda V.R. et al., 2016).
На противагу з групою iGlar значно більша частка пацієнтів із ЦД 2 типу, недостатньо контрольованим за допомогою БІ, які отримували iGlarLixi, досягла глікемічних показників зі сприятливим впливом на масу тіла, відсутністю додаткового ризику гіпоглікемії та низьким рівнем побічних ефектів із боку ШКТ (Aroda V.R. et al., 2016).
Ефективність та безпечність застосування iGlarLixi (Соліква) порівнювали з базально-болюсним режимом ІТ, використовуючи ретроспективний аналіз, підібраний за показником схильності, досліджень LixiLan-L та GetGoalDuo‑2 (Meier J.J. et al., 2017; Tabak A.G. et al., 2020). У кожну з груп порівняння увійшло 195 пацієнтів, які мали порівняні демографічні та вихідні характеристики глікемії.
У результаті було виявлено, що iGlarLixi (Соліква) ефективніше знижувала рівень HbA1c: середня різниця між групами становила -0,28% (95% ДІ 0,13-0,43; р=0,0002). До того ж профіль безпеки iGlarLixi (Соліква) також мав переваги перед базально-болюсним режимом ІТ. Так, оцінена різниця зміни ваги між групами iGlarLixi (Соліква) та базально-болюсної ІТ становила -1,32 кг (95% ДІ 0,72-1,91; р<0,0001). Застосування iGlarLixi (Соліква) також було асоційоване з нижчим ризиком гіпоглікемій.
Таким чином, фіксована комбінація БІ та ліксисенетиду, представлена в препараті Соліква, має такі переваги (Rosenstock J. et al., 2016; Gough S. et al., 2014):
- досягнення цільових рівнів ГПН та ППГ, що покращує глікемічний контроль та зменшує ризик резидуальної гіперглікемії;
- відсутність додаткового ризику гіпоглікемії проти БІ (незважаючи на кращий глікемічний контроль);
- відсутність впливу або зниження маси тіла;
- повільна титрація знижує ризик побічних реакцій з боку ШКТ проти монотерапії арГПП‑1;
- може успішно використовуватися пацієнтами, яким не підійшло лікування арГПП‑1;
- простий режим використання, що підвищує прихильність пацієнтів до лікування.
Друга частина робочої програми заходу була присвячена аспектам практичного досвіду застосування фіксованої комбінації інсуліну гларгін та ліксисенатиду (Соліква) на прикладі клінічного випадку.
Клінічний випадок
Пацієнтка Ясміна, 54 роки, звернулася до клініки зі скаргами на прогресуюче збільшення маси тіла та недостатній контроль цукру крові, незважаючи на прийом трьох ПЦЗП та ін’єкцію БІ. ЦД 2 типу діагностований пацієнтці 16 років тому. Важливими анамнестичними даними є професія Ясміни. Вона працює виконавчим асистентом, і «побічними ефектами» її роботи є нездорове харчування та малорухливий спосіб життя. Коморбідна патологія включає ожиріння, дисліпідемію, гіпертонічну хворобу, неалкогольну жирову хворобу печінки та подагру.
Протягом останніх 4 років пацієнтка отримує таке лікування:
- метформін 1000 мг 2 р./день + глімепірид 4 мг/день + сітагліптин 100 мг/день;
- інсулін гларгін 42 Од ввечері;
- аторвастатин 40 мг 1 р./день, лізиноприл 40 мг 1 р./день, амлодипін 5 мг 1 р./день, гідрохлортіазид 25 мг 1 р./день, ацетилсаліцилова кислота 81 мг 1 р./день.
Результати фізикального огляду та лабораторних тестів
- АТ 124/73 мм рт. ст.; ІМТ [індекс маси тіла] 32,5 кг/м2.
- HbA1c 8,6% (6 та 12 міс тому був >8,5%).
- ГПН приблизно 6,7-7,8 ммоль/л; ППГ >13,9 ммоль/л.
- Діабетична ретинопатія.
- [швидкість клубочкової фільтрації] ШКФ 54 мл/хв/1,73 м2.
- Мікроальбумінурія.
Цілі лікування
Як бачимо, показники ГПН пацієнтки близькі до цільових, однак ППГ при цьому значно підвищена. Велика кількість препаратів, які приймає Ясміна, викликає в неї занепокоєння й погано вписується в ритм її життя. Отже, необхідно скорегувати лікування для досягнення цільового рівня HbA1c <7% та максимального спрощення режиму ЦЗТ.
Варіанти модифікації ЦЗТ
Терапевтичні опції включають:
- титрацію БІ;
- додавання арГПП‑1;
- перехід на фіксовану комбінацію
БІ/арГПП‑1 (Соліква);
- додавання прандіального інсуліну під час найбільшого прийому їжі;
- перехід на премікс-інсулін.
Оскільки пацієнтка скаржиться на прогресуючий набір маси тіла, її рівні ГПН близькі до цільового, а кількість ПЦЗП та ін’єкцій і без того погіршує якість її життя, титрація БІ, перехід на інсулін премікс або додавання прандіального інсуліну є не найкращими лікувальними режимами. Відповідно, потрібно призначити пацієнтці арГПП‑1 або ж замінити БІ на фіксовану комбінацію Соліква.
Фіксована комбінація Соліква проти окремої ін’єкції арГПП‑1: доказові дані
Ефективність глікемічного контролю при одночасному старті комбінації Соліква, якщо порівняти з віддаленим призначенням БІ та арГПП‑1, оцінювалася в умовах реальної клінічної практики (Rosenstock J. et al., 2020). Пацієнтів було поділено на 5 груп:
- група А – її учасники почали використовувати арГПП‑1 та БІ одночасно, інтервал ≤30 днів;
- група В – інтервал між БІ та арГПП‑1 склав 30-90 днів;
- група С – 91-180 днів;
- група D – 181-270 днів;
- група Е – 271-360 днів.
Вихідні демографічні та клінічні характеристики були порівняними в усіх групах.
У результаті виявилося, що пацієнти групи А частіше досягали цільового рівня HbA1c проти учасників з інших груп. Крім того, пацієнти, які розпочали лікування БІ та арГПП‑1 одночасно, також мали більшу ймовірність досягнення цільових рівнів глікемії, ніж ті, хто розпочав терапію в різні дні. Маса тіла знижувалася в усіх учасників дослідження через 6 та 12 міс терапії, за виключенням групи D – через 12 міс лікування.
Подібні результати були отримані в ще одному порівняльному ретроспективному обсерваційному дослідженні одночасного та відстроченого в часі застосування БІ та арГПП‑1 (Peng X.V. et al., 2020).
Модифікація ЦЗТ
Після аналізу всіх переваг і недоліків Ясміні було призначено:
- iGlarLixi 30 Од перед сніданком (найбільший прийом їжі);
- самостійний моніторинг ГПН та титрація iGlarLixi по 2-4 Од до досягнення цільового рівня ГПН <5,6 ммоль/л;
- продовжити прийом метформіну, відмінити глімепірид та сітагліптин.
Ініціація та титрація препарату Соліква
Загальна схема ініціації та титрації препарату Соліква має такий вигляд. Якщо пацієнт отримував <30 Од БІ, треба починати з дози 20 Од (жовта ручка), а якщо >30 Од – з 30 Од (оливкова ручка).
Титрація дози проводиться 1 р./тиж, до цільових рівнів глікемії. Якщо ГПН >7,2 ммоль/л, ми додаємо 2 Од Солікви; якщо 4,4-7,2 ммоль/л – дозу не змінюємо; якщо <4,4 ммоль/л – дозу зменшуємо на 2 Од.
Контроль терапії
Протягом наступних 8 тиж поцієнтка дотитрувала дозу iGlarLixi з 30 до 52 Од. При цьому ГПН коливалася в межах 5,0-6,1 ммоль/л. Не спостерігалося небажаних реакцій з боку ШКТ, епізодів гіпоглікемії, а маса тіла залишалася стабільною.
Через 6 міс після ініціації iGlarLixi було встановлено дозу 50 Од, рівень HbA1c становив 7,2% (знизився на 1,4%), маса тіла знизилася на 2 кг, а режим терапії був зручним для пацієнтки.
Потенційні переваги iGlarLixi (Соліква) в різних клінічних ситуаціях
Фіксована комбінація в препараті Соліква має низку переваг не лише в описаному вище клінічному випадку. Результати досліджень підтвердили, що iGlarLixi однаково ефективний в досягненні глікемічних цілей незалежно від: вихідного рівня HbA1c (Niemoeller E. et al., 2018); віку пацієнта; тривалості ЦД (Blonde L. et al., 2018); вихідного ІМТ пацієнта (Wysham C., 2017).
Таким чином, препарат Соліква є терапевтичною опцією, яка може допомогти подолати низку важливих перешкод у лікуванні ЦД 2 типу завдяки полегшенню досягнення цільових рівнів HbA1c у пацієнтів, в яких базальний інсулін ± ПЦЗП виявилися недостатньо ефективними. При цьому фіксована комбінація добре переноситься, не чинить негативного впливу на масу тіла та ризик розвитку гіпоглікемії. Режим терапії у вигляді ін’єкції 1 р./день і легкість процесу титрації зменшують навантаження на пацієнта, що покращує його прихильність до терапії, а отже, і ефективність лікування.
Список літератури знаходиться в редакції.
Підготувала Ганна Кирпач
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (51) 2020 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
Нещодавні дослідження показали, що прогноз за різних поширених захворювань, ендокринних, автоімунних розладів і навіть прогресування раку пов’язані з концентрацією вітаміну D у плазмі. Завдяки експресії гена 1α-гідроксилази (CYP27B1) клітини імунної системи (В-, Т- та антигенпрезентувальні клітини) здатні продукувати активний метаболіт кальциферол – речовину з імуномодулювальними властивостями. Рецептори до вітаміну D (vitamin D receptor, VDR) експресують на поверхні імунних клітин. Доведено зв’язок між поліморфізмом генів VDR або CYP27B1 і патогенезом автоімунних ендокринних захворювань. Метою огляду є вивчення впливу вітаміну D, наслідків його дефіциту та корисної ролі добавок із ним при деяких ендокринних розладах, які часто спостерігають у клінічній практиці. ...
Збудник COVID‑19, SARS-CoV‑2, з яким людство вперше стикнулося у 2019 р., поширився по всьому світу, заразивши мільйони людей. Сьогодні, через тягар війни та економічної нестабільності, тема COVID‑19 не сприймається так гостро, як ще кілька років тому, хоча насправді вона не втратила своєї актуальності. Саме сучасному стану проблеми COVID‑19 у світі та в Україні була присвячена доповідь директора ДУ «Інститут ендокринології та обміну речовин імені В.П. Комісаренка НАМН України», академіка Національної академії медичних наук України, члена-кореспондента НАН України, віце-президента НАМН України, президента Асоціації ендокринологів України, професора Миколи Дмитровича Тронька під час першого у 2024 р. засідання науково-освітнього проєкту «Школа ендокринолога», яке відбулося 20-24 лютого. ...
Протягом останніх 60 років метформін є найпоширенішим цукрознижувальним засобом і рекомендований як препарат першої лінії для осіб з уперше виявленим цукровим діабетом (ЦД) 2 типу. Сьогодні понад 200 млн осіб із ЦД 2 типу в усьому світі щодня застосовують метформін як монотерапію або в комбінації. Препарат усе частіше використовують для лікування гестаційного ЦД та в пацієнтів із синдромом полікістозних яєчників. ...
Двадцять восьмого лютого 2024 року виповнилося 80 років від дня народження директора ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (далі – Інститут), віцепрезидента НАМН України, академіка НАМН України, члена-кореспондента НАН України, заслуженого діяча науки та техніки, лауреата Державної премії України, доктора медичних наук, професора Миколи Дмитровича Тронька....