Тест генерации тромбина – уникальный метод интегральной оценки системы гемостаза

Тест генерации тромбина (ТГТ) представляет собой лабораторный метод определения динамики образования и инактивации in vitro ключевого фермента гемостаза – тромбина. Плазменная система (в которой функционирует тромбин), ответственная за образование и последующее угнетение тромбина в крови, вызовет тенденцию к тромбозу в случае избытка свободного тромбина (гиперкоагуляция) или приведет к кровоточивости при недостаточной активности тромбина (гипокоагуляция).
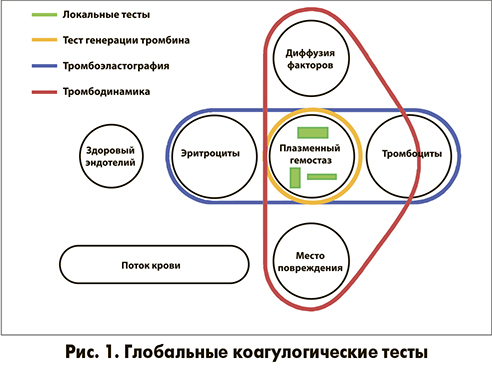
ТГТ относится к так называемым глобальным коагулогическим тестам, к которым также принадлежат такие методы, как тромбоэластография и тромбодинамика [7]. Результаты глобальных тестов позволяют оценить работу системы гемостаза в целом (рис. 1).
Тромбин (фактор свертывания IIа) является важнейшим компонентом системы гемостаза и представляет собой витамин К- зависимый белок, который относится к ферментам класса гидролаз (сериновая протеаза), катализирующих гидролиз пептидных связей, образованных остатками аргинина и лизина (рис. 2).
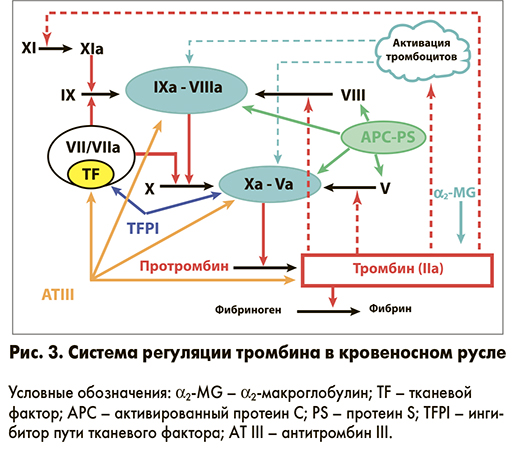
Предшественником тромбина (фактор IIa) является протромбин (фактор II), синтез которого происходит в печени. В комплексе факторов Ха-Va-II на фосфолипидной поверхности происходит ограниченный протеолиз протромбина, в результате которого образуются не сколько активных структур с различной молекулярной массой – мезотромбин, α- , β- и γ-тромбин. Наиболее значимым продуктом является сериновая протеаза – α-тромбин. На молекуле тромбина имеется 4 сайта связывания для субстратов, ингибиторов, кофакторов и ионов кальция [8]. Такая способность тромбина позволяет ему активно функционировать не только в твердой фазе, но и в токе крови, выполняя при этом многочисленные функции (рис. 3).
Основные функции тромбина в системе гемостаза:
- образование фибрина из фибриногена (огра ниченный протеолиз фибриногена до мономера фиб рина);
- усиление активации системы гемостаза по принци пу положительной обратной связи (активация факторов V, VII, VIII, XI);
- активация фактора XIII (участие в стабилизации сгустка);
- активация клеточного звена (агрегация тромбоци тов);
- в комплексе с тромбомодулином активация про теина С;
- ограниченный протеолиз плазматической карбо ксипептидазы В до активной формы – активируемого тромбином ингибитора фибринолиза (TAFI);
- стимуляция выброса из эндотелиоцитов тканевого активатора плазминогена.
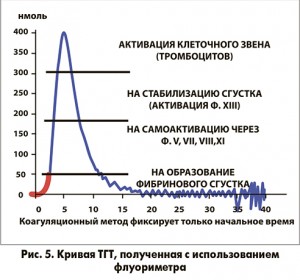
Кроме вышеперечисленных функций, тромбин участвует также в активации сосудистого эндотелия, процессах репарации, ускорении ангиогенеза, миграции и роста клеток. Способность системы свертывания крови генерировать тромбин определяет коагуляционный потенциал крови. Главной причиной разработки ТГТ послужило то обстоятельство, что по выходу фибрина нельзя судить о повышенном тромбогенном потенциале системы свертывания, так как лишь часть тромбина идет на образование сгустка (все тесты, основанные на определении времени образования сгустка, регистрируют только начальную фазу образования тромбина, или около 5% от общего тромбина). Таким образом, необходимо было разработать такой тест, который бы позволил оценить динамику изменения концентрации тромбина в образце плазмы крови и количественно определить суммарный эффект от взаимодействия всех факторов системы свертывания, что может служить интегральным показателем состояния гемостаза [1].
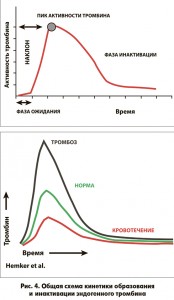
Впервые такой тест под названием «тест генерации тромбина» для оценки состояния системы свертывания крови у больных, страдающих гемофилией, был предло жен в 1953 г. R. Macfarlane и R. Biggs [2]. Однако он имел ряд существенных методических недостатков, в связи с чем группа исследователей под руководством H. Hemker из Маастрихтского университета [3] видоиз менила технологию выполнения данного теста и разра ботала автоматизированный метод детекции генерации тромбина. Первоначально H. Hemker и S.Wielders [4] был предложен специфический для этого фермента хромогенный субстрат, который не обладал высокой степенью аффинности к тромбину. Более того, фотомет рическое определение хромогена не позволяло использовать плазму, богатую тромбоцитами, которые существенно влияли на оптическую плотность. После анализа основных недостатков метода с применением хромогенного субстрата в 2003 г. H. Hemker [5, 6] предложил использовать очень специфичный, медленно реагирующий флуорогенный субстрат – пептид, меченный 7-амино-4-метилкумарином (Z-Gly-Gly-Arg-AMC) (рис. 4).
В настоящее время для проведения ТГТ используют такие планшетные флуориметры, как BioTek® FLx 800™ TC, BMG Labtech FLUOstar OPTIMA, Molecular Devices Gemini/SpectraMax®, Perkin Elmer® Victor Wallac, TECAN Genios™, Thermo Fluoroskan®, или автоматический анализатор Ceveron alpha (включает флуоресцентный модуль) с использованием набора Technothrombin® TGA Kit.
Методика определения ТГТ с помощью флуориметра основана на том, что в лунках планшета инкубируется смесь образца исследуемой плазмы с активатором. В качестве активатора выступает рекомбинантный человеческий тканевой фактор и отрицательно заряженные фосфолипиды (фосфатидилсерин : фосфатидилэтанол амин : фосфатидилхолин – 20:20:60). После инкубации смеси при температуре 37° С для запуска свертывания в лунки флуориметра вносится буфер, содержащий иони зированный кальций и флуорогенный субстрат. Образующийся тромбин расщепляет субстрат, в результате чего высвобождается молекула флуорофора. Это излучение автоматически регистрируется флуориметром через равные промежутки времени. Интенсивность свечения пропорциональна скорости изменения флуоресценции в данный момент времени, а следовательно, и концентрации образовавшегося тромбина. На основании измерений посредством специального программного обеспечения (программа Thrombinoscope) выстраивается кривая генерации тромбина (рис. 5).
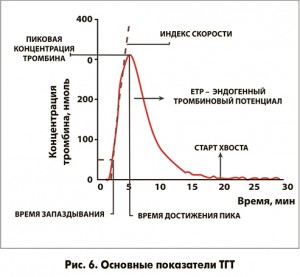
В кривой ТГТ оценивают следующие показатели:
- время запаздывания (lag time, мин) – время от момента внесения смеси флуорогенного субстрата и ионизированного кальция в лунку с образцом и активатором до момента отклонения флуоресцентного сигнала от основной горизонтальной линии более чем на 2 стандартных отклонения;
- пиковая концентрация тромбина (peak thrombin, нмоль/л) – максимальная концентрация тромбина, достигаемая в процессе его генерации в образце;
- время достижения пика (time to peak, мин) – время, за которое в образце достигается максимальная концентрация тромбина;
- эндогенный тромбиновый потенциал (ETP, нмоль/мин) – площадь под кривой генерации тромбина (рис. 6).
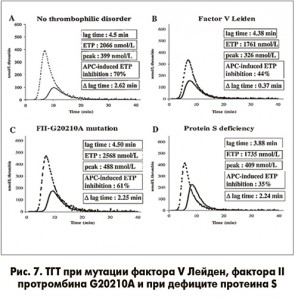
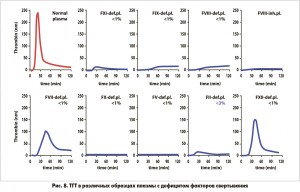
Метод ТГТ нашел широкое практическое применение в диагностике тромбофилии (рис. 7) [13] и гемофилии (рис. 8).
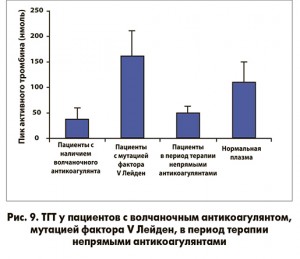
Результаты ТГТ у пациентов с волчаночным антикоагулянтом, мутацией фактора V Лейден и в ходе терапии непрямыми антикоагулянтами представлены на рисунке 9.
Важность применения ТГТ состоит в том, что показатели рутинно использующихся клоттинговых тестов (протромбиновое время, активированное частичное тромбопластиновое время, тромбиновое время) в клинико-диагностических лабораториях чаще всего остаются неизменными даже при возникновении тромбоза [9]. При определении уровня фибриногена, активности фактора свертывания VIII и фактора Виллебранда, а также антитромбина, протеинов С и S могут выявляться отклонения от референтного интервала, что не позволяет судить о наличии гиперкоагуляции в целом, так как изменения отдельных компонентов свертывающей системы могут быть нивелированы в организме включением компенсаторных механизмов [10].
Например, показатели коагулограммы могут находиться в пределах нормы, в то время как в функциональном ТГТ выявляется повышение параметров, что свидетельствует о наличии гиперкоагуляции. При этом если врачклиницист будет руководствоваться только данными коагулограммы, то не будет назначена своевременная антикоагулянтная терапия. Обратная ситуация может наблюдаться в случае, когда изменение отдельных показателей коагулограммы не сопровождается изменением ТГТ. Так, у пациента могут быть повышены фактор VIII, фактор Виллебранда и D-имер, на основании чего врачклиницист может предположить наличие гиперкоагуляции и назначить антикоагулянтную терапию для предотвращения тромбоза. Однако увеличение активности отдельных прокоагулянтных факторов может быть минимизировано повышением активности антикоагулянтных факторов, показатели ТГТ будут в таком случае в норме. Следовательно, учитывая только данные коагулограммы, можно получить ложноположительное представление о наличии у пациента гиперкоагуляции при ее реальном отсутствии.
При мониторинге антикоагулянтной терапии у больных, получающих варфарин, руководствуясь правилом достижения целевого значения МНО, при котором терапия считается адекватной у пациентов с одинаковыми значениями МНО, показатели ТГТ могут значительно отличаться.
Существует мнение, что мониторинг терапии низкомолекулярными гепаринами не обязателен по причине линейной зависимости их влияния на активный фактор X.Мониторинг в случае необходимости проводится по ис следованию динамики анти-Xa-активности. Об изменениях свойств системы гемостаза предлагается судить по изменению активности только одного фактора. Как показали последние исследования, при назначении одинаковых доз фраксипарина недостаточная доза наблюдалась в 13% случаях, передозировка – также в 13%. Эта работа демонстрирует необходимость лабораторного контроля эффекта введения низкомолекулярного гепарина с помощью глобальных тестов, а также непра вомерность суждения о гемостазе в целом по изменению всего лишь одного показателя – анти-Xа-активности [12].
Какие бы изменения не происходили на этапах меж факторных взаимодействий в процессе активации свертывания, они в конечном итоге окажут влияние на количество и скорость образования и инактивации тромбина. Динамическая оценка генерации тромбина с помощью ТГТ отражает состояние системы гемостаза в целом и может служить интегральным показателем баланса про и антикоагулянтных механизмов [11].
Таким образом, ТГТ является универсальным мето дом оценки тромбогенного потенциала гемостаза и может быть использован в научных исследованиях и с целью:
- диагностики тромбофилии (врожденной и приобретенной), в т. ч. в педиатрии;
- выявления гемофилии;
- мониторинга терапии гемофилии при наличии ингибитора фактора VIII;
- мониторинга антикоагулянтной терапии, направленной на ингибирование тромбина и фактора Xa;
- контроля эффективности всех групп антикоагулянтов (в т. ч. новых);
- оценки активности гемостаза при беременности;
- контроля ДВС-синдрома.
Литература
- Hemker H.C., Beguin S. Thrombin generation in plasma: its assessment via the endogenous thrombin potential. Throm. Haemost. 1995; 74(5): 134-138.
- Macfarlane R.G., Biggs R. A thrombin generation test: the application in haemophilia and thrombocytopenia. J. Clin. Pathol. 1953; 6: 3-8.
- Hemker H.C., Giesen P.L., Ramjee M. et al. The thromgram: monitoring thrombin generation in platelet-rich plasma. Thromb. Haemost. 2000; 83 (4): 589-591.
- Hemker H.C., Weilders S., Kessels H. et al. Continuous registration of thrombin generation in plasma, its use for the determination of thrombin potential. Throm. Haemost. 1993; 70 (4): 617- 624.
- Hemker H.C., Giesen P., Al Dieri R. et al. Calibrated automated thrombin generation measurement in clotting plasma. Pathophysiol. Haemost. Thromb. 2003; 33; 4-15.
- De Smedt E., Al Dieri R., Spronk H.M. et al. The technique of measurement thrombin generation with fluoogenic substrates: 1. Necessity of adequate cali bration. Thromb. Haemost. 2008: 100 (2): 343-349.
- Серебрийский И.И. «Глобальные» и «локальные» тесты системы гемо стаза в диагностике гиперкоагуляционного синдрома. Справочник заведующего клинико-диагностической лабораторией. 2012; 12.
- Долгов В.В., Свирин П.В. Лабораторная диагностика нарушений гемо стаза. – М., 2005, С. 228.
- Hemker H.C., Al Dieri R., Beguin S. Curr. Opin. Hematol. 2004; 11: P. 170-175.
- Van Veen J.J., Gatt A., Makris M. // Br. J. Haematol. 2008. 142 (6): 889-903.
- Hemker H.C., Al Dieri R., De Smedt E. et al. // Thromb. Haemost. 2006; 96: 553-561.
- Наместников Ю.А., Головина О.Г., Папаян Л.П. Значение теста генера ции тромбина в клинической практике. Онкогематология. 2011: № 2,
- Hezard N., Bouaziz-Borgi L. Utility of Thrombin-Generation Assay in the Screening of Factor V G1691A (Leiden) and Prothrombin G20210A Mutations and Protein S Deficiency. - Clinical Chemistry 2006; 52 (4): 665-670.
Медична газета «Здоров’я України 21 сторіччя» №2 (375), січень 2016 р.
СТАТТІ ЗА ТЕМОЮ Діагностика
Еритроцити, або червоні кров’яні тільця, є найпоширенішим компонентом клітин крові, які становлять 40-45% їхнього обсягу. Плазматична мембрана еритроцитів має унікальну будову, що надає їм біологічних і механічних властивостей, необхідних для виконання специфічних функцій. Основна функція еритроцитів в організмі – це транспорт кисню, опосередкований гемоглобіном. Вони активно беруть участь як в артеріальних, так і у венозних тромбозах [1]. Гемоглобін – висококонсервативний білок, який завдяки своїй здатності зворотно зв’язувати кисень бере участь у процесах, що лежать в основі аеробного життя на планеті Земля. Головна роль цього білка полягає у підтримці клітинного гомеостазу. Однак завдяки майже 200-річним дослідженням гемоглобіну тепер відомо, що цей білок також відіграє важливу роль в інших метаболічних процесах, як-от передача сигналів у клітинах, модуляція запальної реакції, за тромбозу при гемолізі еритроцитів тощо [2-4]....
У сучасному світі онкологічні захворювання становлять чи не найбільшу загрозу життю людини, поступаючись тільки серцево-судинній патології [1]. Більшість неінфекційних хвороб людини, зокрема й онкологічні захворювання, є багатофакторними, і їх розвиток пов’язаний у тому числі з генетичними чинниками. Це, з одного боку, підвищує з віком ризик виникнення хронічних захворювань, а з іншого – дає змогу разом з лікарем розробити заходи з їх профілактики, раннього виявлення й ефективного лікування [2]....
Власна патоморфологічна лабораторія – необхідність для всіх клінік ендоскопічного, хірургічного й онкологічного профілю. Одним із видів діяльності такої лабораторії є проведення інтраопераційних досліджень. Ці дослідження виконують для визначення тактики подальшого оперативного втручання під час операції. Тому створення лабораторії на колесах, що може надавати результати патоморфологічного дослідження в будь-якому місці та ще під час операційного втручання, стало логічним рішенням для Медичної лабораторії CSD LAB, найбільшої патоморфологічної лабораторії України та Східної Європи....
Нефракціоновані (НФГ) і низькомолекулярні гепарини (НМГ) є препаратами, що широко використовуються та запобігають артеріальним і венозним тромбозам. Однак їхнє застосування також пов’язано з парадоксальною реакцією, що зумовлює потенційно небезпечний для життя протромботичний стан, результатом чого є серйозні ускладнення (гангрена, ампутація кінцівок) або фатальні наслідки. Гепарин-індукована тромбоцитопенія (ГІТ) – це імуноопосередкована відповідь на введення гепарину, який спричиняє небезпечний для життя тромбоз і є клінічно значущим негеморагічним ускладненням. ГІТ вважається потенційно загрозливим для життя станом за терапії гепарином, що спричиняє утворення нових згустків крові, а не сприяє запобіганню утворення нових тромбів. Хоча при введенні гепарину імунна реакція зустрічається досить часто (від 8 до 50%), клінічні ускладнення у разі ГІТ виникають у ≈0,2-3% пацієнтів, які приймають гепарин протягом >4 дні; частіше спостерігаються в жінок [1-3]. У цьому стані тромбоцити різко знижуються до рівня ≥20×109/л. Смертність становить 10-20%....