Досвід ендоваскулярного лікування хворих з обструктивною формою гіпертрофічної кардіоміопатії
 Алкогольна септальна абляція (АСА) здатна модифікувати одну з критичних ознак симптоматичного пацієнта з гіпертрофічною кардіоміопатією (ГКМП), а саме – перешкоджання кровотоку через вихідний тракт лівого шлуночка (ЛШ) аномально гіпертрофованою перетинкою. Після усунення обструкції симптоми запаморочення, задишки та стенокардії протягом наступних 3-6 міс зменшуються разом із регресом гіпертрофії. Цих результатів можна досягти також шляхом виконання хірургічної міоектомії, проте АСА забезпечує менший ризик перкутанного втручання для пацієнтів похилого віку та хворих із супутніми захворюваннями, а також для осіб будь-якого віку, котрі мають відповідну анатомію.
Алкогольна септальна абляція (АСА) здатна модифікувати одну з критичних ознак симптоматичного пацієнта з гіпертрофічною кардіоміопатією (ГКМП), а саме – перешкоджання кровотоку через вихідний тракт лівого шлуночка (ЛШ) аномально гіпертрофованою перетинкою. Після усунення обструкції симптоми запаморочення, задишки та стенокардії протягом наступних 3-6 міс зменшуються разом із регресом гіпертрофії. Цих результатів можна досягти також шляхом виконання хірургічної міоектомії, проте АСА забезпечує менший ризик перкутанного втручання для пацієнтів похилого віку та хворих із супутніми захворюваннями, а також для осіб будь-якого віку, котрі мають відповідну анатомію.
ГКМП – генетично зумовлене захворювання серця, що характеризується збільшенням товщини стінки ЛШ, і її виникнення не пояснюється виключно зростанням навантаження тиском.
Поширеність цього захворювання становить 1 випадок на 500 дорослих осіб і 0,3-0,5 на 100 тис. дітей на рік. Чоловіки хворіють майже втричі частіше за жінок (чоловіки – 0,26%, жінки – 0,09%). В Україні частота виявлення ГКМП у популяції становить 0,47% випадків. Згідно з даними Всесвітньої організації охорони здоров’я щороку від цього захворювання помирає від 3,5 до 8,0% хворих. Основною причиною летальних випадків є раптова смерть, яка значно частіше трапляється при обструктивній ГКМП.
ГКМП успадковується за аутосомно-домінантним типом, і ризик успадкування захворювання дітьми від батьків становить 50%. Розвиток ГКМП здебільшого зумовлений мутаціями в генах, які кодують саркомерні білки міокарда (в 60% підлітків і дорослих). Пацієнти з ГКМП, як правило, скаржаться на загрудинний біль, задишку, стомлюваність, слабкість, серцебиття, рідко дебютом захворювання може бути раптова смерть.
Методи лікування
Пацієнтів із симптоматичною обструктивною ГКМП лікують за допомогою методів, перелічених нижче.
- Перша лінія лікування в симптоматичних хворих передбачає призначення медикаментозних препаратів (бета-блокатори, блокатори кальцієвих каналів та інші негативні інотропні засоби, що сповільнюють частоту серцевих скорочень і покращують наповнення серця).
- Для пацієнтів із постійними симптомами чи за наявності прямих показань виконують АСА чи хірургічну міоектомію для покращення кровотоку з ЛШ.
- Ресинхронізаційна терапія та імплантація кардіовертера-дефібрилятора.
Обов’язковими для всіх хворих є уникнення дегідратації, запобігання вживанню великої кількості алкоголю та зниження надмірної маси тіла.
Критерії відбору пацієнтів з обструктивною ГКМП для виконання АСА
Під час прийняття рішення про виконання АСА слід чітко дотримуватися критеріїв відбору пацієнтів. Згідно з рекомендаціями Європейського товариства кардіологів (ESC) до них належать:
- обструкція вихідного тракту (ВТ) ЛШ із градієнтом тиску >50 мм рт. ст. у спокої чи максимально спровокована;
- товщина міжшлуночкової перетинки (МШП) ≥16 мм (за даними ехокардіографії – ЕхоКГ);
- серцева недостатність ІІІ-ІV функціонального класу за класифікацією NYHA.
Слід зауважити, що на момент втручання хворі мають перебувати на максимально переносимих дозах медикаментозної терапії.
Техніка виконання АСА
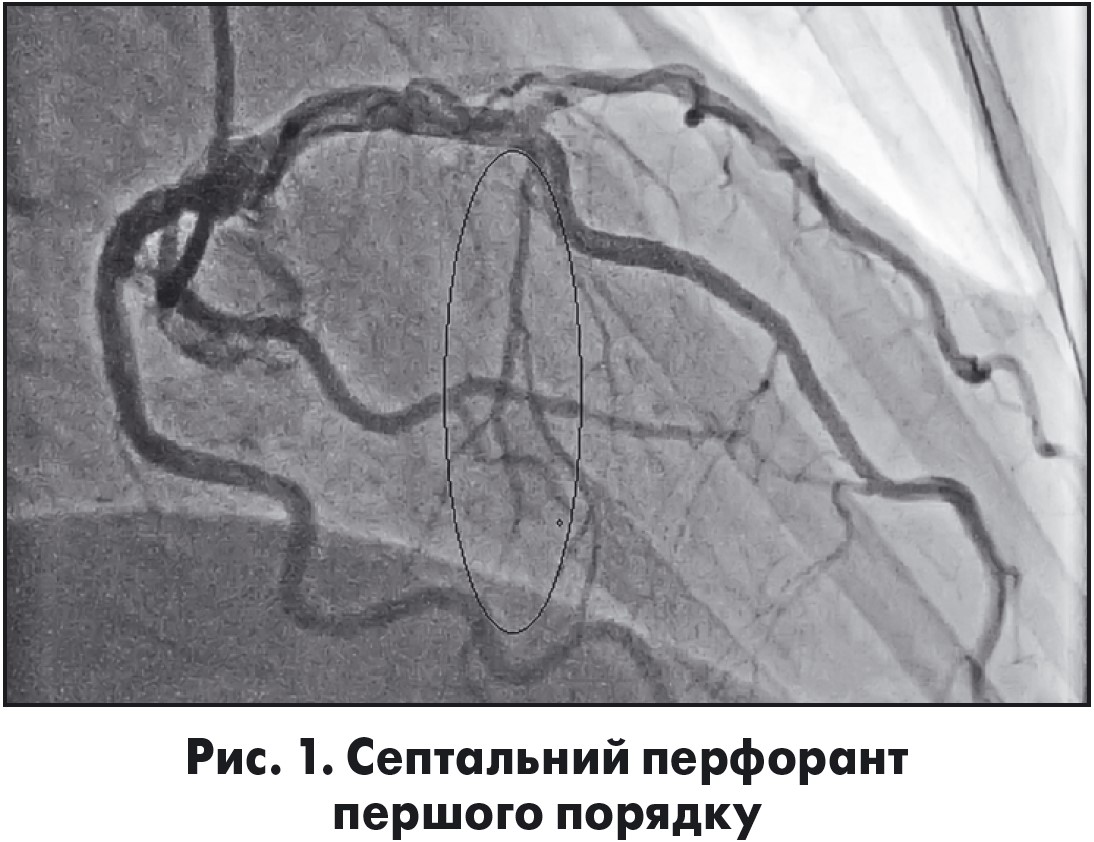
Для проведення АСА використовують септальний перфорант, як правило, першого, значно рідше другого чи третього порядку, що відходять від передньої міжшлуночкової артерії. В окремих випадках віддають перевагу септальним перфорантам інших гілок лівої та правої коронарних артерій (рис. 1).
|
|
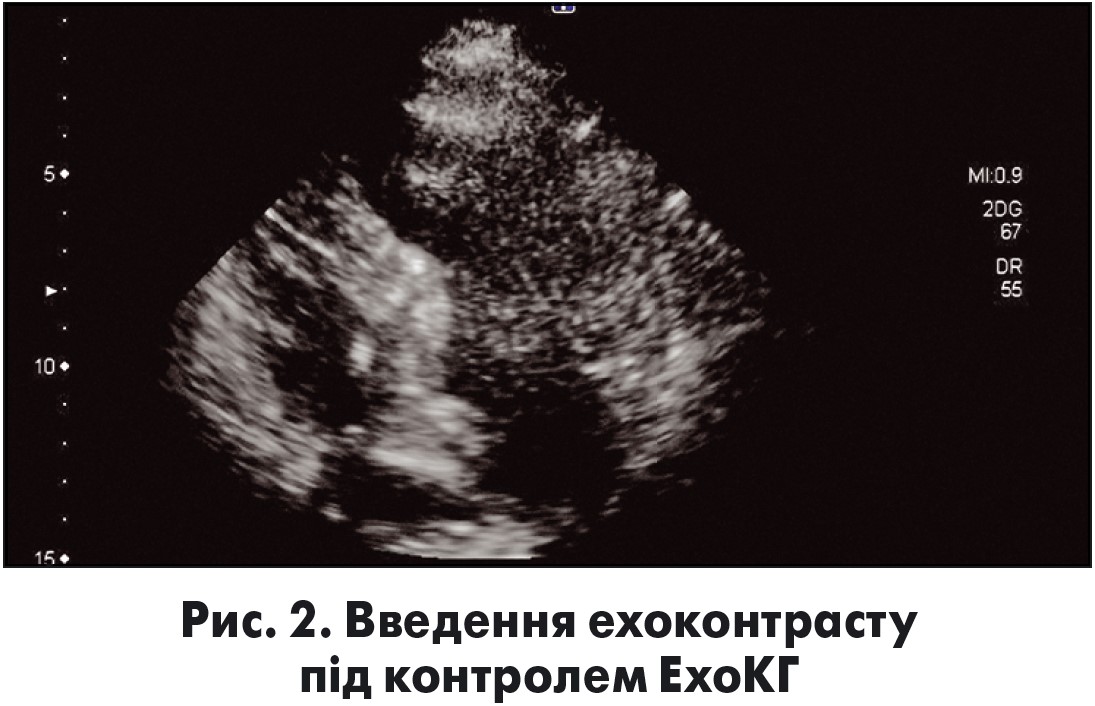
Для точної візуалізації джерела кровопостачання ділянки МШП, яка спричиняє обструкцію ВТ ЛШ, використовують ехоконтраст (рис. 2).
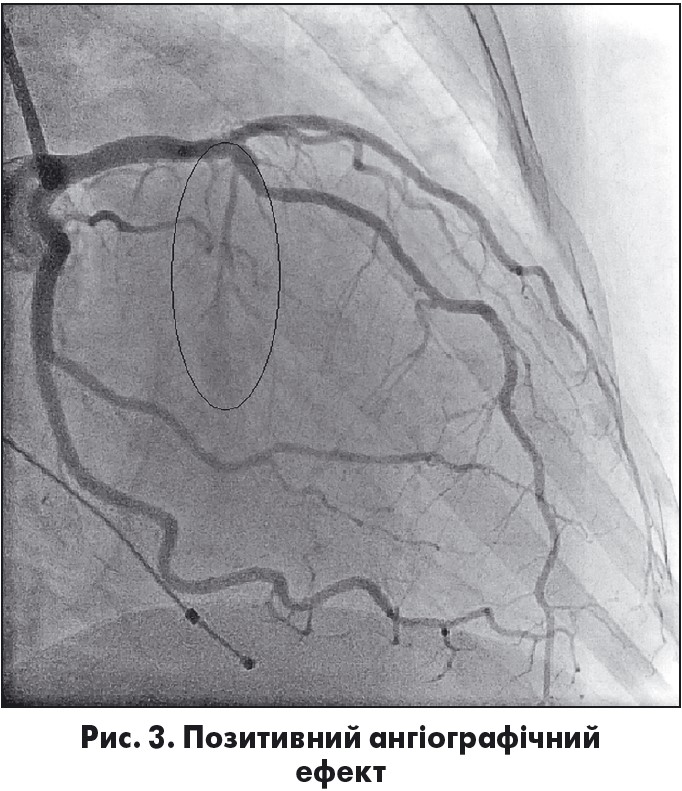
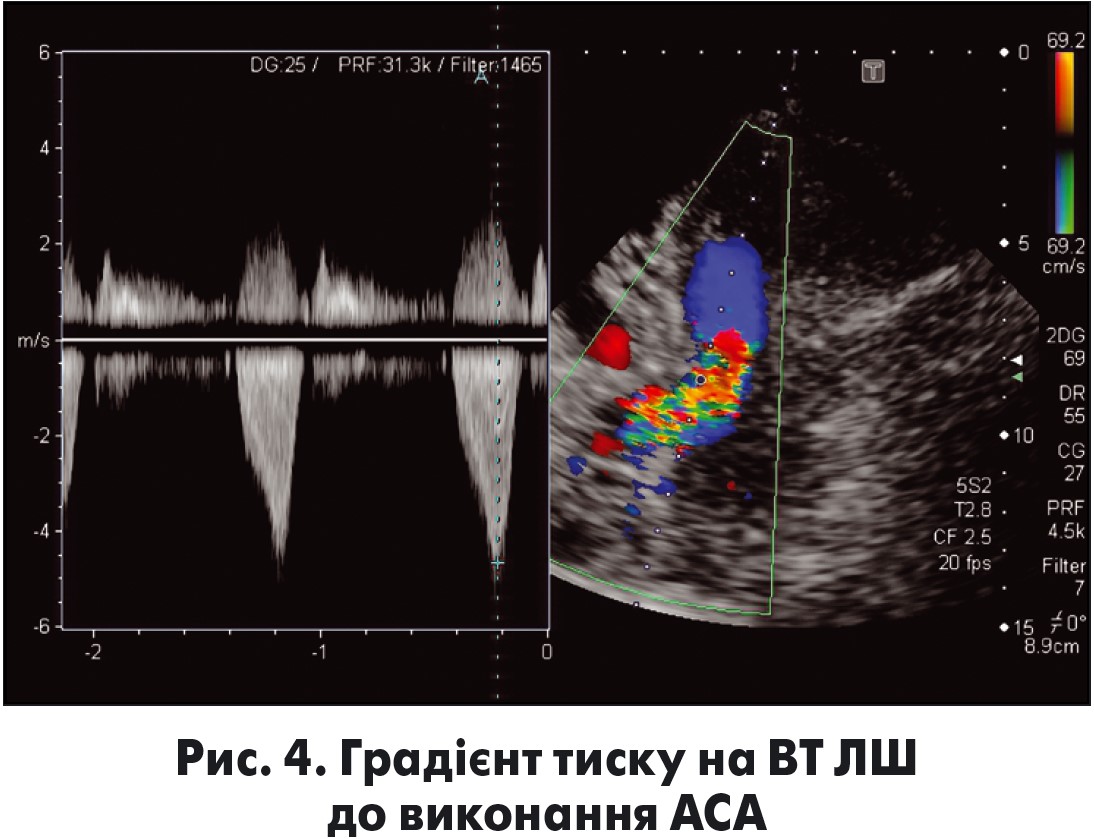
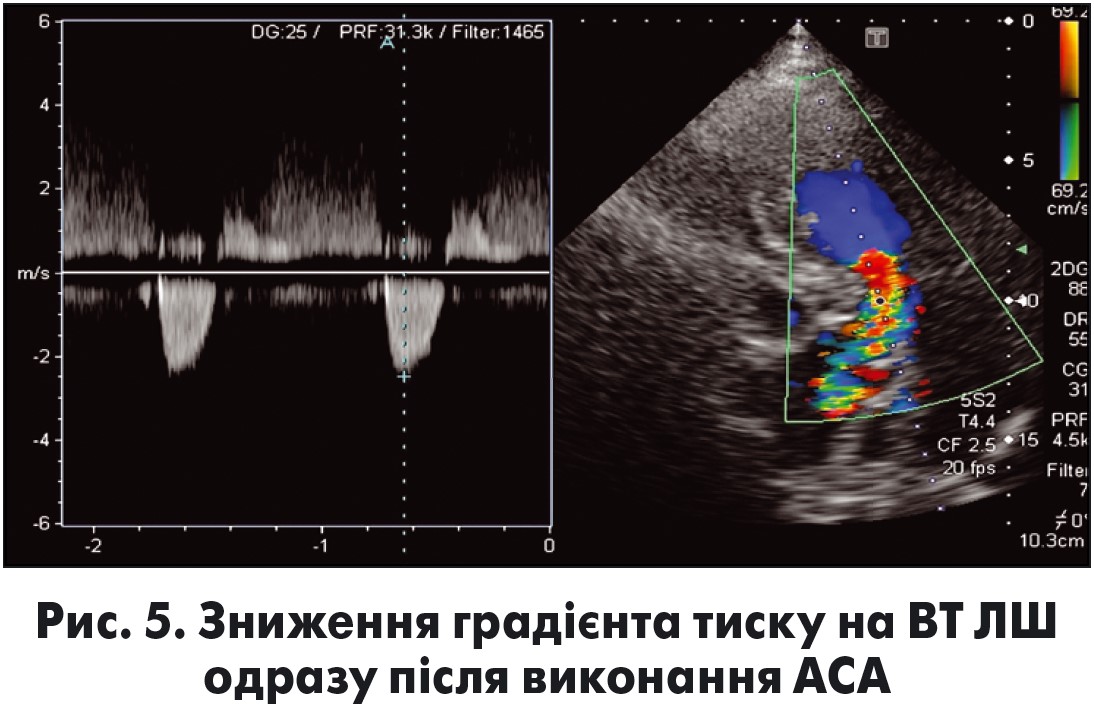
Після візуалізації ділянки МШП, яка обтурує ВТ ЛШ, переходять до введення 96-98% етилового спирту. Процедуру припиняють після досягнення позитивного ангіографічного (рис. 3) та гемодинамічного (рис. 4, 5) ефектів або при досягненні максимально допустимого об’єму спирту.
Власний досвід
Упродовж 2010-го – першого півріччя 2017 року у відділенні ендоваскулярної хірургії та ангіографії ДУ «Інститут серця МОЗ України» 96 пацієнтам із обструктивною формою ГКМП було виконано АСА.
Хворі були поділені за статтю та віком. Чоловіки становили близько третини (n=38) усіх хворих, жінок було приблизно вдвічі більше (n=58). Наймолодшому пацієнтові було 19 років, найстаршому – 73 роки.
Пацієнтам, яким планувалося проведення АСА, було виконано низку інструментальних досліджень:
- ЕхоКГ (у спокої та після навантаження – проба Вальсальви);
- коронарографія;
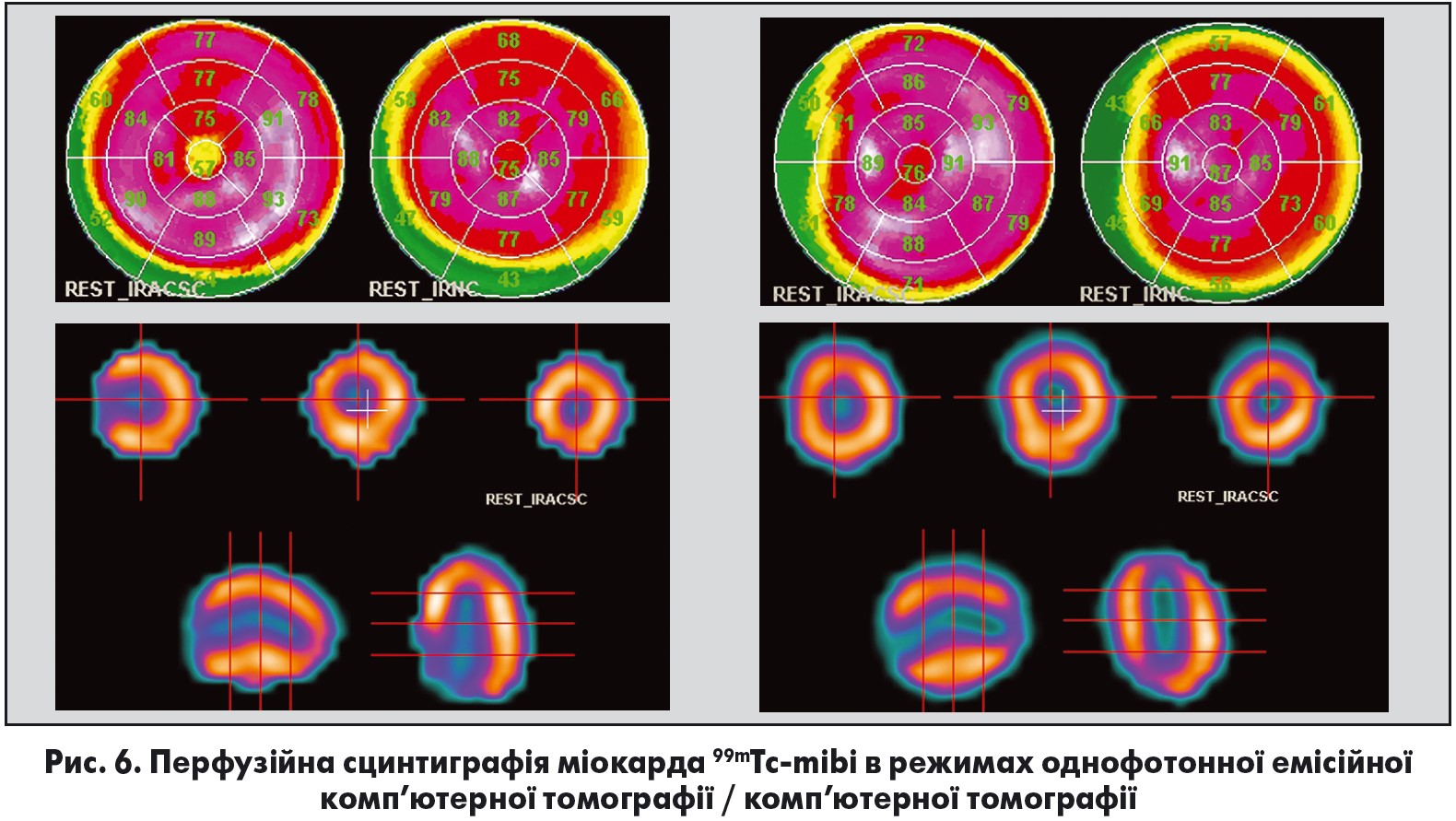
- міокардіосцинтиграфія з 99mTc-mibi (рис. 6).
З метою запобігання повній атріовентрикулярній блокаді безпосередньо перед процедурою кожному пацієнту було імплантовано тимчасовий електрокардіостимулятор.
Середній градієнт тиску на ВТ ЛШ одразу після проведення АСА становив:
- 96,89 мм рт. ст. (max – 300; min – 50) – до втручання;
- 37,2 мм рт. ст. (max – 78; min – 10) – після втручання.
Одноразово АСА було виконано 76 хворим (79,1%). На другу добу проводилося визначення рівня тропоніну І. Після виконання АСА у хворих виникли такі ускладнення:
- фібриляція шлуночків (під час процедури) – усунено за допомогою проведення електроімпульсної терапії (200 Дж одноразово);
- псевдоаневризма стегнової артерії в місці пункції – усунено мануальною компресією;
- повна атріовентрикулярна блокада – в усіх випадках виконано імплантацію постійного електрокардіостимулятора;
- дисекція інтими основного стовбура лівої коронарної артерії – гемодинамічно не значуща.
Летальність становила 1% (1 хворий).
Уперше методика АСА була застосована Sigwart у 1994 році. Це був початок нової ери в історії лікування обструктивної форми ГКМП. Відтоді тривають дискусії між кардіохірургами й фахівцями з ендоваскулярних методів лікування стосовно ефективності та переваг відкритого (міоектомія) та ендоваскулярного (АСА) методів лікування. До основних переваг АСА зараховують коротший період госпіталізації, меншу болючість процедури й запобігання ускладненням, що виникають після кардіохірургічної операції та внаслідок застосування апарата штучного кровообігу.
Наразі АСА залишається ефективним методом як самостійного, так і стадійного лікування обструктивної ГКМП і є методом вибору в лікуванні пацієнтів із цим захворюванням. За умови дотримання чітких критеріїв відбору хворих на виконання АСА відсоток ускладнень після її проведення надзвичайно низький.
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 5 (54) листопад 2017 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....