Систематичний огляд та метааналіз ризиків припинення або неприхильності до прийому ацетилсаліцилової кислоти серед 50 279 пацієнтів з ішемічною хворобою серця
Результати
У проспективному дослідженні Collet і співавт. (2004) за участю 1358 пацієнтів, яких госпіталізували з гострим інфарктом міокарда (ІМ) та спостерігали протягом місяця, нещодавнє припинення прийому АСК асоціювалося зі значним підвищенням 1-місячного ризику смерті, ІМ або кровотечі навіть після поправки на потенційні супутні фактори. Інфаркт міокарда спостерігався в середньому через 11,9±0,8 дня після відміни АСК. Примітно, що в 64% випадків припинення прийому АСК відбувалося за рішенням лікаря перед плановим хірургічним втручанням.
Подібні результати відзначалися в дослідженні Ferrari і співавт. (2005) серед 1236 пацієнтів з гострим коронарним синдромом (ГКС). Нещодавня відміна АСК мала місце в 4,1% усіх коронарних подій і 13,3% повторних ГКС. Крім того, спостерігалася чітка кореляція між припиненням прийому АСК і розвитком ІМ з елевацією сегмента ST. Затримка між відміною АСК і настанням гострої коронарної події дорівнювала в середньому 10,0±1,9 дня.
Newby і співавт. (2006) повідомили віддалені результати в пацієнтів з високою прихильністю до лікування АСК порівняно з такими у хворих із неприхильністю (зокрема, таких, які не розпочали призначену лікарем терапію препаратом, приймали його непостійно або почали приймати, а потім припинили лікування) після встановленого діагнозу ІХС. Прихильність до прийому АСК забезпечувала потужний захисний ефект стосовно загальної смертності (відносний ризик – ВР – 0,58; 95% довірчий інтервал– ДІ – 0,54-0,62) упродовж 7 років спостереження, що свідчить про довготривалі переваги лікування АСК та доводить наявність ризиків, пов’язаних з припиненням прийому АСК або низьким комплаєнсом.
Iakovou і співавт. (2005), спостерігаючи 2229 пацієнтів після черезшкірного коронарного втручання (ЧКВ) з успішною імплантацією стента з лікарським покриттям, встановили, що припинення антитромбоцитарної терапії призводить до різкого зростання ризику смерті, нефатального ІМ і тромбозу стента. Ці події мали місце у 29% осіб, які припинили прийом АСК та/або тієнопіридину.
Dacey і співавт. (2000) виконали дослідження типу «випадок – контроль» за участю 8641 пацієнта після аортокоронарного шунтування (АКШ). Прийом АСК протягом тижня перед втручанням супроводжувався зниженням ризику госпітальної летальності та не збільшував частоту повторних втручань з приводу кровотечі, кількість дренажних трубок у грудній порожнині або переливань крові.
Дослідження Mangano і співавт. (2002) підтвердило ці дані, а також засвідчило, що відновлення прийому АСК упродовж 48 год після АКШ значно зменшує ризик госпітальних подій, зокрема смерті від будь-яких причин, ІМ, інсульту, ниркової недостатності та брижової ішемії, і не порушує загоєння ран.
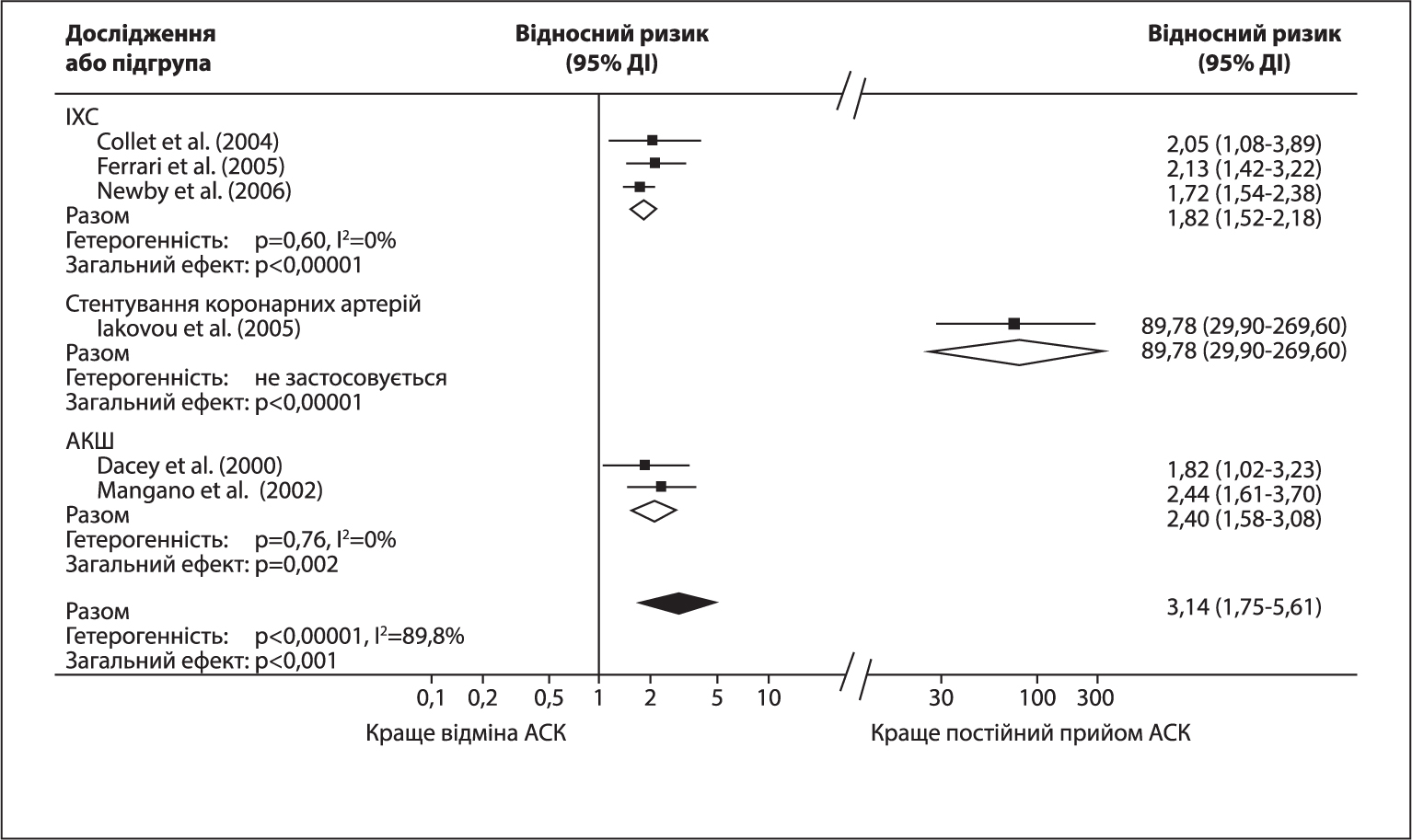
На рисунку представлені результати метааналізу вищенаведених досліджень – загальні та для окремих підгруп. У дослідженнях, до яких залучали пацієнтів із ГКС або хворих, що отримували вторинну профілактику ІХС, ризик кардіоваскулярних подій у разі відміни або неприхильності до прийому АСК зростав майже удвічі (ВР 1,82; 95% ДІ 1,52-2,18; р<0,00001). У пацієнтів після кардіохірургічних втручань припинення прийому АСК або низький комплаєнс також асоціювалися зі значним підвищенням цього ризику (ВР 2,20; 95% ДІ 1,58-3,08; р=0,002).
Рис. Ризик тромботичних подій у пацієнтів, що припинили прийом АСК
або мали низьку прихильність до її прийому
Загалом та в кожній підгрупі припинення прийому АСК достовірно асоціювалося з підвищеним ризиком тромботичних подій. В усіх підгрупах підвищення ризику є клінічно та статично однорідним, за винятком пацієнтів після ЧКВ з імплантацією стента з лікарським покриттям (дослідження Iakovou et al.), у яких ризик зростав майже в 90 разів – набагато більше, ніж у будь-якій іншій підгрупі.
Об’єднання зазначених підгруп підтвердило наявність високодостовірного взаємозв’язку між припиненням / неприхильністю до прийому АСК та кардіоваскулярними подіями (ВР 3,14; р=0,0001). Між відміною АСК та настанням тромботичних подій проходило в середньому 10,66±0,41 дня. Цей період узгоджується з тривалістю життя тромбоцитів і свідчить, що в разі обов’язкої відміни АСК перед інвазивними втручаннями в пацієнтів з високим ризиком кровотечі прийом препарату слід відновити якомога раніше.
Обговорення
Метааналіз, що об’єднав 6 досліджень та понад 57 тис. пацієнтів, продемонстрував значне підвищення ризику кардіоваскулярних подій у середньому через 10 днів після припинення прийому АСК у широкій популяції пацієнтів з ризиком розвитку або наявною ІХС. Ризик однаково зростав у пацієнтів із ГКС та у хворих після АКШ; це чітко вказує на те, що переваги від прийому АСК не обмежуються якоюсь специфічною популяцією пацієнтів. Дуже значне (майже в 90 разів) підвищення ризику після відміни АСК у пацієнтів, яким виконували ЧКВ з імплантацією стента з лікарським покриттям, пояснюється високим ризиком тромбозу стента.
У попередніх дослідженнях були отримані вказівки на можливість безпечного продовження прийому низьких доз АСК у пацієнтів, яким проводять малі (наприклад, стоматологічні) хірургічні втручання (Madan et al., 2005). У систематичному огляді Burger і співавт. (2005) встановили, що періопераційна відміна АСК передувала 10,2% гострих кардіоваскулярних подій; продовження періопераційного прийому АСК хоча й підвищувало частоту кровотеч, проте не призводило до зростання тяжких геморагічних ускладнень (за винятком, можливо, внутрішньочерепних втручань та трансуретральної простатектомії).
На думку авторів, прийом АСК можна безпечно продовжувати в усіх пацієнтів з низьким ризиком кровотечі, у також у хворих із вищим геморагічним ризиком у разі малих некардіальних втручань (наприклад, на шкірі) або АКШ. Пацієнтам, яким плануються великі кардіальні або некардіальні хірургічні втручання, зазвичай рекомендують відміну АСК за 3 дні до операції з подальшим відновленням прийому не пізніше ніж через 3 дні після втручання з використанням парентерального антикоагулянта (нефракціонованого або низькомолекулярного гепарину) протягом цього перехідного періоду. У пацієнтів після ЧКВ з імплантацією стента з лікарським покриттям, особливо впродовж перших тижнів після стентування, у разі неможливості відтермінувати хірургічне втручання до епіталізації стента (≥4 міс для цільнометалевих стентів, ≥3 та ≥6 міс для стентів, покритих сиролімусом або паклітакселом відповідно) прийом АСК та/або тієнопіридину переривати не рекомендовано через дуже значне підвищення тромботичного ризику.
Незважаючи на те що найчастіше використовувані пероральні антитромбоцитарні препарати, а саме АСК і клопідогрель, здатні забезпечувати подібний антитромботичний ефект, вони суттєво відрізняються за механізмом дії, профілем безпеки та вартістю. Так, АСК не лише пригнічує синтез тромбоксану А2 шляхом незворотного зв’язування з циклооксигеназою, а й демонструє інші вазопротекторні ефекти, як-от індукція синтезу оксиду азоту нейтрофілами та ендотеліоцитами. Крім того, АСК навіть у низьких дозах має протизапальний ефект, а запалення в пацієнтів кардіоваскулярного профілю асоціюється з гіршим прогнозом. При цьому тієнопіридини мають інший механізм дії (інгібування рецепторів АДФ) і позбавлені корисних плейотропних ефектів.
Висновки
У пацієнтів з ІХС низька прихильність до лікування АСК або припинення прийому АСК має значний негативний вплив на прогноз. Відміна АСК у таких хворих може здійснюватися лікарем лише у випадку, коли ризик кровотечі або інших небажаних ефектів перевершує ризик кардіоваскулярних атеротромботичних подій.
Довідка «ЗУ»
Міжнародні та національні кардіологічні товариства рекомендують застосовувати АСК у дозі від 75 мг як для первинної профілактики тромбозів і серцево-судинних захворювань (наприклад, ГКС) у пацієнтів з факторами серцево-судинного ризику (вік, стать, артеріальна гіпертензія, цукровий діабет, гіперхолестеринемія, ожиріння, сімейний анамнез серцево-судинних захворювань), так і для вторинної профілактики з метою зниження частоти тромботичних ускладнень у пацієнтів з гострою та хронічною формами ІХС, захворюваннями периферичних артерій і порушеннями мозкового кровообігу в анамнезі. Для досягнення максимального антитромбоцитарного ефекту при призначенні АСК у низьких дозах слід надавати перевагу препарату без кишковорозчинної оболонки, що забезпечує початок усмоктування діючої речовини в шлунку.
Призначаючи тривалу терапію для профілактики серцево-судинних катастроф, лікар має бути впевнений у якості препаратів.
В Україні представлені препарати АСК європейського виробництва компанії Takeda GmbH (Германія) – Кардіомагніл (таблетки, вкриті плівковою оболонкою; одна таблетка містить 75 мг АСК) і Кардіомагніл Форте (таблетки, вкриті плівковою оболонкою; одна таблетка містить 150 мг АСК).
Список літератури знаходиться в редакції.
Стаття друкується в скороченні.
Biondi-Zoccai G.G., Lotrionte M., Agostoni P. et al.
A systematic review and meta-analysis on the hazards
of discontinuing or not adhering to aspirin among 50, 279 patients at risk for coronary artery disease.
Eur Heart J. 2006 Nov; 27 (22): 2667-2674.
Переклав з англ. Олексій Терещенко
UA/CVM/1217/0115
Стаття друкується за підтримки компанії ТОВ «Такеда Україна».
Медична газета «Здоров’я України 21 сторіччя» № 23 (420), грудень 2017 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....