Чому зростає кількість призначень препаратів метформіну для лікування цукрового діабету 1 типу?
 Протягом майже століття, з 1922 р., у лікуванні цукрового діабету (ЦД) 1 типу (а іноді й ЦД 2 типу) традиційно використовують препарати інсуліну. Це дозволяє в разі недостатньої кількості β-клітин підшлункової залози й ендогенного інсуліну ефективно поповнювати рівень цього гормона і контролювати концентрацію глюкози в крові, запобігаючи в такий спосіб розвитку ускладнень.
Протягом майже століття, з 1922 р., у лікуванні цукрового діабету (ЦД) 1 типу (а іноді й ЦД 2 типу) традиційно використовують препарати інсуліну. Це дозволяє в разі недостатньої кількості β-клітин підшлункової залози й ендогенного інсуліну ефективно поповнювати рівень цього гормона і контролювати концентрацію глюкози в крові, запобігаючи в такий спосіб розвитку ускладнень.
Препарати інсуліну – найпотужніші, однак не ідеальні цукрознижувальні медикаменти. Як показали численні дослідження, правильне використання цих засобів та хороший глікемічний контроль не завжди дозволяють уникнути атеросклеротичних (або, як їх раніше називали, макросудинних) серцевосудинних ускладнень ЦД, що зумовлюють приблизно 70% випадків передчасної смерті від інсульту, інфаркту міокарда та ін. Останні спостереження демонструють, що препарати інсуліну, окрім позитивних ефектів, мають низку негативних властивостей, які можуть проявлятися як протягом короткого терміну, так і у віддаленій перспективі (табл. 1).
Препарати інсуліну є основою терапії пацієнтів із ЦД 1 типу, прийом цих лікарських засобів запобігає розвитку мікросудинних ускладнень (ретинопатії, нефропатії, нейропатії), проте не в змозі попередити атеросклеротичні (макросудинні) серцеві ускладнення і появу злоякісних новоутворень, а саме ці фактори найчастіше є причиною передчасної смерті хворих на ЦД [7].
Атеросклеротичні (макросудинні) ускладнення при інсулінотерапії
У пацієнтів із ЦД 1 типу ризик розвитку серцевосудинних захворювань та смерті зазвичай у 35 разів вищий за такий у загальній популяції, при цьому деякі дані свідчать, що цілеспрямоване обмеження глікемії може сприятливо впливати на зазначені показники [89]. Так, якщо у хворого на діабет рівень HbA1c нижчий цільового – 6,9% (52 ммоль/моль), то імовірність виникнення в нього кардіоваскулярної патології та смерті зменшується, але все ж у середньому є удвічі більшою, ніж у здорових осіб [9].
Артеріальна гіпертензія є найважливішим фактором ризику інсульту, артеріальний тиск і ЦД можуть взаємодіяти синергічно і значно збільшувати вірогідність виникнення гострого порушення мозкового кровообігу. Загалом 73% чоловіків і 66% жінок із ЦД 1 типу мають підвищений артеріальний тиск або отримують антигіпертензивні препарати [9].
Ожиріння, дисліпідемія, резистентність до інсуліну, гіперглікемія та ЦД – це потужні незалежні чинники ризику виникнення серцевих подій. Очікувана тривалість життя, що оцінювалася серед учасників із ЦД 1 типу віком 20 років, знижується на 13 та 11 років для жінок і чоловіків відповідно порівняно з такими в популяції без ЦД 1 типу, причому саме серцевосудинні захворювання є частою причиною їх передчасної смерті [9].
У пацієнтів із дисліпідемією зниження рівня холестерину ЛПНЩ на 5% зменшує серцевосудинну смертність на 5%, а підвищення вмісту холестерину ліпопротеїнів високої щільності (ЛПВЩ) на 5%, здебільшого пов’язане з обмеженням тригліцеридів (жирів) за рахунок корекції харчування, знижує ризик коронарних подій на 20% [10].
Інсулінорезистентність достовірно асоціюється із серцевосудинними захворюваннями при ЦД 2 типу [11]. Еуглікемічний clampтест у підлітків з ЦД 1 типу, які мають нормальну вагу, засвідчив наявність стійкості до дії інсуліну [5, 1217]. Високі дози інсуліну необхідні для компенсації інсулінорезистентності (особливо в тканинах печінки), але водночас це призводить до надмірного збільшення маси тіла. Таким чином, у хворих підліткового віку потрібно застосовувати більш ефективні стратегії ведення ЦД, щоб відтермінувати виникнення серцевосудинної патології, ретино та нефропатії [13].
У двох масштабних дослідженнях за участю пацієнтів із ЦД 2 типу – UGDP (University Group Diabetes Program) та UKPDS (United Kingdom Prospective Diabetes Study) – було вперше показано, що в групі інтенсивної терапії інсуліном не спостерігалося зменшення ризику макросудинних ускладнень [1], незважаючи на значне зниження частоти виникнення мікросудинних порушень. За деякими винятками, цей висновок було підтверджено в більшості рандомізованих контрольованих досліджень (ACCORD, ADVANCE та VADT): раннє втручання із забезпеченням інтенсивного глікемічного контролю за рахунок використання традиційних цукрознижувальних препаратів та інсулінотерапії не є корисним у цілому [18].
Ризик виникнення злоякісних новоутворень при інсулінотерапії
Епідеміологічні дані свідчать, що люди з діабетом мають значно вищі ризики розвитку багатьох форм раку. Останнім часом з’ясувалося, що прийом цукрознижувальних препаратів також може асоціюватися зі збільшенням поширеності деяких видів онкопатології; утім, доступні дані є обмеженими та суперечливими [7]. У низці епідеміологічних досліджень продемонстровано, що ризик виникнення кількох видів раку (грудної залози, колоректального, печінки та підшлункової залози) пов’язаний з інсулінорезистентністю й опосередковується через інсуліноподібний фактор росту 1 (ІФР‑1). Хоча основним місцем продукції ІФР‑1 є печінка, на відміну від інсуліну він виробляється багатьма типами клітин. Наявні дані вказують на те, що інсулін та рецептори ІФР‑1 опосередковують численні процеси: регулюють проліферацію, диференціацію, апоптоз клітин, транспорт глюкози та енергетичний обмін, забезпечуючи передачу сигналу через субодиниці інсулінового рецептора; таким чином, вони відіграють ключову роль у визначенні долі клітини щодо виникнення раку [19].
Дані низки недавніх досліджень показали, що у хворих на ЦД, які отримують інсулін, ризик виявлення раку різних локалізацій є підвищеним; натомість препарати метформіну можуть мати протекторну дію в пацієнтів із ЦД і без діабету [20]. Уперше ця проблематика вивчалася в аналізі німецької бази даних страхування 127 031 пацієнта із ЦД (Hemkens, 2009) [21]. Було встановлено статистично значимий дозозалежний зв’язок між раком і використанням одного з аналогів інсуліну порівняно з відповідним показником для інсуліну НРХ. У пацієнтів, які приймали щоденну дозу такого аналога (10 МОд/д), ризик раку підвищувався на 9% (відносний ризик (ВР) 1,09); у разі використання дози 50 МОд/д ризик раку зростав до 31% [21]. Ці результати спонукали редакторів відомого журналу Diabetologia, офіційного видання Європейської асоціації з вивчення діабету, та її керівництво виконати 3 додаткових дослідження з безпеки призначення інсуліну. Подальший аналіз проводився з використанням баз даних Шотландії, Швеції та Великої Британії [20].
Шведське дослідження (115 тис. дорослих, дані реєстру раку за 20062007 рр.) показало значне підвищення ризику раку грудної залози приблизно в 6 тис. хворих, які отримують інсулінотерапію [20]. У шотландському дослідженні (Colhoun, 2009) було оцінено дані 36 254 пацієнтів, які приймали інсулін; зафіксовано 715 випадків раку [22].
У ретроспективному когортному дослідженні (n=62 809), проведеному у Великій Британії, учасників було розподілено на 4 групи лікування: монотерапії метформіном, монотерапії похідними сульфонілсечовини, комбінованої терапії (метформін/сульфонілсечовина) та інсулінотерапії. Порівняно з лікуванням метформіном інсулінотерапія була пов’язана з підвищеним ризиком розвитку колоректального раку (ВР 1,69) або підшлункової залози (ВР 4,63), але не раку грудної та передміхурової залози. Скоригований ВР раку становив 1,42 для групи монотерапії інсуліном, 1,36 – для монотерапії похідними сульфонілсечовини та 1,08 – для комбінації метформіну та сульфонілсечовини [23]. Результати показали, що тільки метформін дозволяв знизити ризик виникнення раку [23]. Додавання метформіну до інсуліну асоціювалося зі зменшенням прогресування раку (ВР=0,54).
Є думка, що стимуляція метформіном AMFактивованої протеїнкінази (AMPK) у пухлинних клітинах призводить до інгібування їхнього росту, принаймні частково, шляхом блокування синтезу специфічних білків [24]. Додаткові спостереження свідчать, що метформін може покращити прогноз за наявності онкопатології.
В опублікованому в США консенсусі «Діабет і рак» (2013) висвітлено потенційні механізми як прямої, так і непрямої дії, за допомогою яких препарати інсуліну або його аналогів можуть впливати на виникнення неопластичних захворювань [25]. Механізмам прямої дії приділено найбільшу увагу: передбачається імовірність взаємодії введених лігандів (або їхніх метаболітів) з раковими клітинами, частково трансформованими клітинами або клітинами, що перебувають під загрозою трансформації. Непрямі механізми дії на клітинимішені вивчалися меншою мірою, але встановлено, що вони включали взаємодію сигнальних молекул (наприклад, глюкагон, адипонектин, ІФР‑1), на рівні або на активність яких впливає введений екзогенний інсулін. Показана можливість потенційного впливу метформіну на блокування проліферації злоякісних клітин, котрий сприяє зниженню ризику розвитку раку або смерті від нього [25, 26].
Щодо призначення метформіну у хворих на ЦД 1 типу
Профілактичні стратегії щодо зниження ризиків серцевосудинних захворювань є аналогічними для пацієнтів із ЦД 2 типу та осіб із ЦД 1 типу [28]. Доволі частими є випадки, коли в пацієнтів із ЦД 1 типу з початковою нормостенією, які протягом багатьох років отримують інсулінотерапію, маса тіла поступово збільшується (аж до розвитку ожиріння). Дійсно, декілька клінічних випробувань, у тому числі DCCT, показують, що інтенсивна терапія інсуліном може призвести до надмірного збільшення ваги у хворих на ЦД 1 типу [27, 29]. Природно, що це не лише погіршує контроль вуглеводного обміну (глюкоза плазми крові, НbА1с, деяких інших показників), а й супроводжується появою або посиленням інсулінорезистентності, значним підвищенням серцевосудинних ризиків (атеросклеротичних). У 3040% пацієнтів з ЦД 1 типу тривала інтенсивна інсулінотерапія пов’язана зі збільшенням маси тіла і подальшим розвитком метаболічного синдрому, який асоціюється з додатковими серцевосудинними ризиками. Звичайно, до цього призводять не тільки використання препаратів інсуліну та спричинене ними підвищення апетиту, а й необізнаність хворих, недотримання рекомендацій лікаря і принципів раціонального харчування, нехтування самоконтролем, відсутність відповідної роз’яснювальної роботи з боку медичних працівників.
Якщо наявне ожиріння, недостатньо просто обговорити з пацієнтом помилки, що мали місце. Виправити ситуацію можна лише шляхом зміни схеми лікування (дозування і препаратів), адже надлишкове введення інсуліну стимулює апетит, а отже, й накопичення жирової тканини. На жаль, арсенал медикаментозних засобів, що можуть знижувати інсулінорезистентність і ризики атеросклеротичних судинних ускладнень у хворих на ЦД 1 типу, вкрай обмежений: з урахуванням ефективності, безпеки та фармакоекономіки для цього підходять тільки препарати метформіну. Тому дослідники зосередили зусилля на додаванні до традиційної замісної терапії ЦД 1 типу таблетованих (метформіну, антагоністів дипептидилпептидази 4 типу та ін.) або ін’єкційних (агоністів глюкагоноподібного пептиду 1 типу) препаратів. Частота використання таблетованих засобів у лікуванні ЦД 1 типу в комбінації з інсуліном у США становить близько 6,5% [17, 18, 26, 30], у Великій Британії (дані за 2016 р.) – 8%. Найчастіше для цього використовують метформін (65% випадків). Наразі частка призначень таблетованих препаратів на додачу до інсуліну при ЦД 1 типу є невеликою, проте вона постійно зростає, наближуючись до 10%.
Метформін є базисним медикаментом у лікуванні ЦД 2 типу, у вагітних жінок – препаратом першої лінії. Головні механізми дії метформіну полягають у пригніченні глюконеогенезу в печінці та підвищенні чутливості до ендогенного інсуліну в різних тканинах, зниження індексу маси тіла (ІМТ) на 1% завдяки терапії метформіном у порівнянні з плацебо зменшує резистентність до інсуліну на 5% [30]. Цей препарат має велику кількість додаткових ефектів, що підтверджено в низці досліджень [31, 32]. Додавання метформіну до інсулінотерапії (як ад’ювантної терапії) дозволяє знизити віддалені серцевосудинні ризики у хворих на ЦД 1 типу та ЦД 2 типу [29, 33]. Нові дослідження демонструють, що застосування метформіну асоціювалося зі зниженням добової дози інсуліну, маси тіла, рівнів загального холестерину, холестерину ЛПНЩ, а також з підвищенням умісту холестерину ЛПВЩ. Не було виявлено суттєвої різниці між групами метформіну та плацебо щодо рівнів HbA1c, глюкози натще або тригліцеридів, ризику тяжкої гіпоглікемії чи діабетичного кетоацидозу [34].
В окремих клінічних дослідженнях показано, що додавання препаратів метформіну до традиційної схеми інсулінотерапії ЦД 1 типу сприяло незначному зниженню сумарної добової дози інсуліну [15, 16, 35, 36]. При цьому в групі плацебо спостерігалося зростання глікемії та рівня НbА1с зі збільшенням сумарної дози введення інсуліну. У підлітків у періоді активного статевого дозрівання погіршення вуглеводного обміну пояснюють активацією інсулінорезистентності, збільшенням рівнів контрінсулярних гормонів, а саме гормона росту і статевих стероїдів. У низці досліджень встановлено значиму цукрознижувальну ефективність додавання метформіну до інсуліну саме в дітей та підлітків із ЦД 1 типу, які мають надлишкову масу тіла або ожиріння [35, 37].
Однак головним є не це. Метформін (бігуанід) помітно зменшує атеросклеротичні серцевосудинні ризики (інсульту, інфаркту) та ризик онкологічних захворювань, тобто пацієнти з ЦД 1 типу, які додатково отримують метформін, проживуть довше, ніж хворі, які лише компенсують недостатність ендогенного інсуліну. Метааналіз декількох десятків клінічних досліджень [39] показав, що додавання метформіну до інсуліну сприяє зниженню маси вісцеральної жирової тканини, співвідношення окружності талії до окружності стегон, систолічного та діастолічного артеріального тиску, маси лівого шлуночка, екскреції альбуміну та концентрації низки прозапальних біохімічних чинників у крові.
У загальній популяції резистентність до інсуліну була визначена важливим фактором виникнення та прогресування атеросклерозу [40, 41].
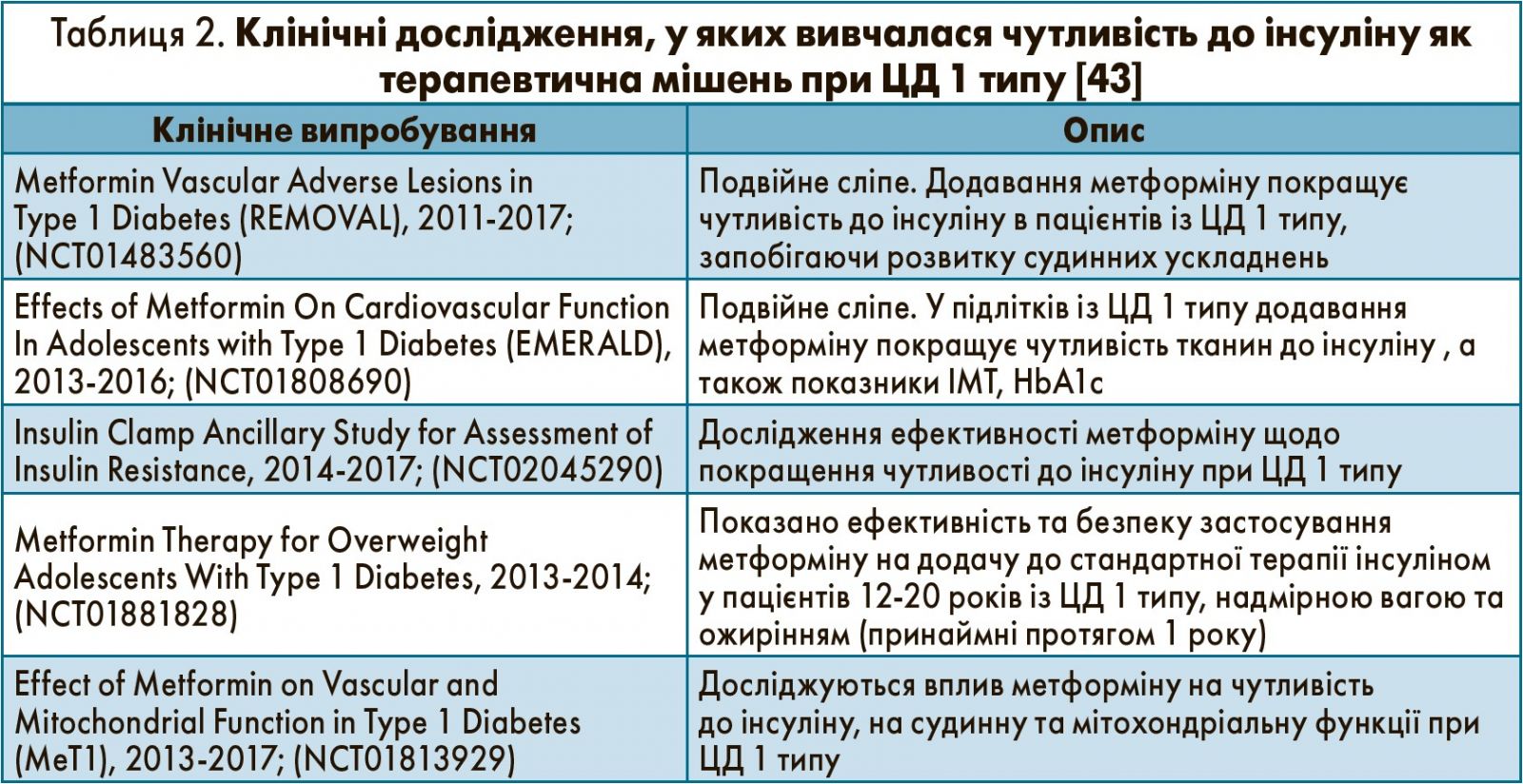
У червні 2017 р. на щорічній науковій сесії Американської діабетичної асоціації, що відбулася в м. СанДієго (США), а також у статті, опублікованій у журналі Lancet Diabetes & Endocrinology, зазначено: використання метформіну в дозі 1000 мг двічі на день протягом 3 років на додачу до інсуліну може забезпечити захист пацієнтів із ЦД 1 типу від атеросклерозу та знизити товщину інтима/медіа внутрішньої сонної артерії. Такі результати отримані в подвійному сліпому плацебоконтрольованому дослідженні REMOVAL за участю 428 дорослих віком ≥40 років із ЦД 1 типу та підвищеним серцевосудинним ризиком [42]. Автори дослідження рекомендують застосовувати метформін у пацієнтів із ЦД 1 типу для зменшення ІМТ, інсулінорезистентності й уповільнення прогресування серцевосудинних порушень (табл. 2).
Таким чином, навіть компенсація ЦД 1 типу не є запорукою попередження атеросклеротичних (макросудинних) ускладнень діабету, від яких помирає переважна більшість хворих. Застосування препаратів метформіну у хворих на ЦД 1 типу, дорослих або дітей, які отримують інсулінотерапію, є важливим доповненням до традиційної схеми, що дозволяє насамперед знизити серцевосудинні й онкологічні ризики. Прямі та опосередковані (плейотропні) властивості метформіну сприяють зменшенню смертності від цих захворювань і подовженню тривалості життя на 16% як у хворих на ЦД [17], так і в осіб без діабету. Частота призначення таблетованих цукрознижувальних засобів хворим на ЦД 1 типу у світі постійно зростає, наближаючись до 10%; зпоміж них саме метформін призначається найчастіше (приблизно у 65% випадків). Метформін розглядають як перспективний препарат у хворих на ЦД 1 типу, він є особливо корисним для осіб з надлишковою масою тіла або ожирінням. Невдовзі очікуємо нових публікацій та оновлення рекомендацій національних діабетичних асоціацій щодо підтримки більш широкого застосування препаратів метформіну у хворих на ЦД 1 типу.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 23 (420), грудень 2017 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
Нещодавні дослідження показали, що прогноз за різних поширених захворювань, ендокринних, автоімунних розладів і навіть прогресування раку пов’язані з концентрацією вітаміну D у плазмі. Завдяки експресії гена 1α-гідроксилази (CYP27B1) клітини імунної системи (В-, Т- та антигенпрезентувальні клітини) здатні продукувати активний метаболіт кальциферол – речовину з імуномодулювальними властивостями. Рецептори до вітаміну D (vitamin D receptor, VDR) експресують на поверхні імунних клітин. Доведено зв’язок між поліморфізмом генів VDR або CYP27B1 і патогенезом автоімунних ендокринних захворювань. Метою огляду є вивчення впливу вітаміну D, наслідків його дефіциту та корисної ролі добавок із ним при деяких ендокринних розладах, які часто спостерігають у клінічній практиці. ...
Збудник COVID‑19, SARS-CoV‑2, з яким людство вперше стикнулося у 2019 р., поширився по всьому світу, заразивши мільйони людей. Сьогодні, через тягар війни та економічної нестабільності, тема COVID‑19 не сприймається так гостро, як ще кілька років тому, хоча насправді вона не втратила своєї актуальності. Саме сучасному стану проблеми COVID‑19 у світі та в Україні була присвячена доповідь директора ДУ «Інститут ендокринології та обміну речовин імені В.П. Комісаренка НАМН України», академіка Національної академії медичних наук України, члена-кореспондента НАН України, віце-президента НАМН України, президента Асоціації ендокринологів України, професора Миколи Дмитровича Тронька під час першого у 2024 р. засідання науково-освітнього проєкту «Школа ендокринолога», яке відбулося 20-24 лютого. ...
Протягом останніх 60 років метформін є найпоширенішим цукрознижувальним засобом і рекомендований як препарат першої лінії для осіб з уперше виявленим цукровим діабетом (ЦД) 2 типу. Сьогодні понад 200 млн осіб із ЦД 2 типу в усьому світі щодня застосовують метформін як монотерапію або в комбінації. Препарат усе частіше використовують для лікування гестаційного ЦД та в пацієнтів із синдромом полікістозних яєчників. ...
Двадцять восьмого лютого 2024 року виповнилося 80 років від дня народження директора ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (далі – Інститут), віцепрезидента НАМН України, академіка НАМН України, члена-кореспондента НАН України, заслуженого діяча науки та техніки, лауреата Державної премії України, доктора медичних наук, професора Миколи Дмитровича Тронька....