Выбор антитромботической терапии у пациентов с фибрилляцией предсердий, подвергающихся чрескожным коронарным вмешательствам
По материалам VIII Научно-практической конференции Ассоциации аритмологов Украины (17-18 мая, г. Киев)
В VIIІ Научно-практической конференции Ассоциации аритмологов Украины по уже сложившейся традиции участвовали не только украинские эксперты в области аритмологии, но и зарубежные специалисты.

Врач-кардиолог, доцент кафедры Варшавского медицинского университета (Польша) Лукаш Колтовски осветил вопросы современной антитромботической терапии у пациентов с фибрилляцией предсердий (ФП), перенесших чрескожные коронарные вмешательства (ЧКВ).
Примерно 8% больных, перенесших ЧКВ, нуждаются в длительном антитромботическом лечении в связи с наличием ФП, механических клапанов сердца, развитием тромбоза глубоких вен нижних конечностей.
Сегодня с целью профилактики тромботических событий (инсультов, системных тромбоэмболий, тромбозов стентов) таким пациентам назначают тройную антитромботическую терапию, которая включает два антиагреганта: ацетилсалициловая кислота (АСК) + ингибитор P2Y12 (клопидогрель/тикагрелор) и пероральный антикоагулянт – антагонист витамина К (АВК) варфарин или один из современных антикоагулянтов – дабигатран, ривароксабан, апиксабан, эдоксабан.
Тройная антитромботическая терапия – эффективный подход для снижения риска развития тромбоэмболических событий, однако ее применение сопряжено с увеличением риска больших кровотечений в 2-3 раза по сравнению с терапией только варфарином, что вполне ожидаемо.
В связи с этим ключевым вопросом антитромботической терапии у пациентов с ФП, перенесших ЧКВ, является безопасность, и с этим вопросом тесно связаны другие – оптимальная длительность лечения и выбор лекарственных средств (антикоагулянтов и/или антиагрегантов) для долгосрочного приема.
Для получения ответов на эти вопросы было организовано открытое рандомизированное многоцентровое исследование WOEST (2013), в котором сравнивали безопасность двойной (АВК + клопидогрель) и тройной (АСК + клопидогрель + АВК) антитромботической терапии у пациентов с ФП, перенесших ЧКВ. Наблюдение за больными в течение одного года показало, что двойная терапия с включением только одного антиагреганта – клопидогреля – связана с меньшей частотой кровотечений без увеличения частоты тромбоэмболических осложнений по сравнению с применением тройной схемы лечения. За счет снижения числа кровотечений смертность среди пациентов, получающих двойную терапию, была на 23% ниже, чем в группе, получавшей тройную.
Результаты исследования WOEST (2013) послужили поводом для пересмотра рекомендаций в сторону максимального сокращения продолжительности тройной терапии у пациентов с ФП, подвергающихся ЧКВ (P. Kirchhof et al., 2016; E.A. Amsterdam et al., 2014).
На сегодня пациентам после планового ЧКВ рекомендуется проведение тройной антитромботической терапии на протяжении 4 нед, а при неотложном ЧКВ в случае острого коронарного синдрома – на протяжении 6 мес, с последующим переходом на терапию клопидогрелем и пероральным антикоагулянтом до 12 мес, а затем – переход на монотерапию антикоагулянтом.
Эффективность и безопасность двойной антитромботической терапии (ДАТ) с использованием нового перорального антикоагулянта – прямого ингибитора тромбина дабигатрана (Прадакса®) оценивали в открытом рандомизированном исследовании RE-DUAL PCI (C.P. Cannon et al., 2017). В нем приняли участие 2725 пациентов с ФП, перенесших ЧКВ, в 414 центрах в 41 стране в период с июля 2014 г. по октябрь 2016 г. Все участники получали стандартную антитромботическую терапию при проведении ЧКВ, а через 120 ч после процедуры были рандомизированы в три группы.
Первая группа пациентов получала тройную терапию: варфарин + ингибитор P2Y12 + АСК в первые 1-3 мес; вторая – двойную терапию: дабигатран (110 мг 2 р/сут) + ингибитор P2Y12, третья – двойную терапию с дабигатраном в дозе 150 мг 2 р/сут + ингибитор P2Y12. В качестве ингибитора P2Y12 все участники получали клопидогрель 75 мг 1 р/сут или тикагрелор 90 мг 2 р/сут в течение как минимум 12 мес. Дозу варфарина корректировали для удержания показателя
Международного нормализованного отношения (МНО) в диапазоне 2,0-3,0. Терапию продолжали 6-30 мес, после ее прекращения пациенты находились под наблюдением еще в среднем 14 мес.
Первичной конечной точкой исследования RE-DUAL PCI являлся первый эпизод большого или клинически значимого малого (CRNM) кровотечения по определению Международного общества по изучению тромбоза и гемостаза (ISTH).
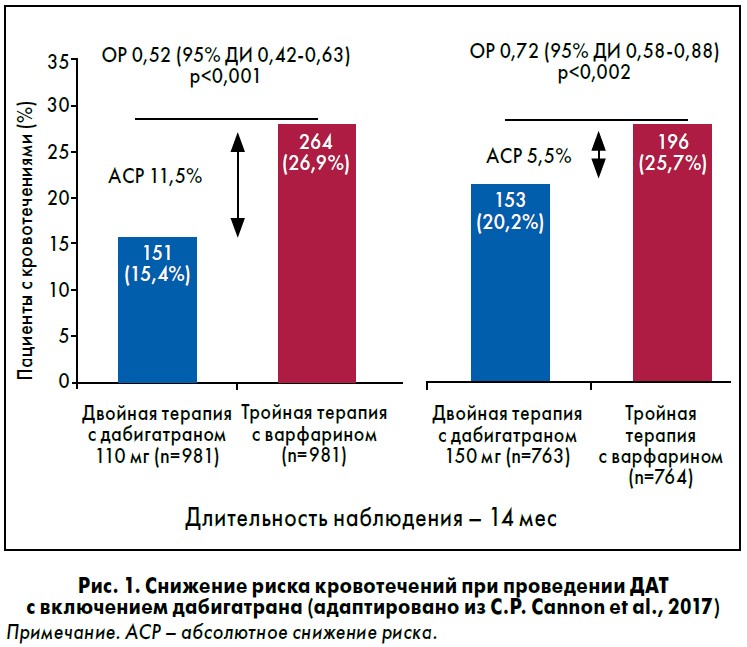 Исследование показало, что двойная терапия с включением дабигатрана значительно снижает риск обоих типов кровотечений в сравнении с тройной терапией: для группы дабигатрана, получавшей 110 мг, абсолютное снижение риска кровотечений составило 11,5% (отношение рисков, ОР 0,54; 95% доверительный интервал, ДИ 0,42-0,63; р<0,001), для группы дабигатрана, получавшей 150 мг, – 5,5% (ОР 0,72; 95% ДИ 0,58-0,88; р<0,001) (рис. 1).
Исследование показало, что двойная терапия с включением дабигатрана значительно снижает риск обоих типов кровотечений в сравнении с тройной терапией: для группы дабигатрана, получавшей 110 мг, абсолютное снижение риска кровотечений составило 11,5% (отношение рисков, ОР 0,54; 95% доверительный интервал, ДИ 0,42-0,63; р<0,001), для группы дабигатрана, получавшей 150 мг, – 5,5% (ОР 0,72; 95% ДИ 0,58-0,88; р<0,001) (рис. 1).
Риск только больших кровотечений так же, как и любых кровотечений, был значительно ниже в группах двойной терапии в сравнении с группой тройной терапии. При оценке частоты кровотечений по критериям TIMI их число также было ниже в обеих группах, получавших двойную терапию.
По частоте наступления вторичных конечных точек в исследовании RE-DUAL PCI оценивали эффективность антитромботической терапии. Главная комбинированная вторичная конечная точка включала тромбоэмболические события (инфаркт миокарда, инсульт, системная эмболия), смерть или внеплановую реваскуляризацию (ЧКВ или аортокоронарное шунтирование). Другие вторичные точки включали наступление тромбоэмболического события или смерти, а также индивидуальные тромбоэмболические события и определенный тромбоз стента.
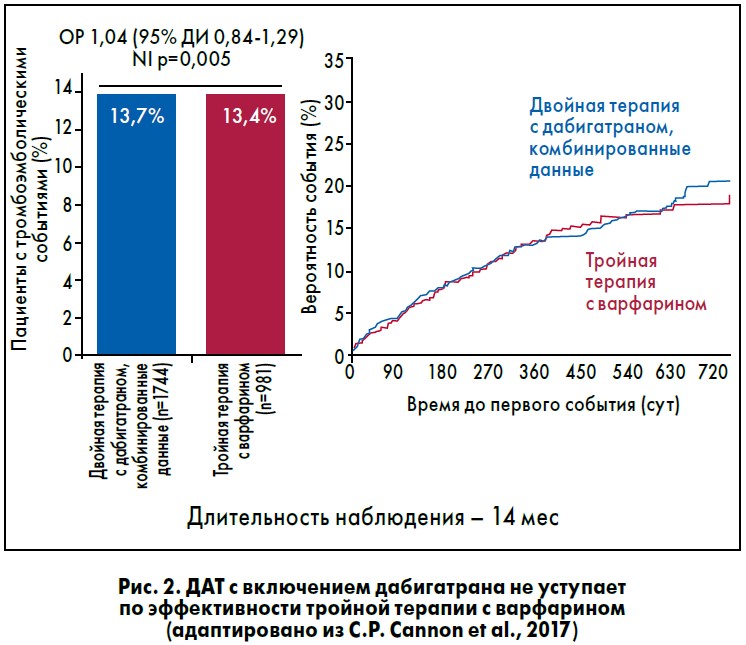 Анализ частоты перечисленных осложнений в различных группах показал, что ДАТ, включающая дабигатран, по эффективности не уступала тройной терапии с варфарином. Частота тромбоэмболических событий, смерти или внеплановой реваскуляризации составила 13,7% в обеих группах двойной терапии и 13,4% – в группе тройной терапии (ОР 1,04; 95% ДИ 0,84-1,29; р=0,005) (рис. 2).
Анализ частоты перечисленных осложнений в различных группах показал, что ДАТ, включающая дабигатран, по эффективности не уступала тройной терапии с варфарином. Частота тромбоэмболических событий, смерти или внеплановой реваскуляризации составила 13,7% в обеих группах двойной терапии и 13,4% – в группе тройной терапии (ОР 1,04; 95% ДИ 0,84-1,29; р=0,005) (рис. 2).
Сходная эффективность двойной и тройной терапии была подтверждена в различных подгруппах пациентов. Доля лиц с установленным тромбозом стентов была низкой во всех группах: 1,5% в группе двойной терапии с дабигатраном 110 мг в сравнении с 0,8% в группе тройной терапии (р=0,15) и по 0,9% в группах двойной терапии с дабигатраном 150 мг и тройной терапии (р=0,98).
Таким образом, у пациентов с ФП, перенесших ЧКВ, двойная терапия дабигатраном и ингибитором P2Y12 приводит к снижению риска развития больших и клинически значимых малых кровотечений по сравнению с тройной терапией, включающей варфарин, ингибитор P2Y12 и АСК.
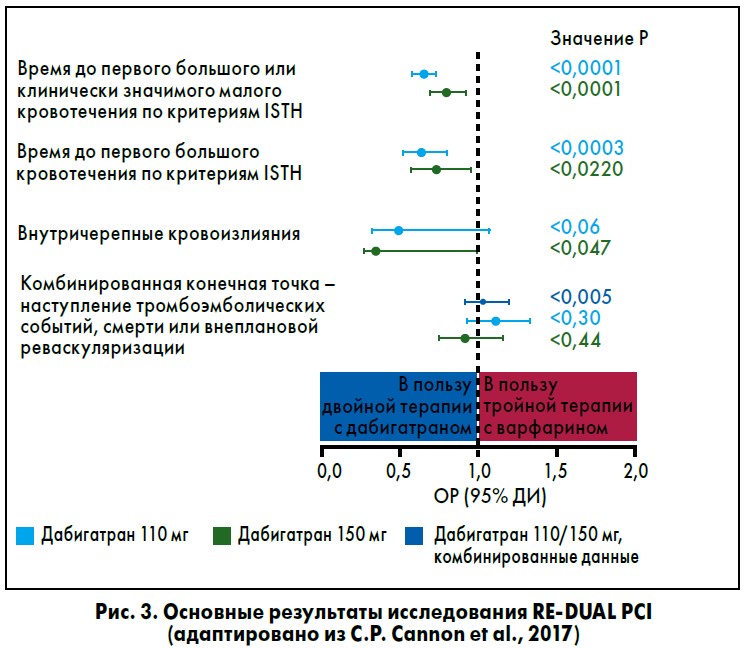
При этом двойная терапия с дабигатраном не уступает тройной терапии с варфарином по эффективности профилактики тромбоэмболических событий. Двойная терапия с дабигатраном в дозах 110 мг 2 р/сут и 150 мг 2 р/сут обеспечивает оптимальный баланс между риском кровотечения и предотвращением тромбоэмболических событий (рис. 3).
 В ходе выступления лектор привел также результаты исследования PIONEER AF-PCI (C.M. Gibson et al., 2016), в котором у пациентов с ФП, подвергавшихся ЧКВ, оценивали эффективность и безопасность терапии другим современным пероральным антикоагулянтом – ривароксабаном, назначавшимся в комбинации с антиагрегантами.
В ходе выступления лектор привел также результаты исследования PIONEER AF-PCI (C.M. Gibson et al., 2016), в котором у пациентов с ФП, подвергавшихся ЧКВ, оценивали эффективность и безопасность терапии другим современным пероральным антикоагулянтом – ривароксабаном, назначавшимся в комбинации с антиагрегантами.
Пациенты были рандомизированы на три группы:
1) терапия ривароксабаном в стандартной низкой дозе 15 мг 1 р/сут + ингибитор P2Y12 (клопидогрель/тикагрелор/прасугрель);
2) ривароксабан в очень низкой дозе 2,5 мг 2 р/сут + ДАТ (АСК 75-100 мг/сут + ингибитор P2Y12);
3) контрольная группа, получавшая стандартную тройную терапию: варфарин + ДАТ. Лечение проводили на протяжении 12 мес; при этом пациенты во второй и третьей группах после 1 или 6 мес терапии оставшийся период до 12 мес получали двойную терапию: ривароксабан 15 мг 1 р/сут + АСК 75-100 мг/сут.
Во всех трех группах получен сходный уровень эффективности, хотя большая ширина ДИ ставит под сомнение данный вывод.
Исследование продемонстрировало меньший риск значимых кровотечений в группах лечения ривароксабаном (как в составе тройной антитромботической терапии в очень низкой дозе, так и в составе двойной терапии в дозе 15 мг) по сравнению с группой, получавшей варфарин + ДАТ.
Обсуждая результаты двух исследований – RE-DUAL PCI и PIONEER AF-PCI, доктор Л. Колтовски отметил, что первое является подтверждающим, а второе – поисковым клиническим исследованием. Так, в исследовании RE-DUAL PCI применяли дозы дабигатрана 110 и 150 мг, для которых ранее доказана эффективность в предотвращении тромбоэмболических осложнений у пациентов с ФП.
В исследовании PIONEER AF-PCI использованы дозы ривароксабана 15/10 мг 1 р/сут и 2,5 мг 2 р/сут. Данные в отношении эффективности этих дозировок для указанной популяции ограничены.
Эффективность дабигатрана в дозах 110 и 150 мг 2 р/сут в предотвращении инсульта была доказана в исследовании RE-LY с участием большого количества пациентов: 6015 участников получали дозу 110 мг 2 р/сут и 6076 пациентов – дозу 150 мг 2 р/сут (S.J. Connolly et al., 2009).
В то же время для ривароксабана 15/10 мг 1 р/сут эффективность в предотвращении инсульта у пациентов с ФП была показана в поисковом исследовании с участием 639 пациентов, проведенном в Японии (M. Hori et al., 2012), но не была доказана для других популяций. Для ривароксабана в очень низкой дозе – 2,5 мг 2 р/сут подобные исследования не проводились вовсе.
Следует отметить также, что в исследовании RE-DUAL PCI продолжительность терапии в каждой группе была заранее определена, а в PIONEER AF-PCI решение о продолжительности тройной терапии, как экспериментальной, так и контрольной, принималось в процессе исследования.
Еще одно важное отличие исследований RE-DUAL PCI и PIONEER AF-PCI – первичные конечные точки, а именно – критерии определения тяжести кровотечений. Если в RE-DUAL PCI использовались четкие критерии ISTH и все исходы были подтверждены независимой комиссией, то в PIONEER AF-PCI анализировались кровотечения с менее жесткими критериями («кровотечения, требующие медицинского вмешательства»), и всего 15% этих событий имели независимое подтверждение.
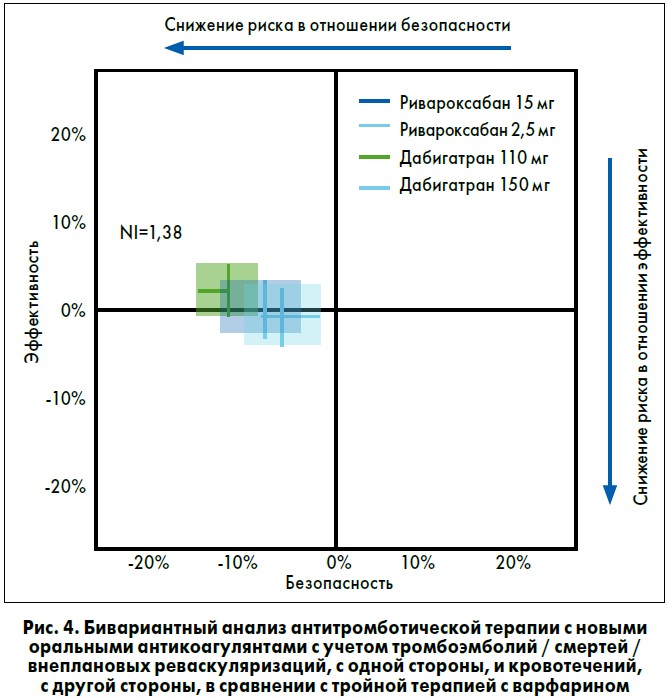 Подводя итоги исследований RE-DUAL PCI и PIONEER AF-PCI, можно обратиться к бивариантному анализу различных схем антитромботической терапии с учетом тромбоэмболий / смертей / внеплановых реваскуляризаций, с одной стороны, и кровотечений – с другой (рис. 4).
Подводя итоги исследований RE-DUAL PCI и PIONEER AF-PCI, можно обратиться к бивариантному анализу различных схем антитромботической терапии с учетом тромбоэмболий / смертей / внеплановых реваскуляризаций, с одной стороны, и кровотечений – с другой (рис. 4).
Очевидно, что применение новых пероральных антикоагулянтов имеет преимущества перед АВК с точки зрения безопасности. При этом выбор дозы дабигатрана 110 или 150 мг позволяет смещать акцент в терапии в сторону безопасности или эффективности в зависимости от индивидуальных рисков пациента с ФП. Например, пожилым людям может быть рекомендован несколько более безопасный вариант – дабигатран в дозе 110 мг 2 р/сут, а молодым с высоким риском инсульта – стандартная дозировка дабигатрана – 150 мг 2 р/сут.
Доктор Л. Колтовски затронул еще одну важную проблему, связанную с антикоагулянтной терапией, – неконтролируемые кровотечения при экстренных хирургических вмешательствах и процедурах, в жизнеугрожающих ситуациях, когда остро стоит вопрос быстрой нейтрализации действия антикоагулянта. В случаях, если используется дабигатран, у этой проблемы есть решение, поскольку для этого препарата уже найден специфический антидот, который зарегистрирован и в Украине, – идаруцизумаб (Праксбайнд), представляющий собой фрагмент моноклонального антитела.
В многоцентровом проспективном открытом исследовании RE-VERSE AD (C.V. Pollack et al., 2017), в котором приняли участие 503 пациента с ФП из 39 стран, получающие дабигатран, оценивали эффективность идаруцизумаба в дозе 5 г внутривенно (2×2,5 г, 50 мл) в отношении нейтрализации антикоагулянтного эффекта дабигатрана.
В исследовании у пациентов группы А диагностировали неконтролируемые кровотечения; пациенты группы В нуждались в неотложных хирургических процедурах. Установлено, что почти у 98% пациентов регистрировали быструю и полную отмену действия дабигатрана, что подтверждалось результатами измерения разведеного тромбинового времени (рТВ). Эффект идаруцизумаба оценивали, анализируя динамику показателей тромбинового времени в разведенной плазме (dTT) и экаринового времени свертывания (ECT).
В группе А медианное время прекращения кровотечений составило 2,5 ч; в группе В медианное время до начала необходимой хирургической процедуры составило 1,6 ч. На протяжении 90 дней после введения идаруцизумаба тромботические события зарегистрированы у 6,3% пациентов группы А и в 7,4% случаев в группе В. Серьезных побочных эффектов при использовании идаруцизумаба отмечено не было. Через 72 ч после введения идаруцизумаба 22,9% пациентов группы А и 66,8% – группы В возобновили прием антитромботической терапии. Через 90 дней ее получали уже 72,8% больных группы А и 90,1% – группы В.
Подводя итог, следует отметить, что для пациентов с ФП, перенесших ЧКВ, характерен высокий риск развития сердечно-сосудистых событий и кровотечений. Современные протоколы рекомендуют индивидуальный подход к выбору двойной или тройной антитромботической терапии на основании оценки относительных рисков кровотечений и тромбоэмболических событий для каждого пациента. При этом следует учесть, что двойная терапия с использованием современных пероральных антикоагулянтов не уступает по эффективности в профилактике тромбоэмболических событий тройной терапии, включающей варфарин; однако первый подход позволяет повысить безопасность лечения.
Подготовила Екатерина Ткаченко
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (58) червень 2018 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....




