Інгібітори mTOR як засіб для подолання резистентності до ендокринної терапії у пацієнток з ЕR+/HER2- раком молочної залози
Гормональна терапія є основою у лікуванні пацієнток з гормон-рецепторпозитивним (HR+) поширеним раком молочної залози (РМЗ). У жінок у постменопаузі перша лінія терапії представлена інгібіторами ароматази (ІА). Однак не у всіх пацієнток отримується відповідь на початкову ендокринну терапію (первинна резистентність), а у жінок, у яких досягнута відповідь на першу лінію терапії, з часом відбувається рецидив і формується вторинна резистентність до лікування. Ефективним методом подолання ендокринної резистентності є застосування інгібіторів білка mTOR.
 У рамках міжнародного онлайн-конгресу UPTODATE IN ONCOLOGY 2020 – АКТУАЛЬНЕ В ОНКОЛОГІЇ 2020 експерт Міністерства охорони здоров’я України за спеціальністю «Онкологія», завідувач кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктор медичних наук, професор Олексій Олексійович Ковальов представив доповідь «Інгібітори mTOR як спосіб подолання ендокринної резистентності у хворих з ЕR+/HER2- раком молочної залози».
У рамках міжнародного онлайн-конгресу UPTODATE IN ONCOLOGY 2020 – АКТУАЛЬНЕ В ОНКОЛОГІЇ 2020 експерт Міністерства охорони здоров’я України за спеціальністю «Онкологія», завідувач кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктор медичних наук, професор Олексій Олексійович Ковальов представив доповідь «Інгібітори mTOR як спосіб подолання ендокринної резистентності у хворих з ЕR+/HER2- раком молочної залози».
– За даними Globocan 2020, за останній рік було зареєстровано загалом 9,2 млн нових випадків раку та 4,4 млн випадків смерті від онкологічного захворювання у жінок. У структурі онкологічної захворюваності у жінок домінує РМЗ – 2 261 419 (24,5%) випадків. Згідно з оновленим Бюлетенем № 21 Національного канцер-реєстру України, протягом 2018 р. у жінок було зареєстровано 14 872 випадки РМЗ, а 5679 осіб померли від цього захворювання. Здебільшого розвивається РМЗ люмінального типу, при якому експресуються естрогенові рецептори (ER+).
Люмінальний РМЗ характеризується молекулярною гетерогенністю. Зокрема, люмінальний РМЗ типу А (ER+/HER2-) включає понад 10 молекулярних підтипів: GATA3, LIV1, EMP2, Mucin1, CCND1, XBP1, HMGCL, CROT, Keratin aMa, DECR2, AR, TFF1. Виділяють низку причин первинної резистентності гормоночутливих пухлин: порушення метаболізму естрогену, низький рівень ендоксифену, модифікація стероїдних рецепторів, порушення процесу фосфорилювання та низька експресія ER, активація альтернативних мітогенних шляхів, висока експресія EGFR та HER2-протеїну, активація сигнального шляху mTOR, розлад метаболізму, епігенетичні механізми, ацетилювання гістонів і метилювання ДНК, порушення регуляції клітинного циклу, ампліфікація CCND1, низька експресія р27kip1, висока експресія НОХВ13. Слід зазначити, що завдяки ауто- та паракринній регуляції може відбуватися проліферація клітин навіть у разі пригнічення ER. У таких ситуаціях саме активація шляху mTOR може бути причиною первинної резистентності до ендокринної терапії. Цікаво, що відкриття інгібітора mTOR передувало виявленню самого протеїну: канадський вчений Suren N. Sehgal (1932-2003 рр.) на острові Пасхи виявив мікроорганізм Streptomyces hygroscopicus, який став основою для створення лікарського засобу рапаміцин (від місцевої назви острова Rapa Nui). Відкриття молекули mTOR належить американському науковцю Michael N. Hail.
Під час пошуку шляхів подолання резистентності РМЗ до ендокринної терапії вивчали різні схеми й стратегії терапії: збільшення дози препарату, комбінація двох ендокринних препаратів, комбінація ендокринного препарату та анти-HER2 терапії, комбінація ендокринного препарату та анти-mTOR терапії. Найкращі результати було отримано у рандомізованому дослідженні III фази BOLERO II, у якому застосування еверолімусу забезпечило позитивний вплив на виживаність пацієнток з ER+/HER2- поширеним РМЗ.
Критеріями включення у дослідження BOLERO II були постменопаузальний статус пацієнток, наявність поширеного ER+/HER2- РМЗ, рефрактерність до терапії летрозолом та анастрозолом (рецидив протягом 1-12 міс після закінчення ад’ювантної терапії). Усі пацієнтки (n=724) були розподілені на 2 групи у співвідношенні 2:1. Учасниці основної групи (n=485) отримували еверолімус (10 мг/добу) та екземестан (25 мг/добу), контрольної групи (n=239) – плацебо та екземестан (25 мг/добу). Через 18 міс спостереження отримано значно довшу виживаність без прогресування (ВБП) в основній групі, ніж у контрольній: 7,8 та 3,2 міс відповідно (відношення ризиків – ВР – 0,45; 95% довірчий інтервал – ДІ – 0,38-0,54; рис. 1). Раннє призначення еверолімусу уже після першого прогресування хвороби дозволило продовжити ВБП пацієнток до 15,24 міс, тоді як медіана ВБП у групі монотерапії екземестаном склала 4,21 міс (рис. 2). Підгруповий аналіз показав, що комбінація еверолімус + екземестан ефективна у пацієнток з/без вісцеральних метастазів і з метастазами в кістках (J. Baselga et al., 2012; D.A. Yardley et al., 2013; G.N. Hortobagyi et al., 2016).
 Рис. 1. Медіана ВБП у дослідженні BOLERO II
Рис. 1. Медіана ВБП у дослідженні BOLERO II
 Рис. 2. Результати раннього призначення еверолімусу після першого прогресування хвороби (J.T. Beck et al., 2014)
Рис. 2. Результати раннього призначення еверолімусу після першого прогресування хвороби (J.T. Beck et al., 2014)
У дослідженні BOLERO II зроблено такі висновки: застосування еверолімусу дозволяє ефективно подолати ендокринорезистентність; визначена оптимальна послідовність ендокринної терапії після прогресування хвороби; еверолімус не є препаратом для «терапії відчаю». Ці відкриття стали підставою для перегляду клінічних настанов провідними міжнародними спільнотами (NCCN, 2018; ASCO, 2019; ESO-ESMO, ABC‑3), які опублікували рекомендації щодо секвенсинг-терапії. Так, призначення еверолімусу на фоні прогресування хвороби після першої лінії терапії є найкращим методом ескалації.
Згідно з останніми настановами NCCN (версія 5.2020), у другій лінії терапії рекомендовано застосування комбінації еверолімусу з екземестаном або фулвестрантом, або тамоксифеном у пацієнток із метастатичним ER+ РМЗ. Застосування цих трьох комбінацій забезпечує значно вищу медіану ВБП порівняно з монотерапією ендокринним препаратом: екземестан ± еверолімус – 7,8 та 3,2 міс; фулвестрант ± еверолімус – 10,3 та 5,1 міс, тамоксифен ± еверолімус – 8,5 та 4,5 міс (N. Kornblum et al., 2019; D.A. Yardley et al., 2013; T. Bachelot et al., 2012).
Еверолімус пригнічує сигнальний шлях mTORC1, але не mTORC2. Для оцінювання потенціалу подвійного інгібітора mTORC1 та mTORC2 вістусертибу, який продемонстрував активність на моделі РМЗ у доклінічному дослідженні, було ініційовано рандомізоване клінічне дослідження II фази MANTA. 333 пацієнтки з ER+ РМЗ, у яких хвороба прогресувала після першої лінії терапії, було розподілено на 4 групи: 1-ша група (n=67) як терапію другої лінії отримувала лише фулвестрант, 2-га група (n=103) – фулвестрант + вістусертиб (щодня), 3-тя група (n=98) – фулвестрант + вістусертиб (2 дні терапії з 5-денною перервою), 4-та група (n=65) – фулвестрант + еверолімус. Результати дослідження не виправдали очікувань позитивного ефекту вістусертибу. Медіана ВБП в усіх групах склала 5,4 міс (95% ДІ 3,5-9,2), 7,6 міс (95% ДІ 5,9-9,4), 8,0 міс (95% ДІ 5,6-9,9) та 12,3 міс (95% ДІ 7,7-15,7) відповідно за порядком (P. Schmid et al., 2019; рис. 3).
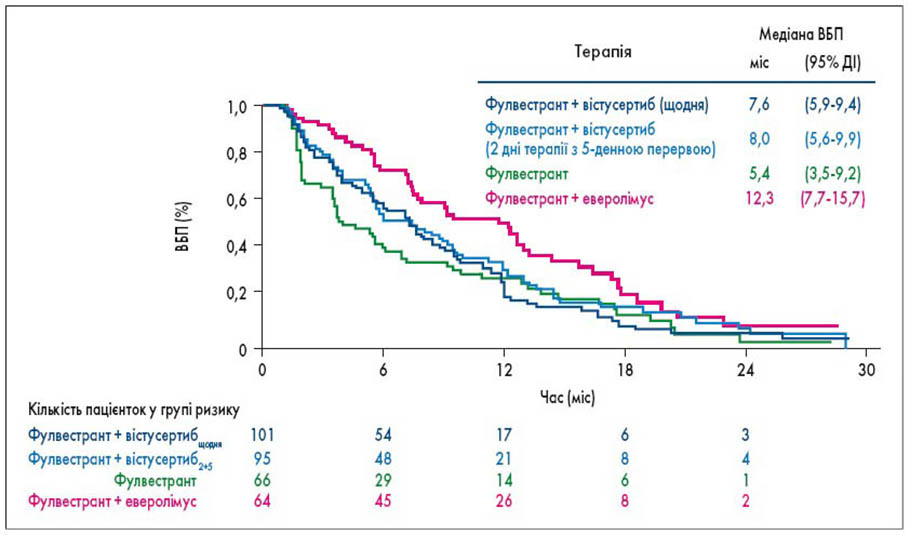 Рис. 3. Медіана ВБП у дослідженні MANTA
Рис. 3. Медіана ВБП у дослідженні MANTA
При порівнянні токсичності гормональної терапії, хіміотерапії та комбінованої терапії (гормональний препарат + хіміотерапія) перший варіант лікування рідше викликає побічні ефекти. Монорежим хіміотерапії не є методом вибору у пацієнток із метастатичним РМЗ (рис. 4). Що стосується комбінованої терапії, то у дослідженні BOLERO II найчастішим побічним явищем 3-4 ступеня, асоційованим із застосуванням еверолімусу й екземестану, був стоматит (8%; J. Baselga et al., 2012). Однак у ході метааналізу досліджень, у яких вивчали ефективність і безпеку еверолімусу у пацієнтів із солідними пухлинами різної локалізації (дослідження BOLERO‑2, BOLERO‑3, RECORD‑1, RADIANT‑2, RADIANT3, EXIST‑1 та EXIST‑2), виявили позитивний кореляційний зв’язок між розвитком токсичності та виживаністю хворих. У пацієнтів, у яких розвинувся стоматит протягом 8 тижнів лікування еверолімусом, медіана ВБП була вищою, ніж у пацієнтів без стоматиту. Зокрема, у дослідженні BOLERO‑2 медіана ВБП у пацієнток зі стоматитом та без нього становила 8,5 та 6,9 міс (H.S. Rugo et al., 2016).
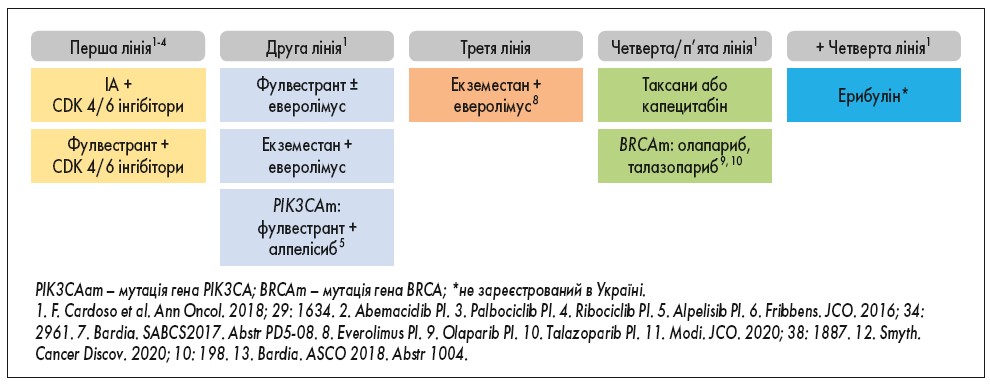 Рис. 4. Алгоритм лікування ER+ метастатичного РМЗ
Рис. 4. Алгоритм лікування ER+ метастатичного РМЗ
Отже, застосування еверолімусу у другій лінії терапії при поширеному ER+ РМЗ дозволяє протидіяти резистентності до ендокринної терапії, що підтверджено результатами рандомізованих клінічних досліджень.
Підготувала Ілона Цюпа
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 1 (68) 2021 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




