Молнупіравір у лікуванні COVID-19: новини з конгресу ECCMID 2022
23-26 квітня в Лісабоні (Португалія) в гібридному форматі – онлайн і наживо – відбувся 32-й Європейський конгрес із клінічної мікробіології та інфекційних хвороб (ECCMID), який залучив понад 14 тис. учасників з усього світу. Як і торік, велика частина наукової програми була присвячена коронавірусній хворобі (COVID-19).
Молнупіравір – інноваційний пероральний противірусний препарат із широкою активністю проти коронавірусів, включно із SARS-CoV‑2. Рандомізоване плацебо-контрольоване дослідження MOVe-OUT, опубліковане в лютому 2022 р., підтвердило перевагу молнупіравіру над плацебо в амбулаторних дорослих пацієнтів із COVID‑19 легкого та середнього ступеня тяжкості за умови, якщо лікування починали в межах 5 днів від появи симптомів [1, 2]. На підставі цих результатів препарат уже схвалений Управлінням із контролю якості продуктів харчування та лікарських засобів США (FDA) за механізмом EAU (emergency use authorization – дозвіл на екстрене використання), а також зареєстрований у 12 інших країнах, включно з Україною. На конгресі ECCMID 2022 фармацевтична компанія MSD представила нові дані дослідження MOVe-OUT.
Нові вірусологічні дані: молнупіравір ефективно усуває SARS-CoV‑2 вже на 3-й день лікування [3]
Вірусне навантаження – це кількість копій вірусу в крові або іншій біологічній рідині. У разі COVID‑19 високе вірусне навантаження призводить до тяжчих симптомів і може збільшувати ймовірність передачі інфекції іншим особам.
У дослідженні MOVe-OUT для визначення ступеня вірусного навантаження використовували ПЛР‑тестування мазків із носоглотки на 1-й день (до лікування), 3-й, 5-й (останній день лікування), 10-й, 15-й і 20-й дні. В аналіз включили дані пацієнтів, для котрих були наявні зразки для визначення РНК SARS-CoV‑2 до та після лікування (n=92 у групі молнупіравіру, n=96 у групі плацебо).
Результати показали, що на 3-й день терапії SARS-CoV‑2 не визначався в жодного з 92 пацієнтів групи молнупіравіру, натомість у групі плацебо вірусне навантаження буле присутнє у 21,8% (n=20/96) хворих. На 5-й день вірус визначався в 0,0% (n=0/91) та 2,2% (n=2/89) учасників у групах молнупіравіру та плацебо відповідно.
Як зазначила головна науковиця MSD, професорка Джулі Стрізкі, цей аналіз фінальних вірусологічних даних дослідження MOVe-OUT підтверджує попередні спостереження про те, що 5-денний курс молнупіравіру 800 мг 2 р/день забезпечує швидші зниження вірусної РНК та елімінацію інфекційного вірусу порівняно з плацебо. Отже, аналіз надав додаткові докази, що молнупіравір допомагає швидше позбутися SARS-CoV‑2, і підтримує основні результаті MOVe-OUT щодо здатності препарату знижувати ризик прогресування до тяжкої COVID‑19.
Вплив молнупіравіру на суб’єктивні симптоми COVID‑19 [4]
Однією з ключових вторинних кінцевих точок у дослідженні MOVe-OUT була вираженість симптомів COVID‑19 за безпосередньою оцінкою пацієнтів. Починаючи з 1-го дня (рандомізація) й до 29-го дня пацієнти вели щоденник, в якому оцінювали тяжкість кожного з 15 симптомів за такою шкалою: «симптом відсутній», «легкий», «помірний» або «тяжкий» (окрім втрати нюху та смаку, для котрих зазначали «так» чи «ні»).
Для кожного симптому час до стійкого зникнення або полегшення визначали як кількість днів від рандомізації до першого з трьох послідовних днів зменшеної тяжкості (без наступного погіршення до 29-го дня спостереження), час до прогресування – як кількість днів від рандомізації до першого з двох послідовних днів погіршення.
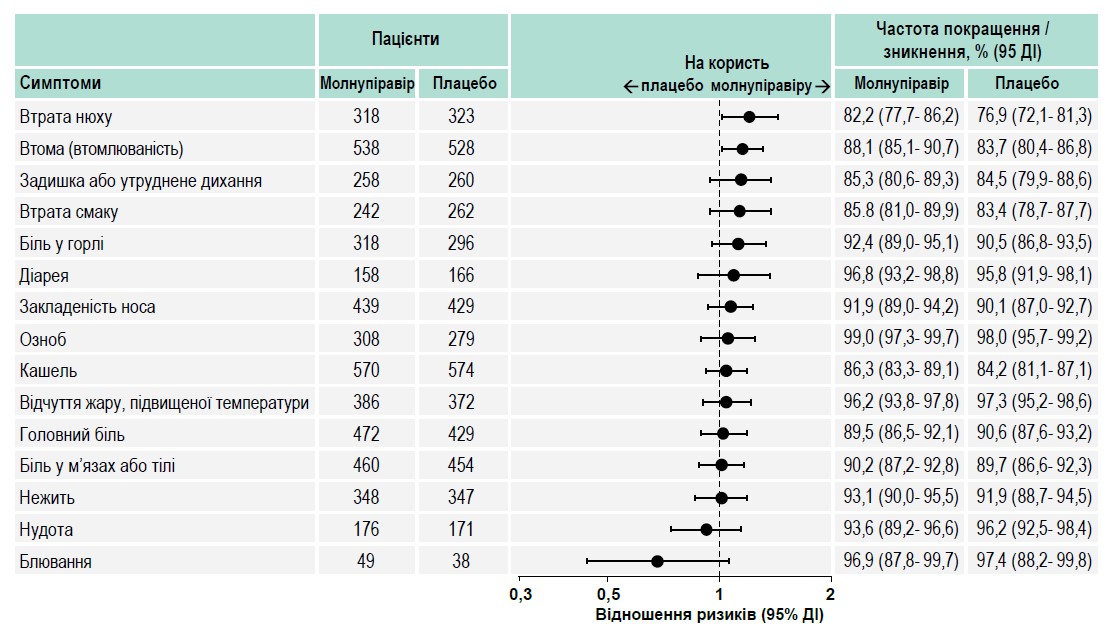
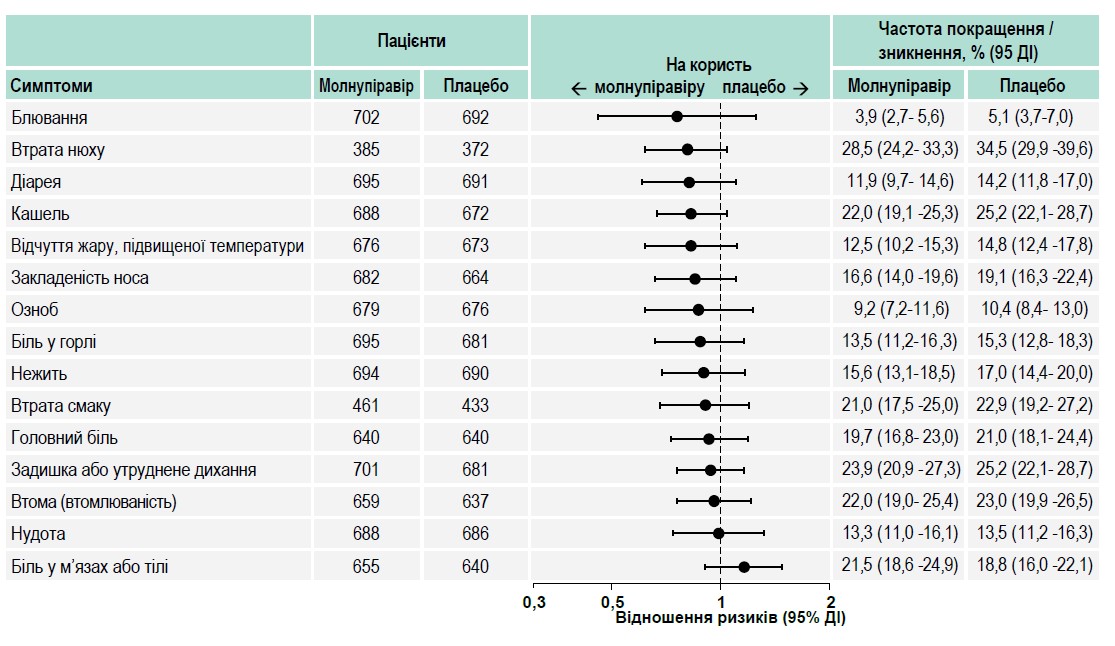
Прихильність пацієнтів до ведення щоденника була високою: >92% учасників в обох групах робили записи впродовж усіх 29 днів. Для більшості симптомів COVID‑19 стійке полегшення або повне зникнення спостерігали з більшою ймовірністю в групі молнупіравіру порівняно з групою плацебо (рис. 1). Так само для більшості симптомів захворювання погіршення було менш імовірним при лікуванні молнупіравіром (рис. 2).
Рис. 1. Час до стійкого покращення / зникнення симптомів до 29-го дня
Рис. 2. Час до погіршення симптомів до 29-го дня
Під час оцінювання окремих симптомів, які часто асоціюються з COVID‑19, включно із задишкою або утрудненим диханням, кашлем, утомою (втомлюваністю), втратою нюху та смаку, було встановлено, що пацієнти групи молнупіравіру значно частіше повідомляли про стійке покращення або повне зникнення цих симптомів на 3-й, 5-й (останній день лікування) та 10-й день.
Середній час до покращення / зникнення симптомів (95% довірчий інтервал – ДІ) для молнупіравіру vs плацебо був таким: задишка чи утруднене дихання – 6 (6-8) vs 9 (6-10) днів, кашель – 10 (9-11) vs 10 (8-11) днів, утома (втомлюваність) – 6 (6-7) vs 7 (6-8) днів, втрата нюху – 10 (9-11) vs 11 (9-14) днів, втрата смаку – 9 (8-10) vs 10 (8-12) днів. Для цих характерних для COVID‑19 симптомів прогресування до тяжкого перебігу також було менш імовірним у пацієнтів групи молнупіравіру на 3-й, 5-й і 10-й дні.
Отже, лікування молнупіравіром порівняно з плацебо забезпечило покращення – зменшення вираженості або повне зникнення – більшості суб’єктивних симптомів COVID‑19.
Результати застосування молнупіравіру в імуноскомпрометованих хворих на COVID‑19 [5]
На сьогодні відомо, що імуноскомпрометовані пацієнти мають вищий ризик прогресування до тяжкої COVID‑19 і гірший прогноз одужання. Крім того, такі хворі можуть довше виділяти вірус порівняно з пацієнтами з нормальним імунітетом. Чинниками імуносупресії, які можуть негативно впливати на перебіг COVID‑19 і затримувати кліренс вірусу, є вміст CD4+ T‑лімфоцитів <200 клітин/мм3, тип злоякісного новоутворення, час від трансплантації, тип трансплантату, а також тип та/або доза хіміотерапії, імунотерапії чи імуносупресивної терапії.
У post hoc аналізі дослідження MOVe-OUT порівняли вірусологічні дані, клінічну ефективність і безпеку терапії в імуноскомпрометованих осіб і пацієнтів із нормальним імунітетом.
Імуноскомпрометовані особи становили 4% від загальної популяції дослідження (57/1408). Стани, які призвели до зниження імунітету, включали активний рак, вірус імунодефіциту людини, імуносупресивну терапію (азатіоприн, голімумаб, метотрексат, такролімус тощо), попередню системну терапію глюкокортикоїдами, а також трансплантацію (кісткового мозку, серця, печінки). Серед імуноскомпрометованих осіб було більше жінок і пацієнтів без ожиріння.
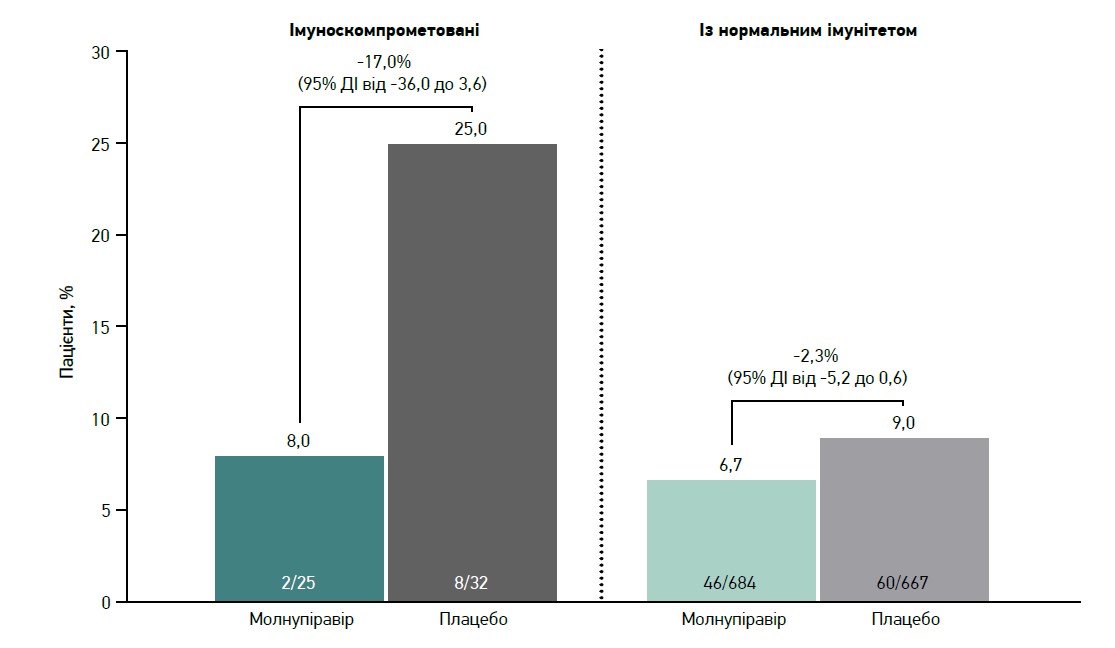
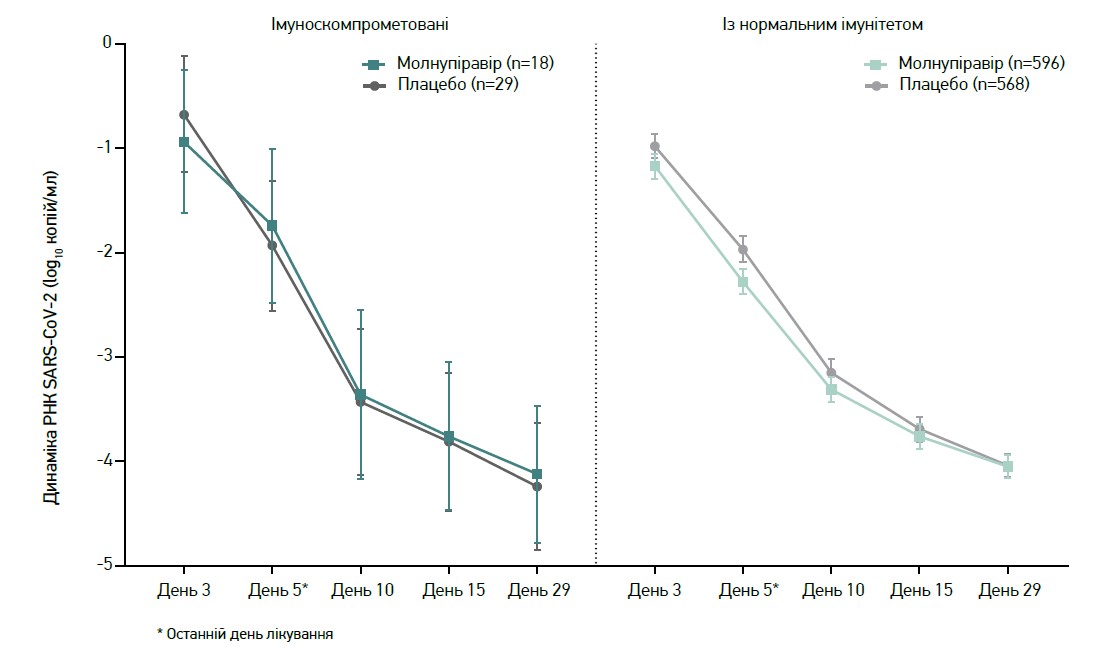
Як показали результати аналізу, імуноскомпрометованих осіб, які були госпіталізовані або померли до 29-го дня, було менше в групі молнупіравіру порівняно з групою плацебо (рис. 3). Середня зміна РНК SARS-CoV‑2 загалом була подібною в імуноскомпрометованих осіб і в пацієнтів із непорушеною імунною функцією (рис. 4).
Рис. 3. Частота госпіталізації або смерті до 29-го дня залежно від стану імунітету
Рис. 4. Динаміка середніх показників РНК SARS-CoV-2
Серед учасників, у яких інфекційний вірус визначався до початку лікування, в групі молнупіравіру не було жодного пацієнта (імуноскомпрометованого чи з нормальним імунітетом), у котрого вірус визначався би в будь-якому з наступних візитів.
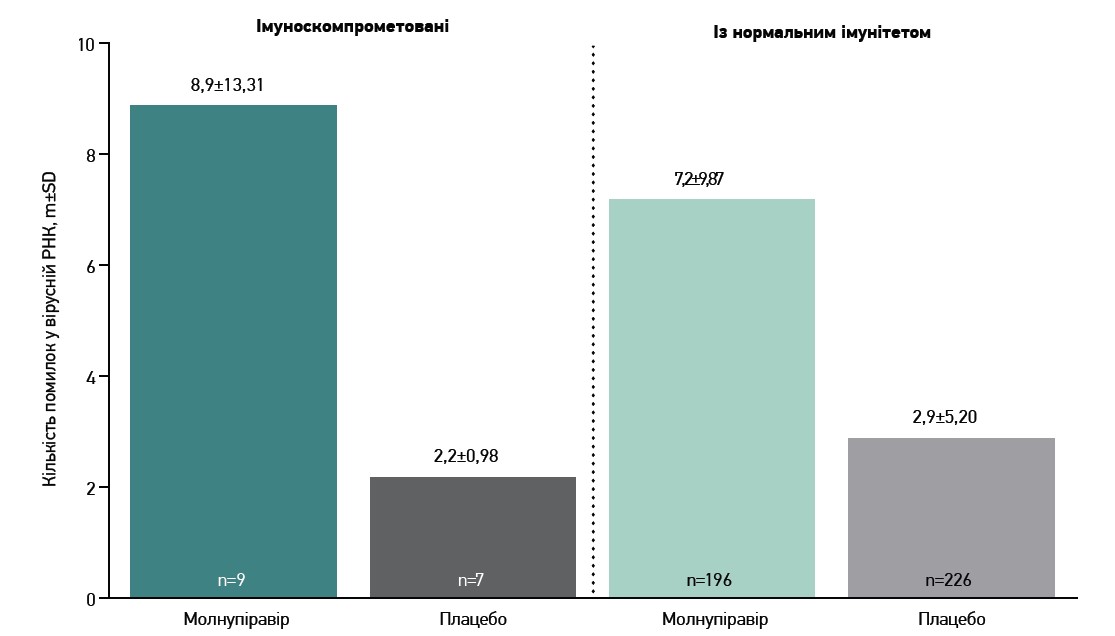
Відносне підвищення помилок у вірусних нуклеотидах на 5-й день загалом не залежало від стану імунітету (рис. 5). Серед викликаних лікуванням замін, ідентифікованих у вірусному реплікаційному комплексі та шиповому білку, в групі молнупіравіру жодна локація білка не була унікальною для імуноскомпрометованих осіб порівняно з пацієнтами з нормальним імунітетом. Окрім того, в імуноскомпрометованих учасників не відзначено замін білків вірусної реплікази NSP‑7, -8, -9 і -10.
Рис. 5. Частота помилок у РНК SARS-CoV-2 на 5-й день
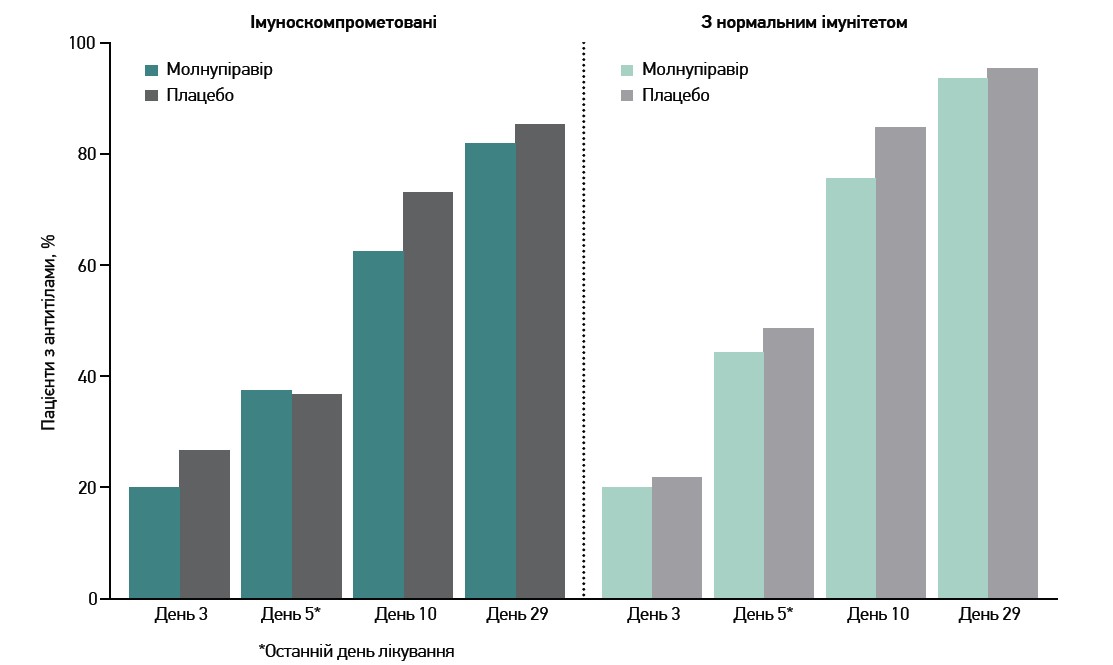
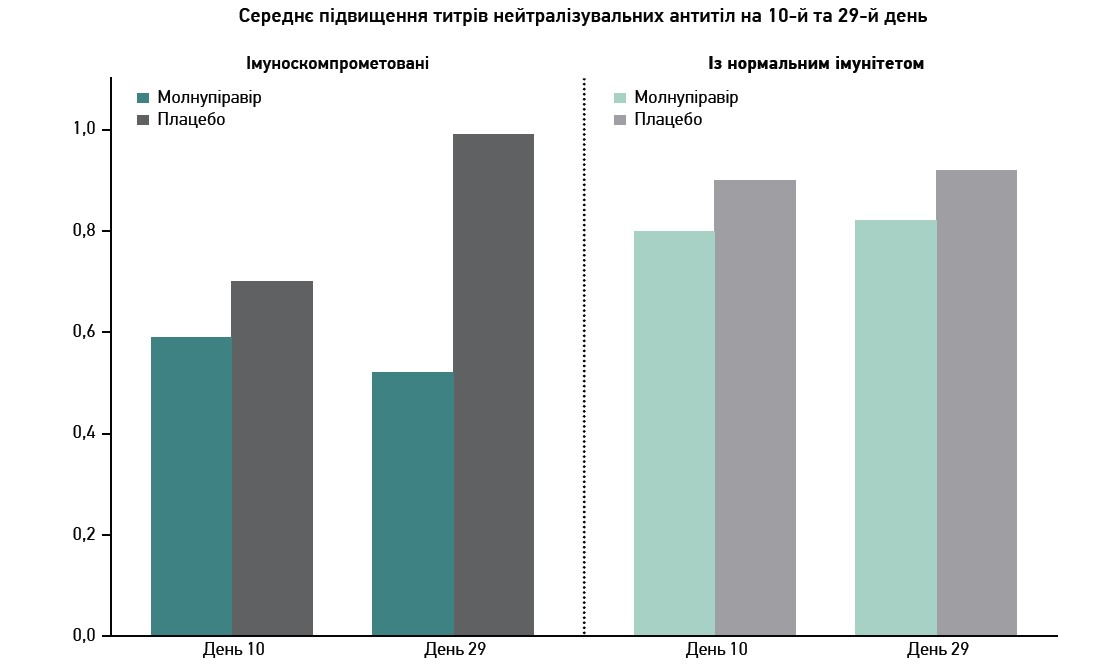
Позитивність за антитілами проти нуклеокапсидного білка SARS-CoV‑2 була загалом схожою в імуноскомпрометованих і нескомпрометованих пацієнтів (рис. 6), так само як і середні зміни титрів нейтралізувальних антитіл на 10-й день (рис. 7).
Рис. 6. Динаміка позитивності за антитілами до нуклеокапсидного білка SARS-CoV-2
Рис. 7. Середнє підвищення титрів нейтралізувальних антитіл на 10-й і 29-й дні
Імуноскомпрометовані пацієнти добре переносили лікування молнупіравіром, частота небажаних подій, зокрема серйозних, у цій популяції була нижчою в групі молнупіравіру порівняно з групою плацебо.
Тобто в пацієнтів зі зниженим імунітетом молнупіравір добре переносився та забезпечував зниження частоти госпіталізації з будь-яких причин або смерті впродовж 29 днів спостереження порівняно з плацебо. Вірусологічні результати від імунного статусу загалом не залежали.
Вплив молнупіравіру на геном SARS-CoV‑2 за даними секвенування нового покоління [6]
Щоби краще вивчити механізм дії молнупіравіру, в дослідженні MOVe-OUT використали секвенування нового покоління (NGS). Спочатку в мазках із носоглотки за допомогою ПЛР зі зворотною транскриптазою кількісно визначали РНК SARS-CoV‑2. Зразки, які містили >600 копій/мл, піддавали повногеномному NGS із застосуванням панелі праймерів Ion AmpliSeq SARS-CoV‑2 на секвенаторі Ion Torrent (Thermo Fisher Scientific, США). Для ідентифікації змін послідовностей РНК SARS-CoV‑2 у групах молнупіравіру та плацебо порівняли вірусні послідовності в зразках, отриманих на 1-й, 5-й, 10-й, 15-й та/або 29-й день.
Дані секвенування були наявні для 445 й 438 пацієнтів до початку лікування та 274 й 307 учасників на 5-й день (останній день лікування) в групах молнупіравіру та плацебо відповідно.
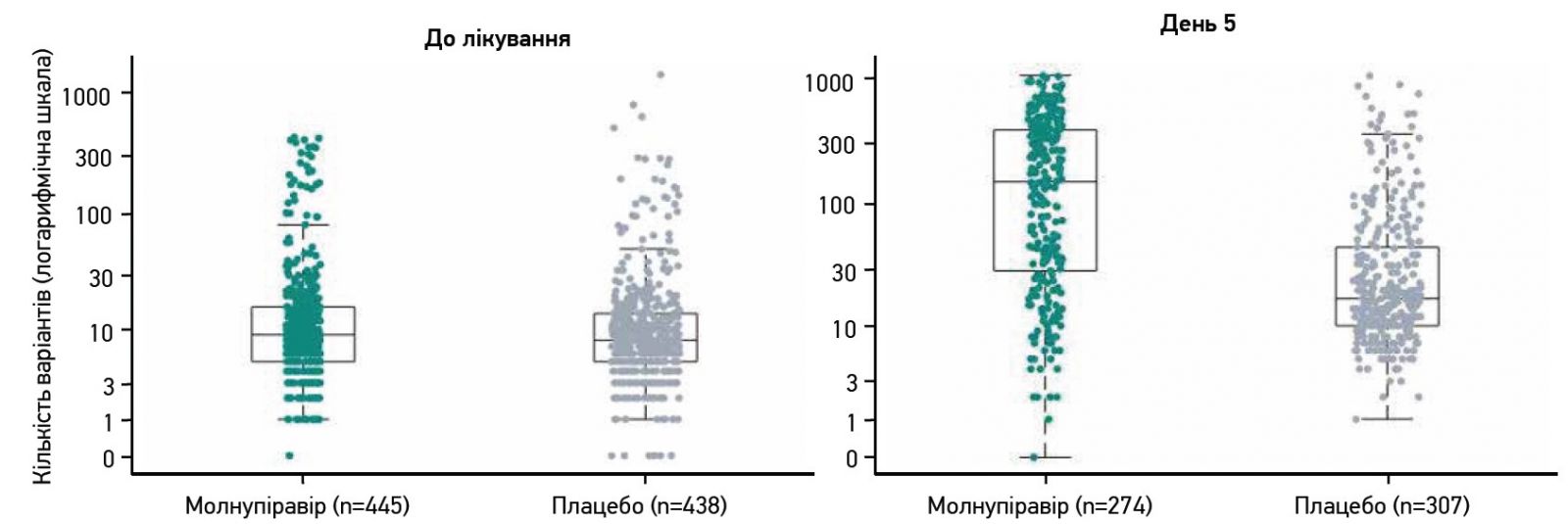
Згідно з механізмом дії препарату, лікування молнупіравіром асоціювалося з вищою частотою низькочастотних помилок у вірусній РНК на 5-й день порівняно з плацебо (рис. 8). Ці зміни були випадковим чином розподілені по всьому геному SARS-CoV‑2.
Рис. 8. Кількість варіантів SARS-CoV-2, визначених до початку та на 5-й (останній) день лікування
Найчастішими нуклеотидними змінами були транзиції (наприклад, С ↔ U, G ↔ A), тоді як трансверсії (як-от G ↔ U, A ↔ U, C ↔ A, C ↔ G) загалом траплялися рідко в обох групах.
Серед транзиційних помилок у групі молнупіравіру транзиції C → A та G → A (середня кількість змін 6,6 та 4,2 відповідно) визначалися частіше, ніж U → C й A → G (1,9 та 1,7 відповідно), що узгоджується з відомим механізмом дії молнупіравіру.
На тлі лікування зміни амінокислот у вірусному реплікаційному комплексі (NSP‑12, NSP‑13, NSP‑14) спостерігалися нечасто. Зміни амінокислот шипового (S) білка реєстрували частіше, проте в жодного пацієнта групи молнупіравіру на 5-й день лікування інфекційний вірус не визначався. Також варто зазначити, що жодний учасник дослідження не був інфікований варіантом SARS-CoV‑2 омікрон.
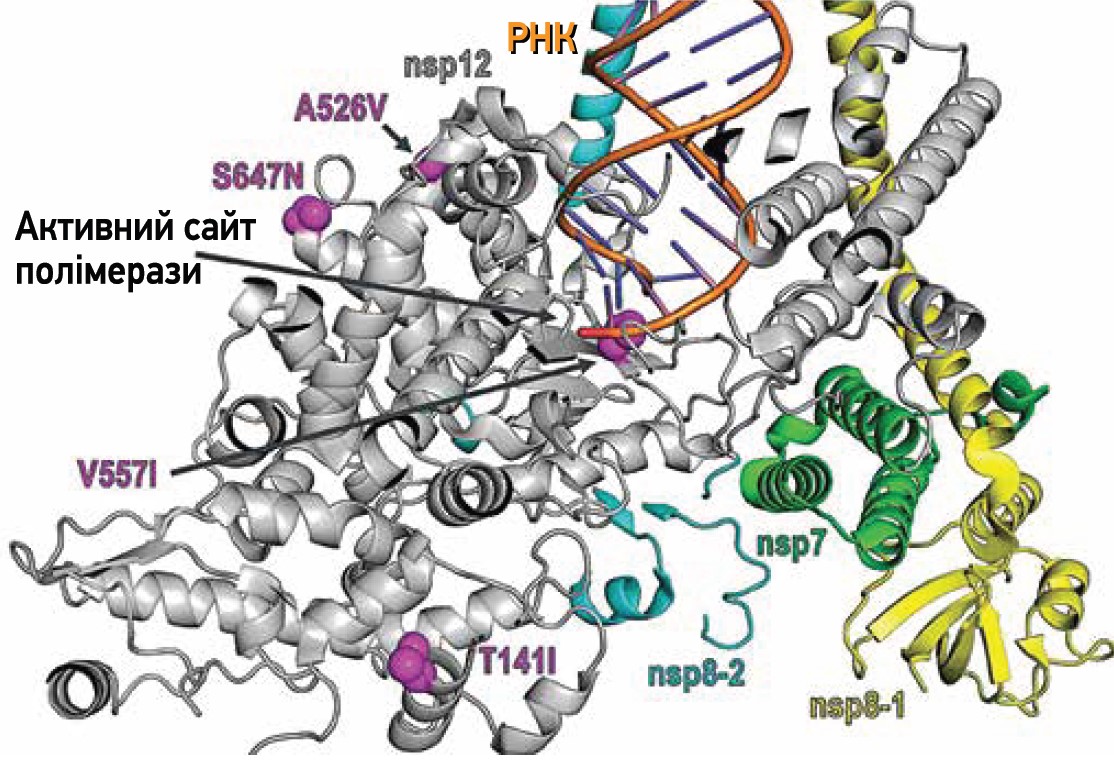
Серед амінокислотних змін у вірусній РНК‑полімеразі NSP‑12 заміни A526V, S647N, T141I та V557I спостерігалися тільки в групі молнупіравіру (рис. 9). Із них лише V557I розташована близько до активного сайту ферменту; як було продемонстровано раніше, схожа заміна (V557L) не впливала на чутливість SARS-CoV‑2 до молнупіравіру.
Рис. 9. Розташування змін амінокислот у NSP-12 реплікаційного комплексу SARS-CoV-2, які виникли тільки на тлі лікування молнупіравіром
Отже, в дослідженні MOVe-OUT лікування молнупіравіром було пов’язано з вищим рівнем помилок у геномі SARS-CoV‑2 порівняно з плацебо. Відповідно до механізму дії препарату та доклінічних даних, молнупіравір специфічно асоціюється зі збільшенням транзицій.
Література
1. Bernal A. J., Gomes da Silva M. M., Musungaie D. B., et al. Molnupiravir for oral treatment of COVID‑19 in nonhospitalized patients. N. Engl. J. Med. 2022 Feb 10; 386 (6): 509-520.
2. Берналь A. Й., Гомес да Сільва М. М., Мусунгайе Д. Б. та ін. Молнупіравір для перорального лікування амбулаторних пацієнтів із COVID‑19. Медична газета «Здоров’я України 21 сторіччя», № 3 (520), 2022 р.
3. New virology data shows the investigational COVID antiviral drug molnupiravir eliminates actively infectious SARS-CoV‑2 virus by day 3 of starting therapy. Press release based on late breaker abstract 4514 at the 32nd European Congress of Clinical Microbiology & Infectious Diseases (ECCMID) Annual Meeting (Lisbon, 23-26 April 2022).
4. 32nd European Congress of Clinical Microbiology & Infectious Diseases (ECCMID) Annual Meeting (Lisbon, 23-26 April 2022). Abstract #4548: Impact of molnupiravir treatment on patient-reported COVID‑19 symptoms in the MOVe-OUT study. Y. Guan.
5. 32nd European Congress of Clinical Microbiology & Infectious Diseases (ECCMID) Annual Meeting (Lisbon, 23-26 April 2022). Abstract #4545: Molnupiravir for the treatment of COVID‑19 in immunocompromised patients: efficacy, safety, and virology results from the phase 3 MOVe-OUT trial. M. Johnson.
6. 32nd European Congress of Clinical Microbiology & Infectious Diseases (ECCMID) Annual Meeting (Lisbon, 23-26 April 2022). Abstract #4865: Effects of molnupiravir on the SARS-CoV‑2 genome: next-generation sequencing data from the MOVe-OUT phase 3 trial. J. Strizki.
Офіційний сайт конгресу: www.eccmid.org
Підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 4 (521), 2022 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Серед препаратів, які мають велику доказову базу щодо лікування пацієнтів із захворюваннями дихальних шляхів з алергічним компонентом, особливий інтерес становлять антагоністи лейкотрієнових рецепторів (АЛТР). Ці препарати мають хорошу переносимість у дорослих та дітей, а також, на відміну від інгаляційних кортикостероїдів (ІКС), характеризуються високим комплаєнсом, тому посідають чільне місце в лікуванні пацієнтів із респіраторною патологією. У лютому відбувся міждисциплінарний конгрес із міжнародною участю «Життя без алергії International» за участю провідних вітчизняних міжнародних експертів. Слово мав президент Асоціації алергологів України, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Зайков із доповіддю «Місце АЛТР у лікуванні пацієнтів із респіраторною патологією». ...
Розбір клінічного випадку...