У пациентов с хронической болезнью почек, не находящихся на диализе, препарат Мирцера®, назначаемый 1 раз в месяц, корригирует и поддерживает стабильными уровни гемоглобина: результаты исследования MICENAS II
Анемия – частое осложнение хронической болезни почек (ХБП), основной причиной которого является дефицит эритропоэтина.
Терапия эритропоэзстимулирующими агентами (ЭСА) у пациентов с ХБП и анемией повышает уровни гемоглобина, уменьшает потребность в переливаниях крови, улучшает качество жизни и способствует регрессу гипертрофии левого желудочка.
ЭСА отличаются высокой эффективностью в ведении анемии почечного происхождения, тем не менее при использовании этих препаратов остается ряд нерешенных вопросов, таких как целевой уровень гемоглобина. В Европейском руководстве по оптимальному ведению заболеваний почек (ERBP, 2009 г.) у пациентов с ХБП целевой диапазон гемоглобина составляет 110-120 г/л, при этом указывается, что он должен быть индивидуализированным с учетом возраста и сопутствующих заболеваний пациента. В то же время публикация результатов исследований CHOIR, CREATE и TREAT вызвала обеспокоенность относительно безопасности более высоких целевых уровней гемоглобина у пациентов с ХБП. В недавних метаанализах было установлено, что жесткая коррекция анемии с помощью ЭСА ассоциируется с повышенным риском развития артериальной гипертензии, инсульта и тромбоза сосудистого доступа при несущественном улучшении качества жизни и отсутствии положительного влияния на гипертрофию левого желудочка по сравнению с частичной коррекцией анемии.
Цели лечения анемии у пациентов с ХБП – частично скорригировать уровни гемоглобина и поддерживать их стабильными в целевом диапазоне на протяжении большей части времени, избегая колебаний уровня гемоглобина и используя как можно более низкую дозу ЭСА. Решению этих задач помогают регулярный мониторинг анемии, назначение препаратов железа и избегание частых изменений дозы ЭСА.
Несмотря на то что все доступные ЭСА обладают сопоставимыми эффективностью и безопасностью, при назначении этих препаратов конкретному пациенту следует учитывать различия в фармакокинетике и фармакодинамике, периодичности и пути назначения, а также в стабильности уровня гемоглобина.
CERA (continuous erythropoietin receptor activator – длительно действующий активатор рецепторов эритропоэтина, препарат Мирцера®) был синтезирован путем интеграции крупной метокси полиэтилен гликоль-полимерной цепи в молекулу эритропоэтина, что придало ей новые свойства (ускоренная диссоциация от рецептора эритропоэтина и более длительное время полувыведения). После регистрации CERA в Европе (2007 г.) было проведено несколько постмаркетинговых исследований, в которых изучалось применение препарата у пациентов с ХБП, не находящихся на диализе. Целью настоящего исследования было оценить результаты лечения анемии препаратом Мирцера® в аналогичной популяции больных в условиях реальной клинической практики.
Методы
 Ретроспективное многоцентровое наблюдательное исследование проводилось в 19 амбулаторных нефрологических отделениях Каталонии (Испания). Набор пациентов осуществляли на протяжении 2010 г. Данные получали в виде электронных индивидуальных регистрационных форм. Все пациенты предоставили информированное согласие, и исследование было одобрено этическими комитетами всех участвующих клиник.
Ретроспективное многоцентровое наблюдательное исследование проводилось в 19 амбулаторных нефрологических отделениях Каталонии (Испания). Набор пациентов осуществляли на протяжении 2010 г. Данные получали в виде электронных индивидуальных регистрационных форм. Все пациенты предоставили информированное согласие, и исследование было одобрено этическими комитетами всех участвующих клиник.
В исследование включали взрослых (≥18 лет) пациентов с анемией и ХБП 3, 4 и 5 стадии (расчетная скорость клубочковой фильтрации <60 мл/мин/1,73 м2), не находящихся на диализе и получавших CERA не менее 6 мес, у которых имелись биохимические и гематологические данные относительно анемии в начале лечения CERA, а также значения гемоглобина через 3 и 6 мес после старта терапии.
Несоответствие вышеуказанным критериям и необходимость в диализе на момент включения служили критериями исключения.
Каждый исследователь собирал данные из историй болезни всех пациентов, которые находились на лечении CERA по крайней мере 6 мес и соответствовали критериям включения.
Результаты
Изначально для участия в исследовании был набран 331 пациент, однако 64 больных были исключены из-за несоответствия критериям включения (ХБП 2 стадия, отсутствие анемии и т.п.). В итоге в анализ вошли 267 пациентов, большинство из которых имели ХБП 3 или 4 стадии (табл. 1). Наиболее частыми причинами ХБП были диабет и сосудистая патология. 38,5% пациентов имели функционирующую трансплантированную почку (табл. 2).
У больных, не подвергавшихся трансплантации, диагноз ХБП был установлен в среднем 8,4±8,9 года назад. У пациентов с пересаженной почкой с момента трансплантации прошло 7,1±4,7 года.
Анемия была диагностирована в среднем за 4,3±4,1 года, а терапия ЭСА начата за 3,0±2,4 года до включения. Средние уровни гемоглобина до начала лечения ЭСА составили 102±9 г/л. 48,2% пациентов ранее не получали ЭСА; 58,1% больных перешли на терапию CERA с другого ЭСА – эритропоэтина бета (n=85; средняя месячная доза 16 694±11 180 МЕ) или дарбэпоэтина альфа (n=50; средняя суточная доза 90,5±56 мкг) (табл. 3).
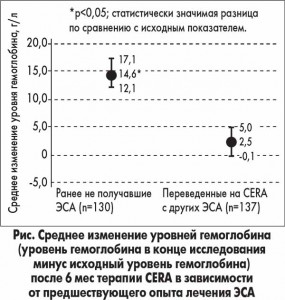
Аналитические данные относительно анемии представлены в таблице 4. У пациентов, ранее не получавших ЭСА, уровни гемоглобина на начальном этапе терапии CERA были более низкими, а в конце лечения они значительно повысились. В то же время у больных, переведенных на CERA с других ЭСА, значимых изменений уровня гемоглобина не наблюдалось (рис.). Показатели обмена железа оставались стабильными на протяжении всего исследования.
Большинство пациентов, не получавших ранее ЭСА, начали лечение CERA в режиме 1 раз в месяц, несмотря на то что на момент включения в исследование рекомендованный междозовый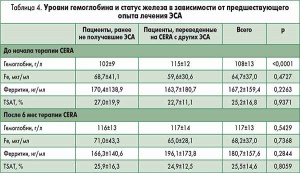 интервал для коррекции анемии составлял 2 нед. Почти все больные, переведенные на CERA с другого ЭСА (92,0%), начали терапию СERA согласно рекомендованной схеме 1 раз в месяц.
интервал для коррекции анемии составлял 2 нед. Почти все больные, переведенные на CERA с другого ЭСА (92,0%), начали терапию СERA согласно рекомендованной схеме 1 раз в месяц.
Как в начале, так и в конце исследования CERA чаще всего назначался в дозе 75 мкг 1 раз в месяц. Дозы, использовавшиеся у пациентов, ранее получавших другие ЭСА, были ниже рекомендованных инструкцией при переводе на CERA.
У пациентов, ранее не получавших ЭСА, стартовая доза CERA с поправкой на массу тела составила 1,3 мкг/кг/мес; финальная доза у больных этой подгруппы, достигших уровней гемоглобина >110 г/л, составила 1,1 мкг/кг/мес.
 Дополнительное лечение анемии в начале исследования включало препараты железа (40,7% пациентов), фолиевую кислоту (12,6%) и витамин В12 (7,4%). В конце исследования эти цифры существенно не изменились (38,5; 14,0 и 7,3% соответственно). Железодефицит (ферритин сыворотки <100 мкг/л или индекс насыщения трансферрина TSAT <20%) был диагностирован у 25% больных, их них 45,6% не получали препаратов железа.
Дополнительное лечение анемии в начале исследования включало препараты железа (40,7% пациентов), фолиевую кислоту (12,6%) и витамин В12 (7,4%). В конце исследования эти цифры существенно не изменились (38,5; 14,0 и 7,3% соответственно). Железодефицит (ферритин сыворотки <100 мкг/л или индекс насыщения трансферрина TSAT <20%) был диагностирован у 25% больных, их них 45,6% не получали препаратов железа.
Обсуждение
Результаты исследования показали, что у пациентов с ХБП, не находящихся на диализе, применение CERA 1 раз в месяц в условиях реальной клинической практики эффективно корригирует и поддерживает уровни гемоглобина. У пациентов, не получавших ранее ЭСА, целевые уровни гемоглобина достигались при назначении CERA в средней стартовой дозе 1,3 мкг/кг/мес, как это рекомендуется в инструкции к препарату. В то же время у больных, переведенных на CERA с других ЭСА, требуемые дозы были ниже по сравнению с рекомендуемыми в инструкции.
Средние уровни гемоглобина, достигнутые с помощью терапии CERA как у ранее не получавших ЭСА (116 г/л), так и уже имевших опыт применения ЭСА пациентов (117 г/л), оставались в высокой степени стабильными на протяжении исследования и находились в рекомендованном диапазоне (110-120 г/л; ERBP, 2009 г.).
Эффективность и безопасность CERA у пациентов с ХБП были продемонстрированы в рандомизированных контролируемых исследованиях. Тем не менее большинство этих исследований проводились с участием больных, находящихся на диализе. Следовательно, опыт применения CERA у пациентов с ХБП, не получающих диализ, является более ограниченным как в условиях клинических исследований, так и в рутинной практике.
У пациентов, ранее не получавших ЭСА, средние уровни гемоглобина статистически значимо повысились на 14,6 г/л и достигли 116 г/л; у больных, переведенных на CERA c других ЭСА, изменения уровня гемоглобина были минимальными (с исходных 115 до 117 г/л). Средняя доза CERA, необходимая для достижения и поддержания целевых уровней гемоглобина, составила 75 мкг/мес независимо от опыта предыдущего лечения ЭСА. Практически такая же доза использовалась в исследовании OASIS в похожей популяции.
Результаты у ранее не получавших ЭСА пациентов согласуются с данными исследований ARCTOS (междозовый интервал 2 нед), CORDATUS (1 мес) и SUPRA (1 мес). При этом дозы, требовавшиеся для достижения целевых уровней гемоглобина, соответствовали рекомендованным в инструкции к препарату, что подтверждает их применимость в условиях реальной клинической практики. Необходимо подчеркнуть, что в настоящем исследовании большинство пациентов, ранее не получавших ЭСА, начали лечение CERA по схеме 1 раз в месяц, притом что на тот момент еще не были опубликованы результаты исследований CORDATUS и SUPRA.
У пациентов, перешедших на исследуемый препарат с других ЭСА, средняя доза CERA была ниже дозы, рекомендуемой инструкцией по применению. Это согласуется с данными других исследований и подтверждает, что у пациентов с ХБП, не находящихся на диализе, доза CERA, необходимая для поддержания стабильных уровней гемоглобина после перевода с короткодействующих ЭСА, составляет <120 мкг/мес. Полученный результат заслуживает дальнейшего изучения, поскольку в новых руководствах рекомендуется применять ЭСА в как можно более низкой дозе, позволяющей достичь целевых уровней гемоглобина, для минимизации риска развития неблагоприятных событий. Таким образом, эффективность более низкой дозы может иметь как клиническую, так и экономическую значимость. Исследование OCEANE также подтвердило эффективность и безопасность CERA в ведении анемии у пациентов с ХБП на этапе додиализа, в том числе перенесших трансплантацию почки. Однако в отличие от исследования OCEANE в настоящем исследовании эффективные дозы CERA (как и уровни гемоглобина и статус железа) были одинаковыми у пациентов с трансплантированной почкой и у больных, не подвергавшихся этой процедуре. Следует отметить, что дозы CERA, применявшиеся у пациентов с трансплантированной почкой, соответствовали таковым в исследовании Anemia Trans Study.
ХБП ассоциируется со сниженной абсорбцией железа и плохой гастроинтестинальной переносимостью пероральных препаратов железа. У пациентов с ХБП и анемией для оптимизации эритропоэза и достижения адекватного ответа на ЭСА необходима нормализация статуса железа. У больных с железодефицитом терапия пероральными или внутривенными препаратами железа позволяет использовать ЭСА в более низкой дозе и повышает вероятность поддержания уровней гемоглобина в целевом диапазоне. В настоящем исследовании адекватный статус железа имели 75% пациентов, однако среди больных с железодефицитом препараты железа получали менее половины. Таким образом, несмотря на последние достижения в коррекции дефицита железа у пациентов с ХБП, возможности для совершенствования все еще сохраняются.
Проведение исследования в условиях реальной клинической практики делает его результаты репрезентативными для широкой популяции больных ХБП, не находящихся на диализе.
Выводы
Ведение анемии с помощью препарата Мирцера® у пациентов с ХБП, не находящихся на диализе, позволяет эффективно достигать целевых уровней гемоглобина и поддерживать их в терапевтическом диапазоне. При этом у пациентов, переведенных на CERA с короткодействующих ЭСА, требовались более низкие дозы по сравнению с рекомендованными в инструкции по применению препарата. Схема назначения 1 раз в месяц продемонстрировала эффективность независимо от предшествующего опыта терапии ЭСА.
Список литературы находится в редакции.
Статья печатается в сокращении.
Martinez-Castelao A., Cases A., Coll E. et al. C.E.R.A. administered once monthly corrects and maintains stable hemoglobin levels in chronic kidney disease patients not on dialysis: the observational study MICENAS II. Nefrologia. 2015; 35(1): 80-6.
Перевел с англ. Алексей Терещенко
СТАТТІ ЗА ТЕМОЮ Нефрологія
14 березня відзначається Всесвітній день нирки та боротьби із захворюваннями видільної системи. За оцінками експертів, хронічна хвороба нирок (ХХН) уразила >850 млн людей у всьому світі та зумовила >3,1 млн смертей у 2019 році. Протягом останніх трьох десятиліть зусилля з лікування ХХН зосереджувалися на підготовці та проведенні нирковозамісної терапії. На особливу увагу заслуговують захворювання нирок, спричинені інфекційними ураженнями, наприклад перенесеними сезонними інфекціями. На запитання щодо цієї теми надала відповіді в своїй доповіді завідувачка нефрологічного відділення МЦ «Діавіта‑Інститут» (м. Київ), позаштатний експерт Національної служби здоров’я України, лікар-терапевт, нефролог, кандидат медичних наук Анна Сергіївна Петрова....
У пацієнтів із хронічною хворобою нирок (ХХН) зниження швидкості клубочкової фільтрації (ШКФ) спричиняє погіршення виведення з організму хлориду натрію, що обумовлює виникнення позитивного натрієвого балансу й артеріальної гіпертензії (АГ). Саме тому підтримання балансу між споживанням і виведенням натрію із сечею є основним викликом під час ведення таких пацієнтів. Низька прихильність до зменшення споживання солі – загальновідома незадоволена клінічна потреба хворих на ХХН [1]....
Прогресування ниркової недостатності з розвитком ускладнень та суттєвим зниженням швидкості клубочкової фільтрації часто потребує проведення гемодіалізу. Цій темі було приділено увагу в рамках 4‑го випуску циклу семінарів «Хвороби нирок та сечовивідних шляхів», який відбувся 27 жовтня. Основні показання до проведення нирковозамісної терапії, клінічні стани, що вимагають її призначення, а також оптимальні терміни початку діалізу були висвітлені в доповіді голови Української національної діалізної асоціації Ігоря Любомировича Кучми «Початок нирковозамісної терапії при ХХН: коли і як»...
Збільшення кількості пацієнтів із хронічною хворобою нирок (ХХН) пов’язане як із демографічним старінням населення, так і зі зростаючою поширеністю судинних захворювань, аутоімунної патології, цукрового діабету. Метою ранньої діагностики та лікування ХХН є уповільнення погіршення функції нирок та запобігання розвитку ускладнень. Наслідки ниркової недостатності включають не тільки порушення видільної та концентраційної функцій, а й вплив на суміжні системи та органи. Зокрема, відомо, що ризик серцево-судинних захворювань зростає при протеїнурії, навіть за відсутності порушення функції нирок....