Алергія як форма запалення
Чи мають антигістамінні препарати протизапальний ефект?
 Згадаймо, що таке запалення. Це комплексний місцевий і загальний захисно-пристосувальний процес, що виникає у відповідь на пошкодження або дію патогенного подразника та проявляється в реакціях, спрямованих на усунення продуктів, а якщо можливо, то й агентів, і забезпечує максимальне відновлення в зоні ушкодження. Механізм запалення є спільним і для людини, і для тварин (зокрема нижчих), незалежно від локалізації, виду подразника та індивідуальних особливостей організму [1].
Згадаймо, що таке запалення. Це комплексний місцевий і загальний захисно-пристосувальний процес, що виникає у відповідь на пошкодження або дію патогенного подразника та проявляється в реакціях, спрямованих на усунення продуктів, а якщо можливо, то й агентів, і забезпечує максимальне відновлення в зоні ушкодження. Механізм запалення є спільним і для людини, і для тварин (зокрема нижчих), незалежно від локалізації, виду подразника та індивідуальних особливостей організму [1].
Патогенні подразники (пошкоджувальні фактори) за своєю природою можуть бути:
- Фізичними (травма, обмороження, опік).
- Хімічними – луги, кислоти, подразнювальні і токсичні речовини.
- Біологічними – збудники інфекційних захворювань: паразити, бактерії, віруси. До біологічних пошкоджувальних факторів належать також імунні комплекси, які складаються з антигена, антитіла і комплементу і спричинюють імунне запалення (алергія, автоімунний тиреоїдит, ревматоїдний артрит, системний васкуліт).
Треба зазначити, що будь-яка алергічна реакція призводить до пошкодження тканин. За певних умов відбувається сенсибілізація організму пацієнта, що супроводжується виробленням імуноглобуліну Е та прикріпленням його на внутрішній поверхні кровоносних судин майбутніх органів-мішеней, що ушкоджуються алергічними реакціями негайного типу внаслідок виходу медіаторів запалення. Таким чином, алергія – це одна з форм переважно хронічного запалення, можливо, найпоширеніша. Чому ж тоді в лікуванні алергії не застосовують нестероїдні протизапальні засоби, які поряд із гормонами рекомендовані при всіх інших формах запалення? Можливо, протиалергічні засоби, передусім антигістамінні препарати (АГП), мають як протиалергічні, так і протизапальні властивості? Давайте розбиратися.
Формування алергічного запалення
Алергічний риніт (АР) характеризується запальною інфільтрацією слизової оболонки порожнини носа різними клітинами. У разі постійного впливу алергенів запалення персистує упродовж усього року, у разі сезонного – має інтермітуючий характер, поступово згасаючи з припиненням дії алергену.
Доведено, що навіть за відсутності симптомів у пацієнтів із персистуючим АР зберігається запалення слизової оболонки порожнини носа – мінімальне персистуюче запалення (рис.). Симптоми персистуючого АР є результатом складної взаємодії тригерних факторів і запальної реакції, що триває. У процесі алергічного запалення формується підвищена неспецифічна реактивність слизової оболонки носа [2]. Алергени, потрапляючи в порожнину носа, частково осідають на війчастому епітелії. Надалі в слизовій оболонці носа утворюються патологічні комплекси «антиген–антитіло», і таким чином розвивається сенсибілізація.
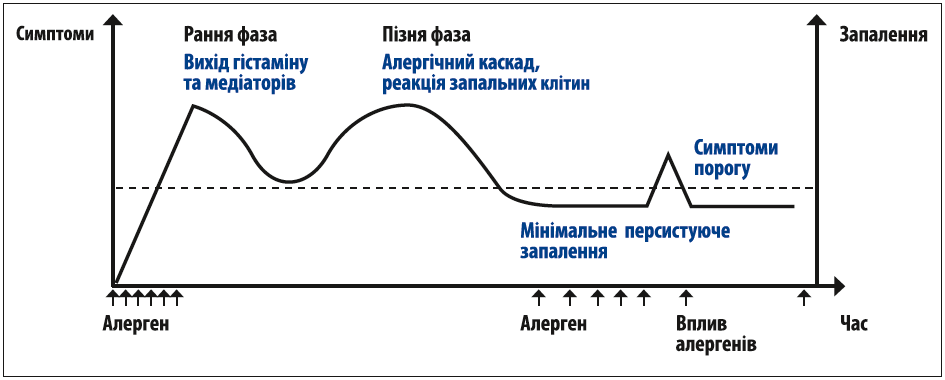
Рис. Часові терміни розвитку алергічного запалення
У разі повторного потрапляння алергенів вже на сенсибілізовану слизову оболонку запускається алергічна реакція типу I згідно з класифікацією R.R.A. Coombs і P.G.H. Gell (1963). Патогенетично АР є наслідком порушення балансу Т-лімфоцитів Th1/Th2 з переважанням Th2-відповіді, що розвивається після дії алергену [3, 4]. Алергічне запалення при АР являє собою каскад процесів, що виникають за участю великої кількості імунних клітин і медіаторів. Основною клітиною ранньої стадії запалення є макрофаг. Цитокіни, які послідовно продукуються макрофагами, разом з еозинофілами відповідальні за розвиток хронічного алергічного запалення [4]. Клітинна відповідь полягає в хемотаксисі клітин, секреції цитокінів, активації та диференціації еозинофілів, епітеліальних клітин, зміні складу лімфоцитів, зменшенні популяції СD4-клітин. Надалі відбувається вивільнення активованими клітинами медіаторів запалення, переважно гістаміну і лейкотрієнів, і складна передача сигналів за допомогою месенджерів іншим клітинам для їх активації.
Медіатори алергічного запалення
- Гістамін є біологічно активною речовиною, що синтезується з гістидину шляхом його декарбоксилювання в апараті Гольджі. Гістамін міститься в більшості тканин організму (у гранулах опасистих клітин, базофілів, гістамінергічних нервових клітинах та ін.) і виконує функцію посередника різноманітних фізіологічних і патологічних реакцій. Стимуляція Н1-гістамінових рецепторів призводить до скорочення гладеньких м’язів (особливо трахеї та бронхів); посилення виділення слизу в дихальних шляхах; дилатація і підвищення проникності капілярів; уповільнення атріовентрикулярної провідності; негативний інотропний ефект; зниження артеріального тиску; рефлекторний викид катехоламінів; посилення вивільнення медіаторів запалення з нейтрофілів.
- Фактор некрозу пухлини (TNF) є основним цитокіном, що синтезується і депонується макрофагами [6]. Макрофаги також продукують інтерлейкіни (IL), такі як IL‑3, IL‑4, IL‑5, IL‑6, IL‑8, IL‑1 та IL‑13 [6, 7]. Усі ці цитокіни, так само як і гістамін, провокують порушення проникності судин і процесів адгезії, проліферації та диференціювання активованих В-лімфоцитів, стимуляцію росту та диференціювання еозинофілів [8]. Еозинофіли є ще одним потужним джерелом цитокінів, особливо в пізній фазі алергічного запалення. Вони можуть синтезувати та вивільняти такі цитокіни, як IL‑1, TNF, IL‑3, IL‑4, IL‑5 та IL‑8 [5, 9]. На тлі АР (як сезонного, так і персистуючого) в назальному слизу після провокації алергеном виявляють підвищені рівні IL‑1, TNF, IL‑6 та IL‑8 [10].
- Лейкотрієни синтезуються з арахідонової кислоти, яка вивільняється під час імунологічної стимуляції різних клітин, що беруть участь у запаленні, за допомогою ферментної системи 5-ліпоксигенази. У ході функціонування останньої природним проміжним продуктом є лейкотрієн А4 – нестабільний епоксид, який, з’єднуючись з водою, може перетворюватися неензиматичним шляхом на дигідроксикислий лейкотрієн В4 (LТВ4) або, з’єднуючись з глутатіоном, – на цистеїніл-лейкотрієн С4 (LТС4). LТС4 за допомогою γ-глутамілтрансферази перетворюється на LТD4 і потім, за допомогою дипептидаз, – на LТЕ4, який зазнає подальшого метаболізму.
Таким чином, під впливом найважливіших медіаторів – гістаміну і лейкотрієнів – починається хемотаксис клітин і формування запальної інфільтрації в слизовій оболонці верхніх дихальних шляхів. Далі відбувається взаємодія з імунною системою, розвиток проліферативно-фібропластичної реакції, хронізація запалення.
Коли виникає запалення, організм отримує больові сигнали від нервових рецепторів. Ці сигнали виникають у результаті складних реакцій і взаємодій між клітинами і хімічними речовинами в організмі за участю простагландинів. Цих медіаторів немає при алергічному запаленні.
- Простагландини – це гормоноподібні хімічні речовини, які виробляються клітинами організму та виконують кілька важливих функцій. Вони сприяють запаленню, необхідному для загоєння, але також є причиною болю і високої температури. Простагландини виробляються у клітинах організму під впливом ферменту циклооксигенази (ЦОГ). Є два ферменти ЦОГ: ЦОГ‑1 і ЦОГ‑2. Обидва ферменти сприяють виробленню простагландинів, які спричиняють запалення. Тут важливо зазначити, що ЦОГ‑1 сприяє виробленню важливих простагландинів, які сприяють згортанню крові і захищають шлунок від дії кислоти. Засоби з групи нестероїдних протизапальних препаратів (НПЗП) не є стероїдами, тобто вони працюють не за стероїдним механізмом, що імітує гормон кортизон, а за механізмом зменшення вироблення простагландинів. Ще наприкінці 1980-х було виявлено, що НПЗП блокують ферменти ЦОГ‑1 і ЦОГ‑2 і знижують рівень простагландинів по всьому тілу. Тому їх широко застосовують у лікуванні всіх видів запалення, крім імунного, у тому числі алергічного [11].
- H1-антигістамінні препарати повсюдно рекомендовані при всіх типах АР незалежно від тяжкості симптомів або сезонності. Вони потенційно здатні контролювати усі прояви АР. Препарати останнього покоління мають також протизапальні властивості, знижують вираженість алергічного запалення [12, 13]. Сьогодні основною метою лікування АР є усунення симптомів, покращення якості життя пацієнтів і запобігання розвитку бронхіальної астми (БА) [3]. Терапевтичні стратегії також спрямовані на зниження кількості прозапальних медіаторів, що вивільняються з активованих клітин, у тому числі макрофагів. Ефективність АГП оцінюють не лише за здатністю блокувати гістамінові рецептори, але й протизапальною активністю, що, на думку багатьох дослідників, підвищує клінічний ефект від їх застосування.
Протизапальні властивості АГП: фокус на левоцетиризин
Одним із ефективних і безпечних блокаторів Н1-рецепторів гістаміну ІІ покоління є левоцетиризин. Крім потужного антигістамінного ефекту левоцетиризин має відчутні протизапальні властивості. Останні спостерігають у разі застосування клінічно значущих концентрацій, які можуть посилити терапевтичну користь препарату. Левоцетиризин – ефективний АГП, про що свідчить його здатність інгібувати свербіж шкіри, спричинений гістаміном, а також пухирі та гіперемію [14-16]. Модель індукованих гістаміном пухирів і запалення на шкірі людини є широко використовуваною відтворюваною стандартизованою методологією, яка дає об’єктивну оцінку ефективності АГП у пацієнтів, у тому числі виявляє будь-які відмінності в початку і тривалості дії.
Левоцетиризин усуває закладеність носа [17, 18], що є вкрай важливою обставиною, оскільки багато АГП у цьому відношенні є недостатньо ефективними.
Насправді вважається, що причиною закладеності носа є не гістамін, а інші медіатори опасистих клітин, у тому числі простагландин D2 і лейкотрієни, що діють узгоджено [19]. Позитивний ефект левоцетиризину на цей важливий симптом АР, імовірно, пояснюється додатковими протизапальними властивостями препарату. Значний інтерес має вплив протизапальних препаратів на прозапальні процеси, відповідальні за прояви алергічних захворювань.
Протизапальні ефекти, які не залежать від блокади H1-рецепторів, були описані для більшості АГП, тоді як вихідна сполука левоцетиризину має значущі добре задокументовані протизапальні властивості як in vivo, так і in vitro [20].
У низці недавніх досліджень in vitro проводилась оцінка того, чи має левоцетиризин подібні властивості. Левоцетиризин in vitro інгібував індуковану еотаксином трансендотеліальну міграцію еозинофілів крізь моношари ендотеліальних клітин дерми або легень людини в таких самих концентраціях, що досягаються в клінічних умовах, або нижчих [21]. Фізіологічно значущі концентрації левоцетиризину пригнічували експресію ICAM‑1 і секрецію IL‑6 і IL‑8 у первинних клітинах носового епітелію людини, інфікованих риновірусом людини. Епітеліальні клітини носа, оброблені левоцетиризином, також демонстрували значно менші титри риновірусів і слабшу активацію NF-κB [22]. Ці дослідження демонструють in vitro протизапальну дію левоцетиризину на різні типи клітин у низьких фізіологічно значущих концентраціях. Проте очевидне питання полягає в тому, яке клінічне значення мають протизапальні властивості цього АГП на додаток до ефекту, що забезпечується блокадою Н1-рецепторів. Відповісти на це питання можуть лише добре проведені дослідження in vivo.
Чипранді та співавт. [23] порівнювали вплив лікування левоцетиризином, дезлоратадином або плацебо на рівні маркерів запалення в носі, назальні симптоми і швидкість потоку повітря в пацієнтів із сезонним АР (САР) у сезон пилку. Учені продемонстрували, що левоцетиризин, але не дезлоратадин або плацебо, значно знижував кількість еозинофілів, нейтрофілів і рівні IL‑8 у зразках назального змиву в сезон пилку, тоді як лікування будь-яким з АГП значно знижувало рівні IL‑4. Крім того, левоцетиризин також був значно ефективнішим, ніж дезлоратадин і плацебо, у полегшенні назальних симптомів і збільшенні швидкості носового потоку в цих пацієнтів порівняно з вихідним рівнем. Такі дані свідчать про те, що опосередковане левоцетиризином поліпшення назальних симптомів і потоку повітря у пацієнтів із САР може бути пов’язане зі зменшенням рівнів запальних маркерів у носових ходах у цих людей. Нещодавно левоцетиризин і дезлоратадин порівнювали за їх здатністю інгібувати спровоковані алергеном пухирі і гіперемію в подвійному сліпому рандомізованому перехресному плацебо-контрольованому дослідженні за участю пацієнтів з алергією [24]. Це цікавий підхід, оскільки використання провокації алергеном імітує ситуацію in vivo. Таким чином, спричинена відповідь полягає в дегрануляції опасистих клітин і вивільненні численних вазоактивних і прозапальних медіаторів на додаток до гістаміну. Секреція цитокінів лімфоцитами, особливо Th2-клітинами, імовірно, відіграє центральну роль у розвитку й підтриманні алергічної запальної реакції. Тому цікаво, що в недавньому дослідженні в пацієнтів із САР вивчали вплив лікування левоцетиризином як на симптоми, так і на кількість еозинофілів у периферичній крові, а також профілі субпопуляцій лімфоцитів. Якщо порівнювати з плацебо, лікування левоцетиризином мало значний позитивний вплив на симптоми, зменшило кількість еозинофілів і прозапальних Т-клітин, а саме: CD4+CD29+, CD4+CD212+ і CD4+CD54+. Треба зазначити, що автори також повідомили про збільшення у периферичній крові числа CD4+CD25+, субпопуляції Т-клітин, до якої можуть належати захисні імунорегуляторні клітини [25].
C.I. Bocsan та співавт. (2015) [26] встановили, що пацієнти з персистуючим АР мають високі рівні прозапальних цитокінів TNF і IL‑8 у плазмі крові.
Левоцетиризин здатний ефективно контролювати симптоми АР, у тому числі закладеність носа. Тривала терапія левоцетиризином дає можливість достовірно знижувати рівні деяких маркерів алергічного запалення в плазмі крові.
Таким чином, є переконливі результати лабораторних і клінічних досліджень, що підтверджують протизапальні властивості АГП, особливо левоцетиризину. А чи можна його призначати при застуді?
Систематичні огляди Кокранівської співпраці неодноразово були присвячені різним методам лікування застудних інфекцій, у тому числі застосуванню цинку, кортикостероїдів, вітаміну С, НПЗП, парацетамолу й іпратропію броміду. Імовірно, дія цих препаратів ґрунтується на пригніченні запалення, що спостерігається при застуді. Під час поширення вірусу збільшується вироблення цитокінів із подальшим залученням у процес інших медіаторів запалення. Цитокіни та медіатори запалення відповідальні за підвищення температури тіла, почервоніння шкіри, закладеність носа, ринорею, сльозотечу і чхання. Унаслідок пригнічення алергічних реакцій за участю імуноглобуліну Е АГП можуть зменшувати запалення і відповідні симптоми застуди.
A.I.M. De Sutter та співавт. (2015) опублікували узагальнювальні результати багатьох досліджень на цю тему. За цими даними, у групі АГП на 26% пацієнтів більше відчували полегшення симптомів застуди протягом перших 2 діб порівняно з групою плацебо. Коли порівнювали симптоми окремо, достовірні відмінності зазначали для закладеності носа і чхання. Однак усі ці засоби ніяк не впливали на тривалість захворювання.
Висновки
- Алергія – це одна з форм переважно хронічного запалення, можливо, найпоширеніша.
- Доведено, що навіть за відсутності симптомів у пацієнтів із персистуючим АР зберігається запалення слизової оболонки порожнини носа – мінімальне персистуюче запалення.
- Дослідження з вивчення механізмів, що лежать в основі ефектів H1-АГП, показали, що крім потужної антигістамінної дії левоцетиризин має протиалергічні/протизапальні властивості, з яких не всі можуть бути пов’язані з блокадою H1-рецепторів. Ці протизапальні властивості спостерігають у разі застосування клінічно значущих концентрацій як in vitro, так і in vivo. Важливо зазначити, що в низці тривалих досліджень (6-18 міс) повідомляли про довгострокові переваги левоцетиризину в дорослих і дітей щодо не лише зменшення вираженості симптомів, таких як закладеність носу, а й покращення якості життя.
- Сьогодні є значна кількість належним чином проведених клінічних випробувань, результати яких демонструють, що левоцетиризин є ефективним засобом із хорошою переносимістю для лікування алергічних захворювань у дорослих і дітей. На сучасному фармацевтичному ринку України левоцетиризин представлений препаратом Алерзин®, виробництва фармацевтичної компанії Egis (Угорщина). Препарат доступний у двох формах випуску: таблетки по 5 мг та оральний розчин в дозуванні 5 мг/мл, що його дозволено до застосування дітям від 2 років. Алерзин® рекомендований при симптомах алергічного риніту та кропив’янки. При хронічних захворюваннях (хронічний алергічний риніт, хронічна кропив’янка) тривалість лікування становить до 1 року.
Cписок літератури – у редакції.
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 3 (60) 2022 р.
СТАТТІ ЗА ТЕМОЮ Алергія та імунологія
Поліпіл (polypill) – фіксована комбінація декількох препаратів в одній капсулі, що має вирішити одразу декілька терапевтичних завдань і водночас спростити режим прийому ліків. Найчастіше поліпіли використовують для лікування та профілактики серцево-судинних захворювань, при цьому вони спрямовані на такі ключові модифіковані фактори ризику, як артеріальна гіпертензія, гіперліпідемія та посилена агрегація тромбоцитів. Нині терапевтичні стратегії на основі фіксованих комбінацій препаратів є надзвичайно актуальними, оскільки, незважаючи на наявність ефективних лікарських препаратів, контроль кардіоваскулярного ризику залишається недостатнім насамперед через низьку прихильність та обмежений доступ до лікування. ...
Збудник COVID‑19, SARS-CoV‑2, з яким людство вперше стикнулося у 2019 р., поширився по всьому світу, заразивши мільйони людей. Сьогодні, через тягар війни та економічної нестабільності, тема COVID‑19 не сприймається так гостро, як ще кілька років тому, хоча насправді вона не втратила своєї актуальності. Саме сучасному стану проблеми COVID‑19 у світі та в Україні була присвячена доповідь директора ДУ «Інститут ендокринології та обміну речовин імені В.П. Комісаренка НАМН України», академіка Національної академії медичних наук України, члена-кореспондента НАН України, віце-президента НАМН України, президента Асоціації ендокринологів України, професора Миколи Дмитровича Тронька під час першого у 2024 р. засідання науково-освітнього проєкту «Школа ендокринолога», яке відбулося 20-24 лютого. ...
Йод є необхідним для життя ссавців компонентом гормонів щитоподібної залози (ЩЗ). В огляді йдеться про важливі наукові відкриття і досягнення в галузі харчування, пов’язані з профілактикою йододефіцитних захворювань (ЙДЗ) у США і в усьому світі, з акцентом на минуле століття (рис. 1). Огляд присвячено сторіччю заснування Американської тиреоїдної асоціації (ATA). ...
Серцево-судинні захворювання (ССЗ) (ішемічна хвороба серця [ІХС], захворювання судин головного мозку, ревматична хвороба серця та інші) протягом багатьох десятиліть є основною причиною смертності населення у світі. Перебіг цих захворювань ускладнюється перенесеною корона вірусною хворобою (COVID‑19). Нині ця проблема є особливо актуальною в Україні в умовах повномасштабного вторгнення рф, оскільки вплив хронічного стресу призводить до зростання захворюваності на ССЗ. У такій ситуації поряд із «протокольною терапією» слід приділити увагу застосуванню біорегуляційного підходу, спрямованого на відновлення саморегуляції, імунного статусу, гармонізації функціонування всіх органів і систем людини. ...




