Лікування розладів ковтання у пацієнтів відділення інтенсивної терапії
Дисфагія є поширеним явищем у пацієнтів відділення інтенсивної терапії (ВІТ), але вона часто залишається недостатньо розпізнаною та неконтрольованою, незважаючи на те що пов’язана з небезпечними для життя ускладненнями, тривалим перебуванням у ВІТ та госпіталізацією. Запропонований у статті експертний висновок щодо діагностики й лікування дисфагії розроблений на основі доказових клінічних рекомендацій та думок лікарів-практиків. Автори рекомендують прийняти ці клінічні алгоритми для надання стандартизованої та високоякісної допомоги, яка передбачає своєчасний систематичний скринінг, оцінку та лікування дисфагії в екстубованих пацієнтів і пацієнтів із трахеостомою у ВІТ.
Ключові слова: дисфагія, критично хворі пацієнти, трахеостомія, постекстубація, відділення інтенсивної терапії, лікування дисфагії, ковтальна терапія, електростимуляція глотки.
Дисфагія, або порушення процесу ковтання, часто зустрічається у пацієнтів ВІТ і може мати різну етіологію. Набуті у ВІТ розлади ковтання є багатофакторними й часто являють собою ускладнення ятрогенної травми. Серед причин даної патології зустрічаються нейроміопатії, які асоційовані з перебуванням у ВІТ, порушення ротоглоткової та гортанної чутливості, порушення когнітивних функцій та рівня свідомості, гастроезофагеальний рефлюкс та дискоординація дихання і ковтання [1-6]. У пацієнтів ВІТ ризик дисфагії зростає за наявності таких факторів: початкове неврологічне захворювання, ургентна госпіталізація, тяжкість захворювання, а також вік ≥65 років, оцінка за шкалою APACHE II ≥15 і тривалість інтубації трахеї зі штучною вентиляцією легень (ШВЛ) ≥72 год [7, 8]. До інших факторів ризику відносять застійну серцеву недостатність, сепсис, гіперхолестеринемію, довготривалі операції та багаторазові інтубації [9].
18% пацієнтів, госпіталізованих у ВІТ, після екстубації не пройшли скринінг на ковтання води [10], у той час як у 41% наявність постекстубаційної дисфагії підтвердилась результатами інструментального обстеження. Із тих, хто мав постекстубаційну дисфагію, у 36% відзначалася так звана тиха аспірація [12]. Загалом, до 93% пацієнтів із трахеостомою мали труднощі з ковтанням [11].
Доведено, що дисфагія має довготривалі та тяжкі наслідки, які зберігаються у більшості пацієнтів ВІТ до моменту виписки зі стаціонару. Цей розлад збільшує 90-денну смертність на 9,2% [10], а смертність протягом наступного року – до 25% [13].
Незважаючи на актуальність проблеми дисфагії у клінічній практиці, її часто недооцінюють і недостатньо ефективно лікують. Навіть за очевидних переваг систематичного скринінгу [10, 22] у літературі з реанімації та інтенсивної терапії немає достатньої кількості відповідних рекомендацій і відсутній чіткий план обстеження [23-26].
Мета авторів полягала в тому, щоб запропонувати доказові клінічні алгоритми лікування дисфагії у пацієнтів із високим ризиком, які перебувають у ВІТ.
Матеріали та методи
План дослідження базувався на модифікованій версії п’ятикрокового методу ACCORD [30]. Він включав створення команди експертів із різних галузей, аналіз літератури та використання спільного досвіду групи для оцінки клінічних доказів, які лежать в основі кожної взаємодії з пацієнтом. Також враховувалася спільна думка експертів щодо найкращого методу лікування, розроблення чітких алгоритмів та їх поширення для практичного використання.
Результати
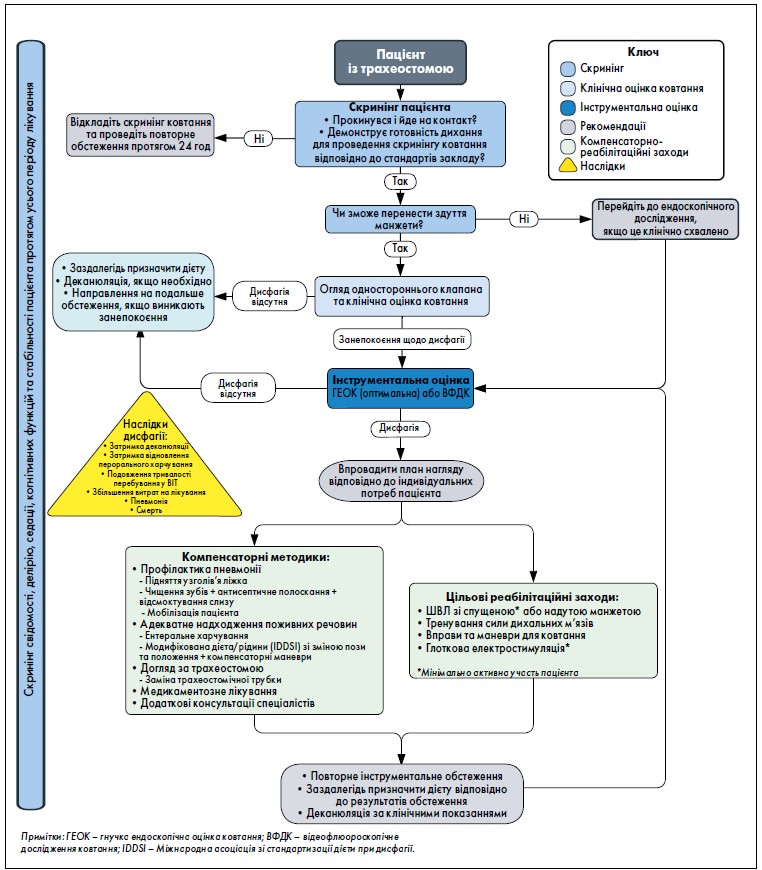
Група експертів дійшла консенсусу на основі аналізу доказів, наявних у літературі, та власного клінічного досвіду. Вони одностайно погодилися з важливістю формування підготовленої багатопрофільної команди медичної допомоги, систематичного скринінгу всіх пацієнтів ВІТ, використання інструментальних досліджень у певних випадках і раннього адаптованого лікування. Вищевказані принципи були впорядковані у двох алгоритмах (рис. 1, 2).
Рис. 1. Клінічний маршрут пацієнта із трахеостомою
Мультидисциплінарна команда
Лікування дисфагії у ВІТ потребує залучення лікарів різних спеціальностей: реаніматологів, неврологів, гастроентерологів, фізіотерапевтів, спеціалістів із дисфагії, медичних сестер та молодшого медичного персоналу, а також дієтологів [3]. Через різноманіття проявів дисфагії до лікування часто залучені логопеди, спеціалізовані отоларингологи – фоніатри, ерго- або фізіотерапевти. Спеціалізована підготовлена команда фахівців, які володітимуть комплексними знаннями виявлення й лікування дисфагії, забезпечить послідовну оцінку розладів ковтання.
Передекстубаційна група
У пацієнтів ВІТ з інсультом порушення прохідності дихальних шляхів і недостатня регуляція виділення секретів є більш надійними предикторами невдалої екстубації, ніж традиційні критерії ефективності самостійного дихання та рівень свідомості пацієнта [32]. З’являються обмежені дані щодо скринінгу та потенційного лікування інтубованих пацієнтів із ризиком невдачі екстубації та трахеостомії. Враховуючи обмежену кількість доказів щодо оцінки та лікування преекстубаційних пацієнтів, цю популяцію не включено в запропоновані алгоритми.
Алгоритми клінічного ведення пацієнтів
Алгоритми, представлені на рис. 1, 2, починаються з оцінки рівня свідомості пацієнта та його готовності до дихання (наприклад, відсутність критично підвищеної частоти дихання). Через нестабільний клінічний перебіг у пацієнтів ВІТ може виникнути потреба у частому повторенні скринінгових обстежень. Рекомендовано проводити скринінг ковтання якнайшвидше у пацієнтів, які перебувають у свідомості, контактні та мають до цього показання.
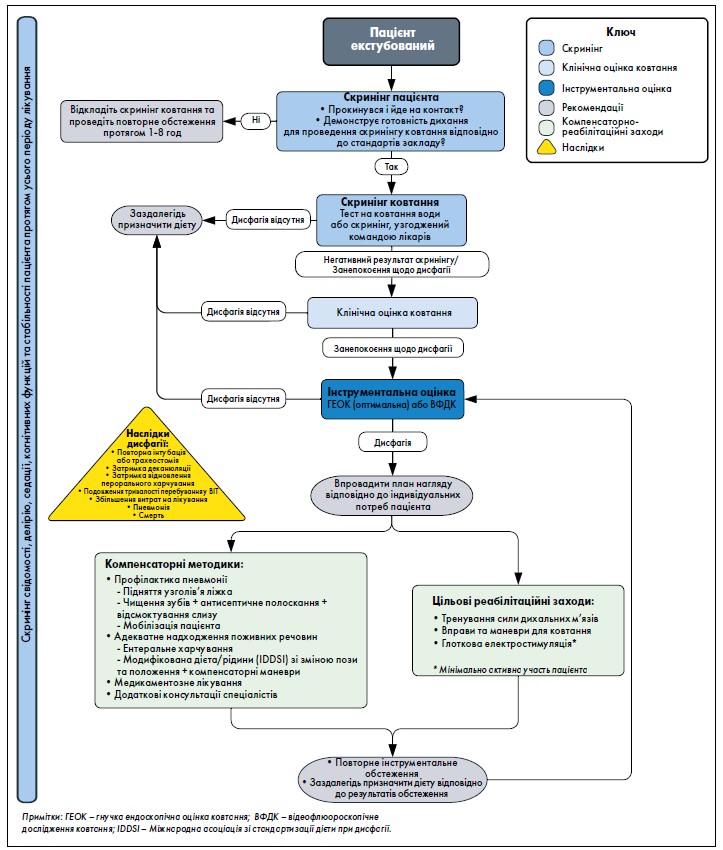
Рис. 2. Клінічний маршрут пацієнта після екстубації
Проте у пацієнтів із трахеостомою варіанти проведення приліжкового скринінгу, як правило, обмежені. Якщо пацієнт прокинувся і демонструє готовність до дихання, можна розглянути можливість здути манжету. Після цього пацієнти розділяються на групу із трахеостомою та групу з екстубацією.
Група пацієнтів із трахеостомою (рис. 1)
Рекомендовано, щоб усі пацієнти із трахеостомою, незалежно від стану вентиляції легень, брали участь в оцінці вбудованого, або одностороннього, клапана (ОСК), як тільки вони зможуть переносити здуття манжети або безманжетну трахеостомічну трубку. Наступним етапом фахівець із дисфагії проводить приліжкову оцінку ковтання, також відому як клінічна оцінка ковтання (КОК) [45-47]. В ідеалі КОК включає: огляд медичної карти, обстеження ротової порожнини, яке включає оцінку черепно-мозкових нервів, оцінку фізіологічного статусу та життєвих показників пацієнта, стану догляду за порожниною рота та регуляції виділення секретів, кашльовий рефлекторний тест (КРТ) [48] та оцінку болюсних проб, якщо це вважається клінічно доцільним. Обмежена КОК, за відсутності ковтальних проб,використовується перед проведенням інструментальної оцінки. Іноді потрібне подальше обстеження, якщо є занепокоєння щодо безпечності ковтання (наприклад, наявна тиха аспірація).
Оцінка дисфагії ідеально доповнюється інструментальними дослідженнями, такими як гнучка ендоскопічна оцінка ковтання (ГЕОК) або відеофлюороскопічне дослідження ковтання (ВФДК) [6, 14, 51-53]. Обидва дослідження вважаються золотим стандартом, однак ГЕОК є пріоритетним в умовах ВІТ, оскільки більш доступне у тяжкохворих пацієнтів: його можна проводити біля ліжка. ГЕОК дозволяє візуально оцінити потенційне ушкодження гортані, контролювати секрецію і проводити сенсорне тестування як доповнення до рідинних і твердих болюсних проб [1, 3, 6, 54, 55].
У разі виникнення підозри на дисфагію під час проведення КОК або підтвердження діагнозу за допомогою інструментального обстеження, слід розробити комплексний план лікування. Він має базуватися на основі специфічних порушень ковтання пацієнта та медичних потреб. Особливу увагу слід приділяти ретельному спостереженню за станом здоров’я хворого, його свідомістю та когнітивними здібностями, включаючи вплив седації, делірію та рівня збудження на його здатність до контакту. У пацієнтів із трахеостомою необхідно зменшити будь-який потенційний ризик зміщення трахеостомічної канюлі під час активного лікування.
Компенсаторні методики, призначені для мінімізації ризику та подальших ускладнень, можуть не покращувати фізіологію ковтання (наприклад, силу, чутливість) [1, 5, 56]. Вони включають підняття узголів’я ліжка, чищення зубів з антисептичним ополіскуванням і відсмоктування слини, а також мобілізацію пацієнта, якщо це вважається доцільним. Для зменшення ротової секреції можуть розглядатися медикаментозні препарати. Коригування дієти та використання постуральних і позиційних змін є більш природним, проте маневри ковтання (наприклад, надгортанний маневр) можуть мати терапевтичну користь. Рівні Міжнародної ініціативи зі стандартизації дієти при дисфагії (IDDSI) рекомендовані як стандартизований спосіб іменування та опису модифікованих текстур харчових продуктів і консистенції густої рідини [57]. Слід використовувати інструментальну оцінку для прийняття рішень щодо дієти пацієнта й постійної потреби у зміні позиції та маневрів.
Необхідно також оцінити доцільність відлучення від трахеостоми для відновлення потоку та тиску повітря через верхні дихальні шляхи для відновлення сенсорної функції й, можливо, зниження ризику аспірації [58], що включає використання вбудованого клапана, або ОСК зі спущеною манжетою, або надманжетної вокалізації (НМВ) із надуванням манжети. Крім того, за наявності медичних показань можна розглянути можливість своєчасної заміни трахеальної канюлі на меншу, оскільки було показано, що це значно швидше покращує переносимість ОСК і перорального прийому їжі [59].
ОСК та НМВ слід застосовувати лише після оцінки стану верхніх дихальних шляхів для забезпечення безпеки пацієнта [58]. Вимоги до безпечного та ефективного використання ОСК включають стабільність пацієнта, толерантність до здуття манжети, можливість видиху через трахеостомічну трубку та через верхні дихальні шляхи, а також стабільну сатурацію кисню, частоту дихання та частоту серцевих скорочень при встановленому клапані [60]. НМВ, яка в основному використовується за допомогою надування манжети, не слід застосовувати до загоєння рани на трахеостомі, оскільки це може призвести до емфіземи шиї. Додаткові протипоказання включають інфекцію або кровотечу в ділянці стоми, якщо потрібне безперервне підгортанне відсмоктування, якщо трахеостомічна трубка знаходиться в неоптимальному положенні або пацієнт не здатний контактувати і координувати зусилля з вокалізації. У пацієнтів із трахеостомою дослідження ОСК може бути найбільш доцільним, оскільки це вимагає від хворого мінімальних зусиль. Це також стосується пацієнтів, яким застосовують періодичні спроби спонтанного дихання або безперервну ШВЛ із використанням вбудованого клапана [61].
Існують також інші реабілітаційні втручання, спрямовані на покращення фізіології ковтання [1, 5, 56]. До них відносяться тренування сили дихальних м’язів, ковтальні вправи та маневри, такі як маневр Мендельсона, і/або нові нейростимуляційні методи лікування, зокрема електростимуляція глотки [1, 23, 55, 62]. Глоткова електростимуляція – це нова методика нейростимуляції для лікування нейрогенної дисфагії [62-66], призначена для відновлення неврологічних компонентів координації та контролю ковтання, порушених внаслідок центральних (наприклад, інсульт, черепно-мозкова травма) або периферичних (наприклад, десенсибілізація після тривалої ШВЛ) уражень [67-74]. Глоткова електростимуляція може бути найбільш доцільним раннім втручанням у тяжкохворих пацієнтів із трахеостомою, оскільки цей підхід вимагає мінімальної участі пацієнта.
На рис. 3 наведено поширені варіанти лікування дисфагії. Лікування має тривати протягом усього часу перебування в стаціонарі під керівництвом спеціаліста з дисфагії, доки пацієнт не досягне стабільного стану та позитивної динаміки. У міру покращення стану хворого рекомендовано проводити переоцінку даних для виявлення змін у його потребах. При виявленні значних клінічних змін команді, яка надає допомогу, рекомендовано повернутися до алгоритму, повторно оцінити стан пацієнта і відповідно змінити індивідуальний план лікування. Якщо стан пацієнта покращується і він відповідає комплексним критеріям готовності до деканюляції, можна розглянути питання про деканюляцію трахеостоми. Стандартизована ендоскопічна оцінка ковтання показує спроможність пацієнта керувати секрецією і допомагає визначити готовність до деканюляції [78,79].
Рис. 3. Сучасні терапевтичні методи
Група пацієнтів із екстубацією (рис. 2)
В екстубованих пацієнтів, які не пройшли скринінг ковтання, рекомендовано проведення КОК із додатковим КРТ і подальшою інструментальною оцінкою оптимально впродовж 24 годин. Як і у пацієнтів із трахеостомою, лікування слід проводити на основі індивідуальних порушень ковтання, спроможності пацієнта до участі в лікуванні та його потреб у лікуванні. Компенсаторні методики та реабілітаційні втручання схожі, але заміна трахеостомічної трубки та використання ОСК і НМВ не показані. Як і раніше, в ідеалі пацієнт має спостерігатися у спеціаліста з дисфагії до досягнення максимального рівня функціонування з подальшою переоцінкою потреб, що змінюються зі зміною плану спеціалізованого лікування. Якщо проблем із дисфагією не виявлено, медична команда може продовжувати моніторинг безпечної переносимості пероральної дієти та ліків і скерувати пацієнта на подальше обстеження, якщо виникнуть проблеми з ковтанням.
Враховуючи відсутність надійних наукових доказів, було розроблено і запропоновано два алгоритми клінічного менеджменту для використання лікарями різних галузей із метою покращення раннього систематичного виявлення та ефективного лікування дисфагії в екстубованих пацієнтів і пацієнтів із трахеостомою у ВІТ. Сучасні можливості лікування обмежені, але нові методи, такі як нейростимуляція, мають потенціал для значного покращення результатів лікування у таких хворих.
Список літератури знаходиться в редакції.
Підготувала Дар'я Чорна
За матеріалами: R. Likar et al. Management of swallowing disorders in ICU patients – A multinational expert opinion. J Crit Care. 2024 Feb;79:154447. doi: 10.1016/j.jcrc.2023.154447. Epub 2023 Nov 2. PMID: 37924574.
Тематичний номер «Хірургія. Ортопедія. Травматологія. Інтенсивна терапія» № 1 (58), 2024 р.
СТАТТІ ЗА ТЕМОЮ Хірургія, ортопедія та анестезіологія
Больовий синдром при хронічних ранах є рутинним явищем хірургічної практики. Рана вважається такою, що тривало не загоюється, якщо, незважаючи на відповідну терапію та достатній термін лікування (4-6 міс), відсутні або практично відсутні ознаки загоєння. Неопіоїдні та опіоїдні анальгетики є основними препаратами, що застосовуються для лікування больового синдрому при ранах. На науково-практичній конференції «Міждисциплінарний підхід у лікуванні коморбідних хірургічних пацієнтів», що відбулася наприкінці 2023 року, тему менеджменту хронічної ранової хвороби представив у доповіді «Контроль болю в хірургії ран та трофічних дефектів м’яких тканин різної етіології» завідувач кафедри хірургії та судинної хірургії Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Сергій Іванович Саволюк. Ключові слова: ранова хвороба, трофічна виразка, ВАК-терапія, больовий синдром, нестероїдні протизапальні препарати, Дексалгін®....
Актуальність проблеми переломів на сьогодні не залишає сумнівів, зокрема в контексті старіння населення та поширеності остеопорозу. Кальцій та вітамін D, виконуючи ключову роль у формуванні та підтриманні щільності кісткової тканини, є необхідними елементами для успішної профілактики переломів, особливо у вразливих груп населення. Також важливим є достатній рівень кальцію та вітаміну D в організмі для оптимального зрощення переломів і посттравматичної зміни кісток. У цьому контексті велике значення має вибір конкретного комплексу Са + D із позицій ефективності, безпеки та високого комплаєнсу. Ключові слова: остеопороз, крихкість кісток, кальцій, вітамін D, профілактика переломів. ...
З установленням центральних венозних катетерів (ЦВК) пов’язані різноманітні ускладнення, включаючи ті, що зумовлені безпосередньо введенням і/або доступом, через який уводиться катетер, а також віддалені (>1 тижня) ускладнення, такі як дисфункція катетера, стеноз або тромбоз центральної вени та розвиток інфекції. Кількість і тяжкість ускладнень зростають зі збільшенням розміру катетера, кількості використовуваних катетерів та часу їх перебування в організмі. У статті наведено огляд сучасних даних щодо ускладнень, пов’язаних із ЦВК, а також стратегії їх профілактики та лікування. Ключові слова: центральний венозний катетер, ускладнення, пункція артерії, пневмоторакс, тромбоз центральної вени, інфекції кровотоку, дисфункція катетера. ...
Восени минулого року в рамках семінару «Академія хірургії, анестезіології та інтенсивної терапії від А до Я: Хірургічні аспекти лікування гострого панкреатиту та його ускладнень. Анестезія у пацієнтів високого ризику» відбулася сателітна сесія, присвячена ефективним стратегіям антибіотикотерапії хірургічної інфекції шкіри, м’яких тканин і кісток. У своїй доповіді доцент кафедри загальної хірургії Львівського національного медичного університету ім. Данила Галицького, кандидат медичних наук Всеволод Васильович Ващук висвітлив сучасні класифікації інфекцій шкіри та м’яких тканин (ІШМТ), ключові принципи контролю джерела інфекції, а також актуальні рекомендації щодо лікування синдрому діабетичної стопи (СДС). ...