Ожирение и сахарный диабет: от скрининга к эффективному лечению и безопасной профилактике
 Неуклонный рост распространенности разнообразной эндокринологической патологии, в том числе ожирения, сахарного диабета (СД) и предиабета, определяет значимость действий семейного врача, делая его одной из главных фигур при оказании первичной эндокринологической помощи. Обследование населения с целью выявления разнообразной эндокринной патологии, проведение профилактической работы, осуществление диагностических и начальных терапевтических мероприятий при СД 2 типа и некоторых заболеваний щитовидной железы, мониторинг состояния пациентов с нарушенным углеводным и липидным обменом, своевременное направление выявленных больных к соответствующим специалистам – вся эта непростая работа ложится на плечи специалистов первичного звена.
Неуклонный рост распространенности разнообразной эндокринологической патологии, в том числе ожирения, сахарного диабета (СД) и предиабета, определяет значимость действий семейного врача, делая его одной из главных фигур при оказании первичной эндокринологической помощи. Обследование населения с целью выявления разнообразной эндокринной патологии, проведение профилактической работы, осуществление диагностических и начальных терапевтических мероприятий при СД 2 типа и некоторых заболеваний щитовидной железы, мониторинг состояния пациентов с нарушенным углеводным и липидным обменом, своевременное направление выявленных больных к соответствующим специалистам – вся эта непростая работа ложится на плечи специалистов первичного звена.
Подобная разносторонность профессиональной деятельности семейного врача аккумулирует в себе самые разнообразные виды медицинской помощи (диагностическую, лечебную, реабилитационную, профилактическую, санитарно-просветительскую, консультативную, организационную), что предопределяет необходимость четкого знания положений современных руководств / алгоритмов по диагностике и лечению эндокринологической патологии. Ожирение и СД 2 типа – самые известные эндокринологические заболевания, неумолимо захватывающие мир и распространяющиеся практически во всех странах со скоростью эпидемии.
Скрининг и диагностика
Ожирение
Диагностика ожирения относительно проста; для того чтобы подтвердить наличие избыточной массы тела / ожирения, равно как и нарушенной толерантности к глюкозе / СД, нет необходимости в проведении таких сложных инструментальных исследований, как компьютерная или магнитно-резонансная томография, – достаточно воспользоваться весами, ростомером, сантиметровой лентой, калькулятором или обратиться в лабораторию.
Абдоминальный (верхний) тип ожирения, при котором жировая ткань распределяется преимущественно в области живота и верхней части туловища, делает фигуру пациентов (как правило, мужчин) похожей на яблоко. Женщинам свойствен иной тип ожирения – бедренно-ягодичный (нижний), позволяющий сравнить телосложение таких пациенток с грушей. Отличить избыточную массу тела от истинного ожирения можно посредством расчета индекса массы тела (ИМТ), используя довольно известную формулу (ИМТ = масса тела [кг] / рост [м]2). При этом следует помнить, что в ряде случаев ИМТ не отражает истинную степень ожирения (у детей с незавершенным периодом роста, лиц старше 65 лет, спортсменов с очень развитой мускулатурой, беременных). Согласно действующим постулатам, считается, что оптимальное значение ИМТ в общей популяции должно составлять приблизительно 21 кг/м2. Такая неточность определения данного показателя обусловлена различными подходами к оценке ожирения, господствующими в странах Европы и Азии (табл. 1).
СД 2 типа
Распространенность другой эндокринологической патологии – СД 2 типа – продолжает неуклонно возрастать: в 2017 г. 58 млн жителей Европы страдали СД, количество больных этой патологией во всем мире составляло 425 млн. По прогнозам экспертов, к 2045 г. в Европейском регионе и в мире уже будет насчитываться 67 и 629 млн больных соответственно, т. е. распространенность данной нозологии возрастет на 16 и 48% соответственно. Согласно данным отечественной статистики, в 2015 г. СД в нашей стране страдал 1 308 751 человек, при этом у 7 из 10 пациентов на момент диагностики заболевания уровень гликозилированного гемоглобина (HbA1c) превышал 9%. Кроме того, при подтверждении диагноза СД многие больные имели самые разнообразные осложнения: 26% – периферическую нейропатию, 17% – прогрессирующую ретинопатию, 6,5% – нефропатию, 4,3% находились на диализе, а 12% пациентов предпринимали безуспешные попытки справиться с язвой нижних конечностей.
В соответствии со Стандартами медицинской помощи при СД (2019), утвержденными Американской диабетической ассоциацией (American Diabetes Association, ADA), диабет классифицируют на следующие основные категории: СД 1 типа (обусловленный аутоиммунной деструкцией β-клеток, как правило, приводящей к абсолютному дефициту инсулина), СД 2 типа (ассоциированный с прогрессирующим снижением секреции β-клетками инсулина, зачастую развивающийся на фоне инсулинорезистентности), гестационный СД и специфические типы диабета (MODY‑диабет молодых, диабет, обусловленный заболеванием экзокринной части поджелудочной железы, лекарственно или химически индуцированный диабет).
Скрининг и диагностика СД, в отличие от таковых при ожирении, предполагают проведение лабораторного исследования для определения уровня глюкозы крови натощак, HbA1c; выполнение теста на толерантность к углеводам; установление концентрации С‑пептида, иммунореактивного инсулина, фруктозамина, глюкозурии; расчет индекса НОМА и выявление антител к клеткам поджелудочной железы (GADA, IAA). В норме основные показатели неизменного углеводного обмена имеют следующие значения: гликемия натощак – <5,6 ммоль/л, постпрандиальная гликемия – <7,8 ммоль/л, HbA1c – <5,6%. Заподозрить наличие СД следует у лиц старше 45 лет, а также у пациентов моложе 45 лет, имеющих хотя бы один фактор риска возникновения диабета. Общепризнанными факторами риска СД 2 типа являются уровень гликемии натощак 5,6-6,9 ммоль и/или постпрандиальной гликемии 7,8-11,0 ммоль/л, HbA1c >5,7%. Риск возникновения этого метаболического заболевания значительно возрастает при наличии наследственной предрасположенности и сопутствующей патологии: артериальной гипертонии, ишемической болезни сердца, нарушении липидного обмена (дислипидемии) и высоком ИМТ (>25 кг/м2). Крайне высок риск развития СД 2 типа у женщин, имеющих детей, масса тела которых при рождении превышала 4 кг, а также у пациенток, страдавших гестационным СД, поликистозом яичников.
Критерии диагностики СД достаточно просты: констатировать наличие этой патологии можно при уровне гликемии натощак в плазме венозной крови >7,0 ммоль/л, либо при определении содержания глюкозы в крови >11,1 ммоль/л, либо при концентрации HbA1c >6,5%. Примечательно, что наличие разнообразных классических симптомов не обязательно для подтверждения диагноза СД: типичные признаки нарушенного углеводного обмена (сухость во рту, жажда, полифагия, полиурия, головная боль, трудность концентрации внимания, неясность зрения, апатия, зуд кожи, слабость) могут практически отсутствовать или беспрерывно беспокоить пациентов. В ряде случаев расставить все точки над «i» помогает пероральный глюкозотолерантный тест (ПГТТ), перед проведением которого не следует менять привычный пищевой рацион или увеличивать физическую активность. Согласно хорошо известной методике проведения ПГТТ, уровень гликемии определяют двукратно – натощак и спустя 2 ч после приема 75 г глюкозы. Залогом получения достоверных результатов ПГТТ является соблюдение пациентом одного значимого условия: во время проведения исследования необходимо избегать физической активности.
В связи с высоким ростом распространенности СД в настоящее время большое внимание уделяют диагностике предиабета – нарушения углеводного обмена, ассоциированного с высоким риском развития СД при значениях гликемии, недостаточных для установления диагноза СД. Предиабет характеризуется нарушением гликемии натощак и/или нарушением толерантности к глюкозе (табл. 2).
Несмотря на кажущуюся безобидность, предиабет предрасполагает к возникновению СД: спустя 10 лет после выявления нарушения толерантности к глюкозе у 50% пациентов диагностируют СД, у 25% больных сохраняется нарушенная переносимость глюкозы, в остальных 25% случаев значения этого теста соответствуют нормативным показателям. При ведении больных СД следует тщательно контролировать уровень HbA1c, оптимальные значения которого должны быть <7%; также необходимо учитывать концентрацию гликемии натощак (4,4-7,2 ммоль/л) и после приема пищи (<10,0 ммоль/л). Выполнение ПГТТ и определение глюкозурии у лиц, страдающих СД, не являются значимыми и целесообразными.
Проведение скрининга предиабета показано и в педиатрической популяции, особенно у детей с избыточным весом, имеющих ≥2 следующих факторов риска: отягощенная наследственность по СД у родственников первой/второй линии родства, принадлежность к расе / этнической группе высокого риска, наличие признаков инсулинорезистентности или состояний, ассоциированных с инсулинорезистентностью, гестационный СД у матери. При выявлении вышеперечисленных факторов следует контролировать вышеуказанные гликемические показатели начиная с 10-летнего возраста либо после наступления половой зрелости; проводить такой скрининг необходимо каждые 3 года.
Лечение и профилактика
Терапия ожирения основывается на нескольких фундаментальных положениях: рационализации питания с уменьшением его калорийности, увеличении двигательной активности, дополнительной фармакологической терапии, проведении бариатрических вмешательств с обязательной психологической поддержкой.
Современные подходы к терапии СД 2 типа разработаны с учетом разнообразных патогенетических механизмов возникновения этого заболевания: нарушения секреции инсулина, снижения инкретинового эффекта, увеличения липолиза и реабсорбции глюкозы, уменьшения поглощения глюкозы, дисфункции нейротрансмиттеров, роста продукции глюкозы печенью и возрастания секреции глюкагона. Основополагающими вехами в развитии СД являются нарушение секреции инсулина вследствие уменьшения количества и/или нарушения функции β-клеток, возникновение инсулинорезистентности с последующим снижением поглощения глюкозы тканями под влиянием инсулина.
В настоящее время во всем мире больным СД назначают несколько групп гипогликемических препаратов, за исключением инсулина: бигуаниды (метформин), производные сульфонилмочевины (гликлазид MR, глибенкламид, глимепирид), глиниды – препараты, воздействующие на постпрандиальную гликемию (репаглинид), ингибиторы α-глюкозидазы (воглебоза), тиазолидиндионы (пиоглитазон), агонисты глюкагоноподобного пептида-1 (лираглутид), ингибиторы дипептидилпептидазы-4 (саксаглиптин, ситаглиптин, вилдаглиптин), ингибиторы натрийзависимого котранспортера глюкозы 2 типа (дапаглифлозин, эмпаглифлозин). Несмотря на такое разнообразие имеющихся сахароснижающих средств, в 2018 г. эксперты ADA и Европейской ассоциации по изучению диабета (EASD) представили новое руководство по лечению гипергликемии у больных СД, в котором четко определили оптимальный препарат для проведения гипогликемической терапии первой линии – метформин.
Метформин
Назначение этого медикамента максимально соответствует провозглашенным целям терапии СД, позволяя предотвратить возникновение осложнений, оптимизировать качество жизни, а также выбрать терапию с учетом наличия сопутствующей патологии (ожирения, сердечно-сосудистых заболеваний, хронической болезни почек). Эксперты ADA и EASD сделали выбор в пользу метформина, учитывая эффективность фармакотерапии в отношении снижения уровня гликемии, а также уделяя большое внимание безопасности лечения и принимая во внимание риск возникновения гипогликемии, влияние препарата на массу тела, возможность его применения при наличии сопутствующих кардиоваскулярных заболеваний, нарушенной функции почек и печени. Доказано, что назначение метформина позволяет не только уменьшить инсулинорезистентность, уровень гликемии, но и снизить интенсивность перекисного окисления липидов, воспалительного процесса, конечных продуктов избыточного гликозилирования, улучшить состояние и функционирование эндотелия, повысить фибринолиз, достичь улучшения микроциркуляции и липидного профиля.
Метформин является препаратом выбора для коррекции гликемии у лиц с сопутствующим ожирением. Предпочтительность назначения метформина, подчеркиваемая в руководствах ADA (2019) и ADA/EASD (2018), основывается на результатах многочисленных рандомизированных контролированных исследований, а также на данных систематических обзоров и метаанализов. Доказано, что 16-недельная терапия метформином ассоциируется с плавным постепенным снижением массы тела начиная с 4-й недели терапии. При этом максимальный эффект в отношении коррекции массы тела развивается у больных СД с сопутствующим ожирением, тогда как у пациентов с нормальным/низким ИМТ влияние метформина на данный показатель признано недостоверным.
В обновленном практическом руководстве ААСЕ/АСЕ «Всеобъемлющий алгоритм лечения СД 2 типа» (2016) значится: «Метформин имеет низкий риск гипогликемии, способствует незначительному снижению массы тела, имеет хорошую антигипергликемическую эффективность в дозе 2000-2500 мг/сут. Метформин характеризуется лучшим профилем кардиоваскулярной безопасности». Поэтому данный гипогликемический препарат следует в первую очередь назначать пациентам с сопутствующей кардиоваскулярной патологией.
Наличие хронической болезни почек не является противопоказанием к назначению метформина, за исключением прогрессирующего течения заболевания: эксперты ААСЕ рекомендуют воздержаться от его применения при 3В, 4 или 5 стадии. В таких случаях необходимо руководствоваться значениями расчетной скорости клубочковой фильтрации (СКФ) (табл. 3).
Согласно положениям документа ADA/EASD (2018), специалистам следует избегать клинической инерции, а при недостижении целевого уровня НbА1с спустя 3-6 мес лечения метформином необходимо назначить еще одно гипогликемическое средство. В случае если концентрация НbА1с превышает целевые значения на 1,5%, эксперты рекомендуют перейти к ранней комбинированной терапии.
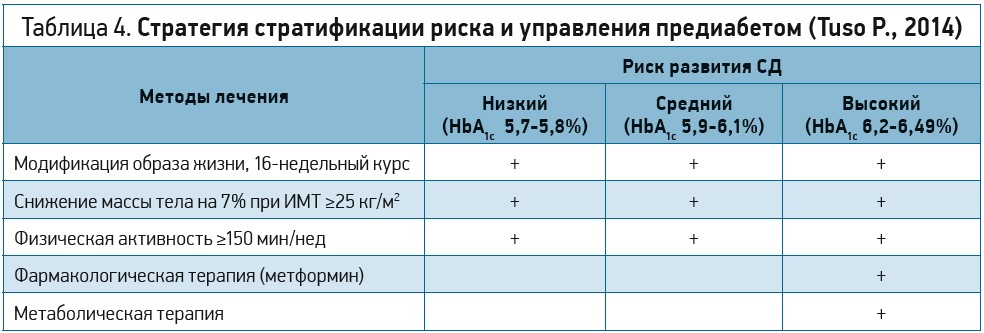
Особое внимание следует уделить профилактическим свойствам метформина. В исследовании DPP зафиксированы впечатляющие факты: заболеваемость СД в группе лиц, принимавших метформин, была на 31% ниже по сравнению с таковой на фоне плацебо (p <0,001). Помимо этого факта, результаты двух исследований DPP и DPPOS убедительно продемонстрировали статистически значимое замедление развития СД у пациентов из группы высокого риска возникновения данной патологии. Максимального эффекта можно добиться при комбинированном вмешательстве: сочетанная модификация образа жизни и назначение метформина позволяют отсрочить возникновение СД как минимум на 10 лет. Авторы исследования DPPOS подчеркнули сопоставимую эффективность метформина и модификации образа жизни в предотвращении повышения глюкозы плазмы натощак и HbA1c. Именно метформин используется для фармакологической терапии предожирения (табл. 4).
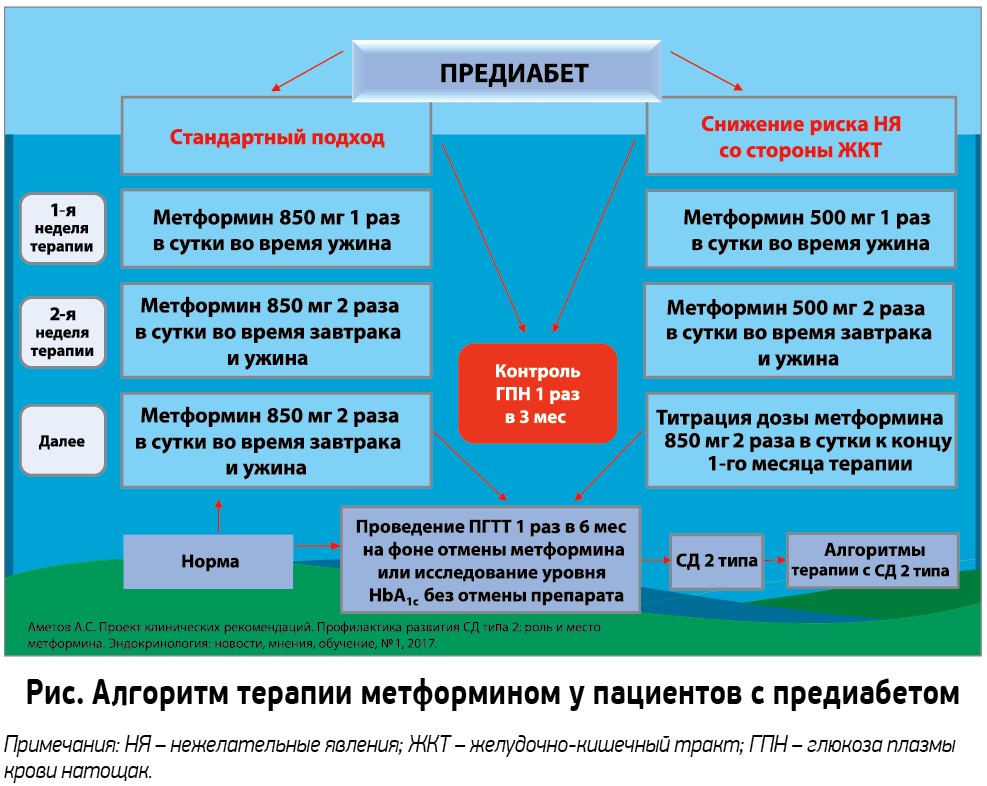
Существует несколько способов назначения метформина (препарата Глюкофаж) при предиабете: хорошо известный стандартный поход и относительно новый метод, направленный на предотвращение возникновения нежелательных явлений со стороны желудочно-кишечного тракта (рис.).
Пациентам с предиабетом, как правило, рекомендуют монотерапию метформином (препаратом Глюкофаж): обычная доза составляет 1000-1700 мг/сут, разделенная на два приема. В данном случае прием метформина следует сочетать с регулярным гликемическим контролем для оценки необходимости дальнейшего применения препарата.
Таким образом, в борьбе с эпидемией ожирения и СД большая роль отводится определению ИМТ и скринингу предиабета – мероприятиям, которые осуществляют семейные врачи. Эффективная терапия СД 2 типа и его безопасная профилактика ассоциируются с применением хорошо изученного лекарственного стредства – метформина (препарата Глюкофаж), занимающего в настоящее время лидирующие позиции в введении как СД 2 типа, так и предиабета.
UA-GLUC-PUB-062019-020
Медична газета «Здоров’я України 21 сторіччя» № 11 (456), червень 2019 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
Нещодавні дослідження показали, що прогноз за різних поширених захворювань, ендокринних, автоімунних розладів і навіть прогресування раку пов’язані з концентрацією вітаміну D у плазмі. Завдяки експресії гена 1α-гідроксилази (CYP27B1) клітини імунної системи (В-, Т- та антигенпрезентувальні клітини) здатні продукувати активний метаболіт кальциферол – речовину з імуномодулювальними властивостями. Рецептори до вітаміну D (vitamin D receptor, VDR) експресують на поверхні імунних клітин. Доведено зв’язок між поліморфізмом генів VDR або CYP27B1 і патогенезом автоімунних ендокринних захворювань. Метою огляду є вивчення впливу вітаміну D, наслідків його дефіциту та корисної ролі добавок із ним при деяких ендокринних розладах, які часто спостерігають у клінічній практиці. ...
Збудник COVID‑19, SARS-CoV‑2, з яким людство вперше стикнулося у 2019 р., поширився по всьому світу, заразивши мільйони людей. Сьогодні, через тягар війни та економічної нестабільності, тема COVID‑19 не сприймається так гостро, як ще кілька років тому, хоча насправді вона не втратила своєї актуальності. Саме сучасному стану проблеми COVID‑19 у світі та в Україні була присвячена доповідь директора ДУ «Інститут ендокринології та обміну речовин імені В.П. Комісаренка НАМН України», академіка Національної академії медичних наук України, члена-кореспондента НАН України, віце-президента НАМН України, президента Асоціації ендокринологів України, професора Миколи Дмитровича Тронька під час першого у 2024 р. засідання науково-освітнього проєкту «Школа ендокринолога», яке відбулося 20-24 лютого. ...
Протягом останніх 60 років метформін є найпоширенішим цукрознижувальним засобом і рекомендований як препарат першої лінії для осіб з уперше виявленим цукровим діабетом (ЦД) 2 типу. Сьогодні понад 200 млн осіб із ЦД 2 типу в усьому світі щодня застосовують метформін як монотерапію або в комбінації. Препарат усе частіше використовують для лікування гестаційного ЦД та в пацієнтів із синдромом полікістозних яєчників. ...
Двадцять восьмого лютого 2024 року виповнилося 80 років від дня народження директора ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (далі – Інститут), віцепрезидента НАМН України, академіка НАМН України, члена-кореспондента НАН України, заслуженого діяча науки та техніки, лауреата Державної премії України, доктора медичних наук, професора Миколи Дмитровича Тронька....