Регуляция адренергического тонуса как фундаментальная предпосылка эффективной антигипертензивной терапии: ключевая роль бета-блокаторов
Место бета-адреноблокаторов (БАБ) в лечении пациентов с артериальной гипертензией (АГ) не раз становилось предметом дискуссий. С появлением ингибиторов ангиотензинпревращающего фермента (ИАПФ), антагонистов кальция (АК), блокаторов рецепторов ангиотензина II (БРА) БАБ и диуретики как традиционные средства стали отходить на второй план и получили роль препаратов сравнения.
При детальном изучении отдельных форм АГ исследователи часто задавались вопросом: а есть ли вообще место для БАБ в терапии АГ?
Позиции БАБ в современных экспертных рекомендациях
В рекомендациях Национального института совершенствования клинической практики Великобритании (NICE) по лечению взрослых пациентов с АГ [2] указано, что БАБ не являются предпочтительными препаратами для терапии АГ, однако их можно применять у пациентов более молодого возраста, особенно:
– при непереносимости или наличии противопоказаний к приему ИАПФ или БРА;
– у женщин детородного возраста;
– у лиц с признаками повышенной симпатической активности.
Что касается последней категории, то таких пациентов – значительное количество. В остальных случаях БАБ рекомендованы в качестве четвертого препарата в комбинации при резистентной АГ. Если терапия начинается с БАБ, и требуется присоединение еще одного антигипертензивного препарата, то вторым препаратом должен быть АК (предпочтение перед тиазидными диуретиками) для снижения риска развития сахарного диабета.
Вместе с тем следует отметить, что рекомендации NICE формируются не только на основании доказательств эффективности и безопасности, но и с учетом фармакоэкономических данных. ИАПФ и АК обеспечивают высокую эффективность, но являются относительно дорогостоящими. Диуретики при достаточно высокой эффективности характеризуются самой низкой стоимостью. Поэтому, исходя из фармакоэкономического анализа, составители рекомендаций NICE 2011 года сделали вывод о том, что антигипертензивная терапия должна основываться на назначении ИАПФ, АК и диуретиков, а БАБ следует переместить на третье-четвертое место.
Американские эксперты в данном вопросе занимают противоречивую позицию. В рекомендациях восьмого Объединенного национального комитета (JNC8) [3] в качестве препаратов первой линии для общей неафроамериканской популяции, включая лиц с сахарным диабетом, предписано начинать терапию с тиазидного диуретика, АК, ИАПФ или БРА (рекомендация умеренной силы – уровень доказательств B). БАБ же не рекомендованы на основании результатов исследования LIFE, в котором на фоне терапии БАБ (атенололом) было зарегистрировано большее количество событий комбинированной конечной точки (сердечно-сосудистая смерть, инфаркт миокарда (ИМ) или инсульт), чем при приеме БРА, преимущественно за счет инсультов. Однако в том же документе указано, что в других сравнительных исследованиях БАБ не отличались от представителей рекомендованных классов первой линии по эффективности, или же данных недостаточно, чтобы сопоставить клинические эффекты.
Рекомендации Европейского общества кардиологов [4] и Национальные украинские рекомендации по лечению АГ ставят БАБ в один ряд с другими препаратами первой линии (ИАПФ, БРА, АК и диуретиками) и предлагают их для начала или продолжения лечения АГ в режиме монотерапии или в комбинациях (класс рекомендаций І, уровень доказательств А).
В последние годы велись дискуссии об ограничении применения БАБ у пациентов с хронической ишемической болезнью сердца (ИБС) и перенесенным ИМ. Активное обсуждение в научном сообществе вызвала публикация результатов обсервационного исследования S. Bangalore и соавт. [5]. Сопоставление исходов при продленном наблюдении за тремя когортами пациентов из регистра REACH (перенесенный ИМ, 14 043 пациента; диагноз ИБС без ИМ, n=12012 и только факторы риска ИБС, n=18653) показало, что применение БАБ не ассоциировалось со снижением риска наступления комбинированной конечной точки (сердечно-сосудистая смерть, нефатальный ИМ или нефатальный инсульт). Авторы исследования отметили, что полученные результаты согласуются с действующими рекомендациями Американской ассоциации сердца и Американского колледжа кардиологов по вторичной профилактике у пациентов с ИБС. Терапия БАБ настоятельно рекомендуется (класс рекомендаций І) для лечения пациентов с сердечной недостаточностью (СН), ИМ или острым коронарным синдромом (ОКС) длительностью до 3 лет после перенесенного ИМ, но более продолжительная терапия получила рекомендацию класса ІІа [6]. Кроме того, рекомендация по применению БАБ у всех остальных пациентов с коронарными и другими сосудистыми заболеваниями была понижена до класса ІІb. Подобным образом в европейских рекомендациях по вторичной профилактике длительная терапия БАБ рекомендуется только у пациентов со сниженной систолической функцией левого желудочка – ЛЖ (класс рекомендаций І) [7].
Вместе с тем сами же авторы исследования отмечают отсутствие данных о том, какие именно БАБ назначались пациентам в рамках регистра REACH. Рекомендации по выбору конкретных БАБ есть только в отношении пациентов с СН, но не с АГ. В период проведения исследования S. Bangalore и соавт. вторым БАБ по частоте назначений в США был атенолол – не лучший вариант для длительной терапии, который в настоящее время не рекомендован даже больным, перенесшим ОКС, после публикации результатов классического метаанализа N. Freemantle еще в конце 1990-х годов [8].
Симпатическая гиперактивация: от ранней стадии АГ до ремоделирования сердца
Не вызывает сомнения физиологическая роль автономной нервной системы в регуляции сердечно-сосудистых функций и контроле артериального давления (АД), как в состоянии покоя, так и при адаптивном ответе на действие средовых стимулов. Одной из самых очевидных и признанных в кардиологии является гипотеза о том, что происхождение, прогрессирование и исходы АГ связаны с дисфункцией автономного контроля сердечно-сосудистой системы, и особенно с аномальной активацией симпатического отдела [9]. Эта гипотеза была подтверждена в экспериментальных и клинических исследованиях. Прямые доказательства ранней активации симпатической нервной системы (СНС) получены в исследованиях у лиц с высоким нормальным АД, с АГ в молодом возрасте, со скрытой АГ, с АГ «белого халата».
Аномально высокие уровни циркулирующих в крови адренергических нейротрансмиттеров – норэпинефрина и эпинефрина – были выявлены в нескольких исследованиях у нормотензивных детей и подростков с семейным анамнезом АГ [10].
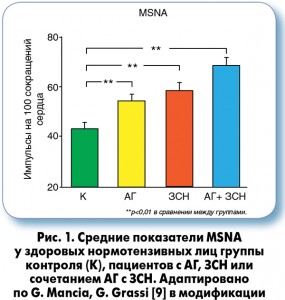
Надежным методом оценки симпатического тонуса является измерение мышечной активности симпатического нерва – muscle sympathetic nerve activity (MSNA), которое стало относительно доступным после появления современных усовершенствованных методов оценки. Сегодня это разновидность микронейрографии с регистрацией импульсов в постганглионарных симпатических волокнах соматических нервов, например n. peroneus, в состоянии покоя и при активации барорефлексов. В исследовании G. Seravalle и соавт. [11] показано достоверное усиление MSNA у лиц с высоким нормальным АД по отношению к лицам с нормальным или оптимальным АД: 51,3±2,0 против 40,3±2,3 и 41,1±2,6 импульса на 100 сокращений сердца соответственно; р<0,01. И это усиление симпатической активности, по мнению авторов, может быть вовлечено наряду с другими факторами в прогрессирование состояния от прегипертензии до клинически явной АГ.
Подобная закономерность наблюдалась в микронейрографических исследованиях у пациентов со скрытой АГ и АГ «белого халата»: амплитуда и частота вспышек активности симпатического нерва были достоверно выше по сравнению с нормотензивным контролем [12-14].
Что касается стадий АГ с поражением органов-мишеней, то усиление влияния СНС убедительно доказано у пациентов, у которых развивается гипертрофия ЛЖ или застойная СН (ЗСН) [15, 16]. Самый высокий тонус СНС наблюдался у пациентов с комбинацией АГ и ЗСН (рис. 1).
В исследовании G. Grassi и соавт. [17] впервые было показано достоверное усиление MSNA у пациентов с нелеченной АГ и диастолической дисфункцией ЛЖ (+28,9%; р<0,05 по сравнению с лицами с сопоставимым повышением АД, но без диастолической дисфункции). Обсуждается, что симпатическая гиперактивация, которая предположительно связана с нарушением барорефлексов, может обусловливать повышение сердечно-сосудистого риска у пациентов с диастолической СН.
Прямые и непрямые показатели нейроадренергической функции указывают на роль гиперактивации СНС в развитии и прогрессировании почечной недостаточности у пациентов с АГ. G. Grassi и соавт. [18] продемонстрировали достоверную обратную корреляцию между снижением скорости клубочковой фильтрации (СКФ) и показателем MSNA (r=-0,59; p<0,0001).
Наконец, получены данные о том, что устойчивая к терапии АГ также является состоянием симпатической гиперактивации, более выраженной по магнитуде, чем у пациентов с контролируемой АГ [19]. В исследовании у пациентов среднего возраста (58,6±2,1 года) с резистентной АГ, которые принимали в среднем по 4,6±0,3 антигипертензивных препарата, показатели АД были достоверно выше (172,2±1,7/100,7±1,2 мм рт. ст.), чем у нормотензивных лиц группы контроля (132,1±1,3/82,1±0,9 мм рт. ст.) и у лиц с контролируемой АГ (135,5±1,2/83,6±0,9 мм рт. ст.; р<0,01). Это сопровождалось достоверным повышением показателя MSNA, скорректированного по частоте сердечных сокращений (ЧСС): 87,8±2,0 против 46,8±2,6 и 59,3±1,7 импульса на 100 сокращений сердца соответственно (р<0,01). По данным регрессионного анализа повышение MSNA, наблюдаемое у пациентов с резистентной АГ, достоверно ассоциировалось с гемодинамическими, гормональными и метаболическими переменными, включая уровни альдостерона в плазме. Таким образом, нарушенные барорефлекторные механизмы наряду с гемодинамическими и нейрогуморальными факторами могут лежать в основе феномена резистентной АГ.
В настоящее время доказана не только ключевая роль симпатической гиперактивации в патогенезе АГ, но и прямое негативное влияние на прогноз. В нескольких исследованиях у разных категорий пациентов хроническая СН (ХСН), почечная недостаточность, инсульт) показано увеличение смертности и частоты неблагоприятных сердечно-сосудистых событий при повышении уровня различных маркеров активации СНС – норэпинефрина в плазме, норэпинефрина в миокарде и показателя MSNA [9].
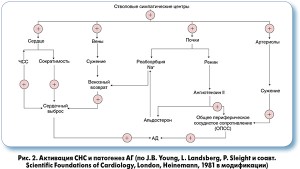
Основным эффектом БАБ является защита органов-мишеней от симпатической гиперактивации, которой, по современным представлениям, отводится главная роль в патогенезе эссенциальной АГ (рис. 2). В свете вышеизложенного представляется рациональной идея раннего включения БАБ в базисную терапию АГ с целью хронического подавления СНС и улучшения прогноза.
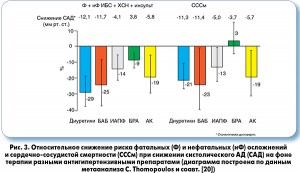
По данным недавно опубликованного метаанализа 68 рандомизированных контролируемых исследований [20], терапия БАБ не уступала по влиянию на смертность и частоту наступления нефатальных конечных точек сердечно-сосудистого континуума терапии другими антигипертензивными препаратами по сравнению с плацебо (рис. 3). В пяти исследованиях с участием в общей сложности более 18 тыс. пациентов БАБ достоверно снижали частоту развития инсультов (на 23%), ИБС (на 12%) и сердечно-сосудистую смертность (на 15%).
По данным двух исследований, на фоне приема БАБ на 43% уменьшился риск развития СН. Авторы метаанализа сделали выводы в пользу традиционной точки зрения: снижение АД, независимо от того, какими препаратами оно достигается, приводит к уменьшению частоты осложнений. БАБ, как и другие антигипертензивные препараты, положительно влияют на прогноз.
Симпатическая активация и риск развития фибрилляции предсердий
Автономная нервная система, особенно баланс адренергического/холинергического тонуса, оказывает отчетливое влияние на риск развития фибрилляции предсердий (ФП). В предсердиях катехоламины могут изменить любой из электрофизиологических механизмов инициации и поддержания ФП. Катехоламины могут вызвать мембранные потенциалы в фазу после деполяризации, усиливая ток ионов Ca2+ и влияя на последующий обмен Na+-Ca2+, а также усиливая автоматизм. Они также могут влиять на механизм re-entry, изменяя возбудимость и проводимость в большей мере, чем терминальную реполяризацию или рефрактерный период. До сих пор не ясно, какие из механизмов являются доминирующими в развитии ФП. Вероятно, это зависит от конкретного заболевания сердца и адренергического тонуса. Например, известно, что СН как основная причина ФП вызывает адренергическую активацию и адаптационные изменения – электрофизиологическое ремоделирование предсердий, нарушения кальциевого гомеостаза [21].
БАБ применяются для лечения пациентов с ФП преимущественно в рамках стратегии контроля частоты желудочковых сокращений за счет эффекта замедления атриовентрикулярного проведения. Однако БАБ также способны уменьшать частоту развития ФП, особенно у пациентов с СН или после операций на сердце, когда адренергический тонус повышен. Постоянная терапия БАБ ремоделирует предсердия, увеличивая рефрактерный период, что сопряжено с антиаритмическим действием. Более того, механизмы подавления ФП под действием БАБ могут ассоциироваться с угнетением аритмогенного тока Ca2+ в совокупности с эффектами адаптации к терапии. Лучшее понимание контроля и вовлечения адренергической системы в базовые механизмы развития ФП при разных заболеваниях сердца может способствовать оптимизации терапии [21].
В рекомендациях Европейского общества кардиологов по лечению ФП в разделе «Фармакологический контроль ритма» указано, что БАБ могут быть особенно полезными при высоком адренергическом тонусе или симптомной ишемии миокарда, которые часто ассоциируются с ФП. Постоянная терапия БАБ в ряде исследований показала себя как эффективная и безопасная в сравнении с плацебо и дигоксином. В крупном исследовании AFFIRM БАБ успешно применялись для жесткого контроля ритма [22].
Другие антигипертензивные препараты также могут влиять на риск развития ФП. Предполагается, что блокаторы ренин-ангиотензиновой системы (РАС) обладают преимуществами, обусловленными их влиянием на предсердное ремоделирование. Вместе с тем некоторые данные указывают на сопоставимый эффект снижения риска развития ФП у пациентов с АГ на фоне длительного приема БАБ. Так, в исследовании по типу «случай-контроль» проанализированы данные 4661 пациента с ФП и 18 642 больных, подобранных по характеристикам лиц контрольной группы из популяции более 680 тыс. пациентов, получающих лечение АГ у врачей первичной практики в Великобритании [23]. Анализ проводился с целью сравнения риска развития ФП среди гипертоников, которые принимали ИАПФ, БРА или БАБ, с референтной группой пациентов, получавших АК (АК выбраны для сравнения, поскольку способны усиливать симпатическую активацию). В результате снижение риска получено во всех подгруппах по сравнению с терапией только АК:
– ИАПФ – отношение шансов (ОШ) 0,75; 95% доверительный интервал (ДИ) от 0,65 до 0,87;
– БРА – ОШ 0,71; ДИ 0,57-0,89;
– БАБ – ОШ 0,78; ДИ 0,67-0,92.
Таким образом, длительная терапия БАБ обеспечивает такой же профилактический эффект в отношении развития ФП, как и блокаторы РАС.
Наименее связанным с адренергической стимуляцией долгое время считается процесс фиброза миокарда, неразрывно связанный с длительным существованием АГ с последующим возникновением СН с сохраненной фракцией выброса (сФВ). Хотя ни один из классических нейромодулирующих классов препаратов в лечении АГ не продемонстрировал столь же явных прогностических успехов в терапии СН с сФВ, БАБ традиционно исключаются из этого перечня, уступая дорогу модуляторам РАС, поскольку они прямо подавляют профибротический потенциал ангиотензина II и альдостерона. Однако картина патогенеза кардиального фиброза, судя по последним фундаментальным данным 2016 года [24], значительно отличается от устоявшегося моновекторного подхода. Известно, что хроническая стимуляция симпато-адреналовой системы ведет не только к гипертрофии миокарда, но и к фиброзу. Умеренная стимуляция β2-адренорецепторов повышает уровень цАМФ, подавляя синтез и секрецию различных форм коллагена. Кроме того, такая стимуляция ингибирует преобразование кардиальных фибробластов в миофибробласты, индуцируемое мощным профибротическим цитокином TGF β. Иным недавно открытым механизмом является усиление продукции β-аррестина, особенно в сердцах лиц с АГ и начальной систолической дисфункцией ЛЖ. Таким образом, мы опять возвращаемся к концепции селективной β1-блокады с сохранением физиологических колебаний в стимуляции β2-адренорецепторов, что достигается назначением селективных β1-БАБ, в частности того же бисопролола (Конкор).
В настоящее время ученые работают над терапевтической стратегией селективного подавления данных цитокинов, однако прием множества препаратов узконаправленного действия – это зачастую прямой путь скорее к полипрагмазии, чем к приверженности к клинически эффективной полипотентной базисной терапии, хотя индивидуально он, несомненно, будет эффективен при правильной стратификации больных.
В заключение следует перечислить клинические состояния и сопутствующие заболевания у пациентов с АГ, при которых терапия БАБ обеспечивает доказанные преимущества или не имеет альтернативы:
• перенесенный ИМ;
• стенокардия;
• тахикардия;
• все формы ФП (пароксизмальная, персистирующая, постоянная);
• ХСН с систолической дисфункцией;
• глаукома;
• беременность (в первую очередь бисопролол);
• ОКС;
• тиреотоксикоз и заместительная терапия тиреоидными гормонами при наличии АГ;
• мигрень;
• эссенциальный тремор;
• периоперационная АГ;
• избыточный прессорный ответ на нагрузку и стресс (гиперреактивность СНС);
• ортостатическая АГ;
• аневризма аорты;
• после аортокоронарного шунтирования.
При лечении АГ достижение эффекта во многих случаях зависит от применения комбинации препаратов. У всех препаратов есть преимущества и недостатки, требующие индивидуализации терапии. Что касается роли БАБ в лечении пациентов с АГ, то на основании рассмотренной доказательной базы можно сделать следующие выводы.
– Исходя из современных представлений о патогенезе эссенциальной АГ, подавление симпатической гиперактивации путем раннего назначения БАБ является фундаментальной предпосылкой эффективной антигипертензивной терапии.
– Назначение БАБ, в том числе в качестве стартовой терапии АГ, имеет под собой убедительную доказательную базу, в том числе в отношении влияния на прогноз и выживаемость пациентов, и рекомендуется Европейским обществом кардиологов наряду с другими препаратами первой линии.
– В ряде клинических ситуаций, таких как сочетание АГ с ИБС, ХСН, патологией щитовидной железы, БАБ обладают неоспоримыми преимуществами.
– Применение кардиоселективных БАБ, таких как бисопролол (Конкор), позволяет избежать побочных эффектов, связанных с периферической блокадой β2-адренорецепторов.
Литература
1. Воронков Л.Г. Пацієнт із ХСН в Україні: аналіз даних популяції пацієнтів, обстежених у рамках першого національного зрізового дослідження UNIVERS / Л.Г. Воронков // Серцева недостатність. – 2012. – № 1 (1). – С. 8-13.
2. Hypertension in adults: diagnosis and management // NICE guidelines [CG127]. – 2011 [Електронний ресурс]. – Режим доступу: https://www.nice.org.uk/guidance/cg127/chapter/1-Guidance.
3. 2014 Evidence-Based Guideline for the Management of High Blood Pressure in Adults. Report From the Panel Members Appointed to the Eighth Joint National Committee (JNC8) / [P.A. James, S. Oparil, B.L. Carter et al.] // JAMA. – 2013. – № 311. – P. 507-520.
4. 2013 ESH/ESC guidelines for the management of arterial hypertension: the Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) / [G. Mancia, R. Fagard, K. Narkiewicz et al.] // Eur Heart J. – 2013. – № 34. – P. 2159-2219.
5. β-Blocker use and clinical outcomes in stable outpatients with and without coronary artery disease / [S. Bangalore, G. Steg, P. Deedwania et al.] // JAMA. – 2012. – № 308. – P. 1340-1349.
6. AHA/ACCF Secondary Prevention and Risk Reduction Therapy for Patients with Coronary and other Atherosclerotic Vascular Disease: 2011 update: a guideline from the American Heart Association and American College of Cardiology Foundation / [S.C. Smith, E.J. Benjamin, R.O. Bonow et al.] // Circulation. – 2011. – № 124. – P. 2458-2473.
7. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: The Task Force for the management of acute coronary syndromes (ACS) in patients presenting without persistent ST-segment elevatio / [C.V. Hamm, J.P. Bassand, S. Agewall et al.] // Eur Heart J. – 2011. – № 32. – P. 2999-3054.
8. beta Blockade after myocardial infarction: systematic review and meta regression analysis / [N. Freemantle, J. Cleland, P. Young et al.] // BMJ. – 1999. – № 318. – P. 1730-1737.
9. Mancia G. The autonomic nervous system and hypertension / G. Mancia, G. Grassi // Circ Res. – 2014. – № 114. – P. 1804-1814.
10. Psychosomatic factors in borderline hypertensive subjects and offspring of hypertensive parents. Hypertension / [C. Perini, F.B. Muller, U. Rauchfleisch et al.] // Hypertension. – 1990. – № 16. – P. 627-634.
11. Sympathetic nerve traffic and baroreflex function in optimal, normal, and high-normal blood pressure states / [G. Seravalle, L. Lonati, S. Buzzi et al.] // J Hypertens. – 2015. – № 33. – P. 1411-1417.
12. Sympathetic neural mechanisms in white-coat hypertension / [P.A. Smith, L.N. Graham, A.F. Mackintosh et al.] // J Am Coll Cardiol. – 2002. – № 40. – P. 126-132.
13. Relationship between central sympathetic activity and stages of human hypertension / [P.A. Smith, L.N. Graham, A.F. Mackintosh et al.] // Am J Hypertens. – 2004. – № 17. – P. 217-222.
14. Neurogenic abnormalities in masked hypertension / [G. Grassi, G. Seravalle, F.Q. Trevano et al.] // Hypertension. – 2007. – № 50. – P. 537-542.
15. Hypertensive left ventricular hypertrophy: relation to peripheral sympathetic drive / J.P. Greenwood, E.M. Scott, J.B. Stoker, D.A. Mary // J Am Coll Cardiol. – 2001. – № 38. – P. 1711-1717.
16. Effects of hypertension and obesity on the sympathetic activation of heart failure patients / [G. Grassi, G. Seravalle, F. Quarti-Trevano et al.] // Hypertension. – 2003. – № 42. – P. 873-877.
17. Sympathetic and baroreflex cardiovascular control in hypertension-related left ventricular dysfunction / [G. Grassi, G. Seravalle, F. Quarti-Trevano et al.] // Hypertension. – 2009. – № 53. – P. 205-209.
18. Early sympathetic activation in the initial clinical stages of chronic renal failure / [G. Grassi, F. Quarti-Trevano, G. Seravalle et al.] // Hypertension. – 2011. – № 57. – P. 846-851.
19. Marked sympathetic activation and baroreflex dysfunction in true resistant hypertension / [G. Grassi, G. Seravalle, G. Brambilla et al.] // Int J Cardiol. – 2014. – № 177. – P. 1020-1025.
20. Thomopoulos C. Effects of blood pressure lowering on outcome incidence in hypertension: 4. Effects of various classes of antihypertensive drugs: Overview and meta-analyses / C. Thomopoulos, G. Parati, A. Zanchetti. // Journal of Hypertension. – 2015. – № 33. – P. 195-211.
21. Workman. Cardiac adrenergic control and atrial fibrillation / A.J. Workman // Arch Pharmacol. – 2010. – № 381. – P. 235-249.
22. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC) / [A.J. Camm, P.Kirchhof, G.Y. Lip et al.] // Eur Heart J. – 2010. – № 31. – С. 2369-2429.
23. Risk for incident atrial fibrillation in patients who receive antihypertensive drugs: a nested case-control study / [B.A. Schaer, C. Schneider, S.S. Jick et al.] // Ann Intern Med. – 2010. – № 152. – P. 78-84.
24. Cardiac fibrosis. The fibroblast awakens / [J.G. Travers, F.A. Kamal, J. Robbins et al. // Circ Res. – 2016. – № 118. – P. 1021-1040.
Статья напечатана при содействии
ООО «Такеда Украина».
UA/CVM/0816/0064b
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....