Впровадження міжнародних рекомендацій щодо ведення пацієнтів зі спінальною м’язовою атрофією у клінічну практику
 Спінальна м’язова атрофія (СМА) – тяжке, інвалідизувальне і небезпечне для життя автосомно-рецесивне спадкове захворювання, що перебігає з ураженням рухових нейронів спинного мозку й порушенням функцій різних органів і систем. СМА є основною генетично зумовленою причиною смерті немовлят та дітей молодшого віку. Важливою особливістю СМА є широкий спектр тяжкості клінічних проявів хвороби – від малосимптомних дорослих форм до захворювань новонароджених із неминучим донедавна летальним прогнозом. СМА не супроводжується когнітивними порушеннями.
Спінальна м’язова атрофія (СМА) – тяжке, інвалідизувальне і небезпечне для життя автосомно-рецесивне спадкове захворювання, що перебігає з ураженням рухових нейронів спинного мозку й порушенням функцій різних органів і систем. СМА є основною генетично зумовленою причиною смерті немовлят та дітей молодшого віку. Важливою особливістю СМА є широкий спектр тяжкості клінічних проявів хвороби – від малосимптомних дорослих форм до захворювань новонароджених із неминучим донедавна летальним прогнозом. СМА не супроводжується когнітивними порушеннями.
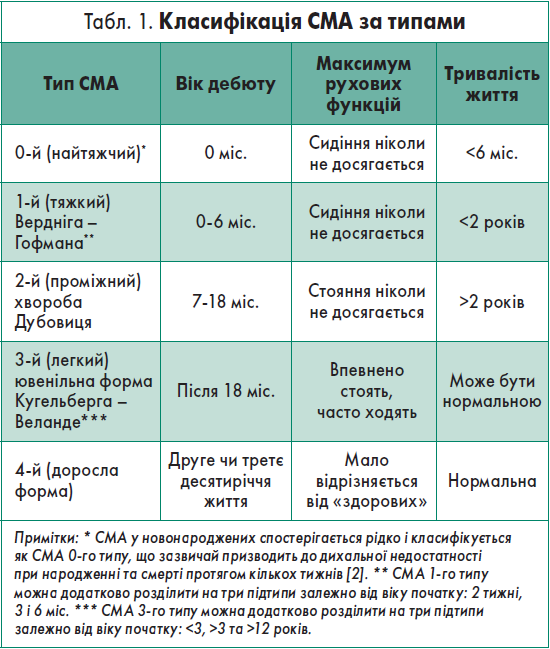
Розрізняють декілька типів перебігу СМА. СМА І типу (або хвороба Вердніга – Гоффмана) маніфестує у віці до шести місяців; діти дуже слабкі вже у перші місяці життя, мають значні труднощі з диханням і ковтанням, прогноз зазвичай несприятливий. СМА ІІ типу дебютує в дитячому віці між 6-м і 18-м місяцями; діти можуть сидіти без сторонньої допомоги, однак ніколи не ходять самостійно. СМА ІІІ типу (або хвороба Кугельберга – Валландера) має м’якший перебіг, маніфестація відбувається після 18 місяців; пацієнти впевнено стоять, часто ходять. СМА ІV типу починається у дорослому віці [1‑6].
Етіологія СМА
Встановлено, що СМА зумовлена зниженням рівня білка SMN (протеїну, що забезпечує виживання мотонейронів) через делеції або точкові мутації в гені виживання мотонейронів SMN1 в екзоні 7, що знаходиться на 5-й парі хромосом 5q13 [1‑3]. У здорових людей ген SMN1 забезпечує продукцію всього необхідного організму білка SMN. При СМА, у зв’язку з пошкодженням гену SMN1, організм хворого використовує лише ген SMN2, на основі якого синтезується біля 90% низькофункціонального нестабільного білка SMN і тільки незначна кількість функціонально повноцінного білка SMN. Його дефіцит є критичним для виживання мотонейронів і чинить негативний ефект на периферичні органи й тканини. Білок SMN у нормі експресується в усіх еукаріотичних клітинах, наявний як у їх ядрах, так і в цитоплазмі та впливає на численні клітинні процеси [1‑4].
Останніми роками продовжує накопичуватися все більше доказів, що дефіцит SMN-білка в інших тканинах та органах має клінічне і патогенетичне значення. Зокрема, виявлені різноманітні структурні й функціональні патологічні зміни у скелетних м’язах, серці та судинах, підшлунковій залозі, печінці, нирках, шлунково-кишковому тракті, кістковій тканині та імунній системі [1‑4].
Діагностування СМА
Встановлення діагнозу СМА базується на клінічній підозрі та підтверджується генетичним тестуванням [7]. Ця клінічна підозра залежить від настороженості медичних працівників. Однак затримка діагностики СМА все ще є значною [8].
Діагностика СМА здійснюється з урахуванням віку початку захворювання та наявних клінічних ознак і симптомів [1‑9]. Процес встановлення діагнозу СМА є відносно легким завдяки поєднанню типових клінічних ознак та симптомів, особливо у пацієнтів зі СМА з дебютом у ранньому дитинстві. Однак часто виникає затримка між появою клінічних ознак та підтвердженням діагнозу при СМА. Затримання встановлення діагнозу може бути тривалим, особливо для пацієнтів, які мають більш легкі, менш специфічні клінічні ознаки та симптоми.
Методи встановлення/підтвердження діагнозу
В основі діагностування СМА лежать молекулярні генетичні аналізи. Генетичне тестування методом мультиплексної лігазної ампліфікації ДНК-зондів (MLPA) чи кількісної полімеразної ланцюгової реакції (кПЛР) із залученням, якщо потрібно, секвенування за Сенгером або наступного покоління належить до обстежень першої лінії при підозрі на СМА, дозволяє виявити делеції та інші мутації у 7-му екзоні 5-ї пари хромосом та підтвердити діагноз. Слід звернути увагу, що за допомогою генетичного тесту тип СМА не визначається. Його встановлюють на основі функціональних можливостей дитини і часу появи перших клінічних симптомів (табл. 1). Клінічний тип СМА визначає лікар-невролог з урахуванням добре зібраного анамнезу, клінічних симптомів і результатів оцінки функціональних можливостей дитини [1‑10].
Скринінг новонароджених
У немовлят, що хворіють на СМА, понад 95% рухових нейронів дегенерують протягом перших шести місяців життя, що свідчить про вузьке терапевтичне вікно [1]. Для таких пацієнтів раннє терапевтичне втручання має вирішальне значення щодо максимізації користі від лікування та порятунку рухових нейронів до прогресування денервації [5, 12, 13]. Цю потребу демонструють дані клінічних випробувань, які підкреслюють переваги якнайшвидшого виявлення СМА [5, 14].
Рання діагностика повинна бути полегшена шляхом СМА-скринінгу новонароджених [13, 14]. Крім того, послідовний висновок у клінічних випробуваннях із вивчення препаратів, що модифікують перебіг хвороби (ХМП), полягає в тому, що лікування виявляє більшу клінічну користь при меншій тривалості СМА [12, 15]. Найзначніші терапевтичні переваги спостерігалися, коли лікування починалося до появи перших клінічних симптомів. Оскільки середній вік діагнозу для СМА із початком при народженні становить приблизно шість місяців, рання діагностика є ключовою для виявлення безсимптомних пацієнтів.
Функціональна класифікація
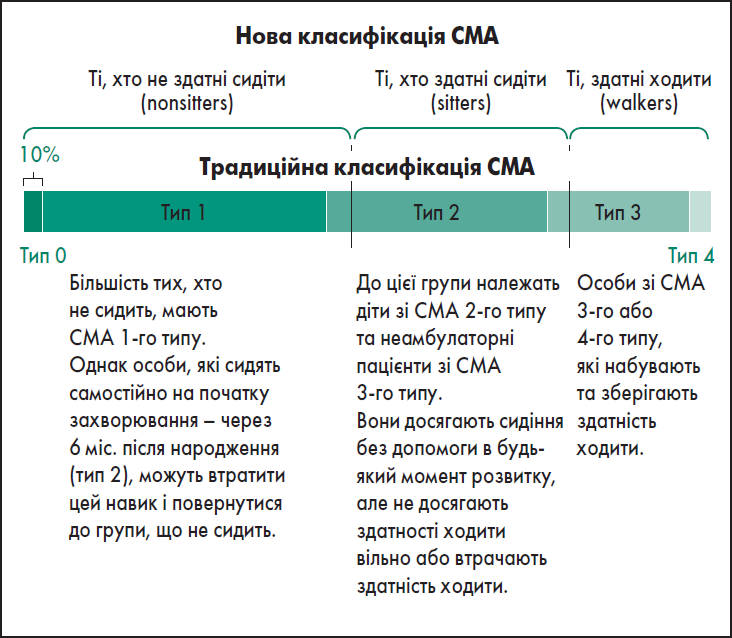
Класифікація підтипів СМА передбачає клінічні фенотипи та прогноз під час діагностики. Однак індивідуальне прогресування захворювання може суттєво відрізнятися від типового сценарію через супутні патології або генотипи. Більш практичним підходом до ведення пацієнтів є розподіл за функціональною класифікацією, тобто поточним станом рухових здібностей: не здатні сидіти (nonsitters), здатні сидіти (sitters), здатні ходити (walkers) (рис. 1) [9, 10].
Рис. 1. Співвідношення клінічної та функціональної класифікацій СМА
Клінічне обстеження при веденні пацієнтів зі СМА включає огляд лікаря, оцінку стану кістково-м’язової системи та пов’язаних з нею функціональних порушень [10]. Обстеження кістково-м’язової системи має відповідати ступеню тяжкості захворювання та включати:
- оцінку трофіки та сили м’язів;
- визначення об’єму й амплітуди рухів у суглобах;
- підрахунок балів за відповідними моторними функціональними шкалами;
- визначення рівня функціональних показників, що відображають повсякденну діяльність, наприклад за шкалою оцінки рівня незалежності (SMAIS).
Функціональні оцінювання слід проводити регулярно. Такий моніторинг дозволить визначити динаміку прогресування хвороби, необхідність змін у веденні пацієнта та відповідь на втручання. Результати індивідуальної оцінки також можуть бути корисними для порівняння з траєкторіями прогресування, про які повідомлялося в останніх дослідженнях [10].
Природний перебіг хвороби
Швидкість прогресування СМА відрізняється залежно від віку та функціональних можливостей [16]. У пацієнтів із раннім початком СМА зазвичай спостерігається швидке прогресування захворювання, тоді як в осіб із більш пізнім початком СМА, які можуть ходити, вона прогресує повільніше [12]. Траєкторія патології у пацієнтів зі СМА останнім часом покращується завдяки активнішому підходу до лікування, навіть у хворих на тяжкі форми СМА.
Еволюція захворювання
Розуміння СМА значно змінилося з часу опису перших випадків захворювань 130 років тому, проведеного Верднігом та Гофманом [10]. У нову еру лікування ХМП виникли проблеми з доступністю медикаментозних методів, які змінюють відомі траєкторії розвитку СМА [10].
Із часу запровадження нових фармакологічних методів лікування СМА спостерігаються траєкторії розвитку захворювання, які суттєво відрізняються від відомого природного перебігу [12]. Наприклад, пацієнти з початком до 6-місячного віку можуть досягти самостійного сидіння, якщо терапію розпочато на ранніх етапах [12]. Попри вражаючий успіх нових препаратів, важливо усвідомлювати, що вони все ще є «лікуванням», а не «гарантією одужання».
З появою нових траєкторій захворювання клінічний підхід до контролю СМА також може змінитись [12]. У дуже тяжких випадках із пренатальним початком медикаментозне лікування навряд чи сприятиме відповідному поліпшенню рухових функцій або зможе запобігти необхідності постійної вентиляції легень; тому фармакотерапія може виявитися недоцільною [12]. Однак початок лікування у пацієнта до появи симптомів може забезпечити майже нормальний моторний розвиток [12].
Лікування
СМА – це спектральне захворювання, яке розглядається як системне і потребує залучення фахівців із різних галузей знань. Згідно з міжнародними рекомендаціями та світовою клінічною практикою, менеджмент пацієнтів зі СМА полягає у використанні поєднання етіопатогенетичних ХМП та підтримувальної терапії.
Для медикаментозного лікування СМА на сьогодні у світі зареєстровано три етіопатогенетичні ХМП, такі як рисдиплам, нусінерсен та онасемноген абепарвовек. Кожний з них використовують разом із підтримувальною терапією. У міжнародних багатоцентрових дослідженнях було показано, що ці препарати забезпечують поліпшення виживаності, дихальної та рухової функції, якості життя пацієнтів зі СМА.
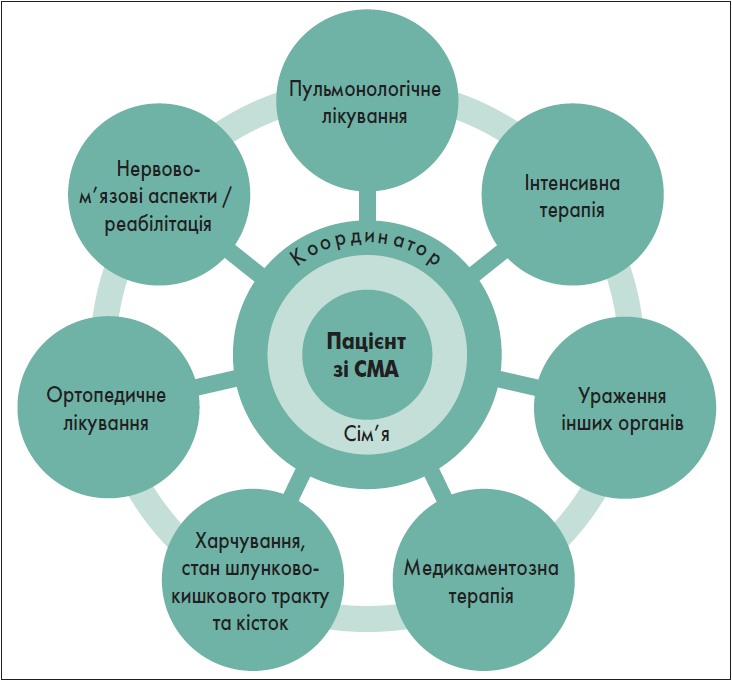
Підтримувальна терапія включає респіраторну підтримку, належне харчування, ортопедичну корекцію, фізичну терапію/реабілітацію, симптоматичне лікування. Найбільш відповідним і ефективним способом забезпечення пацієнтів зі СМА необхідною допомогою зазвичай є залучення міждисциплінарної команди фахівців. Схема міждисциплінарного підходу представлена на рисунку 2.
Рис. 2. Мультидисциплінарний підхід у лікуванні СМА
Незалежно від того, чи отримує пацієнт зі СМА етіопатогенетичне медикаментозне лікування, належна підтримувальна терапія, що включає контроль симптоматики, і профілактика ускладнень разом із забезпеченням психологічного й соціального добробуту є основою для досягнення найкращої можливої якості життя пацієнтів. Оптимальний контроль перебігу хвороби потребує співпраці багатьох фахівців у сфері охорони здоров’я.
Комплексна стандартна підтримувальна терапія при СМА детально описана у міжнародних рекомендаціях 2018 р. До першочергових заходів такої терапії належать [1‑11]:
- Респіраторна підтримка – пацієнти зі СМА 1-го та 2-го типу потребують інвазивної або неінвазивної вентиляції легень (постійної чи тимчасової), забезпечення відкашлювання та санації дихальних шляхів тощо. У разі розвитку респіраторних ускладнень хворі можуть потребувати інтенсивного лікування у відділенні реанімації та інтенсивної терапії.
- Гастроентерологічна підтримка включає забезпечення належного харчування через назогастральний зонд або гастростому та корекцію гастроентерологічних порушень.
- Ортопедична корекція включає використання ортезів (тутора), корсетів (для корегування постави), вертикалізаторов, хірургічну корекцію сколіозу.
- Вакцинація.
- Супутня симптоматична терапія (муколітики, інгібітори протонної помпи, препарати для профілактики нудоти і блювання, профілактики та лікування дисбіозу, закрепу тощо).
- Фізична реабілітація – вправи для поліпшення рухової та дихальної функції, самообслуговування.
Самостійна підтримувальна терапія (без етіопатогенетичного лікування) при СMA не може змінити перебіг основного захворювання.
Розбіжності у наданні медичної допомоги
Ведення пацієнта згідно зі стандартами медичної допомоги вже на ранніх етапах особливо важливе для хворих на СМА із раннім початком. Міжнародний комітет із залученням медичних працівників та фахівців щодо роботи з пацієнтами розробив рекомендації для контролю перебігу захворювання і терапії дітей, осіб молодого віку, дорослих зі СМА. Рекомендації для сімей були опубліковані 2007 р. під назвою «Міжнародні стандарти лікування СМА». Відтоді з’являється дедалі більше свідчень про те, що пацієнти зі СМА та їхні родини можуть очікувати вищої якості життя, ніж було можливо в минулому, переважно завдяки розвитку медицини й появі нових можливостей терапії. Стало очевидним, що оригінальні стандарти вже належним чином не відображали покращень та змін у підходах до лікування й контролю перебігу хвороби.
Надання медичної допомоги пацієнтам зі СМА з розробкою міжнародних рекомендацій поліппшилося. Проте їх впровадження у клінічну практику в різних країнах відрізняється.
За результатами опитування пацієнтів зі СМА 2-го та 3-го типу та їхніх родин виявлено, що хоча вплив поточного клінічного стану та очікувань хворих сприймається респондентами схожим чином, відмінності між країнами Європи щодо системи догляду все ще існують [17]. Географічні розбіжності спостерігаються у наданні респіраторної підтримки, використанні неінвазивної вентиляції легень (НІВЛ), фізичної терапії та реабілітації. Наприклад, більшу частку трахеостомій проводять у Східній Європі (Білорусії, Молдові, Польщі, Україні). НІВЛ є більш загальною практикою в Західній Європі (таких країнах, як Австрія, Бельгія, Фінляндія, Франція, Німеччина, Ірландія, Італія, Іспанія, Швеція, Швейцарія та Велика Британія) [17].
При опитуванні дитячих неврологів та дитячих респіраторних спеціалістів Канади було показану значну різницю у відношенні лікарів до різних аспектів медичної та психологічної допомоги пацієнтам із СМА 1-го типу [18]. У деяких регіонах Канади НІВЛ при хронічній дихальній недостатності застосовують у 3,6 раза менше та як профілактику респіраторних ускладнень – у тричі менше, ніж в інших регіонах. Більш ніж половина респондентів вважають, що при інтубації у зв’язку з гострою респіраторною подією ймовірність успішної екстубації без трахеостомії низька, хоча є докази успішної екстубації дітей зі СМА. Значну варіабельність між регіонами було продемонстровано щодо застосування трахеостомії, призначення респіраторного обладнання, оцінки клінічного та психологічного стану дітей зі СМА.
Розробка освітньої платформи «SoC For All» («Стандарти лікування СМА для всіх»)
Існує очевидна потреба в адаптації міжнародних рекомендацій до української системи охорони здоров’я та навчанні лікарів впровадженню міжнародних і національних настанов щодо менеджменту пацієнтів зі СМА у клінічну практику. Для підготовки національних медико-технічних документів зі стандартизації медичної допомоги при СМА вже створена і працює робоча група МОЗ України. Окрім того, Інститут неврології, психіатрії і наркології НАМН України (м. Харків) брав участь у розробці спеціальної міжнародної освітньої платформи «SoC For All» («Стандарти лікування СМА для всіх») разом з Європейськими клініками Італії, Франції та Польщі за підтримки компанії Hoffmann-La Roche.
Поліпшення впровадження стандартів лікування спінальної м’язової атрофії на міжнародному рівні: платформа «SoC For All»
На конгресі Всесвітнього товариства нервово-м’язових захворювань, який відбувся в онлайн-форматі 20‑24 вересня 2021 р., було представлено проєкт, над яким працювала група науковців із 10 європейских країн, включно з Україною. Мета проєкту – вдосконалення впровадження стандартів лікування пацієнтів зі спінальною м’язовою атрофією (СМА) на міжнародному рівні завдяки розробці платформи «SoC For All» («Стандарти лікування СМА для всіх»). Пропонуємо до вашої уваги огляд презентованих результатів.
Стандарти лікування пацієнтів із нервово-м’язовими захворюваннями були вдосконалені з розробкою міжнародних рекомендацій, проте їх впровадження у практику в різних країнах світу варіює. Було розроблено програму навчання для підвищення інформованості та знань про СМА, впровадження стандартів лікування для пацієнтів зі СМА та поліпшення доступу до стандартизованої багатопрофільної допомоги, що надається місцевими спеціалізованими центрами по всьому світу.
Зокрема, створено сім модулів, які висвітлюють практичні питання ведення пацієнтів зі СМА та можуть бути використані для навчання багатопрофільної команди, що здійснює догляд за хворими. Ці навчальні модулі доступні на платформі «Стандарти лікування СМА для всіх» (https://smasoc.global). Ведеться робота з розробки відповідної секції для пацієнтів.
Методи
Процес було розпочато з опитування спеціалістів із захворювань нервово-м’язової системи та фізіотерапевтів із різних країн з метою оцінки загальних знань про сучасну практику ведення пацієнтів зі СМА, а також визначення прогалин у знаннях та їх застосуванні в клінічній практиці (рис. 1).
Рис. 1. Процес розробки багатопрофільних загальних стандартів лікування СМА
Адаптовано за C. Lilien et al., 2021
Багатопрофільний комітет експертів із захворювань нервово-м’язової системи використав дані міжнародного опитування щодо загальних стандартів лікування СМА для розробки навчальних модулів, забезпечення освітньої роботи та підтримки.
Результати
Платформа стандартів лікування
У міжнародному опитуванні, в якому взяли участь 39 медпрацівників із п’яти країн (як-то Польша, Україна, Сербія, Росія, Болгарія), були виявлені основні проблеми, пов’язані з лікуванням СМА: брак мультидисциплінарних груп; труднощі з належним скеруванням пацієнтів, зокрема до спеціалістів із респіраторної терапії, і застосуванням вентиляції легень; недостатнє залучення фахівців із фізіотерапії/реабілітації, а також неефективна освіта щодо СМА для членів багатопрофільних груп і пацієнтів.
Навчальні модулі платформи стандартів лікування СМА наведені в таблиці 1, а приклади змісту модулів – на рисунках 2‑4.
Рис. 2. Респіраторна підтримка (модуль 4) та стадії кашлю
Адаптовано за C. Lilien et al., 2021
Рис. 3. Фізична реабілітація (модуль 6) та аспекти реабілітації для пацієнтів зі СМА, які здатні сидіти
Адаптовано за C. Lilien et al., 2021
Рис. 4. Роль лікарів первинної ланки та пацієнтів/доглядальників (модуль 7) та членів мультидисциплінарної команди
Адаптовано за C. Lilien et al., 2021
Рис. 5. Бібліотека ресурсів пацієнта: приклад контенту
Адаптовано за C. Lilien et al., 2021
Впровадження тренінгу зі стандартів лікування СМА
- Для запровадження змін у практику лікування пацієнтів зі СМА на локальному рівні важливо здійснювати навчання спеціалістів загальним стандартам лікування СМА та надавати вказівки й підтримку для подальшого забезпечення таких змін (рис. 6).
- У 2021 р. було здійснено підготовку фахівців у великих регіональних центрах (англійською мовою, в режимі онлайн). У майбутньому планується проводити очні тренінги.
- Тренінги включають також самоосвіту та безперервне навчання на цій платформі.
- Навчальні модулі наразі перекладаються різними мовами для забезпечення навчання медичних працівників у регіональних медичних центрах.
- Відгуки про здійснену підготовку фахівців у крупних регіональних центрах були надзвичайно позитивними (рис. 7). Близько 85% спеціалістів вважали, що зміст навчального модуля був чудовим, а >90% оцінили рівень контенту як належний для їхнього навчання.
Тренінги 66 фахівців із п’яти країн (Болгарії, Польщі, Росії, Сербії та України) наразі завершено.
Рис. 6. Передача знань щодо загальних стандартів лікування СМА
Адаптовано за C. Lilien et al., 2021
Рис. 7. Хмара ключових слів, що узагальнюють відгуки фахівців
Висновки
- Існувала очевидна потреба у розробці програми загальних стандартів лікування СМА (SMA «SoC For All»), і ця програма була дуже добре сприйнята.
- Доступність навчання місцевими мовами є важливою для успішного впровадження, оскільки більшість лікарів у країнах, де проводять тренінги, не володіють англійською.
- Надання пацієнтам та доглядальникам важливої інформації, яка допомагає рятувати життя в надзвичайних ситуаціях, було визнано важливою частиною програми.
- Для задоволення всіх потреб та врахування перспектив важливо залучати всіх членів багатопрофільної команди, а також асоціації пацієнтів.
- Успішна реалізація платформи загальних стандартів лікування СМА може бути запроваджена у декількох країнах і потенційно використовуватися щодо інших рідкісних захворювань.
Список літератури знаходиться в редакції
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 3 (58) 2021 р.
СТАТТІ ЗА ТЕМОЮ Неврологія
Стрес і тривожність чинять потужний несприятливий вплив і на самопочуття окремих індивідуумів, і на загальний стан здоров’я всієї популяції світу. Цей несприятливий вплив значно підсилили пандемія COVID‑19 та війна в Україні (Celuch M. et al., 2023)....
16-17 лютого в Києві відбувся науково-практичний майстер-клас «Хронічний стрес сьогодення: обрані запитання про здоров’я жінки в різні вікові періоди». Під час заходу виступили фахівці різних спеціальностей, було обговорено важливі аспекти жіночого здоров’я як психологічного, так і фізичного. Доповіді присвячувалися різноманітним питанням, зокрема репродуктивним проблемам, онкологічним захворюванням, психосоматичним розладам. Під час події виступила засновниця Академії довголіття Dr. Skytalinska, віцепрезидент Асоціації дієтологів України, лікар-дієтолог Оксана Василівна Скиталінська. Доповідь Оксани Василівни була присвячена впливу тривалого стресу на харчування та пов’язані з цим наслідки для здоров’я жінок. Окрім пояснення механізмів негативного впливу стресу, під час доповіді лікарка також надала важливі практичні рекомендації стосовно здорового харчування....
Події останніх 5 років є неабияким викликом для психічного стану кожного українця: спочатку – пандемія коронавірусу та запроваджені через неї карантинні обмеження, а далі – повномасштабне російське вторгнення, що триває уже понад 2 роки. Все це спричиняє погіршення психічного здоров’я населення. Такі надзвичайні ситуації, що характеризуються загрозою з невизначеною тривалістю, створюють масивне стресове навантаження, яке підсилюється відчуттям самотності та відчуженості, підвищують тривожність, а також є підґрунтям розвитку психічних розладів. Відомо, що ці стани порушують розумову діяльність, тобто перешкоджають концентрації та аналізу інформації. ...
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....





.png)
.png)
.png)
.png)
.png)
.png)
.png)