Дієтичні рекомендації щодо мігрені: реалії та перспективи
Мігрень є хронічним виснажливим, подеколи інвалідизувальним захворюванням, яке часто спричиняє суттєве зниження якості життя. На мігрень страждають приблизно 2% населення світу. Хронічна мігрень призводить до значних економічних витрат для суспільства. Наприклад, у США прямі та непрямі витрати на мігрень перевищують 20 млрд доларів на рік. Багато пацієнтів, у яких традиційне лікування мігрені виявилося малоефективним, часто шукають додаткових втручань, які могли би полегшити перебіг захворювання (зменшити частоту, вираженість і тривалість нападів), включаючи й корекцію харчування. Про сучасні можливості модифікації перебігу мігрені за допомогою дієтичних рекомендацій у межах науково-практичної конференції «Дні нутриціології та дієтології в Одесі» розповів віцепрезидент Асоціації дієтологів України, доцент кафедри внутрішньої медицини № 1 Національного медичного університету ім. О. О. Богомольця (м. Київ), кандидат медичних наук Олександр Аркадійович Мартинчук.
 Доповідач зазначив, що спроби контролювати перебіг мігрені за допомогою харчування мають свою тривалу передісторію. Протягом століть шлунково-кишкові прояви нападів мігрені спонукали до висунення численних дієтологічних гіпотез щодо етіології мігренозного болю. Також накопичилося чимало свідчень про можливість існування зворотного зв’язку, тобто здатність біологічних механізмів мігрені впливати на харчовий раціон. Не виключається поєднання обох поглядів: хвороба впливає на раціон, а спожиті продукти харчування – на прояви хвороби. Також висувається гіпотеза стосовно того, що мікробіота кишечнику впливає на мозок через вісь «кишечник – мозок», хоча доказів цього також недостатньо.
Доповідач зазначив, що спроби контролювати перебіг мігрені за допомогою харчування мають свою тривалу передісторію. Протягом століть шлунково-кишкові прояви нападів мігрені спонукали до висунення численних дієтологічних гіпотез щодо етіології мігренозного болю. Також накопичилося чимало свідчень про можливість існування зворотного зв’язку, тобто здатність біологічних механізмів мігрені впливати на харчовий раціон. Не виключається поєднання обох поглядів: хвороба впливає на раціон, а спожиті продукти харчування – на прояви хвороби. Також висувається гіпотеза стосовно того, що мікробіота кишечнику впливає на мозок через вісь «кишечник – мозок», хоча доказів цього також недостатньо.
Більшість досліджень щодо зв’язку дієти та мігрені не досягають бажаного порогового рівня для складання доказових дієтичних рекомендацій, часто через низьку якість і непослідовний дизайн, неузгодженість результатів і невідповідний розмір вибірки (Martin V. T., 2016). Однак лікарю важливо надати пацієнту з мігренню обґрунтовані рекомендації щодо особливостей харчування. Якщо хворий самостійно вдаватиметься до пошуку певних харчових тригерів шляхом вилучення тих чи інших продуктів або намагатиметься слідувати певним моделям харчування, це може призвести до серйозних несприятливих наслідків.
Тому на сьогодні важливо розуміти, які докази наразі існують і що ми можемо порекомендувати хворим. Можливо, дієтичні рекомендації допоможуть не всім пацієнтам із мігренню, оскільки індивідуальну ефективність такого лікування спрогнозувати досить важко, проте вони й не зашкодять. У багатьох осіб дієтичні втручання можуть зменшити тягар мігрені завдяки скороченню кількості нападів і зниженню ризиків хронічної коморбідності; вони можуть виявитися менш затратними, зручнішими та матимуть менше побічних ефектів, аніж фармакологічні втручання.
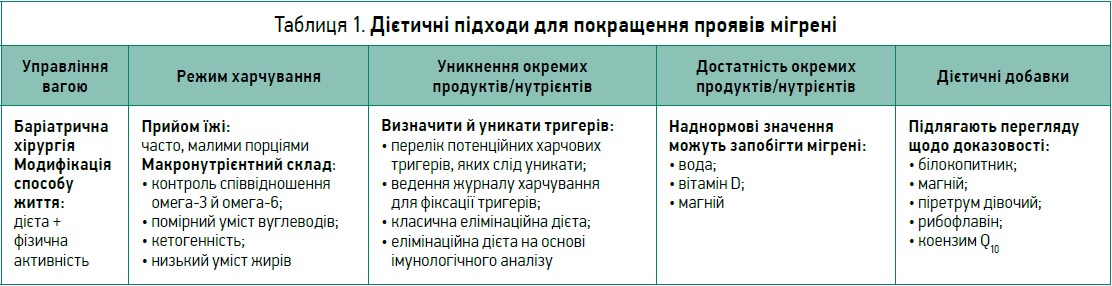
На сьогодні Американська академія неврології виокремлює такі немедикаментозні напрями для покращення проявів мігрені: управління вагою, режим харчування, уникнення окремих продуктів, достатність окремих продуктів, використання дієтичних добавок (табл. 1). Розгляньмо докладніше, які переваги та недоліки має кожен із цих підходів.
Співвідношення омега‑3 й омега‑6 поліненасичених жирних кислот
Режим харчування за раціоном, здатним забезпечити підвищене співвідношення омега‑3 й омега‑6, порівняно з типовою американською дієтою демонструє найвищий рівень доказовості щодо пом’якшення нападів мігрені. Зокрема, J. D. Mann і співавт. (2018) у 12-тижневому дослідженні продемонстрували, що в пацієнтів групи високого вмісту омега‑3 (1500-2000 мг на добу) та низьким умістом омега‑6 (загалом <2% добового калоражу) спостерігалося значніше зменшення кількості днів із головним болем на місяць, аніж у групі лише з низьким умістом омега‑6 (-8,8 проти -4,0), а також вираженіше зменшення тривалості головного болю на день (-4,6 проти -1,2 год). Окрім того, відзначалися відмінності в балах оцінки впливу головного болю НІТ‑6 (-7,5 проти -2,1), поліпшення психологічною стану та пов’язаної зі здоров’ям якості життя.
Проте надзвичайно низький рівень споживання омега‑6, забезпечений у цьому дослідженні для обох груп лікування, є малореалістичним у сучасних умовах харчування. Омега‑6 жирні кислоти містяться у великих кількостях у первинних рослинних оліях, які використовуються при харчовій обробці (олії каноли, соняшнику, кукурудзи й сої) та в багатьох закладах харчування, тому суттєво знизити споживання цих жирів видається малоймовірним.
Дещо пізніше було показано, що дієта з високим співвідношенням омега‑3 й омега‑6 порівняно дає змогу впливати на пул циркулювальних ліпідних медіаторів (оксиліпінів), які спонукають запуск мігренозного нападу (Ramsden C. E. et al., 2021).
Мігрень і голод
Природні експерименти з релігійними постами та регулярні постування в нічний період дають підстави визнати голодування тригером як головного болю, так і нападів мігрені. Тому наразі загальні рекомендації щодо запобігання нападам мігрені, спричиненим голодуванням, імітують рекомендації з контролю рівня глюкози в крові в осіб із діабетом:
- уникати тривалих періодів без їжі;
- 5-6-разове харчування, що включає прийом білкової їжі невеликими порціями;
- уникати вживання продуктів із високим умістом рафінованих цукрів;
- споживати продукти з високим умістом складних вуглеводів і клітковини.
Механізм впливу голоду на мігрень наразі недостатньо вивчений. Спроби пов’язати його з рівнем глюкози крові виявилися безуспішними, оскільки виявилося, що низький рівень глікемії безпосередньо не провокує головний біль. Заміри рівня глюкози в крові натще між нападами в різних дослідженнях не виявили жодних закономірностей при порівнянні людей із мігренню та здоровою контрольною групою (Pearse J., 2015).
! Незважаючи на недостатню кількість прямих доказів на користь дієтичних втручань для уникнення мігренозних нападів, спричинених голодуванням, сучасні рекомендації щодо регулярного прийому їжі з переважанням складних вуглеводів є низькоризиковими, нескладними для виконання та відповідають загальним дієтичним рекомендаціям.
Підтримка гідратації
Головний біль є поширеним симптомом зневоднення, що може спричинити напад мігрені в схильних до неї осіб. Відсутність добре спланованих інтервенційних досліджень із відповідним дизайном не дає змоги виявити чіткі відмінності або порекомендувати вживання конкретної кількості рідини пацієнтам із мігренню. Проте, враховуючи безліч переваг належної гідратації та її відносно невелику складність, пацієнтів із мігренню можна орієнтувати на послідовне дотримання наявних норм споживання рідини.
Згідно з Довідником харчових раціонів США адекватний рівень споживання води становить 2,7 л для дорослих жінок (із них приблизно 2,2 л у формі рідин, а решта – вода, що надходить із харчових продуктів) і сумарно 3,7 л води для дорослих чоловіків (із них приблизно 3,0 л рідин). Європейське агентство з безпеки харчових продуктів рекомендує дещо нижчий рівень споживання води – сумарно 2,0 л води на добу для дорослих жінок і 2,5 л води на добу для дорослих чоловіків.
Вплив мігрені на контроль метаболізму
Активація гіпоталамуса (зокрема, центру голоду й насичення), що спостерігається під час продромальної фази мігрені, збігається з періодами посиленого потягу до певних продуктів і порушеннями харчової поведінки.
Рівні нейромедіаторів, гормонів і адипоцитокінів відрізняються в мігренозних пацієнтів порівняно з контрольною групою, впливаючи на голод/насичення або контроль метаболізму. Наприклад, рівень орексину А був вищим під час больової фази хронічної мігрені, рівень серотоніну був знижений у періоди між нападами, в мігренозних пацієнтів була виявлена більша резистентність до інсуліну, а також підвищений рівень адипоцитокінів (Rainero L. et al., 2018).
За деякими даними, загальна симптоматика мігрені (біль та інші прояви поганого самопочуття) може впливати на вибір їжі в тому сенсі, що люди з більшою ймовірністю віддадуть перевагу зручності та простоті, а це зазвичай не відповідає профілю корисного харчування в більшості сучасного світу. Сукупно ці спостереження можуть виявитися корисними для пояснення добре описаної кореляції між ожирінням і мігренню, а покращене розуміння цього аспекту в майбутньому може стати підґрунтям ефективніших втручань для профілактики та лікування ожиріння при мігрені.
Підтримка здорової маси тіла
Наразі відомо, що ожиріння пов’язане як з більшою поширеністю мігрені, так і з більшим ризиком прогресування від епізодичної до хронічної мігрені. У більшості проведених досліджень спостерігалося покращення симптомів мігрені після зниження ваги в пацієнтів із надмірною масою тіла й ожирінням після виконання баріатричних хірургічних втручань або зміни способу життя (включаючи дієту) в дорослих і підлітків. Хоча втрата ваги може сприяти зменшенню наявних симптомів, профілактика майбутнього набору ваги також може виявитися важливою для запобігання подальшим загостренням мігрені та розвитку її хронічних форм.
Обмеження кофеїну в раціоні
Дані щодо обмеження вживання кофеїну пацієнтами з мігренню є неоднозначними. Відомо, що в людей із мігренозними станами хронічне вживання кофеїну підвищує ризик розвитку хронічної мігрені та рикошетного головного болю. Разом із тим приблизно в половини постійних споживачів кофеїну після різкого припинення його споживання спостерігається синдром відміни зі зростанням частоти та тяжкості мігренозних нападів, що триває зазвичай 1-2 тиж. Різке припинення споживання кофеїну через 1 міс призводить до покращення симптомів мігрені вищими темпами, ніж у тих, хто знизив споживання кофеїну частково або лишив незмінним. Також було показано, що різке припинення споживання кофеїну може підвищити ефективність лікування гострої мігрені трипланами (Lee C. B. et al., 2013).
Отже, припинення споживання кофеїну може зменшити частоту нападів мігрені в довготривалій перспективі або ж підвищити ризик розвитку рикошетного головного болю.
Вживання алкоголю
Здатність алкоголю спричиняти головний біль, зокрема напади мігрені, є загальновідомим явищем. Пацієнти, що страждають на мігрені, виявляються більш схильними до похмільного головною болю, відчуваючи його частіше й у відповідь на менші дози алкоголю. Також буває складно відрізнити абстинентний головний біль (відкладена реакція на алкоголь) від болю, тригером якого виступив алкоголь (негайний головний біль, спричинений алкоголем).
Наразі не існує опублікованих доказів того, що утримання від алкоголю покращує симптоми мігрені, а також має вплив на якість життя (Panсonesi A. et al., 2011). З огляду на можливі соціальні міркування щодо утримання від алкоголю, особи, які страждають на мігрень, можуть знайти переваги в тому, щоб уживати рідше, в помірних кількостях та усвідомлювати інші тригери. Утім, зовсім не обов’язково уникати алкогольних напоїв узагалі.
Мігрень і потяг до продуктів. Харчові тригери
У періоді, що передує мігренозному нападу, часто змінюється потяг до харчових продуктів. Нещодавно виявлено активність гіпоталамуса, що передує нападу мігрені. Це свідчить про біологічне підґрунтя тяги до певних продуктів під час цієї фази (Houle T. T., 2013).
Якщо це спонукає пацієнтів уживати продукти, які вони інакше не обрали б (наприклад, шоколад), цей зв’язок може пояснити, чому люди пов’язують конкретні та рідко вживані ними продукти з нападом мігрені. Тому пацієнти починають розглядати ці продукти як тригери мігрені й виокремлювати «безпечні» та «небезпечні», на їхню думку, продукти.
Уникання підозрюваних харчових тригерів без доказів призводить до дотримання безпідставної обмежувальної дієти (з незбалансованими наслідками з боку споживання нутрієнтів, соціальними наслідками, крайніми обмеженнями у виборі харчових продуктів), розвитку стресу та тривожності у зв’язку з необхідністю дотримання переліку «заборонених» продуктів. Окрім того, пацієнти втрачають час, який можна було би використати на лікування, засноване на доказах. На сьогодні підхід вилучення харчових продуктів із метою запобігання мігренозним нападам не підтвердив своєї ефективності.
Безглюгенова дієта (без целіакії)
Накопичені дані свідчать про можливе існування зв’язку між глютеном і мігренозними нападами, оскільки в популяції люди як із целіакією, так і з непереносимістю глютену без целіакії (НГБЦ) мають вищі показники поширеності мігрені. Тож, якщо в людини мігрень відзначається на тлі відповідних гастроентерологічних скарг, часто рекомендують провести діагностичний пошук щодо целіакії. У разі підтвердження діагнозу доцільно вилучити глютеновмісні продукти з харчування. У мігренозних пацієнтів часто спостерігається значне покращення симптомів мігрені після початку безглютенової дієти (Mormile R., 2014). Профілактичне вилучення глютену особам із мігренню не рекомендоване, оскільки чинить негативний вплив на мікробіоту кишечнику, спричиняє розвиток ожиріння, підвищує ризик настання несприятливих серцево-судинних подій.
Неточність діагнозу НГБЦ залишається проблемою при проведенні повторюваних досліджень, а дослідження втручань на основі безглютенової дієти не показали послідовних переваг щодо мігрені в пацієнтів із НГБЦ.
Вплив кетогенної дієти на перебіг мігрені
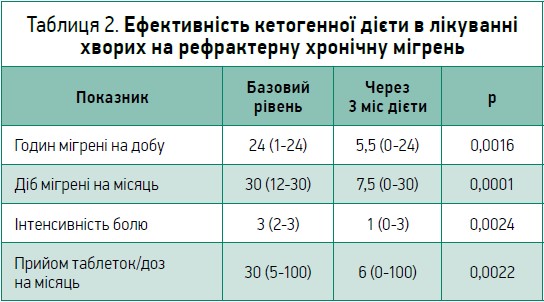
Кетогенна дієта є визнаним засобом лікування резистентної епілепсії, й останнім часом її розглядають для лікування хронічної мігрені й інших видів головного болю. Нещодавнє тримісячне дослідження D. Bongiovanni та співавт. за участі пацієнтів із хронічною рефрактерною мігренню свідчить про досить добрі результати щодо профілактики нападів мігрені, їхньої тривалості й інтенсивності (табл. 2).
Утім, залишається відкритим питання щодо тривалості такого лікування. Можна цілком обґрунтовано припустити, що тільки-но кетоз переривається й метаболізм глюкози відновлюється, після повернення до звичайної дієти (з вуглеводами), через кілька днів симптоми відновляться.
Майбутні напрями досліджень впливу дієти на мігрень
Нові напрями досліджень лежать у площині тих трендів, які мають місце в сучасному медичному науковому світі.
Мікробіом і вісь «кишечник – мозок»
Хоча прямі докази зв’язку мікробіоти кишечнику та мігрені все ще обмежені, гіпотетично можна припустити наявність такого взаємовідношення на підставі зв’язку між мікробіотою та її впливом на ентеральну й центральну нервові системи.
Загалом мікробіота кишечнику сприяє засвоєнню нутрієнтів шляхом метаболізації неперетравних харчових сполук, захищає від колонізації кишечнику патогенами, регулює формування та функціональність імунітету господаря, а також модулює функції нейронів. Ця діяльність мікробіоти кишечнику може впливати на центральну нервову систему нервовим, імунологічним, ендокринним і метаболічним шляхами.
Імовірно, поширеніші види пробіотичних мікроорганізмів можуть забезпечити переваги при мігрені, сприяючи поліпшенню функції мікробіоти, конкурентному вилученню патогенів і підтримці належної проникності кишечнику. Крім того, можуть існувати специфічні для штаму впливи на неврологічні або імунологічні процеси, характерні для патофізіології мігрені.
Sensenig і співавт. досліджували призначення комбінованого пробіотичного препарату, що містив декілька видів бактерій (Lactobacillus adiophilus, Lactobacillus bulgaricus, Enterococcus faecium, Bifidobacterium bifidum), біоактивні пептиди, амінокислоти та вітамінний комплекс, протягом 90 днів у дорослих, які впродовж 1 року повідомляли про скорочення щонайменше на 2 напади мігрені на місяць. Результати показали, що приблизно 60% учасників відчули майже повне зникнення симптомів мігрені, а 20% відзначили значне поліпшення якості життя.
Нещодавно De Roos і співавт. повідомили, що 12-тижневе призначення ще однієї багатовидової добавки з 5,0×109 КОУ 8 різних штамів лактобактерій у щоденній дозі сприяло значному зниженню частоти й інтенсивності мігренозних нападів. Кількість днів із мігренню знизилася з 6,7 до 5,2 на місяць. Однак ці результати не отримали підтвердження, коли ті самі дослідники надалі випробовували ту саму пробіотичну суміш, дозу та тривалість у паралельній групі під час плацебо-контрольованого рандомізованого клінічного дослідження.
Нарешті, Маrtami та співавт. протягом 10 тиж випробовували 14-штамну пробіотичну суміш у порівнянні з групою плацебо під час подвійного сліпого рандомізованого клінічного дослідження та зафіксували зниження частоти й тяжкості як хронічної, так і епізодичної мігрені порівняно з плацебо.
На жаль, ми поки що не знаємо, який саме мікробний пейзаж є типовим для пацієнтів із мігренню, тому не зовсім зрозуміло, що саме потрібно корегувати. Втім, отримані позитивні результати свідчать про правильний напрям майбутніх досліджень.
Інший намічений напрям досліджень спрямований не на зміну мікробіому, а на можливість використання міжіндивідуальних відмінностей для створення персоналізованих харчових рекомендацій. Існує ймовірність, що проведені дослідження дієт із позитивним виливом па мігрень могли досягти цього впливу через дію на мікробіом. Для подальшого прогресу потрібні дослідження з метою визначення ентеротипів або закономірностей дисбіозу, які виникають у пацієнтів із мігренню та різними її категоріями. Потрібно також провести дослідження з метою визначити, чи існують індивідуальні відмінності у відповідь на дієтичні втручання, зумовлені ідентифікованими мікроорганізмами.
Вплив дієти на кальцитонін-ген-зв’язаний пептид
Здатність харчових продуктів і харчових компонентів впливати па експресію та секрецію кальцитонін-ген-зв’язаного пептиду (CGRP) відзначалася в обмежених лабораторних дослідженнях. R.J. Cady та P. L. Durham спостерігали значне зниження експресії CGRP у клітинах тригемінальних гангліїв щурів після 14-денного вживання їжі, збагаченої какао, порівняно з контрольною групою. Екстракти виноградних кісточок та імбиру, а також чистий хімічний петазин (імовірний активний компонент рослинної харчової добавки білокопитнику) зменшують секрецію CGRP у клітинних моделях. Зважаючи на нещодавні фармацевтичні успіхи щодо CGRP, вплив раціону людини на цей пептид є цікавим, але невивченим напрямом для досліджень.
Висновки
- Сучасні дані свідчать про те, що наявність, тип, частота та ступінь тяжкості мігрені можуть бути пов’язані з різними аспектами харчування людей, які живуть із болем та інвалідністю внаслідок мігрені.
- Більшість рекомендацій щодо мігрені наразі узгоджується із загальними доказовими рекомендаціями, спрямованими на здорове харчування.
- Дослідження, що встановлюють зв’язок між мікробіомом і мігренню, перебувають іще в зародковому стані, й зарано рекомендувати дієтичні втручання, спрямовані на зміну мікробіому з метою впливу на мігрень. Такі дослідження можуть становити один із напрямів для встановлення терапевтичної мети для майбутніх випробувань.
- Зазираючи в майбутнє, можна сподіватися, що дієтичні рекомендації щодо мігрені допоможуть безпосередньо контролювати захворювання, уповільнювати його прогресування та запобігати ускладненням через пов’язані з дієтою коморбідності, включаючи ожиріння, діабет і серцево-судинні захворювання.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 5-6 (522-523), 2022 р.
СТАТТІ ЗА ТЕМОЮ Неврологія
Стрес і тривожність чинять потужний несприятливий вплив і на самопочуття окремих індивідуумів, і на загальний стан здоров’я всієї популяції світу. Цей несприятливий вплив значно підсилили пандемія COVID‑19 та війна в Україні (Celuch M. et al., 2023)....
16-17 лютого в Києві відбувся науково-практичний майстер-клас «Хронічний стрес сьогодення: обрані запитання про здоров’я жінки в різні вікові періоди». Під час заходу виступили фахівці різних спеціальностей, було обговорено важливі аспекти жіночого здоров’я як психологічного, так і фізичного. Доповіді присвячувалися різноманітним питанням, зокрема репродуктивним проблемам, онкологічним захворюванням, психосоматичним розладам. Під час події виступила засновниця Академії довголіття Dr. Skytalinska, віцепрезидент Асоціації дієтологів України, лікар-дієтолог Оксана Василівна Скиталінська. Доповідь Оксани Василівни була присвячена впливу тривалого стресу на харчування та пов’язані з цим наслідки для здоров’я жінок. Окрім пояснення механізмів негативного впливу стресу, під час доповіді лікарка також надала важливі практичні рекомендації стосовно здорового харчування....
Події останніх 5 років є неабияким викликом для психічного стану кожного українця: спочатку – пандемія коронавірусу та запроваджені через неї карантинні обмеження, а далі – повномасштабне російське вторгнення, що триває уже понад 2 роки. Все це спричиняє погіршення психічного здоров’я населення. Такі надзвичайні ситуації, що характеризуються загрозою з невизначеною тривалістю, створюють масивне стресове навантаження, яке підсилюється відчуттям самотності та відчуженості, підвищують тривожність, а також є підґрунтям розвитку психічних розладів. Відомо, що ці стани порушують розумову діяльність, тобто перешкоджають концентрації та аналізу інформації. ...
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....