Тромбоцитопенія і рак грудної залози
Тромбоцитопенія у пацієнтів зі злоякісними пухлинами може розвиватися внаслідок багатьох причин: пухлинної інфільтрації кісткового мозку, мієлосупресії хіміопрепаратами або променевою терапією, периферичного споживання тромбоцитів через дисеміновану внутрішньосудинну коагуляцію або імуноопосередковане руйнування. У цьому огляді представлені дані щодо потенційного розвитку тромбоцитопенії в пацієнтів, які отримують профілактику або лікування з приводу раку грудної залози (РГЗ).
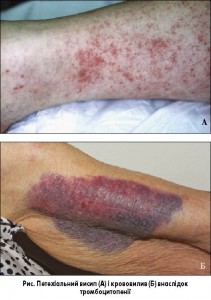
У нормі кількість тромбоцитів у дорослих становить 150-450 тис. на мм3, або 150-400×109/л. У більшості випадків тромбоцитопенія не супроводжується симптомами і діагностується випадково за результатами загального аналізу крові. Пацієнти можуть скаржитися на нездужання, загальну слабкість і підвищену втомлюваність. У деяких пацієнтів, особливо при значному зниженні тромбоцитів, можуть спостерігатися зовнішні кровотечі (наприклад, з носа, ясен), збільшення об’єму і тривалості менструальної кровотечі, синці, пурпура і петехії (рис.).
Тромбоцитопенія як перший симптом РГЖ
Клінічний випадок 1 (Wahid et al., 2000)
Пацієнтка, 40 років, звернулася до лікаря з приводу періодичної кровотечі з ясен і кон’юнктиви протягом останніх 2 тижнів. Лихоманка, фоточутливість, ерозії в ротовій порожнині, артрит в анамнезі відсутні, будь-яких ліків за останній час не застосовувала. Під час загального огляду виявлено пухлину 3×2 см у лівій грудній залозі, втягнення лівого соска і збільшений лівий пахвовий лімфатичний вузол. Дослідження мазку периферичної крові показало наявність гігантських тромбоцитів за відсутності лейкоеритробластозу. Ознак мікроангіопатичного гемолізу і дисемінованої внутрішньосудинної коагуляції, які можуть асоціюватися з метастатичною карциномою, також не було. Пацієнтка отримала 28 одиниць тромбоцитарної маси без поліпшення рівня тромбоцитів (<10×109/л). У мазку кісткового мозку виявлено підвищену кількість мегакаріоцитів і невеликі вогнища метастатичних пухлинних клітин. Цитологічне дослідження біоптату грудної залози підтвердило діагноз інфільтруючої протокової карциноми. Результати серологічних тестів щодо вірусів денге, Епштейна – Барр та імунодефіциту людини були негативними, так само як і тести стосовно ревматоїдного фактора, антинуклеарних антитіл і вовчаковий антикоагулянтний тест. Встановлено діагноз метастатичної карциноми грудної залози та ідіопатичної тромбоцитопенічної пурпури, розпочато лікування метилпреднізолоном внутрішньовенно 1 г/добу протягом 3 днів, потім преднізолон перорально 60 мг/добу 18 днів. Рівень тромбоцитів підвищився до 30×109/л, кровотеча зупинилася після 7 днів кортикостероїдної терапії. На 10-й день лікування преднізолоном рівень тромбоцитів становив 82×109/л, на 22-й день – 271×109/л. Після початку кортикостероїдної терапії пацієнтка отримала 60 мг/м2 доксорубіцину, проте відповідь пухлини була відсутньою. Після 7 міс спостереження було відзначено часткове зменшення первинної пухлини, рівень тромбоцитів стабілізувався.
У наведеному клінічному випадку наявність ізольованої тяжкої тромбоцитопенії, гігантських тромбоцитів і підвищення кількості мегакаріоцитів у кістковому мозку, а також рефрактерність до трансфузії тромбоцитарної маси свідчать про імуноопосередкований механізм тромбоцитопенії.
Гормональна терапія
Тамоксифен – селективний модулятор естрогенових рецепторів, який широко застосовується для профілактики РГЗ у жінок і лікування РГЗ у жінок і чоловіків. Тромбоцитопенія, обумовлена прийомом тамоксифену, – рідкісний побічний ефект, який розвивається ймовірно внаслідок імунологічного механізму з утворенням антитіл проти тромбоцитів (Nasiroglu et al., 2007). У присутності препарату ці антитіла зв’язуються з глікопротеїнами на поверхні тромбоцитів і руйнують їх (Visentin & Lu, 2007). Крім того, тамоксифен може пригнічувати функцію тромбоцитів за рахунок зниження пероксинітриту і підвищення оксиду азоту в тромбоцитах, що призводить до подовження часу кровотечі (Scognamiglio et al., 2007). Отже, тамоксифен може впливати на кількість і якість тромбоцитів у сприйнятливих осіб (Nayak & Schmaier, 2012).
Клінічний випадок 2 (Samini et al., 2010)
Пацієнтка, 41 рік, після діагностування папілярної карциноми грудної залози in situ протягом 3 років приймала тамоксифен. До початку лікування рівень тромбоцитів становив 300×109/л; через 3 роки він знизився до 54×109/л. Антинуклеарні антитіла і ознаки дисемінованої внутрішньосудинної коагулопатії були відсутні; виявлені сироваткові антитіла проти глікопротеїну IIb/IIIa. Гістологічне дослідження біоптату кісткового мозку: без патології. Встановлено діагноз ідіопатичної тромбоцитопенічної пурпури (ІТП). З огляду на рівень тромбоцитів >50×109/л лікування не призначали. Після 3 років подальшого спостереження було встановлено, що вміст тромбоцитів залишився на тому ж рівні.
Також повідомлялося про розвиток тромбоцитопенії в пацієнток, які приймали інгібітор ароматази екземестан. За даними Управління з контролю якості харчових продуктів та лікарських препаратів США (FDA), серед 3767 пацієнтів з побічними ефектами під час лікування екземестаном у 110 спостерігалася тромбоцитопенія. Факторами ризику цього ускладнення були вік >60 років, прийом препарату <1 міс і діагноз РГЗ.
Променева терапія
Променева терапія як самостійний метод лікування зазвичай не викликає тромбоцитопенії. Однак остання може виникнути, якщо пацієнт отримав значну дозу опромінення в області тазу, у разі хіміопроменевої терапії або поширення метастазів у кістковий мозок. Manus і співавт. (1997) визначили такі фактори розвитку тромбоцитопенії в пацієнтів, які отримують променеву терапію: одночасна хіміотерапія (підвищення ризику в 45 разів), великий об’єм опромінення кісткового мозку, метастази в головному мозку або кістках і раніше отримана хіміотерапія.
Хіміотерапія і таргетна терапія
Хіміотерапія зазвичай призначається при РГЖ 2-4 стадії і є найбільш доцільною при естроген-рецептор-негативних пухлинах. Найчастіше застосовуваними схемами є AC (циклофосфамід, доксорубіцин), TAC (циклофосфамід, доксорубіцин, доцетаксел), CMF (циклофосфамід, метотрексат, 5-фторурацил) та ін. Внаслідок цитотоксичної дії ці та інші хіміопрепарати можуть спричиняти пригнічення кісткового мозку і, відповідно, тромбоцитопенію.
У лікуванні пацієнток з карциномами грудної залози, позитивними стосовно рецептора людського епідермального фактора росту 2 типу (HER2/neu), широко застосовується трастузумаб (гуманізовані антитіла проти HER2) як ад’ювантна терапія або при розвитку метастазів. Трастузумаб відносять до так званих таргетних препаратів, проте він може викликати низку «позацільових» побічних ефектів, у тому числі тромбоцитопенію.
Клінічний випадок 3
Пацієнтка, 70 років, мала встановлений у 2008 р. діагноз місцевопоширеної гормон-рецептор-позитивної HER2-позитивної карциноми грудної залози. Вона отримала неоад’ювантну хіміотерапію послідовною схемою з антрацикліном і таксаном, хірургічне лікування і променеву терапію. Після операції їй як учасниці дослідження HERA було призначено анастрозол і трастузумаб. Контрольні огляди були негативними аж до липня 2012 р., коли візуалізація виявила метастази в кістках. Була запланована друга лінія терапії трастузумабом і пероральним вінорельбіном. У день введення навантажувальної дози трастузумабу (8 мг/кг) загальний аналіз крові був без відхилень. Менше ніж за 24 год після інфузії пацієнтка була госпіталізована з дифузними петехіальними кровотечами і екхімозом на нижніх кінцівках, губах і слизовій оболонці щік за нормальної температури тіла й відсутності гемодинамічних порушень. Рівень тромбоцитів складав 2×109/л за нормальних рівнів гемоглобіну і лейкоцитів. Через 6 год після госпіталізації рівень тромбоцитів становив 0×109/л. Призначено імуноглобулін у високій дозі (1 г/кг внутрішньовенно 7 днів) і переливання тромбоцитарної маси. Інші причини тромбоцитопенії були виключені на підставі нормального згортання, нормальних рівнів D-димеру, імуноглобулінів, білірубіну і лактатдегідрогенази, незміненої ниркової функції, відсутності шистоцитів у мазку крові, нормальної активності дизінтегрину і металопротеїнази з мотивом тромбоспондину 1 типу, 13 члена (ADAMTS-13). Через 12 год після госпіталізації рівень тромбоцитів почав відновлюватися. Через 6 днів після інфузії трастузумабу спостерігався генералізований сверблячий екзематозний висип, пов’язаний з виробленням специфічних антиідіотипових антитіл. Висип розрішився спонтанно впродовж 48 год. Пацієнтка була виписана на 13-й день з призначенням преднізону перорально в низькій дозі. Терапію трастузумабом не продовжували.
Профілактика і лікування тромбоцитопенії
У разі виникнення тромбоцитопенії на тлі хіміо- або хіміопроменевої терапії можливі стратегії включають зниження дози хіміопрепарату або інтенсивності опромінення, відміну причинного препарату або переведення на іншу, менш токсичну щодо тромбоцитів схему терапії. Протягом багатьох років чи не єдиним методом лікування тяжкої тромбоцитопенії залишалося переливання тромбоцитарної маси. Проте ця процедура наражає пацієнтів на відомі ризики, а в разі імунного генезу тромбоцитопенії є абсолютно неефективною.
Після відкриття в 1994 р. тромбопоетину великі сподівання були покладені на застосування відповідних препаратів для профілактики або лікування тромбоцитопенії в пацієнтів з раком за аналогією успішного застосування еритропоетину або гранулоцитарного колонієстимулюючого фактору в пацієнтів з анемію чи нейтропенією відповідно. Рекомбінантні тромбопоетини першого покоління в ранніх дослідженнях зменшували тромбоцитопенію, викликану хіміотерапією, проте їх подальшу розробку було зупинено через розвиток антитіл проти ендогенного тромбопоетину.
Нещодавно в Україні став доступним Емаплаг – рекомбінантний тромбопоетин людини другого покоління для підшкірного введення, який має високий профіль безпеки і не викликає розвитку антитіл проти ендогенного тромбопоетину. Препарат успішно пройшов випробування в низці досліджень і дозволений до застосування для лікування тромбоцитопенії в пацієнтів із солідними пухлинами. Емаплаг рекомендується пацієнтам з рівнем тромбоцитів <50×109/л або у випадках, коли лікар вважає за потрібне підвищити кількість тромбоцитів.
Підготував Олексій Терещенко
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...