Оценка терапевтического и профилактического потенциала препарата Канефрон® H в лечении гестационного пиелонефрита у беременных
 Гестационный пиелонефрит (ГПН) – одно из самых распространенных и серьезных заболеваний, возникающее в середине и во второй половине беременности. Почти у 6% женщин ГПН осложняет протекание беременности и является одной из ведущих причин неакушерской дородовой госпитализации. В работе представлены результаты открытого многоцентрового проспективного сравнительного (в параллельных группах) исследования 60 беременных женщин с диагнозом «гестационный пиелонефрит».
Гестационный пиелонефрит (ГПН) – одно из самых распространенных и серьезных заболеваний, возникающее в середине и во второй половине беременности. Почти у 6% женщин ГПН осложняет протекание беременности и является одной из ведущих причин неакушерской дородовой госпитализации. В работе представлены результаты открытого многоцентрового проспективного сравнительного (в параллельных группах) исследования 60 беременных женщин с диагнозом «гестационный пиелонефрит».
Введение
Гестационный пиелонефрит – острый инфекционно-воспалительный процесс с преобладающим поражением интерстициальной ткани, канальцевого аппарата и стенок чашечно-лоханочной системы почки, который впервые развился во время настоящей беременности [1, 2]. Как уже отмечалось, ГПН служит одной из основных причин неакушерской дородовой госпитализации [3, 4]. Ранее эпидемиологические данные показывали, что у беременных заболеваемость ГПН достигает 10% [5], но с улучшением дородового наблюдения частота острого пиелонефрита (ОПН) в последние годы снизилась. В настоящее время используется понятие «острый и хронический пиелонефрит гестационного периода», которое включает в себя пиелонефрит (ПН), возникающий во время беременности, родов и в послеродовой период.
Симптомы ОПН беременных такие же, как и при вторичном ОПН другого происхождения. Заболевание начинается остро, ему часто свойственно тяжелое течение с интоксикацией. Клиническая картина включает боли в пораженной почке, повышение температуры тела гектического характера, часто наблюдаются: головная боль, общая слабость, значительное ухудшение общего состояния, озноб. Иногда присутствует симптоматика почечной колики. Возможно развитие уросепсиса [6, 7].
ГПН чаще возникает во время первой беременности и отрицательно влияет на ее течение и состояние плода (высокая частота прерывания беременности, анемии, ранние гестозы и преэклампсии, задержки роста и дистресс плода) [3], а новорожденные нередко имеют признаки внутриутробного инфицирования. Кроме того, такие дети легче подвергаются гнойно-септическим заболеваниям в постнатальном периоде жизни [4]. Частота бессимптомной бактериурии не увеличивается во время беременности по сравнению с небеременными [8], но физиологические и анатомические изменения, вызывающие мочевой стаз во время беременности, повышают риск развития клинической картины заболевания [9], особенно в середине беременности [10], чаще всего – с правой стороны [3, 7].
Некоторое неблагоприятное влияние на мочевые пути оказывают изменения гормонального фона беременных. Очевидно, что гормоны беременности в первые месяцы вынашивания плода влияют на тонус всех мочевых путей, но в результате увеличения матки определенную роль играют механические факторы, нарушающие отток мочи из почек [2, 11].
Следует отметить, что ГПН отрицательно влияет на организм не только матери, он способствует развитию гипотрофии плода, уменьшению массы тела новорожденного, увеличивает опасность мертворождения.
Сегодня лечение ГПН у беременных следует признать довольно агрессивным, в частности всех пациенток направляют в стационар, где они проходят курс антибиотикотерапии (АБТ) до афебрильных показателей в течение 24 ч и улучшения клинической симптоматики [12, 20], чтобы минимизировать возможность повреждения почек и отрицательное влияние на плод.
У 20% женщин после перенесенного ГПН функция почек остается пониженной [7]. Важно, чтобы в период гестации применялись не обладающие эмбриотоксическим действием средства, каковыми являются, например, препараты на растительной основе [5, 11].
Сегодня в арсенале практикующих врачей имеется препарат Канефрон® Н, содержащий компоненты растительного происхождения и отличающийся хорошей переносимостью, отсутствием отрицательного влияния на плод и достаточно широким и успешным опытом применения в акушерстве, что делает этот препарат особенно привлекательным для лечения ГПН [3].
Целью исследования стало изучение возможностей улучшения лечения ГПН с помощью фитопрепарата Канефрон® Н.
Материалы и методы
Было проведено открытое моноцентровое проспективное сравнительное (в параллельных группах) исследование с участием беременных (n=60), имеющих воспалительное заболевание верхних мочевых путей: острый ГПН. В зависимости от выбранной тактики лечения больные были распределены на 2 равные группы: основная группа (n=30) получала АБТ для купирования клинической симптоматики и лабораторных проявлений в течение 7 дней + Канефрон® Н в стандартных дозировках с последующим переходом на Канефрон® Н в течение 3 мес с целью профилактики рецидива инфекционно-воспалительного процесса.
Группа сравнения (n=30) получала стандартную АБТ с целью купирования клинической симптоматики и лабораторных проявлений в течение 7 дней без дальнейшей терапии препаратом Канефрон® Н.
Канефрон® Н назначали в виде раствора (водно-спиртовой экстракт) по 50 капель 3 р/сут или по 2 таблетки 3 р/сут в течение 30 дней.
Пациентки были отобраны в группы методом слепой выборки. Для того чтобы оценить эффективность проведенных реабилитационно-профилактических мероприятий, в исследование включены беременные с ГПН, возникшим до 30-й нед беременности.
Критериями включения были установленный диагноз «гестационный пиелонефрит» и возраст пациенток 18-45 лет.
Критериями исключения были: пороки развития мочевыделительной системы; индивидуальная непереносимость компонентов препарата Канефрон® Н; наличие коралловидных камней и конкрементов, нарушающих уродинамику; сахарный диабет; хроническая почечная недостаточность; отсутствие согласия на участие в исследовании.
Пациентки в обеих группах были сопоставимы по возрасту (от 19 до 35 лет), паритету, наличию соматической патологии, сроку госпитализации. Все беременные получили консультации терапевта, уролога, гинеколога, нефролога. Лечение проводилось в условиях стационара.
Клиническими методами обследования были: общеклинические анализы крови и мочи, уровень креатинина и мочевины сыворотки крови, УЗИ. Проведение бактериологических исследований – на момент поступления, на 14-й, 35-й и 90-й день после начала терапии. Мочу на бактериальный посев и чувствительность к антибактериальным препаратам получали с помощью катетера Нелатон 6 Fr., клинически значимым показателем бактериурии считали >105 КОЕ уропатогена/мл в моче.
Ультрасонографическое обследование почек осуществляли с регистрацией пульсационного индекса (ПИ) и индекса резистентности (ИР) в почечной артерии и сегментарных, междолевых и дуговых артериях почки. УЗИ и, в случае необходимости, ядерно-магнитное резонансное исследование рекомендованы Европейской ассоциацией урологов (EAU‑2015, степень В) для обследования этой когорты пациенток вследствие минимального воздействия таких методик на развитие плода. Рентгенологические и радиоизотопные исследования беременных противопоказаны из-за возможного вредного воздействия на плод. Нежелательны и эндоскопические исследования.
Статистическая обработка вариационных рядов включала подсчет средних величин (М) и средних ошибок (м). Сравнение вариационных рядов осуществлялось с помощью критерия Стьюдента.
Результат
Средний возраст беременных на момент постановки диагноза составлял 23±6,23 года (± среднее стандартное отклонение), для 39 (65%) женщин это была первая беременность.
Беременные с острым воспалительным процессом в почках были госпитализированы в стационар на таком сроке гестации: 12-16 нед – 11 (17,5%) женщин, 16-22 нед – 22 (36,7%) женщины, 23-30 нед – 27 (45,8%) женщин. Все пациентки на момент поступления получали антибактериальные препараты цефалоспоринового ряда, а при получении посева беременные продолжали прием либо же их в течение 7 дней переводили на другой антибактериальный препарат согласно чувствительности.
Наиболее распространенными жалобами при поступлении в стационар были: боль в пояснице (96,2%), дизурия (70,2%), повышение температуры тела >38 °С (64,4%), озноб (31,9%) и другие (50,3%). В общем анализе мочи в 100% случаев была пиурия, а в 38,2% – микроскопическая гематурия. Средние показатели гемоглобина при поступлении составляли 111±6,7 г/л. Средний показатель лейкоцитов в крови составлял 12,1±4,6×109/л.
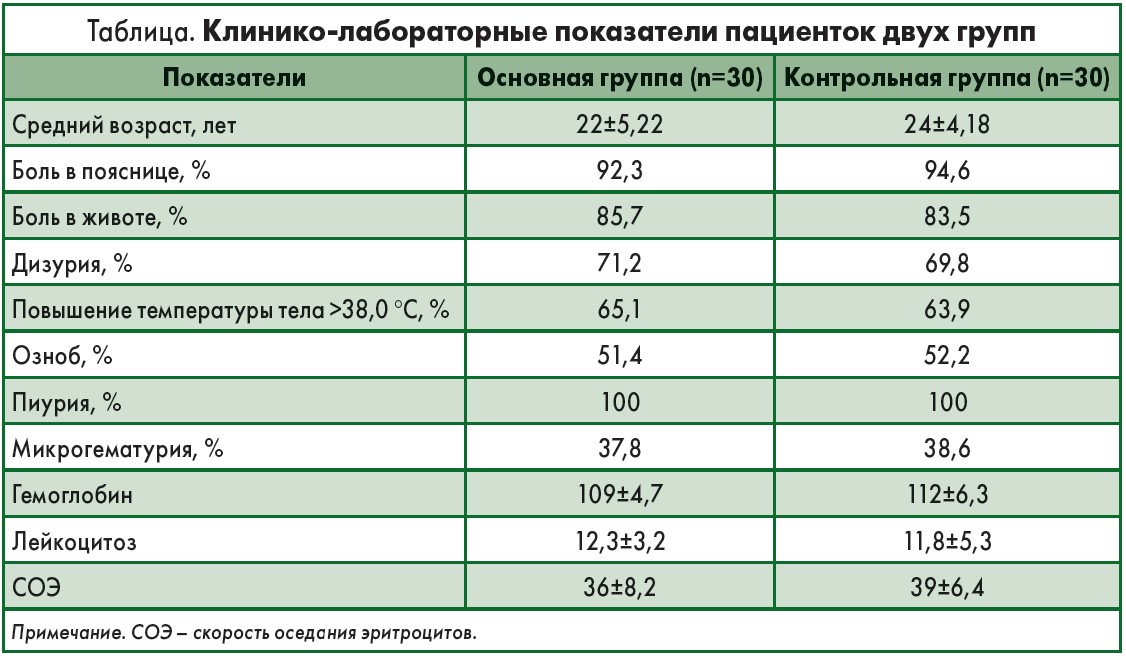
Средняя температура тела при поступлении составила 37,5±0,9 °C, а симптом Пастернацкого был положительным чаще с правой, чем с левой стороны: в 76 из 120 (63,3%) случаев против 29 из 120 (24,2%) случаев соответственно, а также был двусторонним в 15 (12,5%) случаях. Клинико-лабораторные показатели по распределению пациенток двух групп приведены в таблице.
Всем пациенткам при поступлении в стационар проводили акушерское УЗИ – результаты у всех женщин были в норме. У 78 (65%) пациенток по данным УЗИ отмечалась нормальная проходимость мочеточников, у 43 (35,8%) был выявлен уретерогидронефроз, при этом 12 из них установили почечные стенты до конца родов, во всех остальных случаях уретерогидронефроза было достаточно коленно-локтевого положения.
Бактериурия была обнаружена у 100% пациенток с преобладанием E.сoli в 84,2% (101 из 120) случаев, другими патогенами были Klebsiella spp. (9,17%, 11 из 120) и Proteus spp. (6,67%, 8 из 120), которые были наиболее чувствительными к цефтриаксону (81,55% случаев), цефазолину (79,5%), амоксициллину + клавулановой кислоте (77,1% случаев), цефотаксиму (72,6%), гентамицину (60,57% случаев).
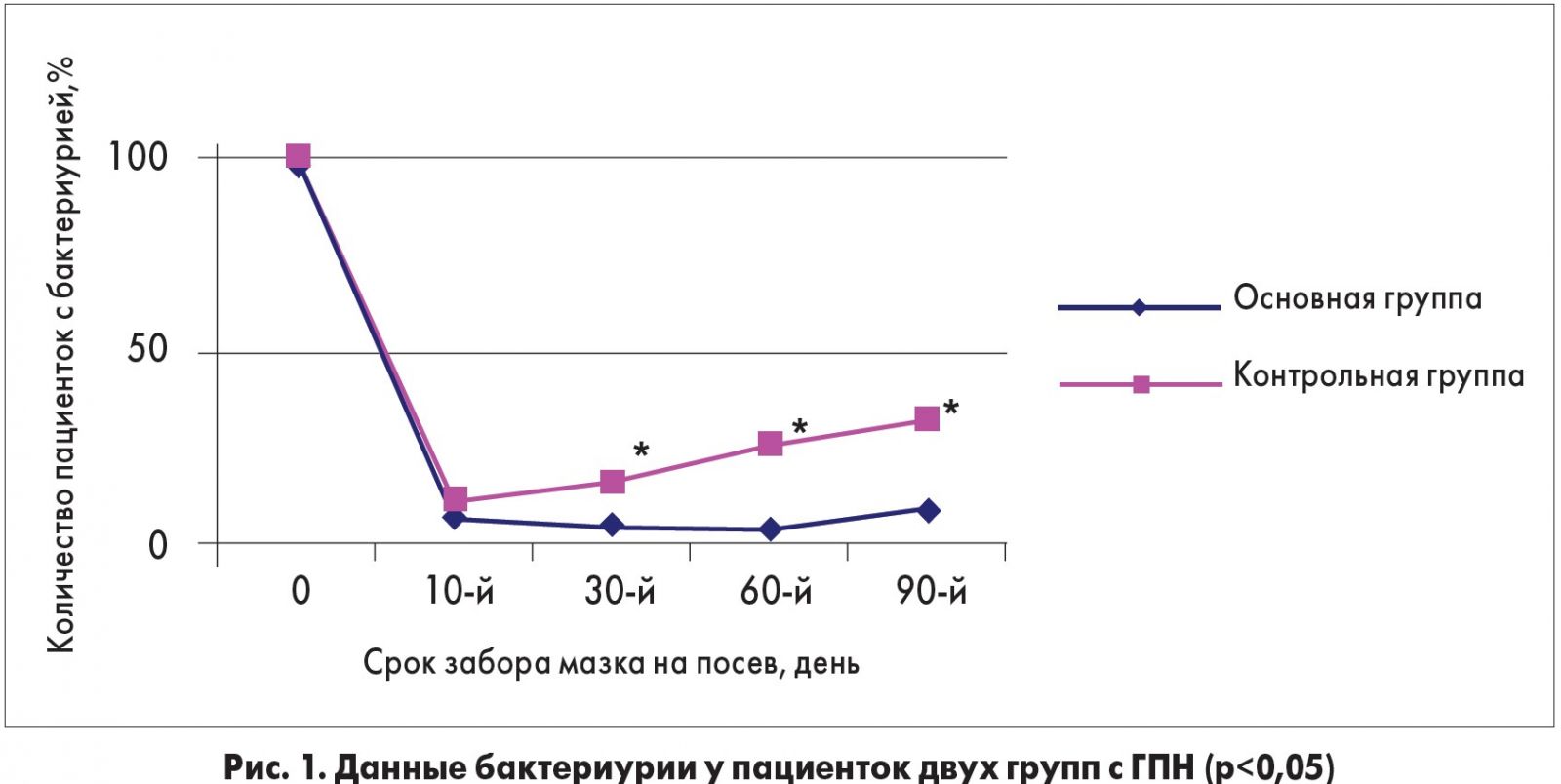
Женщинам из основной группы с целью реабилитации продлили лечение с помощью Канефрона Н, в контрольной группе лечение не было назначено. На 10-е сут в основной группе с ГПН бактериурия была обнаружена у 3 (10%) женщин, в контрольной – у 4 (13,3%) пациенток с ГПН (р>0,05); на 30-е сут в основной группе бактериурия была обнаружена у 2 (6,67%) пациенток, в контрольной – у 5 (16,7%) (р<0,05); на 60-й день в основной группе – у 2 (6,67%), в контрольной – у 8 (26,7%) (р<0,05); на 90-й день – у 3 (10%) и 10 (33,3%) соответственно (р<0,05). Результаты бактериурии у пациенток двух групп с ГПН представлены на рисунке 1.
Как видно из рисунка, на 30-й день в основной группе количество пациенток с бактериурией по сравнению с группой контроля было меньше в 2 раза, на 60-й день – в 4 раза, на 90-й день – в 3 раза соответственно.
Рецидив заболевания произошел у 1 (3,33%) пациентки из основной группы и у 3 (10%) пациенток из контрольной группы (p<0,05).
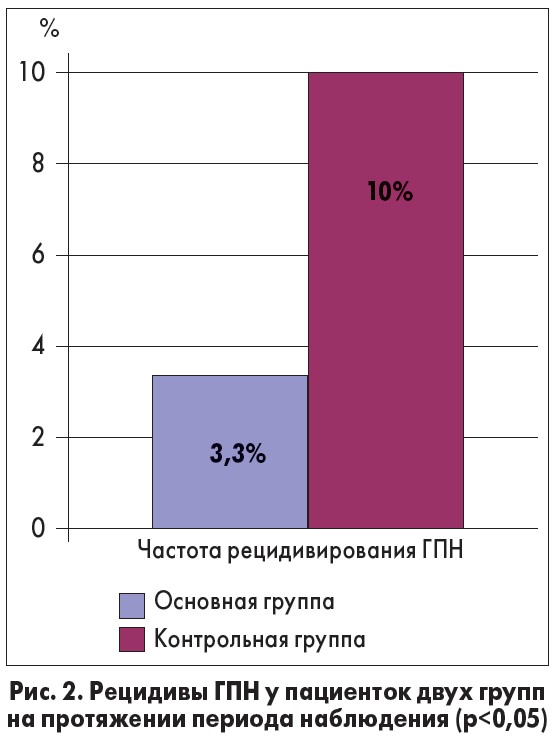 Рецидивы ПН у пациенток двух групп с ГПН представлены на рисунке 2.
Рецидивы ПН у пациенток двух групп с ГПН представлены на рисунке 2.
Рисунок четко демонстрирует, что рецидивы ГПН возникали значительно реже у пациенток основной группы.
По данным допплерографического обследования почечных артерий при ОПН отмечен патологический рост значений ПИ (1,63±0,15), ИР (0,73±0,12) и объемной скорости кровотока на уровне почечной артерии (417±29 мл/мин). АБТ способствовала восстановлению почечного кровотока и нормализации показателей ИР и ПИ в обеих исследуемых группах (р>0,5). Через 30 дней с момента начала лечения в основной группе показатели ИР и ПИ находились в физиологических пределах (0,59±0,04 и 1,12±0,13 соответственно), в то время как в контрольной группе они были очевидно выше (0,71±0,09 и 1,33±0,12 соответственно), что свидетельствовало о высоком риске рецидива (p<0,05).
Объемная скорость кровотока на уровне почечной артерии в основной группе (Канефрон® Н) составила 283±28 мл/ мин, в группе сравнения – 302±32 мл/мин (р>0,5). Перенесенный ГПН осложнил угрозой выкидыша 9 (7,5%) беременностей, преждевременных родов – 14 (11,7%) беременностей, что и произошло в 3 (2,5%) случаях. Побочных эффектов у беременных после приема препарата Канефрон® Н не было, пациентки отмечали его хорошую переносимость.
Обсуждение
По данным T.F. Patterson и соавт. (1997), частота бессимптомной бактериурии не возрастает во время беременности по сравнению с небеременными [4], но физиологические и анатомические изменения, вызывающие мочевой стаз в период вынашивания плода, повышают риск развития клинической картины заболевания [17], особенно в середине беременности [16], и больше с правой стороны [7].
Средний возраст беременных на момент постановки диагноза в нашем исследовании составил 23±6,23 года, у 39 (65%) женщин это была первая беременность. Для сравнения – в исследовании L.C. Gilstrap (1991) первая беременность была у 75% [9].
Особенности патогенеза заболевания позволяют утверждать, что основной причиной возникновения гипотонии мочевых путей и нарушения уродинамики являются нейрогуморальные факторы, возникающие на фоне механического давления увеличенной матки на мочеточники. Гипотония мочеточников в сочетании с их обструкцией увеличенной маткой приводит к уростазу, застою мочи в мочеточниках и чашечно-лоханочной системе почек, что способствует инфицированию [14, 15].
В своих исследованиях L.C. Gilstrap и соавт. (2001) и L.K. Millar и соавт. (2003) изучали, как влияет наличие ПН на здоровье матери и плода [8, 11]; было установлено, что лихорадка в первом триместре беременности во время органогенеза ассоциировалась с тератогенностью, выкидышем и преждевременными родами.
В нашем исследовании в 84,2% (101 из 120) случаев была высеяна E. сoli, обладавшая 82% чувствительностью к цефтриакcону, что сопоставимо с результатами предыдущих исследований, осуществленных А. Faundes и соавт. (2008) и Y.D. Fan и соавт. (2011) [7, 18].
Лечение ГПН начинают с восстановления нормального оттока мочи из почки. Для этого применяют терапию положением: больной рекомендуют лежать на «здоровом» боку, с приподнятой в изножье кроватью, принимать коленно-локтевое положение. В некоторых случаях даже эта простая процедура приводит к снижению остроты воспалительного процесса в почке благодаря уменьшению давления увеличенной матки на мочеточник. Если показанная консервативная терапия неэффективна, а при обследовании выявлены нарушения оттока мочи из пораженной почки, можно применять стентирование мочеточника. Как правило, катетер-стент удается провести без помех через весь мочеточник к почечной лоханке, причем выделение из него мочи частыми каплями или даже струей начинается на высоте 13-20 см от мочевого пузыря, то есть как раз над тем уровнем, где матка прижимает мочеточник к самому узкому месту костного кольца таза. Катетер-стент целесообразно оставлять на несколько недель после родов.
Параллельно при необходимости проводят АБТ с применением наименее токсичных антибактериальных препаратов, особенно до 12-й нед беременности. После этого срока можно расширить перечень антибактериальных препаратов, в частности назначить аминогликозиды и др. Это связано с тем, что до 12-й нед заканчивается формирование основных органов и систем плода.
Для лечения ОПН беременных EAU‑2015 (степень А) рекомендует: цефтриаксон 1-2 г внутривенно или внутримышечно каждые 24 ч; азтреонам 1 г внутривенно каждые 8-12 ч; пиперациллин-тазобактам 3,375-4,5 г внутривенно каждые 6 ч; цефепим 1 г внутривенно каждые 12 ч; имипенем-циластатин 500 мг внутривенно каждые 6 ч; ампициллин 2 г внутривенно каждые 6 ч; гентамицин 3-5 мг/кг/сут внутривенно в 3 приема.
Таким образом, у беременных ОПН даже с тяжелым течением сегодня успешно лечится и не считается препятствием к благоприятному разрешению беременности. У большинства женщин физиологические изменения со стороны мочевых путей, вызванные беременностью, после родов исчезают без каких-либо последствий. Вместе с тем следует отметить, что у женщин, перенесших ОПН, нарушения уродинамики не всегда проходят бесследно. Чаще всего следствием этого заболевания является ХПН, реже – мочекаменная болезнь и другие заболевания.
Итак, беременные женщины, перенесшие ПН, у которых в 25-30% определяется послеродовой ПН, более остальных женщин склонны к развитию почечных заболеваний вследствие перенесенного длительного нарушения уродинамики [16, 19]. ГПН может возникнуть в послеродовой период в первые дни или недели после родов, когда еще не полностью восстановился тонус мочевых путей.
К факторам риска послеродового ПН следует отнести: гормоны беременности (3 мес) и расширение мочевых путей (около 1,5 мес); воспалительные заболевания половых органов; осложнения послеродового периода (гипотония матки, кровотечения и др.). В случае послеродового ПН проводят тщательное урологическое обследование, включая рентгенологическое и радиоизотопное исследование, для определения состояния почек и мочевых путей, а также выявления или исключения любых других причин ПН – аномалий мочевой системы, туберкулеза, камней в почках.
Заслуживающие внимания данные приводят N. Pazos Otero и соавт. (2007), изучавшие данные 4700 беременных в течение года. Уровень заболеваемости ПН составил 0,21%, у всех исследуемых был высеян один возбудитель – E. coli. Во всех случаях прогноз был благоприятный [17].
Профилактика ОПН осуществляется по двум основным направлениям: превентивное лечение хронической мочевой инфекции и улучшение оттока мочи из почек с помощью позиционных упражнений: больной рекомендуют периодически становиться в коленно-локтевую позу, лежать только на боку, противоположном стороне преимущественного расширения почечной лоханки, с приподнятой в изножье кроватью.
При выполнении этих упражнений особое значение уделяют профессиональному инструктажу пациентки врачом и акушеркой. Во всех указанных положениях уменьшается давление матки на мочеточники, улучшается отток мочи, значительно уменьшается расширение почечных лоханок. Это подтверждается данными ультрасонографии, под контролем которой желательно проводить профилактику ПН.
Таким образом, сочетание противомикробного и противовоспалительного свойств препарата Канефрон® Н позволило достоверно снизить уровень бактериурии и количество рецидивов у пациенток с ГПН. Канефрон® Н – это хорошо зарекомендовавшее себя лекарственное средство на растительной основе для лечения инфекций мочевыводящих путей у беременных, поскольку он имеет стандартизированный состав и оптимальный комплекс эффектов, необходимых для успешной терапии указанных заболеваний. Важно отметить, что широкий спектр растительных компонентов, обладающих антибактериальным действием, значимо уменьшает риск бактериальной резистентности и обусловливает эффективность препарата Канефрон® Н в условиях длительной профилактической терапии. Немаловажным преимуществом препарата Канефрон® Н является его абсолютная безопасность для пациентов с инфекциями мочевыводящих путей, особенно у беременных.
Выводы
1. Препарат Канефрон® Н достоверно уменьшает развитие бактериурии у пациенток основной группы, в сравнении с таковыми из группы контроля, на 30-й день – в 3 раза: у 2 из 30 женщин (6,67%) против 5 из 30 (16,7%) соответственно, на 60-й день – в 4 раза: у 2 из 30 (6,67%) против 8 из 30 (26,7%) соответственно, на 90-й день – в 3 раза: 3 случая из 30 (10%) против 10 (33,3%) соответственно.
2. Фитопрепарат Канефрон® Н статистически достоверно в 3 раза уменьшает частоту рецидивов заболевания у пациенток основной группы, в сравнении с таковыми из группы контроля, в течение периода наблюдения: у 1 из 30 (3,33%) против 3 из 30 (10%) соответственно.
Список литературы находится в редакции.
EUREKA: Health Sciences, № 3
Тематичний номер «Урологія. Нефрологія. Андрологія» № 2 (13), червень 2018 р.
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
У лютому відбулася щорічна Всеукраїнська науково-практична конференція «Малоінвазивні технології в урології», присвячена актуальним проблемам сучасної урології. Пропонуємо огляд найцікавіших доповідей, що прозвучали в рамках заходу....
Інфекції сечовивідних шляхів (ІСШ) у всьому світі посідають провідне місце серед інфекційних захворювань дорослого населення. Поряд із тим серед фахівців зростає занепокоєння щодо триваючого зростання стійкості бактерій до більшості антибіотиків. Експерти провідних міжнародних товариств наголошують на необхідності розсудливого і виваженого призначення антимікробних препаратів. Про основні принципи раціональної антибіотикотерапії в урології, зокрема при проведенні діагностичних і хірургічних втручань, ми попросили розповісти завідувача відділу відновної урології та новітніх технологій ДУ «Інститут урології ім. акад. О.Ф. Возіанова НАМН України», доктора медичних наук, професора В’ячеслава Миколайовича Григоренка. ...
Процедура трансректальної біопсії простати супроводжується високим ризиком інфекційних ускладнень, тому проведення антимікробної профілактики при цьому втручанні є обов’язковим. Однак зростання антибіотикорезистентності, а також нещодавні рекомендації щодо обмеження призначень фторхінолонів значно звужують спектр можливих варіантів такої профілактики. Міжнародною мультидисциплінарною групою експертів на основі літературних джерел та клінічного досвіду було розроблено ряд настанов стосовно запобігання інфекційним ускладненням при біопсії простати та обґрунтовано доцільність і переваги призначення з цією метою фосфоміцину ...
Кількість людей, які страждають і помирають від вірусного гепатиту В (ВГВ), можна порівняти з кількістю хворих на коронавірусну хворобу 2019 року (COVID‑19), яка наразі викликає велике занепокоєння в усьому світі. Тому вкрай важливим залишається питання передачі вірусу, у тому числі через статеві клітини. Попередніми дослідженнями встановлено, що гени ВГВ, інтегровані в людські сперматозоїди, здатні до реплікації та експресії після передачі ембріонам. Однак досі це явище не було підтверджено клінічними дослідженнями у пацієнтів. Автори вивчали особливості інтеграції ВГВ у геном сперматозоїдів пацієнтів та аналізували можливі клінічні наслідки для потомства ...