Місце макролідів у лікуванні гострого бронхіту бактеріального ґенезу
24-25 червня 2021 року відбувся ІІ Міжнародний медичний онлайн-форум міжсекторальної взаємодії лікарів STOP INFECTIONS, що об’єднав фахівців різних медичних спеціальностей для обговорення проблеми зниження ефективності антибіотиків (АБ) і пошуку нових підходів у боротьбі з АБ‑резистентністю (АБР). Учасники мали змогу прослухати доповіді провідних експертів з різних країн щодо цього питання з метою підвищення компетентності та покращення результатів для пацієнта.
Доцент кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П. Л. Шупика (м. Київ), кандидат медичних наук Людмила Володимирівна Юдіна присвятила свою доповідь питанням необхідності застосування та вибору АБ у терапії гострого бронхіту (ГБ).
На початку свого виступу спікерка звернула увагу на те, що кашель з гострим початком є однією з найчастіших причин звернення по амбулаторну медичну допомогу. В переважній більшості випадків такий кашель – симптом ГБ. Згідно з визначенням, ГБ характеризується гострим розвитком кашлю, що триває не більше 3 тиж (незалежно від наявності мокротиння), за відсутності ознак пневмонії та хронічних захворювань легень, які можуть бути причиною кашлю. Отже, діагноз ГБ є по суті діагнозом виключення.
Етіологія ГБ
Основна причина ГБ – віруси (зокрема, аденовіруси, коронавіруси, віруси Коксакі, ентеровіруси, віруси грипу та парагрипу, респіраторно-синцитіальний вірус, риновіруси тощо), на які припадає ≈90% випадків захворювання. За даними мікробіологічних досліджень, ГБ має бактеріальну природу менше ніж у 10% випадків. У 45% випадків ГБ бактеріальної етіології вдається виявити типові збудники (Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Staphylococcus aureus) і приблизно у 25% – атипові патогени (Mycoplasma pneumoniae, Chlamydophila pneumoniae, Bordetella pertussis).
ГБ може розвиватися у відповідь на екстремальні температури повітря, хімічні сполуки (оксиди азоту, двоокис сірки, отруйні гази), різноманітні алергени (пилок рослин, органічний пил).
Незважаючи на незначний внесок бактеріальних збудників в етіологічній структурі ГБ, це захворювання на сьогодні вважається найпоширенішою причиною помилкового призначення АБ. За різними даними, в 70-90% випадків лікарі первинної ланки в разі ГБ вважають необхідним призначити АБ, при цьому на користь таких дій у лікарів є свої вагомі аргументи: побоювання «пропустити» тяжке захворювання (наприклад, пневмонію), намагання уникнути можливих медико-юридичних проблем (негативна реакція пацієнтів, звинувачення лікаря в некомпетентності). Нерідкими є випадки, коли пацієнти самі вимагають призначення АБ. Звісно, що така ситуація сприятиме подальшому зростанню АБР, але це мало цікавить конкретного пацієнта.
Отже, широке призначення АБ з метою лікування ГБ є помилковим. Як при цьому не пропустити ГБ бактеріальної етіології? З високою імовірністю про бактеріальну природу захворювання свідчать такі ознаки:
→ зниження температури тіла до субфебрильних цифр;
→ наявність слизово-гнійного чи гнійного мокротиння;
→ ознаки інтоксикації;
→ змінені фізикальні дані;
→ можливі зміни в загальному аналізі крові (кількість лейкоцитів ≥10,4×109/л).
Також слід пам’ятати про ознаки, які свідчать на користь ГБ, зумовленого атиповими збудниками.
Так, для мікоплазмових бронхітів характерні лихоманка, фарингіт, міалгії, астенія та позалегеневі ускладнення. Захворювання може виліковуватися спонтанно протягом 1-2 тиж, але нерідко триває 4-6 тиж з усіма проявами хвороби, включаючи кашель зі слизовим мокротинням.
Клінічна картина хламідійних бронхітів, окрім проявів ГБ, включає фарингіт і ларингіт. Звичайними ознаками захворювання є осиплість голосу, субфебрилітет, постійний кашель, який часто залишається сухим (мокротиння зазвичай слизове та не буває гнійним). У хворих на бронхіальну астму хламідійна інфекція нерідко провокує почастішання нападів ядухи.
Лікування ГБ бактеріальної етіології
Під час призначення антибактеріальної терапії обов’язково слід ураховувати найімовірніший збудник захворювання, спектр активності АБ, місцеві дані щодо резистентності. АБ вибору в лікуванні бактеріальних інфекцій нижніх дихальних шляхів є β-лактами, макроліди чи фторхінолони. На сьогодні з цією метою найчастіше застосовують β-лактами, однак масове застосування препаратів цього класу зумовлює постійне зростання АБР, а також поступову втрату їхньої ефективності. Перед призначенням β-лактам слід обов’язково розглянути клінічні ситуації, за яких ці АБ можуть не спрацювати чи спричинити побічні ефекти:
→ алергія на β-лактами;
→ передбачувана атипова флора;
→ лікування β-лактамом в останні 3 міс;
→ наявність алергічних захворювань (бронхіальна астма, атопія тощо).
Поширеність резистентних збудників
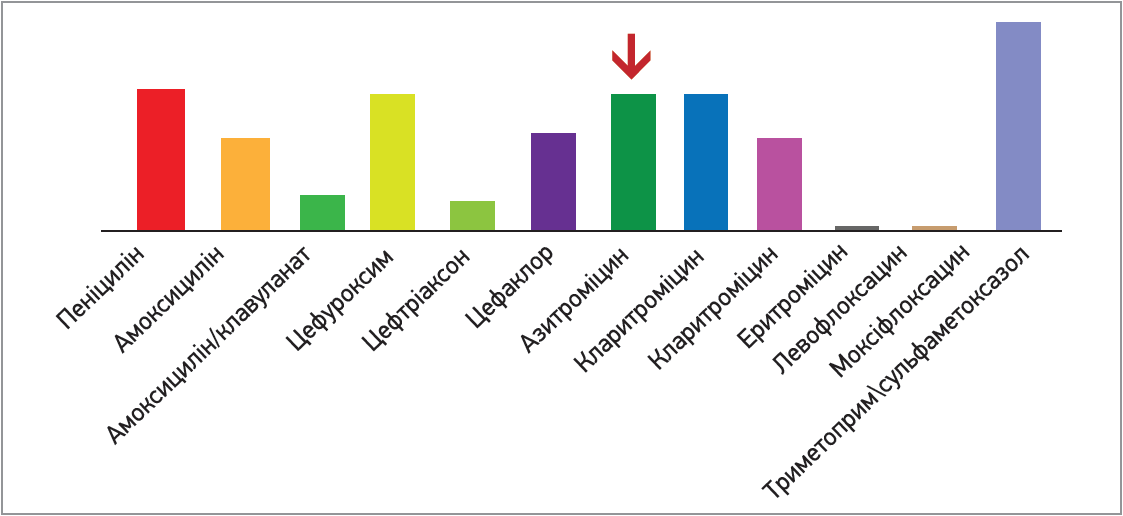
Об’єктивні дані щодо АБР в Україні надають результати SOAR (Survey of Antibiotic Resistance) – проспективного багатоцентрового мікробіологічного дослідження; його мета – вивчення поширеності резистентних штамів S. pneumoniae та H. influenzae, які були виділені в дітей і дорослих з негоспітальними інфекціями дихальних шляхів у різних регіонах України. Згідно з отриманими даними, стійкість пневмокока до азитроміцину в Україні становить 16,0% (рис. 1).
Рис. 1. Поширеність нечутливих штамів S. pneumoniae до АБ в 2014-2016 роках
Рис. 2. Вплив макролідів на пригнічення цитохрому Р450 у печінці
У південних регіонах США частота цієї резистентності є ще вищою і сягає 30,9-43,2%. Цікаво, що в 1995 р. (у США) резистентність S. pneumoniae до макролідів ледь сягала 10%, але паралельно з виходом на ринок азитроміцину і зростанням його продажів показники резистентності почали зростати, сягнувши 20% наприкінці 1990-х рр. і 30% – у ранні 2000-ні рр. Аналогічну тенденцію відзначили також і фінські науковці: збільшення стійкості S. pneumoniae до макролідів було пов’язане з недоцільним використанням цієї групи АБ, зокрема азитроміцину. Для запобігання подальшому зростанню такої резистентності слід уникати некоректного застосування макролідів.
Проблема резистентності до макролідів
Стійкість мікроорганізмів до макролідів у >90% випадків визначається двома механізмами: виробленням ферменту метилази (модифікація мішені) й активним виведенням АБ з мікробної клітини (ефлюкс). У штамів S. pneumoniae, S. pyogenes частіше за все спостерігається останній механізм. 16-членний макролід спіраміцин не «виштовхується» із клітини (на відміну від 14- й 15-членних макролідів азитроміцину та кларитроміцину), а резистентність до нього є менш вираженою, ніж до інших макролідів. Спіраміцин активний щодо 75% штамів S. pyogenes і S. pneumoniae, резистентних до 14- та 15-членних макролідів, а також проти атипових патогенів: Mycoplasma pneumoniae, Chlamydophila pneumoniae, Legionella pneumophila. Натомість амоксицилін, амоксицилін/клавуланат, цефуроксим і цефтріаксон на ці бактерії не діють.
Інші переваги спіраміцину
Особливістю спіраміцину є його здатність створювати високі внутрішньоклітинні та позаклітинні концентрації у вогнищі інфекції на тривалий період часу. На відміну від 14-членних макролідів спіраміцин здатен зв’язуватися не з одним, а одразу із трьома доменами 50S субодиниці рибосоми (тобто міцніше), що забезпечує триваліший антибактеріальний ефект, а неміцне зв’язування з білками плазми дає спіраміцину можливість добре проникати в тканини організму. Концентрація спіраміцину в тканинах (легені – 45 мг/кг, мигдалики – 29,5 мг/кг, інфікована слизова оболонка приносових пазух – 21,5 мг/кг) у декілька разів перевищує МПК90 для більшості збудників респіраторних інфекцій. Спіраміцину властивий своєрідний парадокс: його висока клінічна ефективність не відповідає помірній активності in vitro.
Спіраміцин не взаємодіє із системою цитохромів Р450 печінки, тому не впливає на метаболізм інших препаратів (рис. 2). Порівняно з іншими макролідами препарат характеризується найменшою здатністю до взаємодії з іншими лікарськими засобами.
На відміну від більшості АБ спіраміцин майже не впливає на шлунково-кишковий тракт; практично не зумовлює діареї, оскільки не має спорідненості до мотиліну – гормона, який виробляється в слизовому шарі шлунково-кишкового тракту; є неактивним щодо бактерій роду Enterobacteriaceae (Escherichia coli, Enterobacter aerogenes), тому не спричиняє розвитку дисбіозу кишечнику.
Зазначені переваги спіраміцину сприяють його більш широкому використанню в клінічній практиці. За даними звіту Всесвітньої організації охорони здоров’я (2016), щороку спіраміцин приймають ≈8 млн пацієнтів; ця кількість постійно зростає.
Наостанок Людмила Володимирівна ще раз нагадала:
- ГБ у більшості випадків спричиняється вірусною інфекцією, тому АБ є неефективними;
- якщо процес затягується на >5-10 днів, слід запідозрити приєднання бактеріальної інфекції та розглянути можливість призначення АБ;
- як препарати першого вибору рекомендовані β-лактами;
- з огляду на значну ймовірність атипових збудників ГБ препаратами вибору можуть бути макроліди;
- зростання резистентності S. pneumoniae до макролідів у всьому світі змушує звернути увагу на спіраміцин, який продовжує бути актуальним у лікуванні інфекцій дихальних шляхів.
На сьогодні спіраміцин залишається одним з небагатьох природних АБ, які продовжують зберігати клінічне значення на тлі зростання резистентності мікроорганізмів.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 16 (509), 2021 р.
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
Риносинусит (РС) є одним із найчастіших захворювань у первинній медичній практиці. Трьома найбільш чутливими й специфічними симптомами гострого РС є виділення з носа, закладеність носа, лицевий і головний біль. Неконтрольований гострий біль значно погіршує якість життя пацієнтів із РС: спричиняє психоемоційні розлади, знижує працездатність і соціальну активність, сприяє хронізації больового синдрому і збільшує вартість лікування. Отже, полегшення болю при РС є найпершим завданням лікаря....
У всьому світі біль у горлі, зумовлений запальними захворюваннями горла (ЗЗГ), є найчастішою причиною звернень до лікарів загальної практики та оториноларингологів; із ним пов’язано ≈25% відвідувань лікаря. За даними Всесвітньої організації охорони здоров’я, >100 соматичних захворювань із провідним інфекційно-залежним і токсико-алергічним механізмом пов’язані саме із ЗЗГ. Здебільшого причина болю в горлі – гостре запалення інфекційного ґенезу: ГТ, ГФ і ГРВІ....
Антибіотикорезистентність (АБР) визнано загрозою для глобального здоров’я, яка щороку спричиняє мільйони смертей в усьому світі. Невідповідне та надмірне використання антибіотиків (АБ) зумовлює підвищення стійкості мікробних збудників і негативно впливає на ефективність цих дуже важливих лікарських засобів. Завдяки Глобальному плану дій щодо АБР Всесвітня організація охорони здоров’я (ВООЗ) працює над поліпшенням нагляду за резистентністю до протимікробних препаратів і скороченням нераціонального використання АБ. ...
Медичні інформаційні кампанії спрямовані на поширення важливих знань про охорону здоров’я серед населення. З урахуванням потреб і інтересів понад семи мільярдів людей у світі міжнародні організації шукають способи етичного обміну важливими відомостями, без упередженості та несправедливості. Обізнаність у сфері охорони здоров’я має вирішальне значення для кожного, оскільки хвороби та інфекції можуть вразити будь-кого в будь-який час. Таким чином, важливо поширювати відомості про охорону здоров’я за допомогою зрозумілих кожному усних, письмових і візуальних засобів. Ця інформація має сприяти соціальному здоров’ю і не містити дискримінаційного контенту. Заходи з підвищення обізнаності про здоров’я допомагають пацієнтам ліпше розуміти стан свого здоров’я, а також можливі варіанти та методи лікування. Кампанія з підвищення обізнаності відрізняється від маркетингу товарів для здоров’я, оскільки не спонукає купувати той чи інший продукт, а намагається сприяти свідомішому ставленню до свого здоров’я. Глобальні дні громадського здоров’я пропонують великі можливості для підвищення обізнаності та розуміння проблем здоров’я і мобілізації підтримки дій від місцевої громади до міжнародної спільноти. ...