Мультиомічний склад грудного молока: роль у розвитку малюкових кольок
Малюкові кольки є однією з найпоширеніших та найскладніших проблем, з якими лікарі-педіатри стикаються у своїй клінічній практиці. Один із факторів, який може впливати на розвиток малюкових кольок, – мультиомічний склад грудного молока, як показали результати нещодавнього дослідження D. Chandran та співавт. (2023). Пропонуємо короткий огляд цього дослідження.
Малюковими кольками називають функціональні шлунково-кишкові розлади, що характеризуються рецидивуючими клінічними епізодами, які не мають ідентифікованої органічної причини. Римські критерії IV (2016) визначають кольки як поведінковий синдром, що включає постійні епізоди плачу, метушливості та дратівливості у здорових немовлят, які зникають до п’ятимісячного віку (P.E. Hyman et al., 2016). Встановлено, що поширеність кольок коливається від 5 до 20% (F. Campeotto, 2020; M.A. van Tilburg, 2015). Стрес, спричинений кольками, створює значне навантаження на немовлят, їхні родини та систему охорони здоров’я (D.M. Roberts et al., 2004). Нездатність заспокоїти дитину, яка плаче, може посилити розчарування батьків, погіршити стосунки в сім’ї й у важких випадках призвести до фізичного насильства над немовлям (A.A. Gelfand, 2016).
Оскільки етіологія дитячих кольок наразі достеменно невідома, рекомендації щодо їх клінічної діагностики визначають необхідність виключити інші органічні захворювання, перш ніж спиратися на суб’єктивні повідомлення про симптоми від батьків (J.D. Johnson et al., 2015). Навіть якщо діагноз встановлено остаточно, сьогодні немає доведених методів лікування, які повністю усували б симптоми. Натомість у деяких рекомендаціях наголошується про важливість консультування батьків щодо природи кольок і пом’якшення їх симптомів (J.M. Sarasu, 2018; J. Cohen-Silver, 2009). Відсутність об’єктивних діагностичних критеріїв і заснованих на доказах стратегій лікування дитячих кольок обґрунтовує потребу в більш глибокому вивченні патофізіологічних процесів кольок, що є дуже важливим для визначення цільової терапії та покращення результатів.
Сьогодні наявні деякі докази того, що склад жіночого молока може змінювати шлунково-кишкові симптоми у немовлят і впливати на їх темперамент (J. Hahn-Holbrook, 2019; S. Perrella, 2021). Попередні дослідження вказують на те, що модифікація дієти матері може полегшити симптоми завдяки зміні складу вуглеводів у жіночому молоці (M. Iacovou et al., 2018). Однак цілком ймовірно, що цей зв’язок зумовлений складною взаємодією між мікробіомом і метаболічними субстратами, які можуть спричиняти запальні реакції кишечнику (R.M. Duar, 2020; C. de Weerth, 2013). Рандомізоване контрольоване дослідження перинатального застосування пробіотиків у 66 матерів, які годували грудьми, виявило зниження рівня інтерлейкіну (ІЛ) 6, ІЛ-10 і трансформуючого фактора росту (TFG) β1 у жіночому молоці, а також зниження ризику появи кольок у немовлят, яких годували грудним молоком (M.E. Baldassarre et al., 2016).
Сьогодні зростає визнання жіночого молока як складної біологічної системи з імуномодулювальними властивостями (R.P. Garofalo, 1999; D. Newburg, 2007). Окрім загальновизнаних запальних білків (наприклад, цитокінів), іншим класом молекул, які присутні в молоці та відіграють важливу роль в імуномодуляції, є мікрорибонуклеїнові кислоти (miR; B.C. Melnik, 2021; B. Lоnnerdal, 2019). Захищені позаклітинними везикулами, miR у жіночому молоці мають здатність проникати в шлунково-кишковий тракт (ШКТ) немовляти та впливати на експресію генів (Y. Liao, 2017; S. Kahn, 2018). Аномальні коливання в експресії специфічних miR корелюють з наявністю і тяжкістю шлунково-кишкових розладів (M. Casado-Bedmar et al., 2022), однак лише в цьому році Desirae Chandran і співавтори опублікували результати першого дослідження, в якому вивчали взаємозв’язок між рівнями miR у грудному молоці та дитячими кольками.
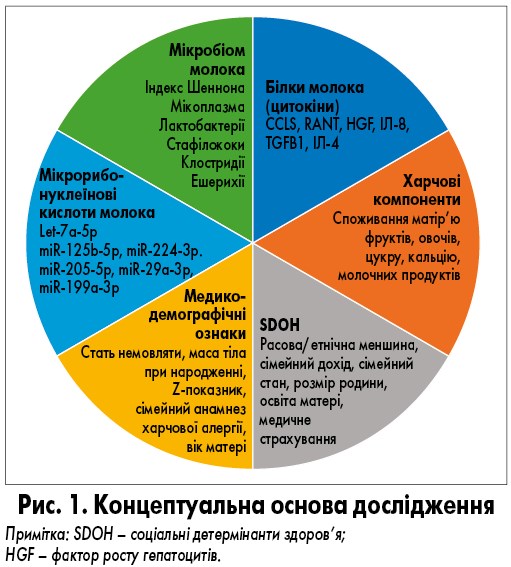 Метою дослідження було виявлення нових компонентів жіночого молока, які модулюють ризик виникнення дитячих кольок. Автори припустили, що рівні специфічних miR, мікробів і цитокінів у жіночому молоці відрізнятимуться у матерів, які годують грудьми немовлят з/без симптомами кольок (рис. 1). У проспективному когортному дослідженні взяли участь 182 діад «мати – немовля» на грудному вигодовуванні.
Метою дослідження було виявлення нових компонентів жіночого молока, які модулюють ризик виникнення дитячих кольок. Автори припустили, що рівні специфічних miR, мікробів і цитокінів у жіночому молоці відрізнятимуться у матерів, які годують грудьми немовлят з/без симптомами кольок (рис. 1). У проспективному когортному дослідженні взяли участь 182 діад «мати – немовля» на грудному вигодовуванні.
Характер і тяжкість симптомів кольок оцінювали у віці 1 місяць за допомогою скороченої версії шкали дитячих кольок (M.L. Cirgin Ellett et al., 2003), що містить 2 підшкали – «незріла шлунково-кишкова система» і «важкий темперамент немовляти». Ці підшкали були спеціально обрані для оцінки як темперамента немовляти, так і супутніх шлунково-кишкових симптомів, які можуть імітувати кольки (наприклад, запору і гастроезофагеального рефлюксу). Немовлята з кольками мали вищий середній бал за модифікованою шкалою дитячих кольок (43±13), ніж немовлята без кольок (31±9). Матері немовлят із симптомами кольок також частіше погоджувалися або повністю погоджувалися з твердженням: «Коли моя дитина починає вередувати, я не можу нічого зробити». Проте не було різниці між групами щодо повідомлень «Моя дитина відригує неперетравленим молоком» або «Моя дитина не відчуває труднощів з дефекацією». Ці результати вказують на те, що група немовлят із кольками була фізіологічно репрезентативною щодо цього стану, а не гастроезофагеального рефлюксу або запору (які часто плутають з кольками). Зразки жіночого молока збирали приблизно через 1 місяць після пологів. Молоко (1-5 мл) зціджували перед годуванням вручну з вимитої милом з водою поверхні соска у пробірки, вільні від РНК. Щоб переконатися, що циркадний ритм і зрілість молока не вплинули на молекулярні характеристики жіночого молока у матерів немовлят з кольками, автори реєстрували годину збору молока та вік дитини під час збору молока. Не було виявлено різниці між часом доби, коли відбувався збір молока, для немовлят із кольками та немовлят без симптомів. Також не було різниці у віці дитини на момент збору.
За результатами дослідження, не було виявлено різниці в рівнях CCL5/RANTES, фактору росту гепатоцитів (HGF), ІЛ-8, TGFβ1, TGFβ2 або ІЛ-4 у молоці матерів немовлят із клінічною симптоматикою порівняно з групою без кольок. Відмінні були лише рівні HGF у жіночому молоці, які безпосередньо пов’язані з модифікованим показником дитячих кольок. При мікробному дослідженні рівні Staphylococcus виявилися вищими в молоці матерів немовлят із кольками порівняно з групою без кольок. Проте не було різниці в рівнях Mycoplasma, Lactobacillus, Clostridium та Escherichia між двома групами. Жоден мікробний фактор не був пов’язаний із тяжкістю симптомів за шкалою дитячих кольок. Завдяки цьому дослідженню отримані нові дані щодо кореляції рівнів miR у жіночому молоці у матерів немовлят із кольками та без. Було виявлено, що рівні miR-omics, зокрема miR-224-3p, miR-125b-5p, let-7a-5p та miR-205-5p, були вищими в молоці матерів, немовлята яких мали симптоми кольок. Рівні miR-29a-3p і miR-199a-3p не відрізнялися між групами.
У дослідженні автори також вивчали комплекс медичних/демографічних факторів, соціальних детермінант здоров’я, харчових компонентів і молекулярних профілів жіночого молока, щоб виявити нові біологічні взаємодії, які можуть сприяти розвитку кольок. Застосовуючи підхід зворотньої регресії, дослідники ідентифікували miR молока, мікроби та цитокіни, які можуть сприяти ризику кольок у немовлят. Зокрема, підвищені рівні HGF, miR-29a-3p та let-7a-5p у молоці були пов’язані з більшою ймовірністю виникнення симптомів кольок, тоді як підвищений рівень Lactobacillus у жіночому молоці, що, на думку дослідників, має захисний ефект, знижував ризик виникнення кольок у немовлят. Три зазначені фактори передбачали наслідки кольок з точністю 76% (чутливість 79% і специфічність 59%). Вплив цих факторів на виникнення кольок перевищив багато медичних/демографічних і соціальних факторів, які раніше пов’язували з ризиком виникнення кольок.
Незважаючи на те, що це перше дослідження, яке спільно оцінює взаємозв’язок між мікробіотою жіночого молока, вмістом miR і цитокінів з дитячими кольками, автори дослідження вважають, що ці висновки значною мірою узгоджуються з попередніми результатами. Наприклад, H. Szajewska і співавт. (J Pediatr, 2013) виявили, що пероральне введення Lactobacillus reuteri сприяє майже 2,5-кратному відносному зниженню ризику виникнення кольок у немовлят протягом 28 днів, що корелює з даними цього дослідження щодо зниження ризику розвитку кольок у 1,78 раза. Докази кореляції підвищених рівнів miR-29a-3p у грудному молоці та ризику розвитку кольок у немовлят узгоджуються з дослідженням кишкового епітелію людини у пацієнтів із діареєю внаслідок синдрому подразненого кишечнику (H. Zhu et al., 2020). Таким чином, підвищений miR-29a-3p у жіночому молоці може призвести до «дірявого кишечнику», що є патофізіологічною основою ряду запальних захворювань ШКТ (A. Michielan et al., 2015).
Сьогодні також з’являються докази того, що HGF жіночого молока відіграє важливу роль у формуванні ШКТ немовлят (C. Hirai et al., 2002). Дослідження клітин тонкої кишки плода, культивованих з жіночим молоком, показало, що рівні HGF пов’язані зі значною трофічною епітеліальною відповіддю. У цьому дослідженні автори підтвердили, що рівні HGF у грудному молоці пов’язані з вираженістю симптомів дитячих кольок. Цей зв’язок може являти собою компенсаторну реакцію складу жіночого молока на унікальні потреби немовляти (J. Bauer, 2011; M.C. Carney, 2017). Наприклад, дослідження доношених немовлят на грудному вигодовуванні виявило, що рівні гіпоксантину, ксантину та тіоціанату в дитячій слині взаємодіють з жіночим молоком, утворюючи активні форми кисню та нуклеозиди, здатні регулювати мікробіоту в ШКТ немовлят (S.S. Al-Shehri et al., 2015).
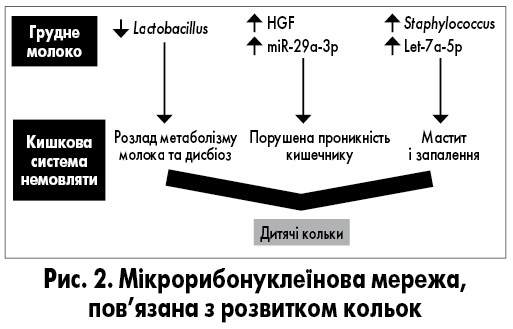 Механізм дитячих кольок включає дисбактеріоз, запалення та підвищену больову чутливість (J.M. Rhoads, 2018; A. Pаrtty, 2017). Поточне дослідження ідентифікує підвищені бактеріальні патогени і запальні miR у молоці матерів, немовлята яких страждають від кольок. Цей висновок узгоджується з дослідженням маститу, опосередкованого бактеріальними ліпополісахаридами в епітеліальних клітинах молочної залози, в якому автори повідомляють про порушення рівня цитокінів грудного молока у відповідь на бактеріальні антигени (L. Chen et al., 2022). Перенесення цих запальних компонентів у кишечник немовляти може сприяти запальному стану та викликати характерні симптоми дитячих кольок (рис. 2). H. Soeorg і співавт. (Pediatr Res, 2017) було підтверджено, що штами Staphylococcus epidermidis у жіночому молоці мають помітну подібність до штамів, виявлених у калі немовлят, яких годують грудним молоком, що свідчить про можливість передачі бактерій від матері дитині. Хоча не всі штами стафілококів є патогенними, Staphylococcus aureus асоціюється з патологічними станами як молочних залоз, так і кишечнику немовляти (S.G. Rimoldi, 2020; N.C. Cheng, 2011).
Механізм дитячих кольок включає дисбактеріоз, запалення та підвищену больову чутливість (J.M. Rhoads, 2018; A. Pаrtty, 2017). Поточне дослідження ідентифікує підвищені бактеріальні патогени і запальні miR у молоці матерів, немовлята яких страждають від кольок. Цей висновок узгоджується з дослідженням маститу, опосередкованого бактеріальними ліпополісахаридами в епітеліальних клітинах молочної залози, в якому автори повідомляють про порушення рівня цитокінів грудного молока у відповідь на бактеріальні антигени (L. Chen et al., 2022). Перенесення цих запальних компонентів у кишечник немовляти може сприяти запальному стану та викликати характерні симптоми дитячих кольок (рис. 2). H. Soeorg і співавт. (Pediatr Res, 2017) було підтверджено, що штами Staphylococcus epidermidis у жіночому молоці мають помітну подібність до штамів, виявлених у калі немовлят, яких годують грудним молоком, що свідчить про можливість передачі бактерій від матері дитині. Хоча не всі штами стафілококів є патогенними, Staphylococcus aureus асоціюється з патологічними станами як молочних залоз, так і кишечнику немовляти (S.G. Rimoldi, 2020; N.C. Cheng, 2011).
Результати дослідження Desirae Chandran і співавт. підтверджують тезу, що складна мережа мікробних, білкових і miR факторів у грудному молоці людини може впливати на ризик розвитку кольок у немовляти. Ці фактори також підтверджують попередні гіпотези щодо впливу дисбактеріозу, проникності кишкового епітелію та запалення на патогенез кольок. У подальшому отримані дані потребують детального вивчення для підтвердження їх як нових терапевтичних цілей у лікуванні дитячих кольок.
Реферативний огляд статті https://www.mdpi.com/2218-273X/13/3/559
Підготувала Ольга Загора
Тематичний номер «Педіатрія» № 3 (69) 2023 р.
СТАТТІ ЗА ТЕМОЮ Педіатрія
Вроджена дисфункція кори надниркових залоз (ВДКНЗ) – це захворювання з автосомно-рецесивним типом успадкування, в основі якого лежить дефект чи дефіцит ферментів або транспортних білків, що беруть участь у біосинтезі кортизолу. Рання діагностика і початок лікування пацієнтів з ВДКНЗ сприяє покращенню показників виживаності та якості життя пацієнтів....
Алергічний риніт (АР) є поширеним запальним захворюванням верхніх дихальних шляхів (ВДШ), особливо серед педіатричних пацієнтів. Ця патологія може знижувати якість життя, погіршувати сон та щоденну продуктивність. Метою наведеного огляду є надання оновленої інформації щодо епідеміології АР та його діагностики, з урахуванням зв’язку з бронхіальною астмою (БА). ...
Американська академія педіатрії (AAP) оновила рекомендації щодо контролю грипу серед дитячого населення під час сезону 2023-2024 рр. Згідно з оновленим керівництвом, для профілактики та лікування грипу в дітей необхідно проводити планову вакцинацію з 6-місячного віку, а також своєчасно застосовувати противірусні препарати за наявності показань. ...
Поширеність і вплив алергічних захворювань часто недооцінюють [1]. Ключовим фактором алергічної відповіді є імуноглобулін (Ig) Е, присутній на поверхні тучних клітин і базофілів. Взаємодія алергену з IgЕ та його рецепторним комплексом призводить до активації цих клітин і вивільнення речовин, у тому числі гістаміну, які викликають симптоми алергії [2]. Враховуючи ключову роль гістаміну в розвитку алергічних реакцій, при багатьох алергічних станах, включаючи алергічний риніт і кропив’янку, пацієнту призначають антигістамінні препарати [3, 4]....





