Переваги спиртового екстракту Serenoa repens як компонента терапії доброякісної гіперплазії передміхурової залози
Сьогодні використання терапевтичного потенціалу рослин – це ефективний і раціональний підхід до лікування доброякісної гіперплазії передміхурової залози (ДГПЗ), обґрунтований багаторічним досвідом учених і клініцистів у всьому світі. Однією з найбільш вивчених фітотерапевтичних сполук із широкою доказовою базою є екстракт плодів пальми пилкоподібної – Serenoa repens.
Ключові слова: доброякісна гіперплазія передміхурової залози, симптоми нижніх сечових шляхів, спиртовий екстракт Serenoa repens, Простамол® Уно, Флосін®.
У США екстракти Serenoa repens застосовуються клініцистами ще з початку XX ст. Серед доведених in vivo та in vitro ефектів препаратів Serenoa repens виділяють:
- антиандрогенну дію, що проявляється інгібуванням 5α-редуктази 1 і 2 типів, уповільненням зв’язування дигідротестостерону з андрогенним рецептором NR3C4, а також інгібуючим впливом на ядерні естрогенні рецептори у тканині передміхурової залози (ПЗ);
- протизапальний ефект, який досягається шляхом пригнічення цикло- та ліпоксигенази;
- антипроліферативні властивості за рахунок пригнічення проліферації епітеліальних клітин ПЗ, індукованої фактором росту фібробластів;
- гальмування зв’язування рецепторів пролактину.
Наявність у ПЗ двох ізоформ 5α-редуктази зумовлює наявність двох можливих напрямків продукування дигідротестостерону з тестостерону. З метою повного припинення проліферації тканини ПЗ необхідно заблокувати обидва шляхи метаболізму андрогенів, що досягається за рахунок антиандрогенного ефекту Serenoa repens. На відміну від інших інгібіторів 5α-редуктази Serenoa repens не впливає на секрецію простат-специфічного антигена, що є значною клінічною перевагою для скринінгу раку ПЗ і моніторингу прогресування пухлини.
Вплив на ключові ферменти, задіяні у патогенезі ДГПЗ
Активність різних екстрактів може відрізнятися, ймовірно, залежно від вмісту жирних кислот. Ліпофільні екстракти плодів Serenoa repens пригнічують активність 5α-редуктази, ферменту, який каталізує перетворення тестостерону на дигідротестостерон. Різні екстракти (гексан, етанол, CO2) продемонстрували різні ступені інгібування (IC50) – від 25 до 2200 мкг/мл залежно від аналізу (Niederprüm et al., 1994; Weisser et al., 1996; Bayne et al., 1999; ESCOP, 2003). Ступінь пригнічення 5α-редуктази спиртового екстракту був вищим, ніж такий гексанового (71 та 59 мкг/мл відповідно) (Koch, 1995). Дозозалежне та неконкурентне інгібування 5α-редуктази спостерігалося як в епітелії ПЗ, так і у стромі: середній інгібуючий ефект етанольного екстракту в концентрації 500 мкг/мл становив приблизно 29% в епітелії та 45% у стромі.
Одну із ключових ролей у патогенезі ДГПЗ відіграє запалення, оскільки ознаки хронічного запального процесу були виявлені у біоптатах 77,4% хворих на ДГПЗ [1]. Застосування екстракту Serenoa repens сприяло значному й статистично достовірному зменшенню вираженості запалення порівняно з контрольною групою за даними REDUCE Trial.
Дослідники вивчали вплив екстрактів на різні ферменти, які беруть участь у запаленні при ДГПЗ. Було встановлено, що спиртовий екстракт інгібує утворення циклооксигеназного тромбоксану B2 (IC50: 15,3 мкг/мл) і синтез продукту 5‑ліпоксигенази LTB4 (IC50: 8,3 мкг/мл). Він також пригнічує синтез простацикліну (PGI2) і простагландину Е2 (PGE2). Гексановий же екстракт впливає на утворення 5α-андростан‑3α, 17β-діолу до 90%, таким чином інгібуючи 5α-редуктазу та 3‑кетостероїд-редуктазу [2].
Чи всі ліпофільні екстракти Serenoa repens однакові?
При порівнянні комерційного гексанового (ES SP 12) та етанольного (CH SP 27) екстрактів (Booker et al., 2014) достовірної різниці виявлено не було, однак у цьому дослідженні жирні кислоти були безпосередньо етерифіковані для газохроматографічного аналізу, без відділення природних вільних жирних кислот від складних ефірів, як це було зроблено Habib і Wyllie (2004).
У літературі містяться дані ряду досліджень, присвячених фармакологічній дії гексанового екстракту Serenoa repens (Carraro J.C. et al., 1996; Debruyne F. et al., 2002; Bent S. et al., 2006). Було доведено, що прийом екстракту супроводжується підвищенням максимальної об’ємної швидкості потоку сечі (Qmax), зменшенням кількості сечовипускань за ніч і не чинить негативної дії на статеву функцію. За даними фітохімічного аналізу E. de Combarieu et al. (2015), екстракт Serenoa repens, поєднаний із СО2 або гексаном, достовірно не відрізняється за складом від етанольного, оскільки виявлені відмінності є меншими, ніж природні фітохімічні відмінності між різними партіями пальмових плодів [3].
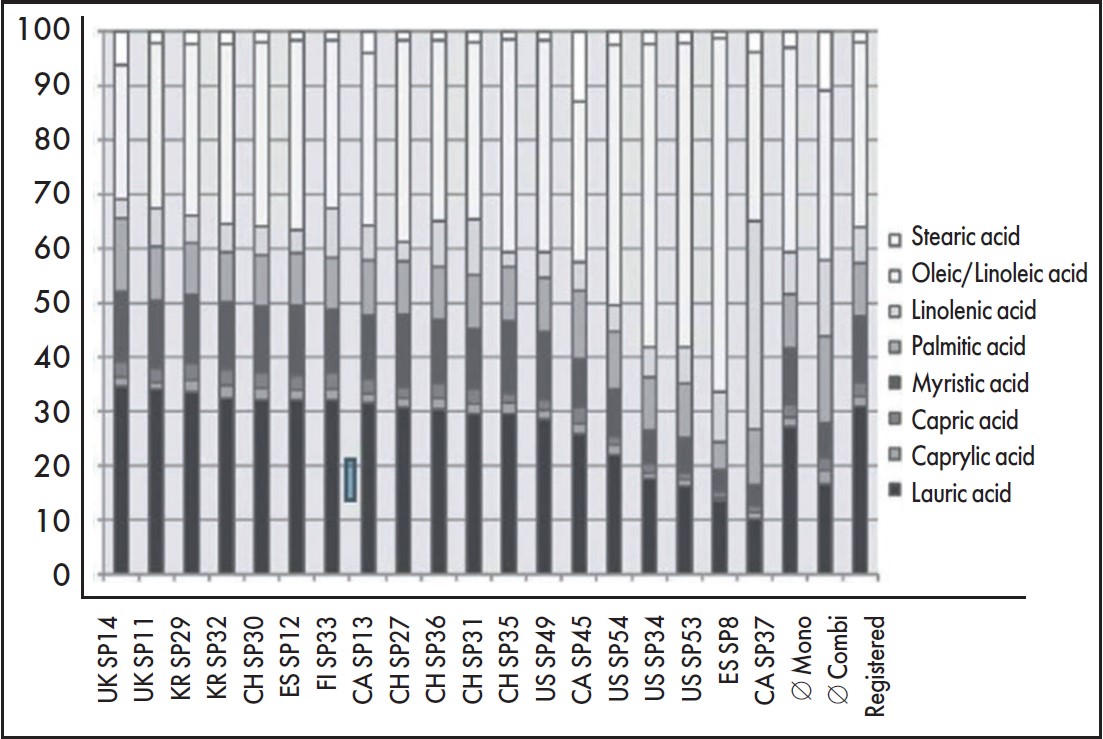
У різних країнах Європи екстракт Serenoa repens представлений різними формами: в Австрії затверджений спиртовий екстракт 90% та 96%, а також гексановий, стандартизований до 85-95% жирних кислот (вільних й етерифікованих). У Бельгії, Нідерландах та Норвегії затверджені препарати Serenoa repens на спиртовій основі (етанол 90, 94 та 96%). В Україні для лікування симптомів ДГПЗ 1-2 стадії за класифікацією Alken використовують оригінальний спиртовий екстракт плодів пальми пилкоподібної Serenoa repens – Простамол® Уно (виробник «Берлін-Хемі», Німеччина). Відповідно до рекомендацій Європейської асоціації урології, біологічні та клінічні ефекти екстрактів одних і тих же рослин різних виробників значно різняться. До того ж відсоток екстракту в усіх препаратах відмінний, що впливає на його ефективність (рис. 1).
Рис. 1. Порівняння складу різних екстрактів Serenoa repens (Booker et al., 2014)
Склад екстракту Serenoa repens, частка активних фіторечовин та умови їх зберігання значною мірою залежать від надійності виробника і якості виробництва. Простамол® Уно зареєстрований у ЄС і за своїми характеристиками відповідає вимогам Європейського агентства з лікарських засобів (EMA). Це досягається завдяки суворому дотриманню технологічних умов виробництва: збір ягід вручну, високий контроль якості, при якому для подальшого процесу відбирається тільки 20% сировини, високотехнологічний процес висушування одразу після збору для максимального збереження фітостеролів і жирних кислот при подальшій екстракції (рис. 2). Тому доказова база щодо Простамол® Уно та його клінічні властивості не можуть бути екстрапольовані на препарати Serenoa repens інших виробників.
Рис. 2. Технологія сушіння ягід впливає на збереження олій та подальшу їх екстракцію
Чому слід віддавати перевагу саме спиртовому екстракту Serenoa repens?
Serenoa repens традиційно використовується як етанольний екстракт. Тривають дискусії щодо фітохімічної та фітофармакологічної еквівалентності екстрактів, виготовлених із різними розчинниками. В огляді Goerne et al. (2014) проаналізовано дані семи контрольованих клінічних досліджень спиртових екстрактів Serenoa repens, які призначалися пацієнтам із симптомами нижніх сечових шляхів (СНСШ) із/без ДГПЗ. Найкращі результати лікування були досягнуті щодо показника об’єму залишкової сечі, пікового потоку сечі, ніктурії, симптомів дизурії, а також показників за Міжнародною шкалою оцінки простатичних симптомів (IPSS) та індексу симптомів Американської урологічної асоціації (AUA-SI) [4].
Mattei et al. (1990) вивчали ефективність спиртового розчину, який приймали пацієнти із ДГПЗ протягом 13 тижнів із оцінкою показників на 30‑й, 60‑й та 90‑й дні. Автори отримали позитивний результат щодо трьох параметрів (дизурія, об’єм сечовипускання та біль/відчуття тиску при сечовипусканні) при застосуванні 160 мг двічі на добу спиртового екстракту Serenoa repens.
Спиртовий екстракт є безпечним, що підтверджується відсутністю побічних ефектів при застосуванні його пацієнтами із ДГПЗ [5]. У дослідженні за участю 634 пацієнтів із ДГПЗ Breza et al. (2005) відзначали покращення СНСШ за шкалою IPSS, а також поліпшення якості життя при прийомі спиртового екстракту Serenoa repens. Використання етанольного екстракту в дослідженні CAMUS (Додаткова та альтернативна медицина для урологічних симптомів) не викликало токсичних наслідків у дозуванні, що втричі перевищувало звичайну клінічну дозу, протягом 18‑місячного періоду спостереження [6]. Загалом було рандомізовано 396 пацієнтів, які приймали 320, 640 і 960 мг етанольного екстракту Serenoa repens щодня або плацебо з інтервалом у 6 міс протягом 18 міс. Статистично значущих відмінностей між групами щодо частоти серйозних або несерйозних побічних ефектів, змін життєво важливих показників, а також частоти припинення дослідження виявлено не було.
Клінічно доведена ефективність Простамол® Уно: дані вітчизняних та міжнародних досліджень
У відкритому дослідженні, проведеному на базі ДУ «Інститут урології ім. акад. О.Ф. Возіанова НАМН України», оцінювали стан чоловіків із ДГПЗ 1 стадії та хронічним абактеріальним простатитом, ускладненим дизуричними явищами, після 30‑денного прийому препарату Простамол® Уно. За результатами дослідження у чоловіків відмічено значне полегшення скарг, пов’язаних із сечовипусканням, зниження частоти ніктурії, а також зменшення кількості балів за шкалою якості життя QoL (Гурженко Ю.М. та співавт., 2005).
Aliaev et al. (2013) доповіли про результати десятирічного спостережного дослідження, у якому вивчалась ефективність безперервного лікування препаратом Простамол® Уно у дозі 320 мг/добу у пацієнтів із ризиком прогресування та симптомами ДГПЗ. За результатами випробування відзначено відсутність прогресування як за суб’єктивними (сума балів за шкалами IPSS, QoL), так і за об’єктивними (об’єм ПЗ, швидкість сечовипускання, об’єм залишкової сечі) критеріями [7].
Застосування Простамол® Уно сприяло зменшенню прогресування симптомів, покращенню індексу якості життя та показників урофлоуметрії у пацієнтів на ранній стадії ДГПЗ за даними дворічного пілотного багатоцентрового рандомізованого контрольованого дослідження [8].
За допомогою шкали IPSS M.F. Trapeznikova et al. (2008) оцінювали ефективність та безпечність застосування монотерапії Простамол® Уно пацієнтами із ДГПЗ, що супроводжувалася хронічним абактеріальним простатитом із СНСШ. Лікування Простамол® Уно сприяло зниженню показників за IPSS з 14 до 6,8 бала та шкалою оцінки симптомів хронічного простатиту Національного інституту охорони здоров’я США (NIH-CPSI) з 18,4 до 12,3 бала, збільшенню Qmax з 12,4 до 18,2 мл/с та покращенню QoL із 3,9 до 1,9 [9].
Доведено, що Простамол® Уно запобігає прогресуванню ДГПЗ, не викликаючи побічних ефектів. Переваги прийому препарату вивчали в багатоцентровому відкритому популяційному рандомізованому порівняльному дослідженні. Препарат призначали у разовій добовій дозі 320 мг протягом 36 міс пацієнтам із початковими симптомами ДГПЗ. Результати дослідження продемонстрували, що у чоловіків, які отримували Простамол® Уно, спостерігалося виражене купірування симптомів за шкалою IPSS, покращення якості життя та зменшення розмірів ПЗ. Натомість у контрольній групі СНСШ прогресували разом зі збільшенням розміру ПЗ [10].
Переваги комбінованої терапії Простамол® Уно + Флосін®
S.V. Razumov et al. (2007) представили висновки 9‑місячного рандомізованого відкритого порівняльного дослідження ефективності та безпечності комбінованого лікування Простамол® Уно і тамсулозином із подальшою монотерапією Простамол® Уно. Було виявлено, що фармакотерапія екстрактом Serenoa repens при помірно виражених симптомах ДГПЗ є безпечною та зіставною за ефективністю з комбінованою терапією [11].
Застосування препарату як компонента комплексної терапії у пацієнтів із ДГПЗ і хронічним простатитом, яка передбачає призначення α1‑адреноблокаторів, здатне покращити показники якості життя й скоротити терміни лікування. У дослідженні Є.А. Литвинця і співавт. (2011) у чоловіків із синдромом незапального хронічного тазового болю комплексна терапія Флосін® (0,4 мг 1 раз/добу вранці після їди) + Простамол® Уно (1 капсула ввечері) забезпечила значне покращення оцінки за шкалою IPSS, якості життя та загального стану при оцінюванні на15‑й і 30‑й дні лікування.
Перспектива довгострокової терапії комбінацією Флосін®/Простамол® Уно щодо якості життя, об’єктивних урологічних показників та впливу на сексуальну функцію у пацієнтів із ДГПЗ 2 стадії оцінювалася у дослідженні ПРОСПЕКТ III. Ефективність застосування комбінованої терапії впродовж трьох років становила 94,1%, що було статистично вищим показником, ніж у контрольній групі (доксазозин і фінастерид) – 89,3% (р<0,05).
Метою дослідження ПРОСПЕКТ IV було вивчити ефективність і безпечність 9‑річної комбінованої терапії Флосін®/Простамол® Уно у хворих на ДГПЗ шляхом оцінки якості життя та можливості поліпшення об’єктивних даних урологічного статусу. У ході дослідження було встановлено високу прихильність пацієнтів до лікування та низьку частоту розвитку небажаних явищ (5,75%; р<0,05) порівняно із хворими, які отримували комбінацію доксазозину і фінастериду (27%, р<0,05) [12].
Клінічна ефективність та високий профіль безпеки спиртового екстракту Serenoa repens доведені результатами численних вітчизняних і міжнародних досліджень. Серед ключових переваг препарату Простамол® Уно слід відзначити відсутність негативного впливу на сексуальну функцію, добру переносимість, протинабрякову й протизапальну дію, інгібування росту тканин ПЗ. Простамол® Уно значно покращує якість життя пацієнтів, зменшує прояви СНСШ, сприяє нормалізації показників урофлоуметрії, а також запобігає прогресуванню ДГПЗ, тому є рекомендованим препаратом для лікування симптомів ДГПЗ 1-2 стадії.
Список літератури знаходиться в редакції.
Підготувала Дарина Чернікова
Тематичний номер «Урологія. Нефрологія. Андрологія» № 3 (30), 2023 р.
СТАТТІ ЗА ТЕМОЮ Урологія та андрологія
У лютому відбулася щорічна Всеукраїнська науково-практична конференція «Малоінвазивні технології в урології», присвячена актуальним проблемам сучасної урології. Пропонуємо огляд найцікавіших доповідей, що прозвучали в рамках заходу....
Інфекції сечовивідних шляхів (ІСШ) у всьому світі посідають провідне місце серед інфекційних захворювань дорослого населення. Поряд із тим серед фахівців зростає занепокоєння щодо триваючого зростання стійкості бактерій до більшості антибіотиків. Експерти провідних міжнародних товариств наголошують на необхідності розсудливого і виваженого призначення антимікробних препаратів. Про основні принципи раціональної антибіотикотерапії в урології, зокрема при проведенні діагностичних і хірургічних втручань, ми попросили розповісти завідувача відділу відновної урології та новітніх технологій ДУ «Інститут урології ім. акад. О.Ф. Возіанова НАМН України», доктора медичних наук, професора В’ячеслава Миколайовича Григоренка. ...
Процедура трансректальної біопсії простати супроводжується високим ризиком інфекційних ускладнень, тому проведення антимікробної профілактики при цьому втручанні є обов’язковим. Однак зростання антибіотикорезистентності, а також нещодавні рекомендації щодо обмеження призначень фторхінолонів значно звужують спектр можливих варіантів такої профілактики. Міжнародною мультидисциплінарною групою експертів на основі літературних джерел та клінічного досвіду було розроблено ряд настанов стосовно запобігання інфекційним ускладненням при біопсії простати та обґрунтовано доцільність і переваги призначення з цією метою фосфоміцину ...
Кількість людей, які страждають і помирають від вірусного гепатиту В (ВГВ), можна порівняти з кількістю хворих на коронавірусну хворобу 2019 року (COVID‑19), яка наразі викликає велике занепокоєння в усьому світі. Тому вкрай важливим залишається питання передачі вірусу, у тому числі через статеві клітини. Попередніми дослідженнями встановлено, що гени ВГВ, інтегровані в людські сперматозоїди, здатні до реплікації та експресії після передачі ембріонам. Однак досі це явище не було підтверджено клінічними дослідженнями у пацієнтів. Автори вивчали особливості інтеграції ВГВ у геном сперматозоїдів пацієнтів та аналізували можливі клінічні наслідки для потомства ...