Современные подходы к тестированию ALK-мутаций при немелкоклеточном раке легкого
Применение алектиниба в лечении ALK-позитивного НМРЛ
 Рак легкого остается наиболее распространенным онкологическим заболеванием в мире. Данная патология является чрезвычайно гетерогенной как с морфологической, так и с генетической точки зрения. Большинство опухолей легкого (~85%) составляет немелкоклеточный рак легкого (НМРЛ), и хотя данный термин интенсивно используется в клинической практике, он крайне недостаточно характеризует заболевание для определения наиболее эффективной тактики лечения. НМРЛ следует обязательно разделять на плоскоклеточный рак и аденокарциному, при которых, даже без учета молекулярно-генетических характеристик, требуется разная тактика лечения.
Рак легкого остается наиболее распространенным онкологическим заболеванием в мире. Данная патология является чрезвычайно гетерогенной как с морфологической, так и с генетической точки зрения. Большинство опухолей легкого (~85%) составляет немелкоклеточный рак легкого (НМРЛ), и хотя данный термин интенсивно используется в клинической практике, он крайне недостаточно характеризует заболевание для определения наиболее эффективной тактики лечения. НМРЛ следует обязательно разделять на плоскоклеточный рак и аденокарциному, при которых, даже без учета молекулярно-генетических характеристик, требуется разная тактика лечения.
Аденокарцинома является наиболее частой морфологической формой рака легкого и составляет около 50% всех его подтипов. При этом в структуре аденокарциномы легкого тоже можно выделить широкий спектр морфологических форм, которые значительно отличаются по клиническим и молекулярным характеристикам, что обуславливает разную чувствительность к терапии.
Но именно молекулярно-генетические характеристики аденокарциномы легкого привели к первым существенным успехам в лечении данного заболевания по сравнению с химиотерапией. С 2000‑х годов идентифицируется все больше мишеней для терапии и разрабатываются все новые препараты, применение которых эффективно при наличии соответствующего генетического нарушения. Так, на сегодняшний день одобрено использование таргетных препаратов при наличии мутаций EGFR, BRAF, транслокаций генов ALK, ROS1, NTRK1/2/3. Таким образом, около 1/4 пациентов с аденокарциномой легкого IV стадии должны получать высокоэффективные таргетные препараты.
Второй (после EGFR) по распространенности мишенью для таргетной терапии, которая в 2011 году позволила добиться существенного повышения частоты объективного ответа, показателей общей выживаемости и выживаемости без прогрессирования практически в 2 раза, стал ген ALK.
Ген ALK кодирует рецепторную тирозинкиназу, относящуюся к семейству инсулинзависимых рецепторов. В норме ген активен только в эмбриогенезе и участвует в нормальном развитии нервной системы, передавая ростовые сигналы через RAS/MAPK и PI3K-сигнальные пути. Ген ALK изначально описан в анапластической крупноклеточной лимфоме, для которой транслокация ALK-NPN является характерной особенностью, благодаря которой ген и получил свое название (Anaplastic Lymphoma Kinase). Позднее, в 2007 году, транслокация ALK была обнаружена и у пациентов с НМРЛ. В большинстве случаев происходит слияние гена ALK с белком ELM4. Белок ELM4 активно экспрессируется в эпителиальных клетках и содержит домен, способствующий димеризации белка. Именно этот домен присутствует в химерном белке ALK-ELM4, а от ALK ему достается киназный домен. В то же время для осуществления киназной активности белку ALK тоже необходима димеризация, которая и приводит к конститутивной активности ALK-ELM4 и стимулированию роста клеток.
В 2010 году появились первые результаты применения кризотиниба у пациентов с ALK-позитивным (ALK+) раком легкого. Высокая частота объективного ответа и существенное увеличение выживаемости без прогрессирования способствовали тому, что кризотиниб стал первым препаратом, одобренным для применения у пациентов с ALK+ НМРЛ в первой линии терапии.
Однако у большинства пациентов, получающих кризотиниб, к концу первого года терапии наблюдается прогрессирование заболевания, связанное с формированием вторичной резистентности. На сегодняшний день хорошо изучены механизмы приобретенной резистентности к кризотинибу, и почти в половине случаев они связаны с вторичными мутациями или амплификацией гена ALK. Это обусловило возможность и необходимость разработки ALK-ингибиторов нового поколения, позволяющих преодолеть данную резистентность.
Сегодня Национальная онкологическая сеть США (NCCN) рекомендует применение алектиниба, церитиниба и бригатиниба как в первой, так и во второй линии терапии после прогрессирования на фоне терапии кризотинибом. Указывается также, что предпочтительным препаратом для первой линии терапии является алектиниб, который станет первым ALK-ингибитором второго поколения, зарегистрированным в Украине. Изначально алектиниб был одобрен для назначения пациентам, заболевание которых прогрессировало на фоне приема кризотиниба. После этого сравнивали эффективность применения алектиниба и кризотиниба в первой линии терапии. По результатам рандомизированного клинического исследования III фазы J-ALEX медиана выживаемости без прогрессирования в группе кризотиниба составила 10,2 месяца, в то время как в группе алектиниба она через 21 месяц не была достигнута. Алектиниб также показал преимущества относительно частоты объективного ответа, которая составила 91,6% (95% доверительный интервал – ДИ – 85,6-97,5%), по сравнению с 78,9% (ДИ 70,5‑87,3%) в группе кризотиниба. Сходные результаты были получены и в другом клиническом исследовании ALEX, в котором в общей популяции пациентов, получавших кризотиниб, медиана выживаемости без прогрессирования составила 11,1 месяца, а в группе алектиниба не была достигнута (на момент первичного анализа, 9 февраля 2017 г.). Еще одним очень важным преимуществом алектиниба, продемонстрированным в данном исследовании, была его высокая эффективность при наличии поражения ЦНС. Так, в группе пациентов без поражения ЦНС на момент начала исследования, которые получали кризотиниб, медиана выживаемости без прогрессирования составила 14,8 месяца, а при наличии метастазов в ЦНС – всего 7,4 месяца, в то время как в группе больных, применявших алектиниб, медиана выживаемости без прогрессирования через 28 месяцев не была достигнута независимо от поражения ЦНС. Общая частота прогрессирования в ЦНС при наличии метастазов в головном мозге составила 58% (95% ДИ 43,4-70,5) в группе кризотиниба и 16% (95% ДИ 8,2-26,2) в группе алектиниба, а при отсутствии поражения ЦНС в начале исследования – соответственно 31,5% (95% ДИ 22,1-41,3) и 4,6% (95% ДИ 1,5-10,6%).
Таким образом, алектиниб проявлял более высокую активность по сравнению с кризотинибом и в неотобранной выборке пациентов, особенно при наличии поражения ЦНС. Это объясняется различиями в физических свойствах самих молекул. Алектиниб проявляет активность против большинства вторичных мутаций, резистентных к кризотинибу. Поэтому при их возникновении алектиниб продолжает проявлять активность, в то время как у пациентов, получающих кризотиниб, наблюдается прогрессирование заболевания. Еще одним важным различием между молекулами является более высокая способность алектиниба по сравнению с кризотинибом, проникая через гематоэнцефалический барьер, задерживаться в ЦНС, чем и объясняется его высокая активность при наличии метастазов в головном мозге и общее снижение частоты прогрессирования в ЦНС.
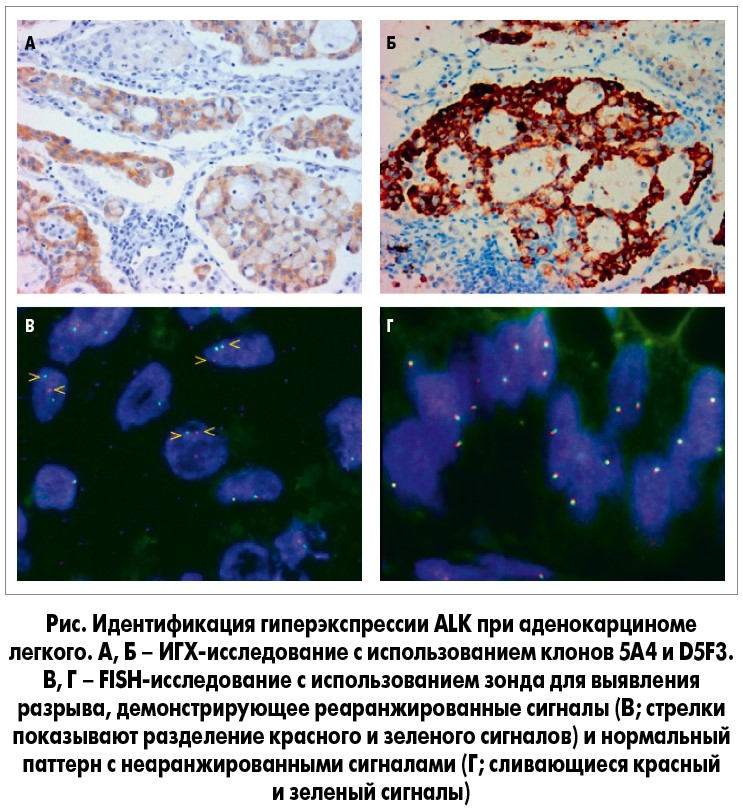
Следует также подчеркнуть, что в исследованиях по изучению эффективности кризотиниба и алектиниба использовали разные методы определения статуса ALK. В регистрационных исследованиях кризотиниба применялся метод флуоресцентной гибридизации in situ (FISH), для которого используются меченные флуорофорами разного цвета фрагменты ДНК, комплементарные 5’- и 3’-последовательностям гена. В норме 5’- и 3’-зонды размещены последовательно, поэтому в препарате сигналы сливаются в один или расположены рядом. При наличии транслокации 5’- и 3’-участки гена ALK разделены, и поэтому сигналы находятся на некотором расстоянии друг от друга. Данный дизайн зондов для определения транслокаций называется break-apart probe (зонды для выявления разрыва). С помощью данного метода можно выявлять любые варианты перестроек гена, но невозможно определить ген-партнер.
Метод FISH обладает практически 100% чувствительностью и специфичностью в выявлении транслокации ALK и долгое время оставался единственным стандартом диагностики. Это объяснялось тем, что имевшееся на тот момент антитело клона ALK1 (DAKO), которое было разработано для определения экспрессии ALK при анапластической крупноклеточной лимфоме, имело чувствительность всего около 70% для выявления транслокации при НМРЛ. Однако впоследствии были разработаны новые клоны антител – 5A4 (Novocastra) и D5F3 (Ventana), обладающие практически 100% чувствительностью к транслокации ALK при НМРЛ. Но в некоторых крупных исследованиях было установлено, что иммуногистохимический (ИГХ) анализ не всегда обладает 100% специфичностью и поэтому может давать ложноотрицательные результаты. Это связано с субъективностью оценки результатов ИГХ-исследования, использованием разных концентраций антител, систем детекции и с интенсивностью окрашивания препаратов. Так, в рамках исследования European Thoracic Oncology Platform Landscape Project тестировалось антитело 5A4 (Novocastra) у 1281 пациента (из 16 госпиталей) с І-ІІІ стадиями аденокарциномы легкого. В результате было выявлено 0% результатов FISH+ при интенсивности ИГХ-окрашивания 0; 4,2% – при интенсивности 1+; 60% – при интенсивности 2+ и 90,9% – при интенсивности 3+.
В лаборатории CSD Health Care также используется антитело клона 5A4 (NovoФcastra), поэтому нами было проведено собственное валидационное исследование по оценке его чувствительности и специфичности выявления транслокации ALK. В его рамках методом FISH с использованием ZytoLight SPEC ALK Dual Color Break Apart Probe (Zytovision) были выполнены исследования у 177 пациентов, в том числе у 109 пациентов – также методом ИГХ-анализа с антителом 5A4 (Novocastra). Частота транслокации ALK, подтвержденная методом FISH, составила 9,6%, причем средний возраст пациентов с ALK+ был почти на 9 лет меньше, чем с ALK-. Обнаруженная частота транслокации ALK была несколько выше указанной в литературе (3-7%), что может объясняться погрешностью из-за небольшого объема выборки пациентов, а также тем, что больным пожилого возраста тестирование в силу разных причин назначается реже, чем молодого. При сопоставлении результатов FISH и ИГХ-анализа негативное предиктивное значение (NPV) ИГХ-исследования составило 98,85%, а положительное предиктивное значение (PPV) – 68,85%. Таким образом, в условиях лаборатории CSD Health Care данный тест обладает практически 100% чувствительностью, но дает около 30% ложноположительных результатов. Это делает возможным его применение в качестве первичного скринингового теста, однако создает необходимость подтверждения ИГХ+ результатов методом FISH.
Что касается антитела D5F3, то изначально частота чувствительности и специфичности выявления с его помощью транслокации ALK была сопоставима с таковой для антитела 5A4. При этом во всех работах демонстрировалась практически 100% чувствительность, а специфичность варьировала от 70 до 98%. Это было связано с применением разного оборудования, систем детекции и оценки результатов окрашивания. Чтобы устранить данные межлабораторные различия, был разработан коммерческий набор реактивов ALK (D5F3) CDx assay (антитело клона D5F3 с системой амплификации и детекции OptiView, Ventana Medical Systems Inc.), который в комплексе с оборудованием для ИГХ-окрашивания BenchMark XT или BenchMark ULTRA (Ventana Medical Systems Inc.) дает наиболее воспроизводимые результаты. Была также разработана бинарная система интерпретации результатов окрашивания ALK (D5F3) CDx assay, согласно которой при любом проценте интенсивно окрашенных клеток результат считается положительным, а при любом другом окрашивании – отрицательным. Комплексный подход позволил повысить воспроизводимость и специфичность результатов ИГХ-исследования почти до 100%, сохранив такую же высокую чувствительность к наличию транслокации ALK. Данный метод одобрен FDA, он определяет статус ALK и в регистрационных исследованиях алектиниба, при его использовании не требуется подтверждение положительного результата методом FISH для назначения препарата. Это делает ALK-скрининг более простым и экономически доступным.
Выводы
- Таргетная терапия при НМРЛ способствует значительному увеличению продолжительности и улучшению качества жизни пациентов с драйверными мутациями (EGFR, ALK, ROS1, BRAF).
- Применение во второй линии терапии ингибиторов ALK второго поколения, например алектиниба, позволяет преодолеть вторичную резистентность опухоли к кризотинибу, а их назначение в первой линии – еще более увеличить выживаемость пациентов по сравнению с таковой в случае использования ингибиторов первого поколения.
- На сегодняшний день приемлемыми являются три стратегии ALK-тестирования: исследование методом FISH; скрининг с антителом клона 5А4 (Novocastra) и последующим подтверждением ИГХ+ образцов методом FISH; применение тест-системы ALK (D5F3) CDx assay (Ventana Medical Systems Inc.) с автостейнером BenchMark (может использоваться как самостоятельный метод, не требующий подтверждения положительных результатов при помощи FISH; рис.).
- Транслокация ALK у больных аденокарциномой легкого в Украине встречается в 9,6% случаев, чаще – у молодых некурящих пациентов.
- Полноценная диагностика НМРЛ на этапе установления диагноза с применением всего спектра возможностей (цитологическое исследование с изготовлением цитоблоков и проведением ИГХ-анализа; патоморфологическое исследование; молекулярное исследование ALK, EGFR) дает возможность своевременно назначить высокоэффективную таргетную терапию.
- Молекулярное профилирование в ряде случаев позволяет повысить эффективность терапии НМРЛ, выявив специфические генетические изменения в опухоли.
Список литературы находится в редакции.
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 2 (58), 2019 р
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...