Роль аналогів гонадотропін-рилізинг-гормону в лікуванні раку передміхурової залози
 Майже 70 років тому було встановлено, що рак передміхурової залози (РПЗ) є гормонозалежним захворюванням. Відтоді для лікування пацієнтів з РПЗ застосовують андрогендеприваційну терапію (АДТ), метою якої є пригнічення секреції андрогенів (передусім тестостерону) яєчками та/або блокування ефектів андрогенів на рівні їх рецепторів. У численних дослідженнях продемонстровано позитивний вплив АДТ на розміри передміхурової залози, прогресування симптомів і виживання пацієнтів. Як АДТ можна використовувати двобічну орхіектомію, аналоги (агоністи й антагоністи) гонадотропін-рилізинг-гормону (ГнРГ), естрогени та антиандрогени. У розвинених країнах аналоги ГнРГ практично витіснили орхіектомію як основний метод АДТ через психологічні наслідки та незворотність хірургічного втручання.
Майже 70 років тому було встановлено, що рак передміхурової залози (РПЗ) є гормонозалежним захворюванням. Відтоді для лікування пацієнтів з РПЗ застосовують андрогендеприваційну терапію (АДТ), метою якої є пригнічення секреції андрогенів (передусім тестостерону) яєчками та/або блокування ефектів андрогенів на рівні їх рецепторів. У численних дослідженнях продемонстровано позитивний вплив АДТ на розміри передміхурової залози, прогресування симптомів і виживання пацієнтів. Як АДТ можна використовувати двобічну орхіектомію, аналоги (агоністи й антагоністи) гонадотропін-рилізинг-гормону (ГнРГ), естрогени та антиандрогени. У розвинених країнах аналоги ГнРГ практично витіснили орхіектомію як основний метод АДТ через психологічні наслідки та незворотність хірургічного втручання.
Механізм дії аналогів ГнРГ при РПЗ
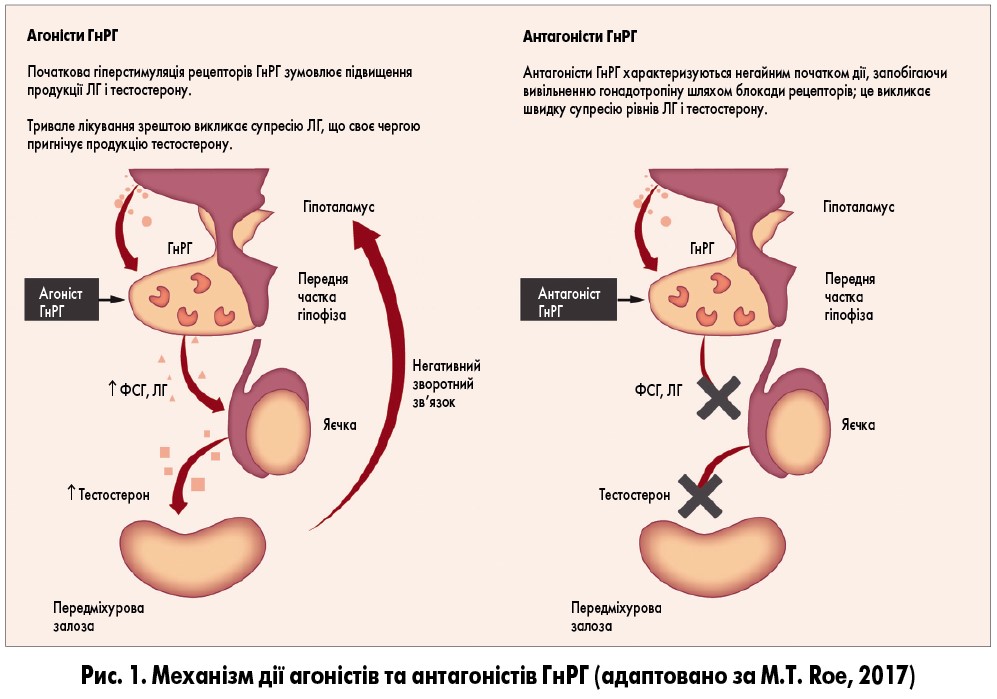
Гонадотропін-рилізинг-гормон продукується гіпоталамусом і регулює сироваткові рівні тестостерону шляхом впливу на вивільнення лютеїнізувального (ЛГ) і фолікулостимулювального (ФСГ) гормонів гіпофізом. ЛГ стимулює секрецію тестостерону, переважно яєчками. Постійна гіперстимуляція гіпофіза зрештою викликає зменшення кількості та чутливості рецепторів ГнРГ, що знижує рівень продукції цього гормону.
Вплив АДТ на рівні гормонів при РПЗ залежить від типу терапії. Орхіектомія забезпечує зниження рівнів тестостерону і дигідротестостерону, при цьому концентрація ЛГ і ФСГ підвищується. Агоністи ГнРГ викликають початковий «спалах» секреції ЛГ, ФСГ, тестостерону та дигідротестостерону, після чого рівні цих гормонів швидко знижуються. Втім при продовженні терапії агоністами ГнРГ рівень ФСГ поступово підвищується (так зване вислизання ФСГ).
У пацієнтів з РПЗ пізніх стадій «спалах» тестостерону на початку терапії агоністом ГнРГ може призводити до збільшення вираженості клінічних симптомів. Для уникнення цього явища можна використовувати короткочасну терапію антиандрогенами першого покоління.
Антагоністи ГнРГ конкурентно зв’язуються з рецепторами ГнРГ гіпофіза і блокують їх, що викликає блокаду секреції ЛГ і ФСГ з подальшою супресією секреції тестостерону, без початкового «спалаху» (рис. 1).
Клінічна ефективність і безпека
Агоністи ГнРГ
Найчастіше застосовують такі агоністи ГнРГ, як лейпрорелін (Елігард, Astellas Pharma), гозерелін (Золадекс, AstraZeneca) та трипторелін (Диферелін®, Ipsen Pharma).
У численних клінічних дослідженнях було продемонстровано, що в пацієнтів з РПЗ пізніх стадій агоністи ГнРГ подовжують загальну виживаність і виживаність без прогресування.
У клінічних рекомендаціях агоністи ГнРГ розглядаються як єдиний клас препаратів, і лікарі часто призначають їх як взаємозамінні. Проте еквівалентність будь-яких двох агоністів ГнРГ не була чітко продемонстрована у прямих порівняльних дослідженнях. Крім того, за даними нещодавно проведеного систематичного огляду, між цими препаратами існують певні відмінності (E.M. Bolton, T. Lynch, 2018). У цей огляд увійшли 16 досліджень, у яких безпосередньо порівнювали ефективність, безпеку, переносимість та зручність застосування гозереліну, лейпрореліну і триптореліну у пацієнтів з РПЗ.
У пацієнтів з РПЗ, які не були кандидатами на хірургічне втручання, рівень тестостерону <1,0 нмоль/л (<29 нг/дл) через 2 міс від початку лікування частіше відзначався у групі триптореліну, ніж у групі лейпрореліну (р=0,02; J.M. Kuhn et al., 1997).
За даними M. Shim і співавт. (2019), після 9 міс застосування агоністів ГнРГ найнижчі рівні тестостерону відзначалися при лікуванні триптореліном; нижчу ефективність забезпечували лейпрорелін і гозерелін (р=0,001). Рівня тестостерону <10 нг/дл було досягнуто в 93,2; 86,4 та 54,2% пацієнтів, які отримували трипторелін, лейпрорелін та гозерелін відповідно.
У дослідженні ІІІ фази у чоловіків із місцевопоширеним або метастатичним РПЗ застосування триптореліну у дозі 22,5 мг (депо-форма для введення через кожні 6 міс) кастраційні рівні тестостерону досягалися у 97,5% пацієнтів після 28 днів і у 98,3% після 12 міс лікування (E.A. Lundstrom et al., 2009). У дослідженні Triptocate LT показано, що при застосуванні депо-форми триптореліну через 6 міс кастраційні рівні тестостерону зберігаються упродовж не менше 3 років від початку лікування (H. Botto et al., 2007).
При лікуванні РПЗ важливо не тільки досягти рівнів тестостерону, еквівалентних таким після кастрації, а й підтримувати їх протягом тривалого часу. За даними T. Pickles та співавт. (2012), ризик «прориву» тестостерону був вищим при застосуванні лейпрореліну для підшкірного введення (10,9%) порівняно з гозереліном (4,8%) і лейпрореліном для внутрішньом’язового введення (5,1%). У дослідженні C.F. Heyns та співавт. (2003), у якому порівнювали лейпрорелін і трипторелін, випадки «прориву» тестостерону (>50 нг/дл) реєстрували тільки в групі лейпрореліну. Важливіше, що 9-місячна загальна виживаність при лікуванні триптореліном була значно вищою порівняно з такою для лейпрореліну (97,0 vs 90,5% відповідно; р=0,033).
Загалом порівнювати виживаність при лікуванні різними агоністами ГнРГ складно через значну неоднорідність у характеристиках пацієнтів і супутній терапії. Проте аналіз, нещодавно проведений британськими вченими, свідчить про кращу виживаність при лікуванні триптореліном порівняно з дегареліксом. Натомість застосування лейпрореліну і гозереліну асоціювалося з нижчою виживаністю порівняно з дегареліксом (L. Uttley et al., 2017).
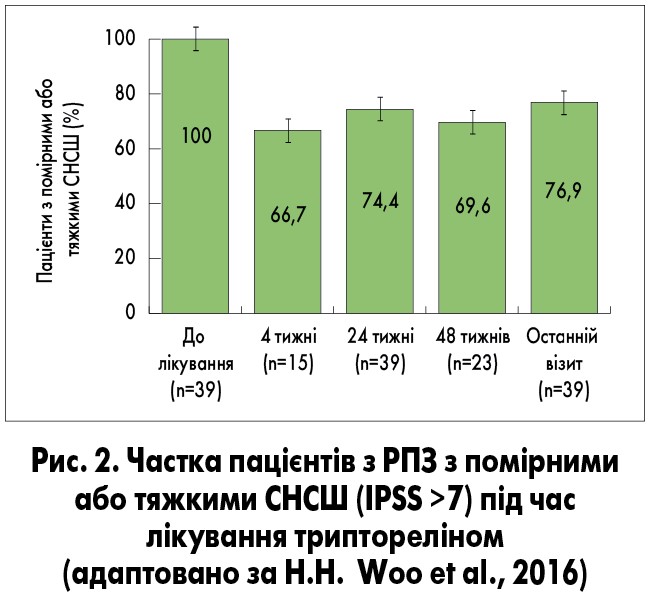 Рак передміхурової залози часто супроводжується симптомами з боку нижніх сечових шляхів (СНСШ). У проспективному багатоцентровому дослідженні H.H. Woo і співавт. (2016), що проводилося в Австралії, вивчали вплив АДТ триптореліном на помірні або тяжкі СНСШ (оцінка за Міжнародною шкалою простатичних симптомів – IPSS >7 балів) у пацієнтів з локалізованим РПЗ Т3/4. Трипторелін застосовували в дозі 11,25 мг через кожні 12 тижнів. На момент включення у дослідження СНСШ турбували всіх пацієнтів, через 48 тижнів лікування частка таких пацієнтів зменшилася до 69,6% (рис. 2). Зниження (покращення) оцінки IPSS на ≥3 бали порівняно з початковою спостерігалося у 47% чоловіків через 4 тижні лікування, у 61% – через 48 тижнів. Трипторелін також сприяв значному поліпшенню якості життя пацієнтів і підтриманню низького рівня простатспецифічного антигену (ПСА; рис. 3, 4).
Рак передміхурової залози часто супроводжується симптомами з боку нижніх сечових шляхів (СНСШ). У проспективному багатоцентровому дослідженні H.H. Woo і співавт. (2016), що проводилося в Австралії, вивчали вплив АДТ триптореліном на помірні або тяжкі СНСШ (оцінка за Міжнародною шкалою простатичних симптомів – IPSS >7 балів) у пацієнтів з локалізованим РПЗ Т3/4. Трипторелін застосовували в дозі 11,25 мг через кожні 12 тижнів. На момент включення у дослідження СНСШ турбували всіх пацієнтів, через 48 тижнів лікування частка таких пацієнтів зменшилася до 69,6% (рис. 2). Зниження (покращення) оцінки IPSS на ≥3 бали порівняно з початковою спостерігалося у 47% чоловіків через 4 тижні лікування, у 61% – через 48 тижнів. Трипторелін також сприяв значному поліпшенню якості життя пацієнтів і підтриманню низького рівня простатспецифічного антигену (ПСА; рис. 3, 4).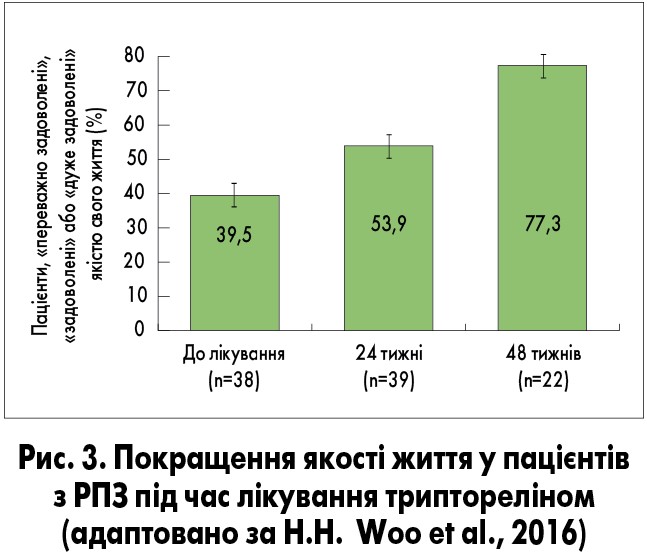
Найчастішими небажаними явищами при застосуванні агоністів ГнРГ є припливи, скелетний біль, головний біль і запор. Профіль безпеки лейпрореліну й триптореліну загалом є порівнянним, за винятком того, що введення триптореліну частіше асоціюється з нудотою і запамороченням, а лейпрореліну – із розладами дихання. В одному дослідженні пацієнти повідомляли про більший дискомфорт у місці введення, зокрема печіння, при застосуванні лейпрореліну порівняно з триптореліном (N.D. Shore et al., 2013). В іншому дослідженні пацієнти й лікарі були більш задоволені лікуванням триптореліном, ніж лейпрореліном, у плані зручності ін’єкцій, локальної переносимості та тривоги, пов’язаної з ін’єкціями. Порівняльних даних щодо зручності застосування триптореліну та гозереліну немає.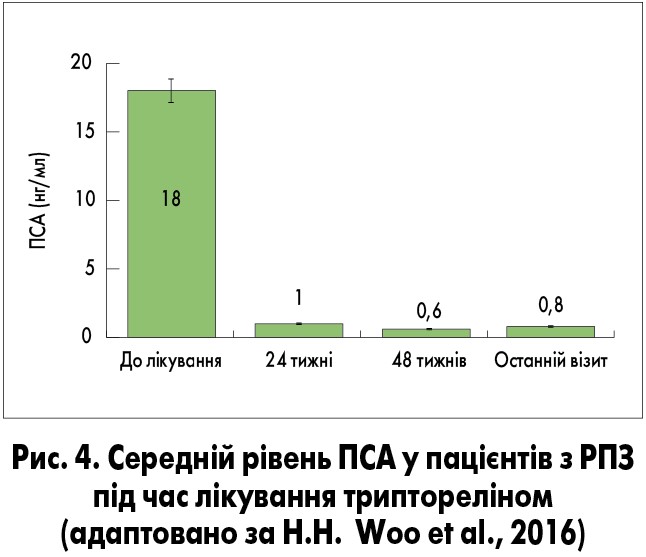
Антагоністи ГнРГ
Сьогодні єдиним антагоністом ГнРГ, схваленим у США та Європі для застосування при РПЗ, є дегарелікс (Фірмагон, Ferring Pharmaceuticals). Антагоніст ГнРГ абарелікс був зареєстрований у США у 2003 р., але у 2005 р. був відкликаний через низький продаж та високу частоту тяжких алергічних реакцій. Інші препарати цієї групи (ганірелікс, елаголікс, релуголікс, центрорелікс) не схвалені для лікування РПЗ.
Доказова база клінічної ефективності дегареліксу при РПЗ, яка використовувалася для його реєстрації, представлена 6 рандомізованими контрольованими дослідженнями ІІІ фази. Дегарелікс порівнювали з лейпрореліном та гозереліном (± бікалутамід). Усі ці дослідження були відкритими, тобто і дослідники, і пацієнти знали, який препарат вони застосовують. Первинною кінцевою точкою у різних дослідженнях були зниження рівня тестостерону <50 нг/дл, зменшення об’єму передміхурової залози, зміна оцінки за IPSS або зниження рівня ПСА. Результати показали, що за впливом на вищенаведені показники дегарелікс принаймні не поступався агоністам ГнРГ.
Ці дослідження стали об’єктом критики через суттєві методологічні недоліки (відкритий дизайн, гетерогенні популяції пацієнтів, ad hoc аналіз, низька статистична цінність) і відсутність даних щодо онкологічної користі (F.P. Secin, 2016; L. Uttley et al., 2017). На думку багатьох експертів і регуляторних органів (зокрема, британського Національного інституту охорони здоров’я і передового досвіду – NICE), щоб продемонструвати перевагу дегареліксу над агоністами ГнРГ, необхідно провести великі проспективні порівняльні дослідження із тривалим періодом спостереження та жорсткими кінцевими точками (S. Salciccia et al., 2016; L. Uttley et al., 2017; I. Tsaur, 2018). Крім того, навіть у розвинених країнах, як-от Велика Британія, у пацієнтів з РПЗ пізніх стадій дегарелікс з великою імовірністю є фармакоекономічно менш ефективним порівняно з триптореліном у комбінації з коротким курсом антиандрогена (L. Lu et al., 2011).
Порівняльна безпека аналогів ГнРГ
Основні побічні ефекти аналогів ГнРГ однакові для агоністів та антагоністів і пов’язані із пригніченням рівня тестостерону: припливи, втома, сексуальна дисфункція, атрофія яєчок, метаболічні порушення, остеопороз, анемія, підвищення ризику розвитку діабету й кардіоваскулярних захворювань.
Антагоністи ГнРГ нe викликають «спалаху» тестостерону та, відповідно, можливого тимчасового посилення вираженості симптомів. Щоб запобігти цьому у разі призначення агоністів ГнРГ, у пацієнтів з підвищеним ризиком використовують короткий курс лікування антиандрогенами. Альтернативною стратегією є початок терапії дегареліксом із подальшим переходом на тривале лікування агоністом ГнРГ. До того ж, у дослідженні J. Asakawaта співавт. (2018) було продемонстровано кращі 5-річні показники загальної виживаності (96,6 vs 74,1%; р=0,006) і канцерспецифічної виживаності (100 vs 84,6%; р=0,027) при заміні дегареліксу на агоніст ГнРГ порівняно із продовженням терапії дегареліксом.
Андрогендеприваційний ефект дегареліксу триває тільки 1 міс, що зумовлює необхідність щомісячних підшкірних ін’єкцій. При цьому місцеві ін’єкційні реакції (індурація, біль) можуть призводити до припинення лікування. Агоністи ГнРГ мають різні депо-форми для внутрішньом’язового і підшкірного введення з періодичністю 1, 3 та 6 міс; крім того, локальні реакції на застосування агоністів ГнРГ є відносно рідкими порівняно з такими на дегарелікс.
У деяких попередніх дослідженнях виявлено, що введення дегареліксу порівняно з агоністами ГнРГ може асоціюватися з нижчою частотою кардіоваскулярних подій у пацієнтів із захворюваннями серця та судин в анамнезі. Втім, ці дані не є переконливими і потребують подальшого уточнення (G. George et al., 2019).
Аналоги ГнРГ у клінічних рекомендаціях
Метою АДТ є зниження рівнів тестостерону до таких, які досягаються шляхом хірургічної кастрації, тобто <50 нг/дл, або <1,7 ммоль/л (існують докази, що більш прийнятним визначенням кастрації є концентрація тестостерону <20 нг/дл).
У рекомендаціях Європейського товариства медичної онкології (ESMO, 2015) АДТ розглядається в цілому, без розмежування на хірургічну чи хімічну кастрацію. Вказується, що АДТ можна застосовувати у комбінації з радикальною променевою терапією (ПТ) при локалізованому (у пацієнтів групи середнього і високого ризику) і місцевопоширеному РПЗ, а також як єдиний метод лікування метастатичного РПЗ (у пацієнтів, які раніше не отримували гормонотерапії).
Відповідно до спільних рекомендацій Європейської асоціації урології, Європейського товариства радіотерапії й онкології та Міжнародного товариства геріатричної онкології (EAU-ESTRO-SIOG, 2018), агоністи ГнРГ тривалої дії є основним видом АДТ. Для антагоністів ГнРГ немає даних щодо тривалої (>12 міс) ефективності, а також даних щодо їх впливу на виживаність. Чіткі переваги антагоністів над агоністами ГнРГ не продемонстровані. Недоліком антагоністів ГнРГ є відсутність депо-форм. Сьогодні немає чітких доказів на користь специфічного типу АДТ (орхіектомія, агоніст чи антагоніст ГнРГ) у пацієнтів з метастатичним РПЗ, за винятком хворих із ризиком компресії спинного мозку, в яких перевагу можуть мати двобічна орхіектомія або введення антагоністів ГнРГ.
Рекомендації EAU-ESTRO-SIOG (2018) щодо АДТ:
- локалізований РПЗ: АДТ у комбінації з ПТ; тривалість АДТ залежить від групи ризику (середній – 4-6 міс; високий – 2-3 роки);
- місцевопоширений РПЗ:
- тривала АДТ у комбінації з ПТ;
- АДТ як монотерапія: у пацієнтів, які не можуть або не бажають отримувати місцеву терапію, з наявністю/відсутністю симптомів та низькодиференційованою пухлиною або рівнем ПСА >50 нг/мл (або підвищенням рівня ПСА більш ніж у 2 рази протягом <12 тиж); ад’ювантна АДТ (± ПТ) після радикальної простатектомії – тільки в пацієнтів із метастазами в лімфатичних вузлах (рN+);
- відстрочена АДТ як монотерапія: у пацієнтів без симптомів, які не можуть або не бажають отримувати місцеву терапію, мають рівень ПСА <50 нг/мл, підвищення рівня ПСА більш ніж у 2 рази протягом >12 міс і високодиференційовану пухлину;
- метастатичний РПЗ:
- АДТ як монотерапія (крім антиадрогенів), у комбінації з доцетакселом або абіратероном;
- АДТ в інтермітуючому режимі: у високомотивованих пацієнтів без симптомів з великою відповіддю ПСА після індукційного періоду.
Застосування АДТ, зокрема аналогів ГнРГ, найкраще описано в останніх рекомендаціях Національної онкологічної мережі США (NCCN, квітень 2019 р.). Відповідно до цих рекомендацій, як АДТ можна застосовувати агоністи ГнРГ (гозерелін, гістерелін, лейпрорелін, трипторелін) у монотерапії чи в комбінації з антиандрогеном першого покоління (нілутамідом, флутамідом, бікалутамідом) або антагоніст ГнРГ дегарелікс.
Залежно від стадії хвороби пропонуються такі варіанти АДТ:
- клінічно локалізований РПЗ (N0M0): агоніст чи антагоніст ГнРГ у комбінації з ПТ (неоад’ювантна, одночасна та/або ад’ювантна АДТ);
- місцевопоширений РПЗ (N1M0):
- агоніст чи антагоніст ГнРГ у комбінації з ПТ (так само, як при N0M0);
- АДТ як єдиний метод лікування: орхіектомія, агоніст або антагоніст ГнРГ (всі варіанти можна комбінувати з абіратероном);
- у пацієнтів з позитивними лімфатичними вузлами після радикальної простатектомії: агоніст ГнРГ, орхіектомія або антагоніст ГнРГ;
- біохімічний (ПСА) рецидив або збереження високих рівнів ПСА після радикальної простатектомії чи ПТ у пацієнтів з М0 РПЗ: орхіектомія, агоніст або антагоніст ГнРГ у комбінації з ПТ;
- метастатичний кастраційно-наївний РПЗ: орхіектомія, агоніст або антагоніст ГнРГ (всі варіанти можна комбінувати з абіратероном або доцетакселом);
- метастатичний кастраційно-резистентний РПЗ: продовження терапії агоністом або антагоністом ГнРГ з додаванням абіратерону, антиандрогенів першого або другого покоління, кетоконазолу (± гідрокортизон), кортикостероїдів або естрогенів.
У рекомендаціях NCCN зазначено, що двобічна орхіектомія (хірургічна кастрація) та застосування аналогів ГнРГ (медикаментозна кастрація) загалом мають однакову ефективність. У пацієнтів з місцевопоширеним захворюванням (N1M0) та в осіб з N1 після простатектомії дегарелікс має нижчу категорію рекомендації (2В) порівняно з агоністами ГнРГ (2А).
У пацієнтів з явними метастазами та ризиком посилення вираженості симптомів внаслідок «спалаху» тестостерону при монотерапії агоністами ГнРГ лікування антиандрогенами має передувати або починатися одночасно з введенням агоніста ГнРГ і тривати принаймні 7 днів.
Практичні висновки
- Хірургічна кастрація та введення аналогів ГнРГ забезпечують однакову ефективність АДТ у пацієнтів з РПЗ. Перевагами аналогів ГнРГ є відсутність психологічного дискомфорту у пацієнтів, зворотність кастрації та можливість лікування в інтермітуючому режимі; головним обмеженням є висока вартість.
- При застосуванні антагоністів ГнРГ рівень тестостерону швидко знижується, натомість агоністи ГнРГ сприяють зниженню концентрації тестостерону після початкового «спалаху». Для зменшення вірогідності посилення вираженості симптомів внаслідок «спалаху» у пацієнтів з підвищеним ризиком (наприклад, у разі загрози компресії спинного мозку чи гострої затримки сечі) можна застосовувати короткий курс лікування антиандрогенами. Альтернативною стратегією є початкове призначення антагоніста ГнРГ з подальшим переходом на тривалу терапію агоністом ГнРГ.
- Дегарелікс не має доведених онкологічних переваг над агоністами ГнРГ; реєстраційні дослідження дегареліксу мали істотні методологічні недоліки і не оцінювали жорсткі клінічні точки.
- Перевагами агоністів ГнРГ порівняно з дегареліксом є велика доказова база, менша вартість, більш зручне застосування, нижча частота локальних реакцій.
- Окремі агоністи ГнРГ можуть відрізнятися за ефективністю, профілем безпеки та зручністю застосування. Нещодавно отримані дані вказують на те, що введення триптореліну асоціюється з вищою виживаністю, а лейпрореліну і гозереліну – з нижчою виживаністю порівняно з дегареліксом.
- Трипторелін 22,5 мг (депо-форма для введення через кожні 6 міс) демонструє високу ефективність у досягненні та підтриманні кастраційних рівнів тестостерону, а також дозволяє підвищити комфортність лікування і комплаєнс пацієнтів завдяки меншій періодичності ін’єкцій.
- Клінічна значимість ефекту «вислизання» ФСГ при лікуванні агоністами ГнРГ і порівняльна кардіоваскулярна безпека аналогів ГнРГ потребують подальшого вивчення.
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 2 (58), 2019 р
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...