Апіксабан: огляд клінічної фармакокінетики та фармакодинаміки
Апіксабан – прямий інгібітор Xa-фактора згортання крові, який отримав схвалення у багатьох країнах за низкою показань. Підставою для реєстрації стали результати ключових клінічних досліджень фази III, які продемонстрували, що апіксабан є вдалою альтернативою наявним антикоагулянтам, таким як антагоністи вітаміну К (АВК) та гепарини низької молекулярної маси (ГНММ), завдяки покращеному профілю користь/ризик. Представляємо до вашої уваги огляд статті Byon et al. (2019), опублікованої у журналі Clinical Pharmacokinetics. У цьому матеріалі підсумовуються фармакокінетичні, фармакодинамічні характеристики та взаємодії апіксабану, а також обговорюється потенціал його практичного впровадження з урахуванням даних глобальної програми клінічних досліджень.
За даними досліджень, у пацієнтів із неклапанною фібриляцією передсердь (НКФП) апіксабан у дозі 5 мг двічі на день достовірно знижував ризик інсульту або системної емболії на 21%, значних кровотеч – на 31%, смерті – на 11% порівняно з варфарином (Granger et al., 2011). Подібним чином, в осіб із НКФП, які не відповідали на терапію АВК або не могли її отримувати, апіксабан зменшував ймовірність розвитку інсульту чи системної емболії більш ніж на 50% порівняно з ацетилсаліциловою кислотою (АСК), без суттєвого підвищення частоти значних кровотеч (Connolly et al., 2011). Апіксабан у дозі 2,5 мг двічі на день перевершив еноксапарин по 40 мг/добу і продемонстрував чисельно зіставну ефективність з еноксапарином у дозі 30 мг двічі на день, не підвищуючи частоти геморагічних подій. Препарати застосовували з метою профілактики венозного тромбоемболізму (ВТЕ) у пацієнтів, яким проводили операції з протезування колінних або кульшових суглобів (Lassen et al., 2009, 2010). Крім того, порівняно з терапією АВК, якій передували ін’єкції еноксапарину в дозі 1 мг/кг двічі на день, апіксабан у режимі 10 мг два рази на день сім днів, а потім 5 мг двічі на день упродовж шести місяців показав не меншу ефективність у лікуванні ВТЕ, але достовірно нижчий (на 69%) ризик значних кровотеч. Після завершення початкової терапії ВТЕ продовжена антикоагуляція схваленою дозою апіксабану 2,5 мг двічі на день достовірно знижувала ризик повторних ВТЕ порівняно із плацебо, не підвищуючи частоти значних кровотеч (Agnelli et al., 2013).
Механізм дії
Апіксабан – сильний прямий високоселективний інгібітор фактора Xa (константа інгібування 0,08 нМоль [0,037 нг/мл] за температури 25 °C) зі зворотною дією, розроблений для перорального прийому (Pinto et al., 2007; Luettgen et al., 2011). Препарат не потребує наявності антитромбіну III для реалізації антитромботичної активності (Ansell, 2007). Апіксабан пригнічує вільний та зв’язаний у тромбі Xa, а також активність протромбінази, наслідком чого є обмеження росту тромбу (Jiang et al., 2009). Також він не має прямого впливу на агрегацію тромбоцитів, але опосередковано інгібує агрегацію, індуковану тромбіном (Wong, 2011). Зв’язок між концентрацією апіксабану в плазмі та його анти-Xa-активністю є лінійним у широкому діапазоні доз.
Фармакокінетика
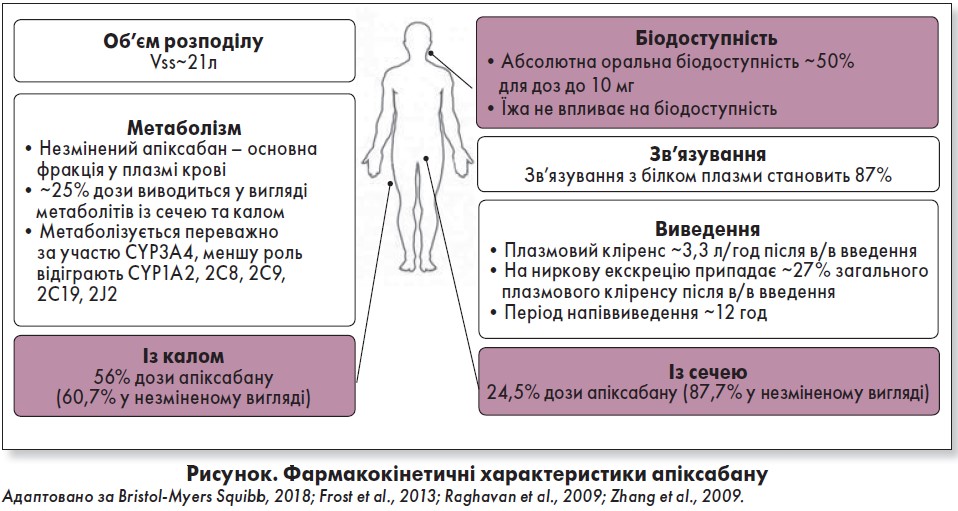
Характеристики всмоктування, розподілу, метаболізації та виведення апіксабану наведені на рисунку. Експозиція апіксабану зростає пропорційно в діапазоні схвалених доз від 2,5 до 10 мг. При прийомі двічі на день стабільна концентрація у плазмі крові досягається на третій день (Frost et al., 2013, 2018).
Особливості фармакокінетики в окремих групах пацієнтів
Вік і стать
Дослідження за участю здорових добровольців обох статей віком 18‑40 років (молоді) та 65‑79 років (похилого віку) показало, що максимальна концентрація у плазмі (Cmax) апіксабану була зіставною, але площа під кривою час/концентрація (AUC) – на 32% більшою в осіб похилого віку (Frost et al., 2015). Виявлено прямий зв’язок між кліренсом апіксабану та креатиніну, отже, відмінності між віковими групами найімовірніше зумовлені зниженням ниркової функції. Субаналізи клінічних досліджень фази ІІІ апіксабану не підтвердили впливу віку на співвідношення користь/ризик, тому корекція дози лише з урахуванням віку не потрібна (Bristol-Myers Squibb, 2018; Agnelli et al., 2013; Halvorsen et al., 2014; Pineo et al., 2013; Ng et al., 2016).
Cmax та AUC апіксабану були на 18 і 15% вищими у жінок, ніж у чоловіків відповідно. Ця відмінність розцінюється як клінічно незначуща (Frost et al., 2015).
Маса тіла
У здорових осіб із низькою масою тіла (≤50 кг) Cmax та AUC апіксабану були на 27 та 20% вищими відповідно, ніж у групі порівняння (65‑85 кг). І навпаки, у пацієнтів із надмірною масою тіла (≥120 кг) спостерігалися нижчі показники експозиції: на 31% Cmax та на 23% AUC (Upreti et al., 2013). Субаналізи клінічних досліджень фази ІІІ не підтвердили впливу маси тіла на співвідношення користь/ризик, тому корекція дози за масою тіла не потрібна (Bristol-Myers Squibb, 2018; Agnelli et al., 2013; Sandhu et al., 2016).
Ураження нирок
Через обмежену участь нирок у виведенні апіксабану (~27%) вплив ниркової дисфункції на експозицію препарату був помірним. Ураження нирок не впливало на Cmax. В осіб із легким зниженням функції (кліренс креатиніну [ККр] 65 мл/хв), помірною (ККр 40 мл/хв) та тяжкою (ККр 15 мл/хв) нирковою дисфункцією AUC апіксабану підвищувалася на 16, 29 та 44% відповідно порівняно зі здоровими особами (ККр 100 мл/хв) (Chang et al., 2016).
Рекомендації з дозування апіксабану мають локальні відмінності. У США не показана корекція дози з урахуванням функції нирок на підставі результатів дослідження фази І, в яких брали участь хворі на гемодіалізі (Bristol-Myers Squibb, 2018; Wang et al., 2016). Пацієнтам із НКФП знижена доза (2,5 мг двічі на день) рекомендована за відповідності принаймні двом із наступних критеріїв: вік ≥80 років, маса тіла ≤60 кг, креатинін сироватки ≥1,5 мг/дл. В Європі знижену дозу (2,5 мг двічі на день) можна призначати лише пацієнтам із НКФП, які мають тяжку ниркову недостатність (ККр 15‑29 мл/хв), а особам із ККр <15 мл/хв або на діалізі апіксабан протипоказаний.
Ураження печінки
Легка (клас А за шкалою Чайлда – П’ю) та помірна (клас В) печінкова недостатність не впливає на фармакокінетику апіксабану. Оскільки пацієнти з тяжкою печінковою недостатністю можуть мати властиві цьому стану порушення коагуляції, і наразі у них мало клінічного досвіду застосування препарату, цій категорії він протипоказаний (Bristol-Myers Squibb, 2018).
Фармакокінетичні взаємодії з іншими ліками
У дослідах in vitro апіксабан не активував і не пригнічував основних ферментів системи цитохрому, а також не втручався у транспортування субстратів P-глікопротеїну (Wang et al., 2010). Отже, вплив апіксабану на фармакокінетику інших лікарських засобів малоймовірний.
З іншого боку, апіксабан метаболізується за участю ферментів CYP3A4/5 та є субстратом для Р-глікопротеїнового транспортера (P-gp) (Wang et al., 2010; Zhang et al., 2013). Тому інші ліки, які є модуляторами CYP3A4 та P-gp, можуть впливати на його фармакокінетику. Найбільший ефект на екпозицію апіксабану чинять кетоконазол – сильний інгібітор CYP3A4 і P-gp, та рифампіцин – сильний активатор CYP3A4 і P-gp. Таким чином, при одночасному прийомі з кетоконазолом Cmax та AUC апіксабану збільшуються у 1,6 та два рази, а з рифампіцином – знижуються на 42 та 54% відповідно. Очікується, що інші потужні інгібітори CYP3A4 та P-gp (як-то ітраконазол, ритонавір) також можуть підвищувати концентрацію апіксабану в крові, а інші потужні індуктори вказаних ферментів (наприклад, карбамазепін, фенітоїн, трава звіробою) – обмежувати його екпозицію (Vakkalagadda et al., 2016; Frost et al., 2015).
У клінічних дослідженнях апіксабану фази ІІІ заборонялося використання сильних інгібіторів та індукторів CYP3A4. З урахуванням обмеженого клінічного досвіду, відповідні рекомендації в інструкції з медичного застосування залежать від схвалених показань та регіону реєстрації. Одночасне призначення апіксабану з сильними інгібіторами CYP3A4 та P-gp здебільшого протипоказане, хоча в деяких країнах, зокрема у США, рекомендоване обмеження дози на 50%. Одночасне призначення апіксабану з сильними індукторами CYP3A4 та P-gp переважно протипоказане, особливо у пацієнтів, які отримують лікування ВТЕ, зважаючи на високий ризик зниження ефективності препарату. В деяких регіонах, зокрема у Європі, допускається одночасне застосування апіксабану з сильними індукторами ферментів з обережністю в осіб із НКФП та тих, яким призначають профілактику ВТЕ після ортопедичних операцій. Немає потреби в корекції дози апіксабану, якщо його використовують паралельно із препаратами, які не визнані сильними інгібіторами CYP3A4 та P-gp, як-от напроксен, дилтіазем, кларитроміцин (Bristol-Myers Squibb, 2018).
Фармакодинамічні взаємодії з антикоагулянтами та антитромбоцитарними препаратами
При комбінованому призначенні еноксапарину (одна доза 40 мг) з апіксабаном (одна доза 5 мг) спостерігався адитивний ефект анти-Ха-активності (Barrett et al., 2012). Через підвищення ризику кровотеч не рекомендоване одночасне застосування з апіксабаном нефракціонованого гепарину та похідних гепарину (зокрема ГНММ), олігосахаридів із Xa-інгібіторною активністю (фондапаринукс), прямих інгібіторів тромбіну ІІ (дезирудин), тромболітичних агентів, антагоністів глікопротеїнових рецепторів IIb/IIIа, тієнопіридинів (клопідогрел), дипіридамолу, декстрану, АВК та інших оральних антикоагулянтів. Фармакокінетичні або фармакодинамічні взаємодії не виникали при паралельному призначенні апіксабану з АСК у дозі 325 мг. Одночасний прийом 500 мг напроксену з апіксабаном не викликав додаткового пригнічення агрегації тромбоцитів, окрім того, яке властиве напроксену (Frost et al., 2014). Подібним чином, одночасне призначення апіксабану з клопідогрелом (75 мг), прасугрелом (навантажувальна доза – 60 мг, потім по 10 мг/добу) або із комбінацією клопідогрел (75 мг) + АСК (162 мг) не викликало збільшення часу кровотечі або ще глибшого пригнічення агрегації тромбоцитів порівняно із прийманням антиагрегантів без апіксабану (Frost et al., 2014; AbuTariff et al., 2014). Незважаючи на ці результати, апіксабан слід застосовувати з обережністю, призначаючи одночасно з нестероїдними протизапальними (включно з АСК), а також іншими антиагрегантними препаратами, оскільки згаданим лікам властиве підвищення ризику кровотеч, а деякі особи можуть демонструвати виразнішу фармакодинамічну відповідь на одночасний прийом антитромбоцитарних засобів з апіксабаном.
Фармакокінетика у великих популяціях пацієнтів
За даними клінічних досліджень апіксабану І‑ІІІ фази, був проведений популяційний аналіз його фармакокінетики при застосуванні щодо кожного з показань (Leil et al., 2014; Byon et al., 2017; Cirincione et al., 2018). Після врахування усіх значимих факторів впливу виявлено, що фармакокінетичні параметри апіксабану демонструють помірну міжіндивідну варіативність: у межах близько 40% для плазмового кліренсу та десь 25% для об’єму розподілу. Залишкова варіативність, яку не можна було пояснити впливом різних чинників, становила приблизно 30%. Терапія апіксабаном не потребує рутинного моніторування показників експозиції, хоча вони можуть бути корисними для прийняття рішень в індивідуальних клінічних випадках, наприклад, при передозуванні або виникненні потреби в екстреному хірургічному втручанні.
Підсумки
- Апіксабан – прямий інгібітор фактора Xa з передбачуваними фармакокінетичними та фармакодинамічними характеристиками, які зберігають стабільність у різних вивчених підгрупах пацієнтів, зокрема в осіб похилого віку та з нирковою дисфункцією.
- Швидкий початок дії, низький потенціал взаємодії з іншими ліками та продуктами харчування, відсутність потреби в рутинному моніторуванні при клінічному застосуванні роблять апіксабан привабливою опцією для спрощення антикоагулянтної терапії.
Підготував Сергій Романюк
Стаття друкується за підтримки компанії «Пфайзер»
PP-ELI-UKR-0037
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (64) червень 2019 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....