Антигипертензивная терапия – как сделать правильный выбор?
.jpg) В рамках научно-практической конференции с международным участием «Медико-социальные проблемы артериальной гипертензии в Украине» (29‑30 мая 2019 года, г. Киев) прозвучал доклад профессора кафедры внутренней медицины 3 ГУ «Днепропетровская медицинская академия МЗ Украины», доктора медицинских наук, профессора Елены Акиндиновны Коваль на тему «Как нам правильно выбирать антигипертензивную терапию в свете рекомендаций ESC 2018 по лечению артериальной гипертензии». Предлагаем вашему вниманию обзорное интервью с автором доклада.
В рамках научно-практической конференции с международным участием «Медико-социальные проблемы артериальной гипертензии в Украине» (29‑30 мая 2019 года, г. Киев) прозвучал доклад профессора кафедры внутренней медицины 3 ГУ «Днепропетровская медицинская академия МЗ Украины», доктора медицинских наук, профессора Елены Акиндиновны Коваль на тему «Как нам правильно выбирать антигипертензивную терапию в свете рекомендаций ESC 2018 по лечению артериальной гипертензии». Предлагаем вашему вниманию обзорное интервью с автором доклада.
? Елена Акиндиновна, какие основные изменения были внесены в рекомендации по лечению артериальной гипертензии Европейского общества кардиологов (ESC, 2018), а что осталось таким, как ранее? Когда начинать лечение?
Классификация артериальной гипертензии (АГ), а также критерии постановки диагноза не изменились. А вот подход к лечению стал жестче. Так, ранее высокое нормальное артериальное давление (АД) – 130‑139/80‑85 мм рт. ст. – не рассматривалось порогом для терапии. В актуальных же рекомендациях ESC указано, что медикаментозное лечение следует начинать в случае очень высокого риска сердечно-сосудистых заболеваний (ССЗ) или при наличии установленного ССЗ, особенно ишемической болезни сердца (ИБС) (уровень доказательности ІІВ).
Кроме того, больным АГ 1-й степени с низким или умеренным риском ССЗ даже без поражения органов-мишеней рекомендована медикаментозная терапия, если модификация образа жизни не дала удовлетворительных результатов (уровень доказательности ІА).
У пожилых пациентов (>65 лет, но ≤80 лет) пороговым значением систолического АД для начала терапии, совокупно с изменением образа жизни, является 140‑159 мм рт. ст. (уровень доказательности ІА).
? Какие приняты целевые уровни АД?
Первой основной целью принято считать снижение АД до 140/90 мм рт. ст. у всех больных. При хорошей переносимости терапии лечение АГ может быть проведено до достижения уровня АД 130/85 мм рт. ст. у большинства пациентов. У больных в возрасте до 65 лет зачастую рекомендовано снижение систолического АД (САД) до 120‑129 мм рт. ст. (уровень доказательности ІА).
Целевые уровни АД у пожилых пациентов (65‑80 лет):
- у лиц ≥65 лет целевое САД рекомендовано на уровне 130‑139 мм рт. ст. (уровень доказательности ІА);
- у больных >80 лет, в случае если исходное систолическое АД ≥160 мм рт. ст., целевой уровень САД – 140‑150 мм рт. ст., с учетом хорошей физической формы (когда нет приступов стенокардии, роста креатинина) и ментального состояния пациентов (нет изменений со стороны головного мозга, ухудшения церебральной дисфункции).
Целевой уровень САД 130‑139 мм рт. ст. у данной когорты пациентов может быть при условии хорошей переносимости терапии (уровень доказательности ІА) (SPRINT, Ambrosius еt al., 2014). Диастолическое АД (ДАД) должно достигать целевого показателя не ниже 80 мм рт. ст.
? С чего начинать лечение?
В рекомендациях ESC (2018) предлагается начать терапию АГ с двухкомпонентной комбинации, желательно в одной таблетке. Предпочтительным является сочетание модулятора ренин-ангиотензин-альдостероновой системы (РААС) и диуретика, в котором блокатор кальциевых каналов (БКК) можно заменить на β-блокатор, а при отсутствии сердечной недостаточности (СН) – иногда применять негидропиридиновый БКК.
Следует отметить, что данный стартовый алгоритм приемлем для большинства клинических ситуаций, которые сопровождаются повышением АД, как, например, неосложненная, резистентная АГ, повышение АД при болезни почек, ИБС, СН, фибрилляция предсердий.
Исключением являются «хрупкие» пожилые пациенты, а также лица с АГ І степени группы низкого риска СС-событий (особенно если уровень АД <150 мм рт. ст.).
? Каким критериям отвечает комбинированная терапия АГ – модулятором РААС и диуретиком – в соответствии с рекомендациями ESC (2018)?
- Данная схема применяется для лечения АГ у молодых пациентов, которое начинается раньше.
- Такая терапия предпочтительна у пожилых больных АГ, когда лечение становится более агрессивным.
- Эффективность антигипертензивной терапии должна быть максимально высокой и при этом органосохраняющей для достижения целевых уровней АД.
- Переносимость должна быть отличной, иначе не получится «удержать» на данной терапии пациентов, особенно молодых и пожилых возрастных групп.
- Модуляторы РААС включены в первую линию терапии во всех группах, равно как и диуретики.
- Показана начальная комбинированная терапия, предпочтительно в виде одной таблетки, так как это повышает приверженность пациента.
? Какую роль предстоит сыграть диуретикам согласно новым рекомендациям ESC (2018)?
В настоящее время много дебатов ведется о том, следует ли отдавать предпочтение тиазидоподобным диуретикам – хлорталидону (ХЛД) и индапамиду – перед гидрохлоротиазидом (ГХТ). Однако прямых сравнений с клиническими исходами (конечными точками) в исследованиях нет. Это честно фиксируется в рекомендациях ESC. Тем не менее, во многих рандомизированных клинических исследованиях (РКИ) ХЛД показал преимущество, в частности, относительно СС-исходов (ALLHAT, Collaborative Research Group, 2002). Данные препараты по-видимому более эффективны в снижении АД и длительности действия по сравнению с ГХТ при сопоставимой частоте побочных эффектов.
? Какие комбинации диуретиков с сартанами являются самыми эффективными?
Сартаны – наиболее хорошо переносимый класс препаратов, не ухудшающий качества жизни пациентов и обладающий органосохраняющими качествами. В метаанализе, где проводили оценку эффективности сартанов в сочетании с диуретиком, показано, что в комбинации с ГХТ наибольшую эффективность имел кандесартан. ХЛД продемонстрировал лучший положительный эффект при совместном применении с азилсартаном медоксомилом (АЗЛ-М) (Drug Saf, 2015).
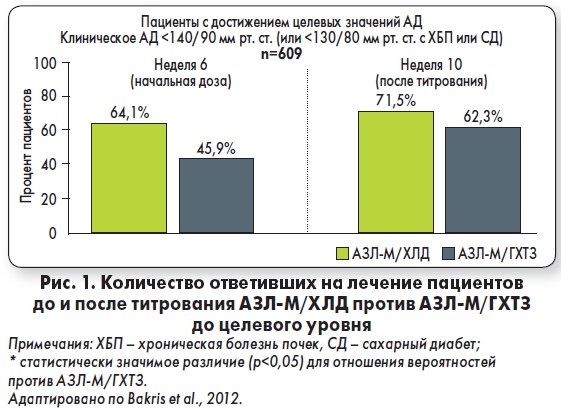
Что касается оценки использования АЗЛ-М + ГХТ в сравнении с АЗЛ-М + ХЛД, по результатам РКИ Bakris еt al. (2012) было показано, что вторая комбинация все же эффективнее (рис. 1).
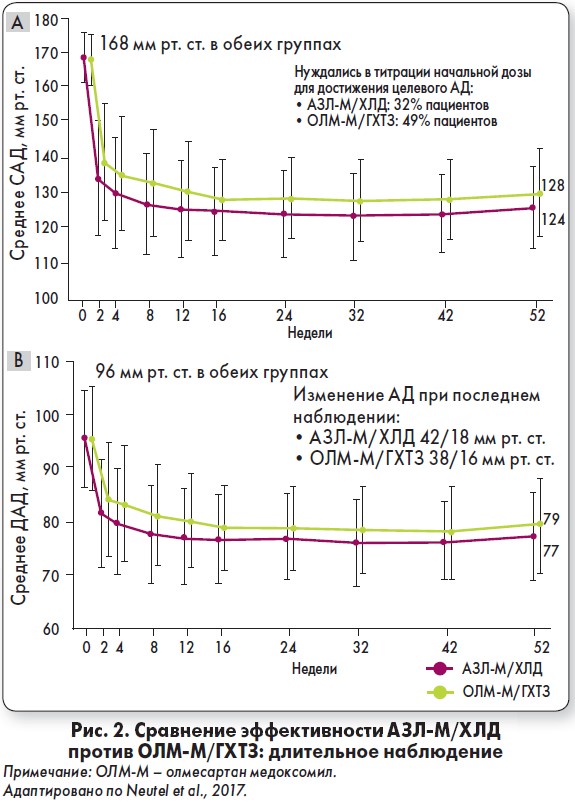
В открытом рандомизированном мультицентровом 52-недельном исследовании в параллельных группах III фазы (n=837) сравнивали эффективность АЗС‑М + ХЛД еще с одной мощной комбинацией – олмесартан медоксомил + ГХТ (Neutel et al., 2017). Полученные данные показали, что в когорте пациентов, которые принимали АЗС‑М + ХЛД, только у трети была необходимость титровать начальную дозу, тогда как при лечении комбинацией олмесартан + ГХТ половина больных требовала пересмотра лечения (рис. 2).
Кроме того, профессор Е.А. Коваль представила новое японское исследование, в котором изучалась целесообразность перевода 40 пациентов с комбинации препаратов, а именно сартана (любого, кроме азилсартана) с диуретиком либо БКК на один только азилсартан (40 мг, что является эквивалентом 80 мг АЗЛ-М) (J Clin Med Res, 2019). Оказалось, что в целом монотерапия азилсартаном по эффективности снижения АД соответствовала комбинации любого другого сартана с диуретиком или БКК. Частота сердечных сокращений также не повышалась и существенно не снижалась. Хотя следует отметить, что после перевода на монотерапию семь пациентов (17,5%) из-за повышения АД нуждались в добавлении к терапии БКК.
Елена Акиндиновна рассмотрела еще одно интересное современное исследование английских и итальянских коллег (J Clin Hypertens, 2018). Авторы сравнивали эффективность антигипертензивной терапии АЗЛ-М с фиксированной комбинацией АЗС‑М + ХЛД у пациентов с АГ II‑III ст. в течение восьми недель.
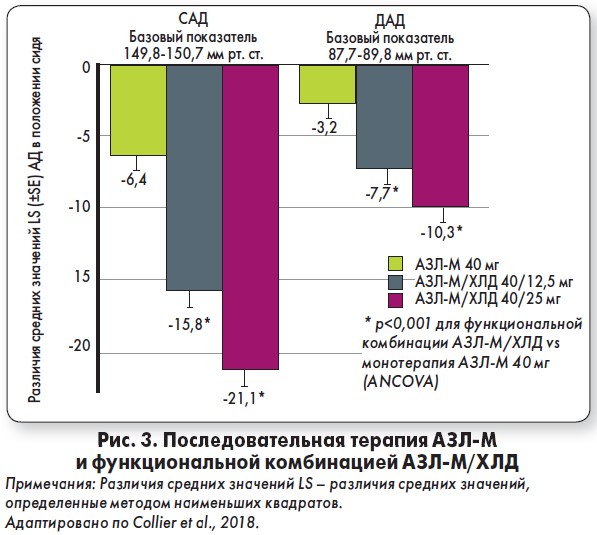
Больные были рандомизированы на три группы:
- 1-я группа (n=133) принимала АЗС‑М в дозе 40 мг;
- 2-я группа (n=127) получала АЗС‑М + ХЛД по 40/12,5 мг;
- 3-я группа (n=135) – лица с тяжелой АГ – принимали АЗС‑М + ХЛД в дозе 40/25 мг.
Почти все пациенты (n=368) завершили исследование несмотря на тяжесть состояния до начала лечения. Показаны высокая эффективность и отличная или хорошая переносимость фиксированных комбинаций (рис. 3).
Более того, интересным является американское исследование по сравнению эффективности монотерапии ХЛД (25 мг) с фиксированной комбинацией АЗС‑М + ХЛД у лиц с АГ II‑III ст. (JRAAS, 2018). Дизайн испытания: 184 пациента принимали ХЛД в дозе 25 мг, 185 – АЗС‑М + ХЛД по 40/25 мг и 182 – АЗС‑М + ХЛД в дозе 80/25 мг. Наблюдение длилось шесть недель. Первичная конечная точка – степень снижения суточного АД и его удержания. По результатам исследования, эффективность фиксированных комбинаций значительно превышала таковую при монотерапии ХЛД. Но при этом более высокие дозы АЗС‑М (80 мг) в сочетании с ХЛД не показали существенного преимущества перед АЗС‑М по 40 мг с ХЛД.
Выводы
1. Фиксированная комбинация АЗС‑М с ХЛД обладает достаточной доказательной базой для применения у пациентов с АГ, тем более, что большинство нуждается в комбинированной терапии согласно рекомендациям ESC по лечению АГ (2018).
2. Данная комбинация обладает стойкой антигипертензивной эффективностью и благоприятным профилем безопасности.
3. Дозовый состав комбинации 40/12,5 и 40/25 мг отобран для клинического применения в результате тщательного анализа интенсивности потенцирования антигипертензивного действия.
4. Учитывая вышеизложенное, фиксированная комбинация АЗС‑М + ХЛД является оптимальной в качестве как первого выбора, так и в случае неэффективности или непереносимости других популярных комбинаций.
Подготовила Наталья Нечипорук
Статья печатается при поддержке
ООО «Такеда Украина»
UA/AZI/0619/0013
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (64) червень 2019 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....