Новый взгляд на проблему метаболического синдрома

В 2014 году в Вашингтоне (США) состоялось заседание кардиометаболической экспертной комиссии (ЭК), темами обсуждения которого стали: оптимизация подходов к метаболическому синдрому (МС), усовершенствование методов оценки кардиометаболических рисков у пациентов, разработка программ профилактики заболеваемости в современных условиях. В заседании комиссии участвовали как независимые эксперты, так и представители более чем 20 различных профессиональных организаций. Результаты обсуждения были опубликованы в журнале Американской коллегии кардиологов.
МС определяется как группа факторов, лежащих в основе кардиоваскулярных и метаболических заболеваний. Наиболее точное клиническое определение МС было дано в 2001 г. Национальной образовательной программой терапии состояний, связанных с холестерином, у взрослых (NCEP ATP III). Согласно этому определению в понятие МС следует включить такие факторы: абдоминальное ожирение, атерогенная дислипидемия, повышенное артериальное давление (АД), инсулинорезистентность (с нарушением толерантности к глюкозе или без нее), провоспалительные и протромботические состояния. Критерием диагноза МС является наличие у пациента ≥3 состояний:
- окружность талии (ОТ) >102 см у мужчин и >88 см у женщин;
- концентрация триглицеридов ≥150 мг/дл (≥1,7 ммоль/л);
- уровни липопротеинов высокой плотности (ЛПВП) <40 мг/дл (<1,0 ммоль/л) у мужчин и <50 мг/дл (<1,2 ммоль/л) у женщин;
- АД ≥130/85 мм рт. ст.;
- уровень глюкозы натощак ≥100 мг/дл (≥6,1 ммоль/л).
В 2005 г. в определение было внесено уточнение: максимально допустимая ОТ у мужчин и женщин азиатского происхождения – 90 см и 80 см соответственно. Однако эти критерии не дают полной характеристики синдрома, не обозначают связь патофизиологических механизмов развития МС с повреждением органов-мишеней, не учитывают расовые, половые различия и социально-экономические условия.
В клинических условиях МС зачастую недооценивается даже по указанным 5 критериям. Так, об уровне аполипопротеина В, о размерах частиц липопротеинов низкой плотности (ЛПНП), об эндотелиальной дисфункции, инсулинорезистентности, о провоспалительных и протромботических состояниях клиницисты забывают достаточно часто. Очевидно, что с увеличением количества факторов, обусловивших МС, возрастает и кардиоваскулярный риск. Например, в исследовании Hoorn (2005), выполненном в Нидерландах, было показано, что кардиоваскулярный риск становится статистически значимым при обнаружении 3 критериев МС у мужчин и 2 – у женщин. Метаанализ 87 исследований с участием 951 083 пациентов показал, что наличие МС было связано с >2-кратным повышением риска развития атеро- и кардиоваскулярных заболеваний и сердечно-сосудистой смертности (Mottillo S. et al., 2010). Исследование Framingham (2006) продемонстрировало, что независимое друг от друга наличие МС и сахарного диабета (СД) 2 типа повышает риск инсульта примерно в 2 раза, а при сочетании этих патологий увеличивается еще больше. При этом кардиоваскулярный риск у пациентов с МС в отсутствие СД 2 типа выше, чем при СД 2 типа без МС (Alexander C. et al., 2003).
Доказана связь МС с ожирением (ОЖ). Исследование Национального общества здоровья и питания (NHANES, США), проведенное в период с 2003 по 2006 г., показало, что МС среди мужчин с нормальной массой тела встречается в 6,8% случаев, с избыточной массой тела (ИМТ) – в 29,8%, при ОЖ – в 65%. У женщин соответствующие показатели составили 9,3; 33,1 и 56,1% (Ervin R. B., 2009). Несмотря на высокую корреляцию МС с ОЖ, иногда у людей с высоким индексом массы тела (ИМТ) отсутствует МС, и наоборот – некоторые лица с нормальным весом имеют признаки МС.
В целом высокий риск МС при ОЖ чаще всего объясняется неудовлетворительным качеством питания и низкой двигательной активностью. Такие факторы, как пол, возраст, расовая принадлежность, также могут играть значительную роль в развитии МС, что объясняется различным типом распределения жира, размерами и функциями адипоцитов. Так, отложение жира преимущественно в области талии менее прогностически благоприятно, чем его накопление в нижней части тела. В связи с этим ИМТ не всегда является корректным показателем в качестве критерия МС, более информативна оценка соотношения ОТ и ИМТ.
Во время обсуждения экспертной комиссией были затронуты 3 основных аспекта: 1) наличие МС прямо коррелирует с кардиоваскулярным риском, однако нет четких критериев его оценки; действующее определение МС не учитывает индивидуальные особенности человека; 2) в настоящее время не разработаны четкие алгоритмы ведения пациентов с МС; 3) существующие рекомендации не отражают эффективность лечебных мероприятий в отношении снижения кардиоваскулярного риска у пациентов с МС.
Методы
В ходе обсуждения члены ЭК создали Кардиометаболический альянс, в состав которого вошли представители Американской кардиологической ассоциации (АСС), Американской ассоциации клинических эндокринологов (AACE), Ассоциации чернокожих кардиологов, а также независимые эксперты.
Целью ЭК стало определение и организация базы фактических данных для поиска ответов на следующие вопросы:
- Что такое МС?
- Какова оптимальная модель ухода за пациентами с МС?
- Какова оптимальная стратегия для реализации этой модели?
Работа альянса была сфокусирована на 3 основных направлениях – четкий разбор МС по компонентам, построение новой модели коррекции МС на основе междисциплинарного подхода и ее внедрение в реальную практику.
Что такое МС и почему это важно?
Определение: от синдрома к болезни
Последние два десятилетия ознаменовались многочисленными дебатами относительно того, какие компоненты МС и в какие сроки в наибольшей степени повышают кардиоваскулярный риск. G. M. Reaven (1988) отметил, что артериальная гипертензия (АГ), инсулинорезистентность, дислипидемия и ОЖ, как правило, образуют симптомокомплекс – так называемый синдром X, наличие которого существенно повышает риск развития атеросклероза и кардиоваскулярных заболеваний. Спустя десятилетие ВОЗ ввела термин МС, в описании которого основной акцент делается на инсулинорезистентность и гипергликемию. Это дало повод для споров на тему: что первично – ОЖ или инсулинорезистентность?
В 1999 г. Европейская группа по изучению инсулинорезистентности (EGIR) модифицировала определение ВОЗ, заменив его термином «синдром инсулинорезистентности». Позднее в докладе NCEP ATP III снова был использован термин МС, объединяющий абдоминальное ОЖ, выражающееся в увеличении ОТ, и провоспалительные/протромботические состояния. Постепенно определение МС расширялось и дополнялось. В 2009 г. сразу несколько международных организаций разработали критерии МС, используемые и сегодня, в МКБ-10 он обозначен как E88.81.
Согласно современным представлениям МС – это хроническое и прогрессирующее патофизиологическое состояние, своего рода кластер факторов риска, образующих сложный синдром с собственными патофизиологическими механизмами. Оно связано с повышенным кардиоваскулярным риском и увеличением вероятности развития СД 2 типа. Важно понимать, что МС – это не просто «переупаковка» воедино его отдельных компонентов, а тяжелое состояние, ассоциирующееся с повышенным кардиоваскулярным риском и увеличением уровня общей смертности, сохраняющимися даже после нормализации/устранения отдельных компонентов МС (Einhorn D. et al., 2003).
Кроме того, МС включает в себя и так называемые дополнительные маркеры риска: повышенный уровень аполипопротеина В; наличие мелких плотных частиц ЛПНП; высокие уровни циркулирующих воспалительных маркеров, таких как С-реактивный белок (СРБ) и фибриноген; микроальбуминурия. После устранения основных компонентов МС может сохраняться повышенный кардиоваскулярный риск как раз за счет этих невыявленных состояний.
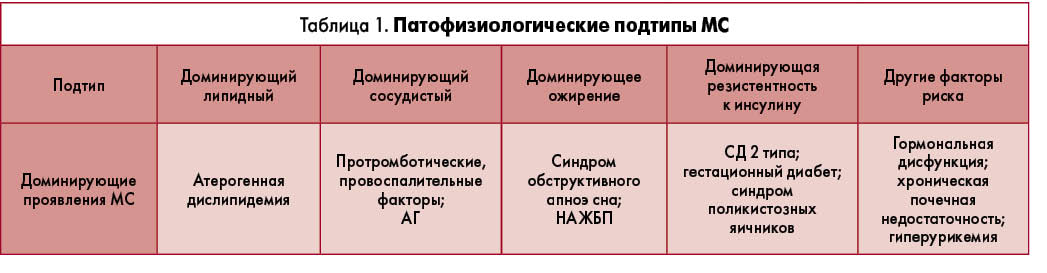
Необходимо помнить, что негативное влияние МС на организм не ограничивается сердечно-сосудистой или эндокринной системами: зачастую его мишенями становятся несколько органов и систем. МС связывают с развитием дислипидемии, гормональными нарушениями (например, синдромом поликистозных яичников), синдромом обструктивного апноэ сна, некоторыми злокачественными новообразованиями, психоэмоциональными расстройствами (например, депрессией), хроническими заболеваниями почек, патологией суставов, неалкогольной жировой болезнью печени (НАЖБП) и др., что подчеркивает необходимость определения патофизиологического подтипа МС с оценкой предрасположенности к тем или иным заболеваниям с целью профилактического и терапевтического контроля над ними.
Основные подтипы МС описаны в таблице 1.
Фокус на патофизиологию
Ожирение. Американская коллегия эндокринологов определяет ОЖ как хроническое заболевание, характеризующееся рядом патофизиологических процессов, которые приводят к увеличению массы жировой ткани и могут сопровождаться повышением уровней заболеваемости и смертности, а также увеличением частоты возникновения МС, тесно связанного с эпидемией ОЖ в США. По последним данным, распространенность МС в США у мужчин и женщин составляет 35 и 33% соответственно (Go A. S. et al., 2014). Предполагается, что к 2030 г. >50% населения США будут страдать ОЖ, следовательно, можно ожидать роста заболеваемости МС в ближайшие 10 лет. Несмотря на тесную корреляцию, само по себе ОЖ не является исчерпывающим дескриптором для МС, как отмечалось ранее, а ИМТ и ОТ не всегда предоставляют адекватную информацию.
Известно, что кардиометаболический риск в большей степени связан с так называемым висцеральным ОЖ, то есть риски определяются не столько степенью избытка массы, сколько типом распределения жира, размерами и функцией адипоцитов. Развитие висцерального ОЖ объясняют неспособностью подкожно-жировой клетчатки накапливать избыток жиров, образующийся при повышенной калорийности пищи. Дефекты созревания и дифференцировки адипоцитов определяют их дисфункцию, проявляющуюся в повышении уровня триглицеридов и накоплении жировой ткани во внутренних органах, сердце, печени, скелетных мышцах. Следующие за этим процессы, такие как повышенный липолиз, изменение гомеостаза глюкозы, избыточная продукция адипоцитокинов и эндотелиальная дисфункция, и являются основой патофизиологических изменений, наблюдаемых при МС.
Инсулинорезистентность. Инсулинорезистентность может быть причиной повышения уровня глюкозы крови натощак, а значит, создавать условия для развития СД 2 типа. В то же время ее выраженность усугубляется с утяжелением симптоматики МС. Инсулинорезистентность связывают с ростом уровней триглицеридов и снижением содержания ЛПВП, повышением активности провоспалительных и протромботических маркеров, таких как ингибитор активатора плазминогена-1, фибриноген, СРБ (Festa A. et al., 2000). Инсулинорезистентность может выступать причиной активации симпатической нервной системы, задержки натрия (с последующей АГ), избытка андрогенов, фактором риска хронического заболевания почек и др.
Резидуальные риски
ЭК отметила, что в рекомендательных документах учтены далеко не все факторы риска МС. Многие из них определяются расовой и культурологической принадлежностью больных, особенностями их метаболизма, конституции и т. д. Кроме того, согласно теории «тикающих часов» существуют факторы, способствующие формированию МС еще до рождения или в самом раннем возрасте: низкая масса плода, гестационный диабет, небольшая окружность головы при рождении, искусственное вскармливание и т. д. (Efstathiou S. et al., 2012). У детей и подростков к развитию МС предрасполагают низкий социально-экономический статус родителей, вредные семейные привычки.
Образ жизни
ЭК признает ведущую роль правильного питания и активного образа жизни в профилактике и коррекции симптомов МС. Так, даже при наличии МС физическая активность снижает кардиоваскулярный риск (Broekhuizen L. et al., 2011). Изменение рациона питания также может существенно уменьшить такие риски (Eilat-Adar S. et al., 2013). К примеру, диета DASH (система питания, рекомендованная при АГ) и средиземноморская диета способствуют снижению АД, уровня триглицеридов, уменьшают кардиоваскулярные и атеросклеротические риски в целом (Estruch R. et al., 2013).
При этом важен системный подход, а не просто насыщение рациона отдельными макро- или микронутриентами. ЭК считает, что изменение образа жизни с целью терапии и профилактики МС имеет приоритетное значение.
Междисциплинарная модель ведения пациентов с МС
В ходе обсуждения ЭК было определено несколько приоритетных направлений ведения пациентов, имеющих МС или подверженных риску его развития:
- комплексный подход к терапии;
- скрининг групп риска по МС;
- учет подтипа МС и индивидуальных особенностей пациента;
- привлечение к проблеме не только конкретного пациента, но и общества в целом с целью коррекции образа жизни.
Ступенчатый подход к МС
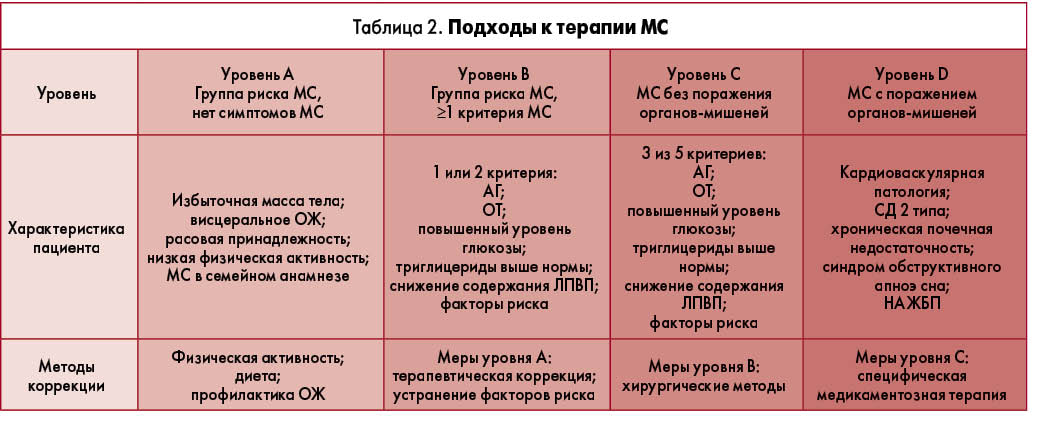
ЭК была разработана схема ступенчатого подхода к терапии МС – начиная с профилактики у лиц повышенного риска и заканчивая лечением пациентов, имеющих выраженную симптоматику МС. На всех этапах важным моментом остается оценка индивидуальных факторов риска (расовая принадлежность, наличие висцерального ОЖ и негативных пищевых привычек, неблагоприятный семейный анамнез и др.).
Основные подходы к терапии описаны в таблице 2.
Построение модели комплексной терапии
По мнению ЭК, для построения успешной модели борьбы с МС одной лишь системы здравоохранения недостаточно. Необходимо вовлекать в процесс профессиональные организации, дошкольные учебные заведения, школы, вузы. Начинать скрининг МС в группах риска необходимо еще в раннем возрасте. Это предполагает систематическое измерение таких показателей, как масса тела, АД, ОТ, уровень триглицеридов и т. д. Полезными могут оказаться пометки о сниженной физической активности, отзывы о качестве питания. Доминирующей стратегией должна стать популяризация здорового образа жизни во всех слоях населения.
Второй важной задачей, по мнению ЭК, является разработка простых и доступных методов оценки висцерального ОЖ (более дешевых, чем магнитно-резонансная или спиральная компьютерная томография). Кроме того, немаловажным является информирование врачей о возможной причастности синдрома обструктивного апноэ сна, НАЖБП к симптомокомплексу МС.
Наконец, необходим междисциплинарный подход к лечению МС, согласно которому терапия носит однонаправленный характер, а не представляет собой несистематические методы воздействия на отдельные диагнозы. Рациональная модель комплексного лечения МС отражена в таблице 3.
Комплексный подход должен быть направлен также на переориентацию работодателей и страховых компаний. МС дорого и нерационально лечить на уровне поражения органов-мишеней, особенно при отсутствии мультидисциплинарного подхода. Профессиональные организации и представители страховой медицины должны понимать, что профилактика МС не требует больших затрат: скрининг и коррекция факторов риска обходятся дешевле, чем терапевтические меры уровней С или D при развернутой картине МС. Задачи органов здравоохранения – профилактическое ориентирование пациента и пропаганда здорового образа жизни с разъяснением механизмов развития МС и его негативных последствий.
Оптимальная стратегия реализации новой модели ведения пациентов с МС
ЭК считает, что в процесс лечения должны быть вовлечены работники здравоохранения, медицинской и фармацевтической промышленности, страховые компании, адвокаты пациентов, руководители отделов и лидеры групп сверстников в учебных учреждениях. Заинтересованными сторонами являются врачи, медсестры, а также диетологи, физиологи, психологи, сертифицированные преподаватели курсов по СД и др. В реализации новой модели должны принять участие и семейные врачи, педиатры, терапевты, акушеры-гинекологи, гериатры, кардиологи и эндокринологи.
Примером расширения знаний населения о МС может служить программа профилактики СД (Diabetes Prevention Program – DPP), распространяющая информацию о заболевании в виде адресной доставки. Пилотное кластерное рандомизированное исследование DEPLOY по профилактике СД и внедрению здорового образа жизни включило в себя лиц из группы YMCA (Young Men’s Christian Association). В группе провели 16 занятий по снижению исходной массы тела на 5-7%, 150 мин в неделю было выделено для умеренных физических нагрузок. Отмечено, что через 4-6 и 12-14 мес в группе отмечено снижение массы тела, АД и уровня триглицеридов. DPP также провела занятия в 14 группах YMCA в г. Нью-Йорке, среди 254 участников у 40,2 и 60,8% достигнуто снижение веса на 5% за 16 нед и 10 мес соответственно (Bozack A. et al., 2012). Конечно, исследования были недостаточно масштабными и весьма ограниченными по времени, однако положительный пример общественного влияния на образ жизни в них прослеживается очень четко.
По мнению ЭК, для профилактики и терапии МС необходима национальная программа поддержки физического воспитания, где было бы предусмотрено создание мест для занятий спортом в шаговой доступности, спортивных зон в парках и зонах отдыха, выделение помещений для таких занятий. Весьма полезным было бы побуждать людей перемещаться преимущественно пешком или на видах транспорта, требующих физической активности. Чрезвычайно важную роль могла бы сыграть программа мероприятий по пропаганде здорового образа жизни среди пациентов диспансерных групп. Так, DPP реализует программу по снижению веса за 2 года. Учебный план DPP включает структурированные рационы питания и умеренные физические нагрузки до 200 мин/нед. За 2 года у 301 рандомизированного пациента с СД 2 типа в группе исследования было достигнуто значительное снижение массы тела, ИМТ, ОТ, уровня глюкозы, инсулинорезистентности по сравнению с контрольной группой. Так, у 46,5% пациентов основной группы отмечалось снижение массы тела на 5%, а у 21,3% – на 10% и более. За 8 лет 50,3% участников из основной группы (по сравнению с 35,7% в группе контроля) потеряли в среднем 5% массы тела, а 26,9% (в группе контроля – 17,2%) потеряли ≥10% от исходной массы тела (Look AHEAD Research Group, 2014).
Пациенториентированная медицинская организация (Patient-Centered Medical Home, PCMH) осуществляет свою деятельность на основании таких принципов:
- комплексная помощь больным;
- уход, ориентированный на пациента;
- координация медицинской помощи;
- оказание доступных услуг;
- повышение качества и безопасности медицинской помощи.
Систематический обзор 31 исследования установил положительное влияние модели PCMH, выражавшееся в уменьшении числа посещений отделения неотложной помощи взрослыми пациентами (хотя это не отразилось на частоте госпитализаций и сумме общих затрат). В другом исследовании в 36 семейных практиках PCMH за 26 мес было отмечено улучшение уровня профилактики и качества ведения хронических заболеваний. Однако данных об оценке самими пациентами вышеперечисленных показателей в исследовании нет (Maeng D.
et al., 2012). Долгосрочные данные исследования также ограничены, так как большинство из этих моделей были реализованы в течение последних 5-10 лет.
Организации по уходу (Accountable Care Organiza-tions – АСО) – еще один механизм для эффективной реализации новой модели ведения пациентов с МС. При этом если PCMH сосредоточена на первичной медицинской помощи, то в структуру ACO включены также больницы и центры специализированной помощи. Большинство АСО создано недавно (до 2 лет), их основная цель – упрощение и удешевление медицинской помощи. Тем не менее за короткий период истории данной сети организаций удалось достичь снижения затрат на посещение амбулаторий, лабораторные услуги, проведение визуализирующих исследований. Помимо сокращения расходов отмечается более низкая обращаемость пациентов АСО в центры неотложной помощи, уменьшение показателя повторной госпитализации, улучшенный контроль АД.
Несколько важных вопросов в ведении пациентов с МС остаются открытыми. Среди безотлагательных мер следует назвать разработку диагностических подходов к определению подтипа МС, методов стратификации рисков и персонализации медицинской помощи. Успех терапии, по мнению ЭК, заключается в комплексном подходе, включающем в себя модификацию образа жизни, применение медикаментов в сочетании с хирургическими методами коррекции ОЖ и других проявлений МС.
Новая модель ведения МС предполагает участие всех заинтересованных сторон – от самого пациента до национальных общественных и медицинских организаций. Своевременный и адекватный скрининг улучшит меры профилактики заболевания, а информированность медицинских работников обеспечит повышенную бдительность и комплексность подхода к терапии пациентов с МС.
Статья печатается в сокращении.
Laurence S. Sperling et al. J Am Coll Cardiol. 2015; 66 (9).
Перевела с англ. Александра Меркулова
Медична газета «Здоров’я України 21 сторіччя» №4 (377), лютий 2016 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....