Парентеральне застосування ацетилцистеїну в комплексній терапії пацієнтів із COVID-19-асоційованою негоспітальною пневмонією: перший клінічний досвід і подальші перспективи
 Коронавірусна хвороба (COVID‑19) вважається однією з найбільших біологічних загроз людству в сучасній історії. Тяжкі клінічні форми цієї інфекції характеризуються виникненням пневмонії з полісегментарним ураженням легень і дихальною недостатністю, а також розвитком гострого респіраторного дистрес-синдрому (ГРДС). Епідеміологічна ситуація ускладнюється відсутністю дієвих етіотропних противірусних засобів та ефективних вакцин. Незважаючи на наявність міжнародних і національних протоколів лікування, серед клініцистів є досить глибокі розбіжності щодо вибору тих чи інших препаратів і способів їх застосування. З огляду на це в більшості клінічних ситуацій на перший план виходить патогенетична та симптоматична терапія COVID‑19. Наведений клінічний випадок якнайкраще, на нашу думку, ілюструє можливості патогенетичної терапії в сьогоднішніх реаліях державної медичної служби України.
Коронавірусна хвороба (COVID‑19) вважається однією з найбільших біологічних загроз людству в сучасній історії. Тяжкі клінічні форми цієї інфекції характеризуються виникненням пневмонії з полісегментарним ураженням легень і дихальною недостатністю, а також розвитком гострого респіраторного дистрес-синдрому (ГРДС). Епідеміологічна ситуація ускладнюється відсутністю дієвих етіотропних противірусних засобів та ефективних вакцин. Незважаючи на наявність міжнародних і національних протоколів лікування, серед клініцистів є досить глибокі розбіжності щодо вибору тих чи інших препаратів і способів їх застосування. З огляду на це в більшості клінічних ситуацій на перший план виходить патогенетична та симптоматична терапія COVID‑19. Наведений клінічний випадок якнайкраще, на нашу думку, ілюструє можливості патогенетичної терапії в сьогоднішніх реаліях державної медичної служби України.
Хворий К. 46 років госпіталізований 19.06.2020 до перепрофільованого в інфекційне відділення терапії центральної районної лікарні з підозрою на пневмонію, асоційовану з COVID‑19. Раніше на диспансерному обліку не перебував, супутньої патології та шкідливих звичок не має. На час госпіталізації скаржився на загальну слабкість, ломоту в тілі, підвищення температури тіла до 37,5 ºС, помірну задишку під час фізичного навантаження та сухий кашель.
 Захворів 16.06.2020, коли з’явилися загальна слабкість, підвищення температури тіла до 37,4 ºС. Контакт з інфекційними хворими заперечує. 17.06.2020 загальний стан погіршився: наростала слабкість, температура тіла підвищилася до 38-39 ºС. Прийом жарознижувальних засобів давав короткочасний ефект. 18.06.2020 хворий звернувся до сімейного лікаря; було взято мазок із зіва та носа для ПЛР‑дослідження на SARS-CoV‑2. Призначено азитроміцин 500 мг 1 р/добу. 19.06.2020 з’явилася задишка, на тлі прийому парацетамолу в дозі 500 мг температура тіла не знижувалася. Пацієнт викликав швидку допомогу та був доставлений до лікарні.
Захворів 16.06.2020, коли з’явилися загальна слабкість, підвищення температури тіла до 37,4 ºС. Контакт з інфекційними хворими заперечує. 17.06.2020 загальний стан погіршився: наростала слабкість, температура тіла підвищилася до 38-39 ºС. Прийом жарознижувальних засобів давав короткочасний ефект. 18.06.2020 хворий звернувся до сімейного лікаря; було взято мазок із зіва та носа для ПЛР‑дослідження на SARS-CoV‑2. Призначено азитроміцин 500 мг 1 р/добу. 19.06.2020 з’явилася задишка, на тлі прийому парацетамолу в дозі 500 мг температура тіла не знижувалася. Пацієнт викликав швидку допомогу та був доставлений до лікарні.
Об’єктивно: стан середнього ступеня тяжкості. Свідомість збережена, орієнтований у часі та просторі. Індекс маси тіла – 26,6 кг/м2. Шкіряні покриви без змін, слизові оболонки блідо-рожевого кольору, вологі. Периферичні лімфовузли не збільшені. Периферичні набряки відсутні. Зів помірно гіперемований. Язик вологий, біля кореня – білий наліт.
Грудна клітка: візуально додаткова мускулатура в акті дихання участі не бере, частота дихання – 20/хв. SpО2 у спокої – 94%. Перкуторно – притуплення легеневого тону в зоні проекції середньої та нижньої часток правої та нижньої частки лівої легені. Аускультативно реєструвалися послаблення везикулярного дихання та вологі дрібнопухирчасті хрипи в нижніх відділах обох легень і середній частці правої.
Серце: гемодинаміка стабільна.
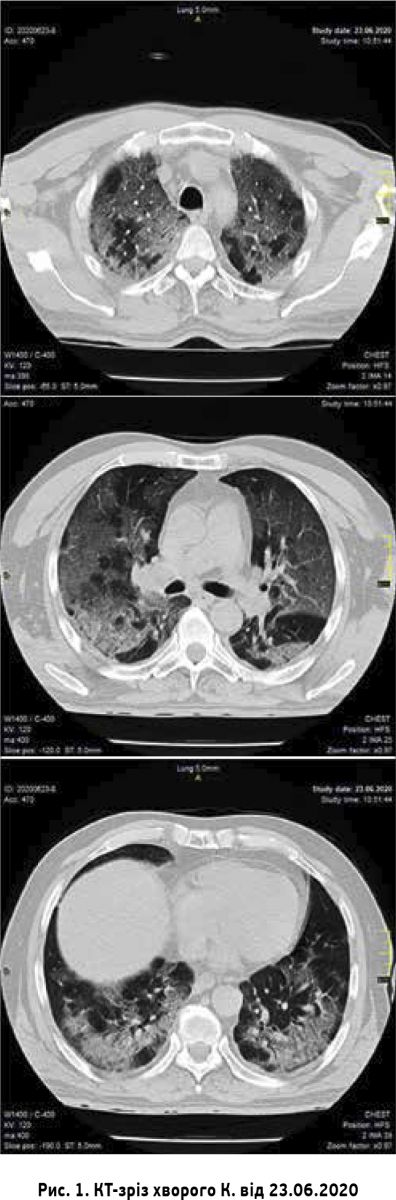
Дані лабораторних та інструментальних методів обстеження: ПЛР‑тест на SARS-CoV‑2 – позитивний. Рентгенографія органів грудної клітки (ОГК) – виявляються малоінтенсивні негомогенні затемнення в середніх-нижніх відділах обох легень (рис. 1). Виконати комп’ютерну томографію (КТ) ОГК, зважаючи на стан хворого, було неможливо. Під час електрокардіографії зареєстровано синусову тахікардію.
Загальний аналіз крові: лейкоцити – 12,0×109/л, еритроцити – 3,86×1012/л, гемоглобін – 123 г/л, ШОЕ – 62 мм/год, лейкоцитарна формула без змін. У загальному аналізі сечі виявлено дріжджові гриби (++).
Біохімічний аналіз крові: С‑реактивний білок (++++), D‑димер – 12 тис. од.
Діагноз: COVID‑19, тяжкий перебіг. Негоспітальна пневмонія, 3-тя клінічна група, двобічне полісегментарне ураження легень, легенева недостатність 2 ступеня.
Стартова терапія включала призначення осельтамівіру 75 мг 2 р/добу впродовж 10 днів, азитроміцину 500 мг 1 р/добу впродовж 6 днів, амоксициліну/клавуланату 1,2 г на 200 мл фізіологічного розчину 2 р/добу внутрішньовенно (в/в) краплинно впродовж 7 днів. Додатково вводили Інгаміст® 3 мл 2 р/добу в/в протягом 10 днів, Інфулган 100 мл 2-3 р/добу в/в за температури тіла понад 38 ºС, Реосорбілакт® 400 мл/добу в/в краплинно впродовж 5 днів, еноксапарин 0,4 мл/добу підшкірно впродовж 7 днів. Окрім того, застосовували омепразол 40 мг в/в протягом 7 днів, дротаверин 2 мл внутрішньом’язово протягом 3 днів, пробіотик усередину 3 р/добу.
На тлі лікування стан хворого погіршувався, наростала задишка (в спокої та під час мінімального фізичного навантаження), збільшувалася інтенсивність кашлю, SpO2 – 90%. Розпочато оксигенотерапію.
 Станом на 23.06.2020 АТ – 90-80/50 мм рт. ст., ЧСС – 100-120 уд./хв, SpО2 – 86-88% на тлі інсуфляції О2, температура тіла – 37,5-38 ºС. Аускультативно в легенях дихання дифузно послаблене, над усією поверхнею – вологі дрібнопухирчасті хрипи.
Станом на 23.06.2020 АТ – 90-80/50 мм рт. ст., ЧСС – 100-120 уд./хв, SpО2 – 86-88% на тлі інсуфляції О2, температура тіла – 37,5-38 ºС. Аускультативно в легенях дихання дифузно послаблене, над усією поверхнею – вологі дрібнопухирчасті хрипи.
З огляду на негативну клінічну динаміку пацієнта переведено до реанімаційного відділення, де він перебував до 26.06.2020. Стан оцінювався як стабільно тяжкий; було вирішено не проводити штучну вентиляцію легень (ШВЛ), натомість застосовувалася високопоточна оксигенотерапія з використанням full face маски. Здійснено корекцію фармакотерапії, а саме: замість амоксициліну/клавуланату призначено меропенем 1000 мг/добу в/в, дексаметазон 8 мг/добу в/в. Також призначено L‑орнітин-L‑аспартат 10 мг на 200 мл фізіологічного розчину в/в краплинно протягом 5-10 днів, триметилгідразиній 10 мл в/в протягом 5-10 днів. Терапію Інгамістом 3 мл в/в продовжено до 15 днів. Із 26.06.2020 додано сульфокамфорну кислоту 2 мг 3 р/добу впродовж 5 днів.
Виконати КТ ОГК не вдавалося, АТ перебував на рівні 90-80/50 мм рт. ст. При спробах припинення оксигенотерапії стрімко наростала задишка та знижувався показник сатурації. Із 01.07.2020 додано Інгаміст 3,0 інгаляційно на фізіологічному розчині через небулайзер, Лефлоцин 750 мг 1 р/добу в/в 10 днів.
Здійснювали моніторинг лабораторних показників: тривалий час зберігалися лейкоцитоз, збільшення ШОЕ до 50-65 мм/год, підвищувалися рівні АЛТ, АСТ до 218 од/л і D‑димеру до 8-10 тис. од. Повторний ПЛР‑тест на SARS-CoV‑2 був позитивний.
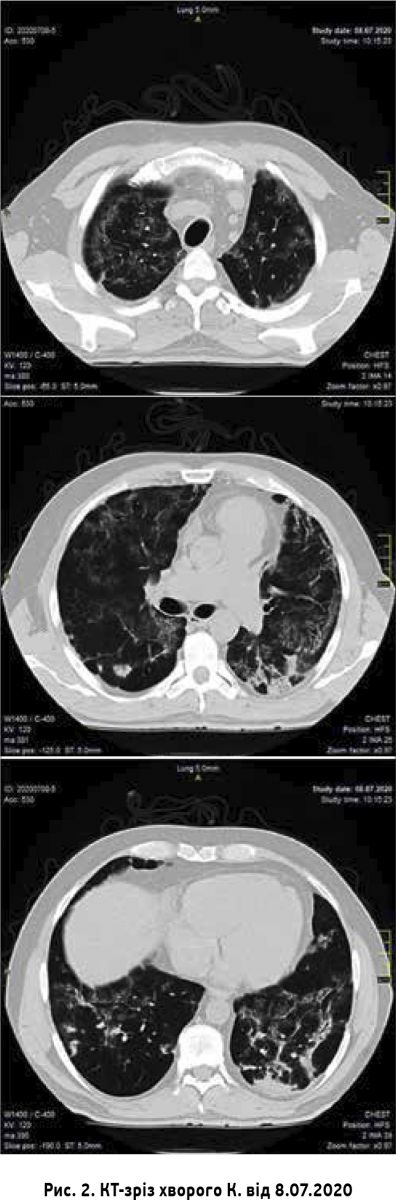
Покращення стану пацієнта зареєстровано з 05.07.2020, що проявлялося зменшенням задишки та кашлю, стабілізацією гемодинаміки, нормалізацією температури тіла, збільшенням періодів часу без кисневої підтримки. Лише 08.07.2020 стало можливим проведення КТ ОГК. За висновком рентгенолога пневматизація обох легень субтотально знижена за рахунок ділянок ущільнення паренхіми за типом «матового скла» зливного характеру, потовщання міжчасточкових перегородок і ділянок консолідації переважно в задньо-нижніх відділах легень. Вільної рідини в плевральних порожнинах немає. Структури межистіння не змінені (рис. 2).
У контрольних лабораторних дослідженнях поступово реєстрували нормалізацію показників. ПЛР‑тест на вірус SARS-CoV‑2 від 23.07.2020 – негативний. 28.07.2020 виконано контрольну КТ ОГК. У порівнянні з КТ ОГК від 8.07.2020 динаміка позитивна у вигляді зменшення об’єму й інтенсивності ділянок «матового скла» та консолідації.
28.07.2020, тобто через 40 днів після госпіталізації, пацієнта виписано зі стаціонару під нагляд сімейного лікаря.
Обговорення
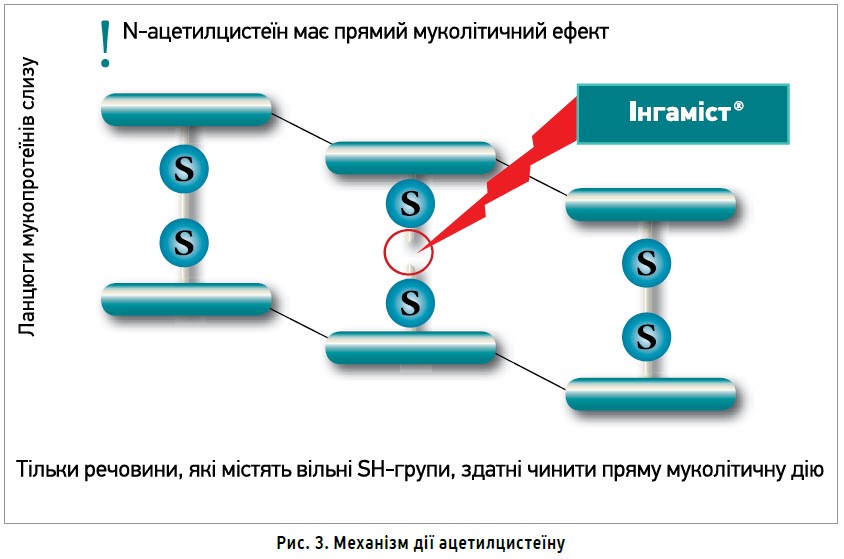
Своєрідним трендом фармакотерапії коронавірусної інфекції є використання добре вивчених препаратів з опосередкованою противірусною активністю й імуномодулювальною дією, потенційно ефективних у разі COVID‑19-асоційованої пневмонії. Серед таких лікарських засобів, призначення котрих є обґрунтованим, особливо в пацієнтів із хронічною бронхолегеневою патологією (хронічне обструктивне захворювання легень, бронхіальна астма, бронхоектази, інтерстиціальні хвороби легень), і не потребує отримання письмової згоди за умови призначення, є ацетилцистеїн. Механізм дії ацетилцистеїну, що відомий широкому загалу лікарів як муколітик, полягає в руйнуванні дисульфідних зв’язків між молекулами муцину (рис. 3). За понад п’ять десятиліть досліджень і клінічного використання цей препарат не перестає дивувати багатогранністю дії.
Ефективність ацетилцистеїну як муколітика, застосовуваного в інгаляціях або інстиляціях, вивчалася в низці досліджень. Результати цих досліджень показали, що ацетилцистеїн (один або в асоціації з антибіотиками) розріджує мокротиння, полегшує відкашлювання та сприяє зменшенню кашлю й ліквідації симптомів бронхолегеневого процесу [1]. Препарат ефективний при гнійному та слизистому мокротинні, його дія не змінюється під впливом інгаляції кисню [2].
Наукові роботи демонструють вплив ацетилцистеїну на синтез сурфактанта. У дослідженні G.C. Mereto та співав. [3] було показано, що ацетилцистеїн, уведений внутрішньом’язово в дозі 300 мг двічі на день, посилює секреторну активність пневмоцитів 2 типу, які беруть участь у синтезі сурфактанта.
У дослідженні було оцінено можливу синергію між антибіотиками й кожним із зазначених далі засобів: N-ацетилцистеїн (NAC), амброксол та аскорбінова кислота – проти 5 клінічних ізолятів Pseudomonas aeruginosa. Ацетилцистеїн продемонстрував вищий синергізм, аніж амброксол й аскорбінова кислота. Показники синергізму становили 80% для ацетилцистеїну, 55% для амброксолу та 15% для аскорбінової кислоти (рис. 4) [4].
Було показано ефективність ацетилцистеїну при внутрішньом’язовому та внутрішньовенному введенні в дозі 300 мг 2 р/день або 500 мг 1 р/день протягом 6 днів у пацієнтів із гострим і хронічним бронхітом [5, 6].
NAC успішно використовувався в ліквідаторів аварії на Чорнобильській АЕС, сприяючи ефективному видаленню елементів депонованого пилу з бронхолегеневого апарату у віддалені після впливу терміни, а також зниженню інтенсивності оксидантних процесів у фагоцитах бронхоальвеолярного простору [7].
У порівнянні з іншими муколітиками ацетилцистеїн має низку переваг (табл. 1). Серед фундаментальних властивостей клітин людського організму є здатність протистояти впливу вільних радикалів, яка реалізується завдяки глутатіону – речовині, здатній існувати як в окисленій, так й у відновленій формі. Одним із трьох компонентів цієї молекули є амінокислота цистеїн, транспортною формою котрої якраз і виступає ацетилцистеїн. Фармакокінетичні дослідження доводять, що введення в організм 1000 мг ацетилцистеїну на добу сприяє значному зростанню вмісту глутатіону [8]. Глутатіон бере участь у передачі внутрішньоклітинних сигналів, контролює активність факторів транскрипції та є «пасткою» для вільних радикалів, які здатні спричиняти цитоліз. Глутатіон також є косубстратом у реакціях детоксикації пероксидів, які каталізуються глутатіонпероксидазою та глутатіонтрансферазою, що запобігає утворенню небезпечних активних форм кисню (пероксид і супероксидні аніони).
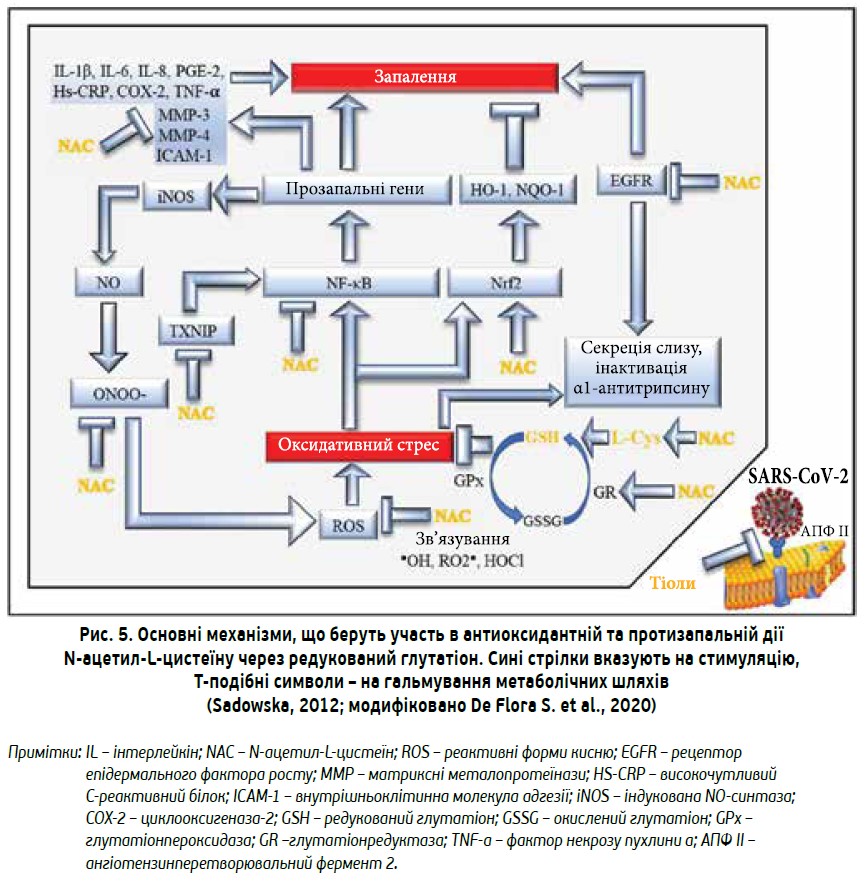
Медико-біологічне значення порушень у системі глутатіону є величезним, адже явища оксидантного стресу супроводжують чималу кількість захворювань, таких як хвороба Паркінсона, ВІЛ‑інфекція, алкогольна хвороба печінки, муковісцидоз тощо. До того ж дисбаланс у системі глутатіону зумовлює прискорене старіння людини [9]. Саме тому використання ацетилцистеїну як антиоксидантного засобу при хронічних запальних захворюваннях є ефективним інструментом як у клінічних дослідженнях, так і в практичній медицині [10] (рис. 5).
У пацієнтів із тяжким перебігом коронавірусної інфекції реєструється збільшення продукції вільних радикалів на тлі зниження антиоксидантної активності захисних механізмів клітин. Це підтверджується, зокрема, даними обмеженого дослідження в період пандемії в Шанхаї (КНР) за участю 198 хворих на СOVID‑19. У 40% пацієнтів реєстрували суттєве підвищення активності глутатіонредуктази, що розглядалось як прояв дисбалансу в системі антиоксидантного захисту [11]. У багатьох оглядах наукових досліджень різними авторами висловлюється припущення стосовно потенційної користі призначення ацетилцистеїну хворим на COVID‑19. Гіперпродукція цитокінів («цитокіновий шторм»), порушення антиоксидантного захисту, надмірне утворення вільних радикалів, порушення мукоциліарного кліренсу в разі втягнення в патологічний процес нижніх дихальних шляхів, бактеріальна суперінфекція, в тому числі спричинена резистентною флорою, – ось далеко не повний перелік патологічних процесів, які обґрунтовують використання ацетилцистеїну в комплексному лікуванні COVID‑19.
Практичний досвід лікування пацієнтів із негоспітальною пневмонією, в тому числі асоційованою з COVID‑19, коли практично завжди в тяжких випадках має місце опортуністична бактеріальна інфекція, вказує на необхідність проведення антибактеріальної терапії. У хворих із тяжкою дихальною недостатністю, особливо тих, які перебувають у відділеннях реанімації та інтенсивної терапії, інфекційний процес у нижніх дихальних шляхах може бути зумовлений антибіотикорезистентними патогенами, стійкість яких визначається, в тому числі, утворенням біоплівок. У цій ситуації неможливо переоцінити здатність ацетилцистеїну руйнувати біоплівки таких збудників, як синьогнійна та кишкова палички, клебсієла, золотистий стафілокок та інші бактерії [12, 13].
Яскравою клінічною ілюстрацією зазначеного ефекту є підвищення ефективності лікування пацієнтів із тяжкою вентилятор-асоційованою госпітальною пневмонією, що було виявлено дослідниками в Ірані. У проспективне рандомізоване подвійне сліпе плацебо-контрольоване дослідження включили 60 пацієнтів, які перебували на механічній вентиляції легень [14]. У складі комбінованої терапії 30 пацієнтів основної групи отримували ацетилцистеїн у дозі 600 мг 2 р/добу через назогастральний зонд, а 30 хворих контрольної групи – плацебо. У групі пацієнтів, які отримували ацетилцистеїн, частота виникнення вентилятор-асоційованої пневмонії була достовірно нижчою, ніж у групі плацебо (26,6% проти 46,6%; P=0,032). Серед пацієнтів основної групи було також встановлено зменшення тривалості перебування у відділенні інтенсивної терапії (14,36±4,69 проти 17,81±6,37 доби; P=0,028) та в стаціонарі (19,23±5,54 проти 24,61±6,81 доби; P=0,03). Частота повного одужання в основній групі була достовірно вищою, ніж у групі плацебо (56,6% проти 30%; P=0,006). При цьому достовірних відмінностей за частотою виникнення небажаних явищ не виявляли.
Значна увага науковців усього світу до ацетилцистеїну в умовах пандемії COVID‑19 зумовлена, зокрема, публікаціями, що вказують на здатність цієї молекули до пригнічення реплікації вірусів [15]. Встановлено, що ацетилцистеїн пригнічував індукцію апоптозу й експресію генів, відповідальних за синтез прозапальних цитокінів і хемокінів (насамперед інтерлейкінів (ІЛ) 6, 8 та інтерферон-індукувального білка – IP‑10) вірусом грипу [16, 17]. Супресія реплікації вірусу грипу ацетилцистеїном відбувалася переважно в ранній фазі інфекції. За умови призначення ацетилцистеїну в комбінації з рибавірином або осельтамівіром смертність лабораторних тварин, інфікованих вірусом грипу, була істотно нижчою [18-20].
Крім експериментальних тваринних моделей, певна противірусна активність ацетилцистеїну спостерігалася й у клінічних дослідженнях. De Flora та співавт. (1997) встановили зменшення інтенсивності клінічних проявів грипу при використанні ацетилцистеїну [21]. В іншому рандомізованому багатоцентровому плацебо-контрольованому дослідженні вивчали ефективність довготривалої терапії ацетилцистеїном із метою профілактики грипу й інших гострих респіраторних вірусних інфекцій (ГРВІ). Ацетилцистеїн у дозі 600 мг 2 р/добу впродовж 6 міс призначали 262 пацієнтам, з яких 78% були віком понад 65 років, а 62% мали супутні нереспіраторні хронічні захворювання. Автори засвідчили зменшення частоти, ступеня тяжкості та тривалості епізодів респіраторної вірусної інфекції. Серед пацієнтів, які приймали ацетилцистеїн, симптоми інфекції були суттєво менш вираженими, ніж у групі плацебо. Дослідники відзначили нормалізацію імунної відповіді в пацієнтів із групи ацетилцистеїну за впливом на клітинну ланку імунітету. Отже, тривалий прийом ацетилцистеїну в зимовий період зменшував тяжкість перебігу грипу/ГРВІ, особливо в пацієнтів із груп ризику, хоча й не запобігав виникненню грипу.
Цікаво, що ацетилцистеїн, як і антибіотики, здатний потенціювати ефект противірусної терапії. Так, у своєму клінічному спостереженні Lai та співавт. повідомили про швидке покращення стану в пацієнта із септичним шоком на тлі грипу A (H1N1), якому призначили комбіновану терапію осельтамівіром з ацетилцистеїном у високій дозі – 100 мг/кг/добу [22].
Найчастіше ацетилцистеїн як у амбулаторній практиці, так і в умовах стаціонару застосовують усередину. Проте лікарю-практику не варто нехтувати лікарськими формами для інгаляційного та парентерального введення. Існують клінічні ситуації, коли пероральне введення лікарського засобу є неможливим. Зокрема, парентеральне введення ацетилцистеїну є пріоритетним у разі перебування пацієнта в комі, при проведенні ШВЛ, необхідності отримати швидкий ефект під час отруєння парацетамолом або тяжкими металами. Наведений клінічний випадок може слугувати прикладом використання такого шляху введення ацетилцистеїну в складі комбінованої фармакотерапії негоспітальної пневмонії тяжкого перебігу. В Україні сьогодні зареєстровано препарат ацетилцистеїну у формі для інгаляційного/парентерального застосування – Інгаміст виробництва вітчизняної фармацевтичної компанії «Юрія-Фарм». Із першого дня госпіталізації хворий К. отримував як муколітичну терапію Інгаміст, який уводився в/в протягом 15 днів. На 12-ту добу стало можливо крім оксигенотерапії застосовувати небулайзерну терапію цим препаратом, яка тривала 7 днів. Інгаміст зарекомендував себе як ефективний і безпечний засіб із муколітичним ефектом. Його своєчасне призначення дає змогу перевести непродуктивний кашель у продуктивний уже на 2-3-й день. Застосування препарату не супроводжувалося появою небажаних ефектів.
Інгаміст показаний за гострих і хронічних захворювань органів дихання, що супроводжуються підвищеним утворенням мокротиння. У разі в/в застосування засіб уводиться повільно краплинно в 0,9% розчині натрiю хлориду чи 5% розчині глюкози. Дорослим пацієнтам застосовують по 1 ампулі 300 мг 1-2 р/добу. Після в/в застосування 600 мг ацетилцистеїну максимальна концентрація в плазмі крові становить 300 ммоль/л, період напіввиведення з плазми крові – 2 год. Загальний кліренс – 0,21 л/год/кг, а об’єм розподілу при плато – 0,34 л/кг. Препарат проникає в міжклітинний простір, переважно розподіляється в печінці, нирках, легенях, бронхіальному секреті. Ацетилцистеїн і його метаболіти виводяться в основному нирками*.
Повідомлення про ефективне застосування парентеральної форми ацетилцистеїну надходять із різних країн. У липні 2020 року в журналі «Клінічна імунологія» опубліковано цікавий клінічний випадок зі США в пацієнта з COVID‑19, дефіцитом глюкозо‑6-фосфат-дегідрогенази (Г6ФД) і гемолітичною анемією. Перебіг захворювання супроводжувався дихальною недостатністю, що прогресувала й від початку потребувала проведення оксигенотерапії з подальшим переведенням пацієнта на ШВЛ і екстракорпоральну мембранну оксигенацію (ЕКМО) [23]. Стартова терапія включала гідроксихлорохін 400 мг/добу. На 5-й день перебування в стаціонарі стан хворого драматично погіршився: прогресувала гіпоксемія та розвинувся значний гемоліз. Зважаючи на прооксидантні властивості хлорохіну та глибоке порушення в системі глутатіону на тлі дефіциту Г6ФД, що й призвело до виникнення гемолітичних порушень, паралельно з посиленням респіраторної підтримки була розпочата терапія ацетилцистеїном у дозі 600 мг кожні 12 год в/в. Стан пацієнта покращився після 14 діб перебування на ЕКМО; врешті, він був виписаний для подальшої реабілітації. Успішне застосування ацетилцистеїну спонукало авторів публікації застосувати препарат у комплексному лікуванні ще 9 пацієнтів із COVID‑19 уже без дефіциту Г6ФД, які потребували проведення ЕКМО. Така терапія сприяла отриманню позитивного клінічного ефекту, що супроводжувався значним зниженням рівнів маркерів системного запалення (С‑реактивного білка та феритину). Попри те що ці клінічні спостереження є досить обмеженими за кількістю, а майже в усіх випадках застосовували системні кортикостероїди, котрі мають потужний протизапальний ефект, автори зробили висновок про доцільність призначення парентерального ацетилцистеїну в лікуванні пацієнтів із тяжким перебігом COVID‑19.
Сьогодні вважається, що в основі патогенезу коронавірусної інфекції лежать імунологічні порушення, котрі проявляються гіперпродукцією цитокінів (фактора некрозу пухлини (ФНП), ІЛ‑1β, –6, –10) унаслідок надмірної антигенної стимуляції імунної системи, а також глибокі зміни в системі антиоксидантного захисту. Численні експериментальні дослідження вказують на здатність ацетилцистеїну ефективно посилювати відновлювальні процеси, поновлюючи резерви глутатіону. Препарат продемонстрував здатність пригнічувати NLRP3-інфламасомний запальний процес in vitro та зменшувати концентрацію ФНП in vivo [24]. Вчені виявили, що ацетилцистеїн спроможний розривати дисульфідні зв’язки в молекулі ангіотензинперетворювального ферменту 2 типу, котрий виступає в ролі рецептора SARS-CoV‑2 на поверхні клітин респіраторного тракту, лімфоцитів, макрофагів, гепатоцитів тощо [25]. Ураховуючи вплив на синтез глутатіону та пригнічення реплікації вірусів, Poe та співавт. вказують на потенційну ефективність ацетилцистеїну в лікуванні COVID‑19 [26].
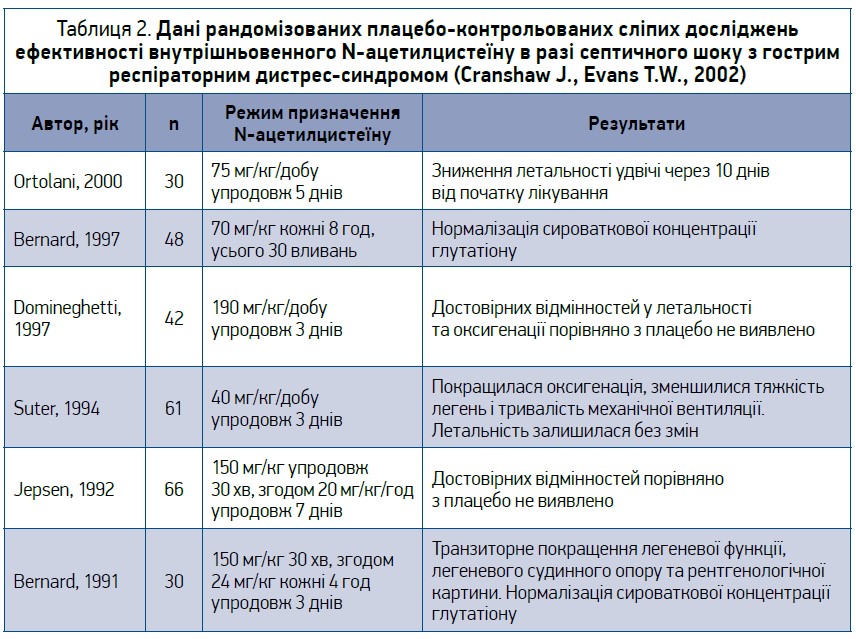
Потенційно фатальним ускладненням COVID‑19 є ГРДС: рівень смертності в цьому разі перевищує 40% [27]. ГРДС зумовлений дифузним альвеолярним пошкодженням, у патогенезі котрого велике значення мають утворення активних форм кисню та перекисне окислення ліпідів. Водночас використання ацетилцистеїну є одним із дієвих способів зменшення вільнорадикального пошкодження альвеолоцитів та їхньої базальної мембрани. Огляд 8 рандомізованих контрольованих досліджень з охопленням 289 пацієнтів із ГРДС, проведений китайськими дослідниками, виявив: попри відсутність переваг щодо зменшення летальності, реєструвалося скорочення тривалості перебування пацієнтів, комплексне лікування котрих включало ацетилцистеїн, у відділеннях реанімації [28] (табл. 2).
Цікавим підходом до фармакотерапії коронавірусної інфекції є спільне використання ацетилцистеїну, оксиду азоту, міді й інших речовин у комбінації з противірусними препаратами, такими як ремдесивір [29]. Із метою корекції імунної відповіді деякі автори пропонують поєднувати ацетилцистеїн з аскорбіновою кислотою, цинком і вітаміном D [30].
Отже, результати лабораторних і окремих клінічних спостережень указують на потенційну ефективність ацетилцистеїну в лікуванні пацієнтів із COVID‑19. Це зумовлено цілою низкою позитивних фармакодинамічних ефектів зазначеного препарату. Проте дані клінічних досліджень є досить неоднорідними: бракує великих рандомізованих плацебо-контрольованих клінічних досліджень, результати котрих формують фундамент доказової медицини в наш час [31].
Віддаючи належне високій професійній кваліфікації, незаперечному сумлінню та безкомпромісній готовності до самопожертви українських лікарів, необхідно зауважити, що незадовільні економічні умови, в яких перебувають наші лікувальні заклади, не дають можливості в багатьох випадках тяжкого перебігу пневмонії виконати ранню етіологічну діагностику (бактеріологічні посіви біологічного матеріалу з виділенням культури й дослідженням чутливості до протимікробних хіміопрепаратів), своєчасно застосувати сучасні променеві методи інструментальної діагностики, моніторувати газовий склад крові та динаміку маркерів системної запальної відповіді в процесі лікування, що подекуди може бути причиною терапевтичних невдач. Унікальність молекули ацетилцистеїну, пов’язана зі швидким муколітичним, потужним антиоксидантним, дезінтоксикаційним ефектами, здатністю підвищувати ефективність протиінфекційних засобів шляхом покращення їх проникності та подолання захисних механізмів патогенної флори, зумовлює необхідність проведення глибших досліджень для чіткого визначення місця препарату в схемах комплексного лікування пацієнтів з інфекціями нижніх дихальних шляхів загалом і COVID‑19 зокрема.
Список літератури знаходиться в редакції.
* Інструкція до препарату Інгаміст, Державний реєстр лікарських засобів України. http://www.drlz.com.ua/
Медична газета «Здоров’я України 21 сторіччя» № 16 (485), 2020 р.
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
Риносинусит (РС) є одним із найчастіших захворювань у первинній медичній практиці. Трьома найбільш чутливими й специфічними симптомами гострого РС є виділення з носа, закладеність носа, лицевий і головний біль. Неконтрольований гострий біль значно погіршує якість життя пацієнтів із РС: спричиняє психоемоційні розлади, знижує працездатність і соціальну активність, сприяє хронізації больового синдрому і збільшує вартість лікування. Отже, полегшення болю при РС є найпершим завданням лікаря....
У всьому світі біль у горлі, зумовлений запальними захворюваннями горла (ЗЗГ), є найчастішою причиною звернень до лікарів загальної практики та оториноларингологів; із ним пов’язано ≈25% відвідувань лікаря. За даними Всесвітньої організації охорони здоров’я, >100 соматичних захворювань із провідним інфекційно-залежним і токсико-алергічним механізмом пов’язані саме із ЗЗГ. Здебільшого причина болю в горлі – гостре запалення інфекційного ґенезу: ГТ, ГФ і ГРВІ....
Антибіотикорезистентність (АБР) визнано загрозою для глобального здоров’я, яка щороку спричиняє мільйони смертей в усьому світі. Невідповідне та надмірне використання антибіотиків (АБ) зумовлює підвищення стійкості мікробних збудників і негативно впливає на ефективність цих дуже важливих лікарських засобів. Завдяки Глобальному плану дій щодо АБР Всесвітня організація охорони здоров’я (ВООЗ) працює над поліпшенням нагляду за резистентністю до протимікробних препаратів і скороченням нераціонального використання АБ. ...
Медичні інформаційні кампанії спрямовані на поширення важливих знань про охорону здоров’я серед населення. З урахуванням потреб і інтересів понад семи мільярдів людей у світі міжнародні організації шукають способи етичного обміну важливими відомостями, без упередженості та несправедливості. Обізнаність у сфері охорони здоров’я має вирішальне значення для кожного, оскільки хвороби та інфекції можуть вразити будь-кого в будь-який час. Таким чином, важливо поширювати відомості про охорону здоров’я за допомогою зрозумілих кожному усних, письмових і візуальних засобів. Ця інформація має сприяти соціальному здоров’ю і не містити дискримінаційного контенту. Заходи з підвищення обізнаності про здоров’я допомагають пацієнтам ліпше розуміти стан свого здоров’я, а також можливі варіанти та методи лікування. Кампанія з підвищення обізнаності відрізняється від маркетингу товарів для здоров’я, оскільки не спонукає купувати той чи інший продукт, а намагається сприяти свідомішому ставленню до свого здоров’я. Глобальні дні громадського здоров’я пропонують великі можливості для підвищення обізнаності та розуміння проблем здоров’я і мобілізації підтримки дій від місцевої громади до міжнародної спільноти. ...