Рекомендації щодо діагностики та лікування гострої тромбоемболії легеневої артерії
У 2019 р. Європейське товариство кардіологів (ESC) спільно з Європейським респіраторним товариством (ERS) розробило оновлені методичні рекомендації з діагностики та лікування гострої тромбоемболії легеневої артерії (ТЕЛА). У документі узагальнено сучасні наукові докази з метою надання допомоги лікарям у виборі найкращих терапевтичних стратегій для пацієнтів із ТЕЛА в конкретній клінічній ситуації.
Впродовж останніх років ESC та інші організації розробили чимало корисних рекомендацій, зокрема щодо ведення пацієнтів із гострою ТЕЛА. Ці документи покликані сприяти кращому наданню медичної допомоги в Європі зокрема та усьому світі на основі даних, зібраних під час рутинної клінічної практики, навчальних матеріалів, що стосуються професійних потреб кардіологів і спеціалістів суміжного фаху, та всебічного огляду опублікованих доказів щодо лікування ТЕЛА. Робоча експертна група виконала оцінку діагностичних та терапевтичних процедур, зокрема співвідношення ризику й користі. Рівень доказовості та сила рекомендацій щодо конкретних стратегій лікування були зважені й визначені відповідно до заздалегідь сформованої класифікації.
Цей документ базується на попередніх настановах ESC стосовно ведення пацієнтів із ТЕЛА, опублікованих 2000, 2008 та 2014 рр. Автори зберегли багато рекомендацій із підтвердженням або посиленням їхньої обґрунтованості, однак також додали нові дані з оптимальної діагностики, оцінки та лікування осіб із ТЕЛА. Сучасні аспекти були інтегровані в попередні наукові здобутки з метою визначення оптимальних та, за можливості, об’єктивно підтверджених терапевтичних стратегій для пацієнтів із підозрюваною або підтвердженою ТЕЛА.
Комплексна діагностика ТЕЛА та контроль ризику
Підвищення обізнаності про венозну тромбоемболію (ВТЕ) та зростання доступності неінвазивних методів візуалізації, переважно комп’ютерно-томографічної (КТ) ангіографії легень, спонукають клініцистів частіше запідозрювати наявність ТЕЛА та проводити діагностичні обстеження, ніж раніше. В минулому показники підтвердження ТЕЛА були низькими (до 5%), що різко контрастує із оцінкою у 50% ще на початку 1980-х рр. (Righini et al., 2015). Отже, дуже важливо, щоб за допомогою сучасних неінвазивних діагностичних стратегій можна було безпечно виключити ТЕЛА у пацієнтів із досить низькою вірогідністю захворювання (Dronkers et al., 2017). І навпаки, позитивний тест повинен характеризуватися адекватною специфічністю для встановлення показань для лікування антикоагулянтами.
Діагностичні стратегії
Для діагностики ТЕЛА використовують різні клінічні оцінювальні методики, вимірювання D-димеру в плазмі крові, процедури візуалізації та ін. За даними 3-місячного спостереження, відмова від антикоагулянтної терапії без дотримання діагностичних стратегій, що ґрунтуються на доказах, була пов’язана зі значним підвищенням частоти епізодів ВТЕ та раптової серцевої смерті (Roy et al., 2006). Науковці визнають, що діагностичний підхід при підозрі на розвиток ТЕЛА може варіювати залежно від наявності та досвіду застосування конкретних тестів у різних лікарнях та клінічних умовах.
Хворі на підозрювану ТЕЛА із гемодинамічною нестабільністю. Клінічна ймовірність ТЕЛА зазвичай висока, і диференційна діагностика включає тампонаду серця, гострий коронарний синдром, розшарування аорти, гостру клапанну дисфункцію та гіповолемію. У разі підозри в пацієнта ТЕЛА високого ризику, на що вказує розвиток гемодинамічної нестабільності, рекомендовано застосовувати приліжкову ехокардіографію (ЕхоКГ) або екстрену КТ-ангіографію легень залежно від клінічних обставин (І, С) (Kucher et al., 2003). У хворого з виразною гемодинамічною нестабільністю підтверджена дисфункція правого шлуночка (ПШ) за даними ЕхоКГ є підставою для проведення негайної реперфузії без подальшого обстеження. Це рішення може бути підкріплене візуалізацією тромбів у правих камерах серця (Torbicki et al., 2003; Koc et al., 2016; Pierre-Justin, Pierard, 2005; Ferrari et al., 2005).
Додаткові приліжкові процедури візуалізації включають трансезофагеальну ЕхоКГ, за допомогою якої можна побачити тромби у легеневій артерії та її основних гілках, особливо у пацієнтів із дисфункцією ПШ. Проте слід обережно виконувати дане тестування в осіб із гіпоксемією. Також приліжкова компресійна ультрасонографія (КУСГ) здатна виявити проксимальний тромбоз глибоких вен (ТГВ). Окрім того, у хворих із підозрюваною ТЕЛА високого ризику та гемодинамічною нестабільністю слід негайно виконати внутрішньовенну антикоагуляцію нефракціонованим гепарином (НФГ), включно з болюсною ін’єкцію з коригуванням за вагою (І, С).
Хворі на підозрювану ТЕЛА без гемодинамічної нестабільності. При підозрі на наявність ТЕЛА без гемодинамічної нестабільності доцільно використовувати затверджені критерії для діагностики цього стану (І, В) (Roy et al., 2006). В осіб із середнім чи високим ризиком ТЕЛА під час обстеження необхідно якомога швидше розпочати антикоагулянтну терапію (І, С). Діагностична стратегія має базуватися на клінічній ймовірності, оціненій за клінічним судженням або валідованими правилами прогнозування (І, А) (Douma et al., 2012; Le Gal et al., 2006; Ceriani et al., 2010; Wells et al., 2001; Lucassen et al., 2011; Musset et al., 2002). В амбулаторних пацієнтів чи доставлених у відділення невідкладної допомоги з низькою/середньою клінічною вірогідністю, або осіб із малоймовірною ТЕЛА для зменшення потреби у проведенні необов’язкової візуалізації та опромінення варто визначати рівень D-димеру в плазмі крові за допомогою високочутливого аналізу (І, А) (Perrier et al., 2005; Wells et al., 2001; Anderson et al., 2007; Righini et al., 2008; van Belle et al., 2006; Kruip et al., 2002; Perrier et al., 1999). Альтернативою фіксованому межовому значенню D-димеру може бути негативний результат тесту на D-димер із застосуванням граничного показника, скорегованого за віком (вік × 10 мг/л у пацієнтів >50 років), для виключення ТЕЛА у хворих із низьким/середнім ризиком або малоймовірною ТЕЛА (ІІа, В) (Righini et al., 2014). Іншим варіантом межового значення D-димеру, фіксованого або скорегованого щодо віку, є рівень білкового фрагмента, адаптований до клінічної ймовірності, з метою виключення ТЕЛА (ІІа, В) (van der Hulle et al., 2017). Визначення D-димеру не рекомендоване у пацієнтів із високим ризиком, оскільки нормальний результат не виключає наявності ТЕЛА навіть при використанні високочутливого аналізу (ІІІ, А) (Di Nisio et al., 2007; Stein et al., 2004). КТ-ангіографія легеневих артерій є методом другої лінії у більшості медичних центрів в осіб із підвищеним рівнем D-димеру та першої лінії – у пацієнтів із високою клінічною вірогідністю ТЕЛА.
В осіб із низькою або середньою клінічною вірогідністю або малоймовірною ТЕЛА при отриманні нормальних даних КТ-ангіографії легень слід виключити діагноз ТЕЛА без наступного тестування (І, А) (Perrier et al., 2005; Anderson et al., 2007; Righini et al., 2008; van Belle et al., 2006). Якщо у пацієнта із середнім або високим ризиком після процедури виявлено дефект наповнення сегментарної або проксимальної зон, рекомендовано встановити діагноз ТЕЛА без додаткового обстеження (І, В) (Stein et al., 2006). У хворих із високою клінічною вірогідністю або ймовірною ТЕЛА за нормальних результатів КТ-ангіографії легень потрібно розглянути можливість виключення діагнозу ТЕЛА без подальшої перевірки (ІІа, В) (van Belle et al., 2006). Додаткові діагностичні методи візуалізації для підтвердження ТЕЛА можна розглянути у випадках дефектів наповнення судин при виявленні ізольованих субсегментарних тромбів. КТ-венографія як доповнення до КТ-ангіографії легень не рекомендована (ІІІ, В) (Stein et al., 2006; Righini et al., 2008).
Якщо перфузійне сканування легенів показало нормальні результати, діагноз ТЕЛА можна відхилити без додаткових тестувань (І, А) (Wells et al., 1998; Anderson et al., 2007; Perrier et al., 1999). Якщо вентиляційно-перфузійна сцинтиграфія (V/Q-сканування) доступна, це оптимальний варіант для пацієнтів із підвищеним D-димером та протипоказанням до проведення КТ-ангіографії легень. Окрім того, варто віддавати перевагу даному методу задля уникнення зайвого опромінення, особливо у пацієнтів молодшого віку та жінок (Brenner, Hall, 2007). Якщо дані V/Q-сканування показують високий ризик ТЕЛА, діагноз має бути підтверджений без додаткових процедур (ІІа, В). У пацієнтів із низькою клінічною вірогідністю та малоймовірною ТЕЛА доцільно розглянути проведення вентиляційно-перфузійної сцинтиграфії у поєднанні з негативним проксимальним результатом КУСГ для виключення ТЕЛА (ІІа, В) (Wells et al., 1998; Anderson et al., 2007; Perrier et al., 1999). Для діагностики ТЕЛА можна також застосовувати вентиляційно-префузійну однофотонно-емісійну КТ (ІІb, В) (Bajc et al., 2008; Gutte et al., 2009; Collart et al., 2002). Якщо у пацієнта із клінічною підозрою на ТЕЛА внаслідок КУСГ виявлено проксимальний ТГВ, діагноз ВТЕ (та ТЕЛА) має бути підтверджений (І, А) (Righini et al., 2008; Le Gal et al., 2006). Коли ж дані КУСГ демонструють лише дистальний ТГВ, слід розглянути можливість додаткового обстеження для підтвердження діагнозу ТЕЛА (ІІа, В) (Righini et al., 2009). Якщо для цього використовують позитивний проксимальний результат КУСГ, потрібно враховувати оцінку тяжкості ТЕЛА для визначення лікування із контролем ризику (ІІа, С) (Meyer et al., 2014). Магнітно-резонансна ангіографія для виключення діагнозу ТЕЛА не рекомендована (ІІІ, А) (Revel et al., 2012; Stein et al., 2010).
Оцінка ступеня виразності ТЕЛА та ризику ранньої смерті
Стратифікація ризику пацієнтів із гострою ТЕЛА обов’язкова для визначення оптимального терапевтичного підходу. Початкова стратифікація ризику ґрунтується на клінічних симптомах та ознаках гемодинамічної нестабільності, які свідчать про високий ризик ранньої смерті. Серед пацієнтів із ТЕЛА без гемодинамічної нестабільності подальша стратифікація ризику потребує оцінювання двох прогностичних критеріїв, як-от:
- клінічні, візуальні та лабораторні показники тяжкості ТЕЛА, здебільшого пов’язані з дисфункцією ПШ;
- наявність коморбідності та будь-яких інших обтяжувальних станів, які можуть негативно вплинути на ранній прогноз.
Гостра правошлуночкова недостатність являє собою швидко прогресувальний синдром із системним застоєм через порушення наповнення ПШ та/або зменшення відтоку крові з ПШ. Це критичний фактор, що визначає клінічні наслідки при гострій ТЕЛА (Harjola et al., 2016). Тахікардія, низький систолічний артеріальний тиск (АТ), респіраторна недостатність (тахіпное та/або низький рівень сатурації [SaO2]), синкопе – окремо або в поєднанні, пов’язані з несприятливим короткочасним прогнозом при гострій ТЕЛА.
Для стратифікації раннього ризику в пацієнтів використовують ЕхоКГ-параметри. Загалом дані про дисфункцію ЛШ на ЕхоКГ виявлено у ≥25% неселективних хворих на гостру ТЕЛА (Kurnicka et al., 2016). Також із цією метою корисними є результати КТ-ангіографії легеневих артерій. Огляд серця у 4-камерному зрізі за допомогою КТ-ангіографії дозволяє виявити збільшення ПШ як показник його дисфункції.
Серед лабораторних біомаркерів корисними є маркери пошкодження міокарда. Підвищені концентрації тропоніну в плазмі крові при надходженні можуть асоціюватися з гіршим прогнозом у гострій фазі ТЕЛА. Лактат є маркером дисбалансу між поступленням і споживанням тканинами кисню та, як наслідок, тяжкої ТЕЛА з явним або неминучим порушенням гемодинаміки. Підвищений рівень креатиніну в сироватці крові та знижена (розрахункова) швидкість клубочкової фільтрації пов’язані з 30-денною смертністю через будь-які причини при гострій ТЕЛА (Kostrubiec et al., 2019). Вазопресин вивільняється при ендогенному стресі, гіпотонії, низькому рівні СО. Стосовно маркерів дисфункції ПШ, перевантаження ПШ тиском унаслідок гострої ТЕЛА корелює зі збільшенням розтягування міокарда, що призводить до вивільнення натрійуретичного пептиду типу B (BNP) і N-кінцевого (NT)-proBNP. Таким чином, рівень натрійуретичних пептидів у плазмі крові відображає тяжкість дисфункції ПШ та гемодинамічний компроміс у разі гострої ТЕЛА (Henzler et al., 2012).
Прогностична оцінка
Рекомендовано виконувати початкову стратифікацію ризику підозрюваної або підтвердженої ТЕЛА на основі наявності гемодинамічної нестабільності у пацієнтів із високим ризиком ранньої смерті (І, В). За відсутності гемодинамічної нестабільності слід проводити подальшу стратифікацію осіб із гострою ТЕЛА для виявлення груп низького та середнього ризику (І, В) (Meyer et al., 2014; Jimenez et al., 2016; Hobohm et al., 2016; Becattini et al., 2017). Також у хворих без гемодинамічної нестабільності слід дотримуватися правил клінічного прогнозування з огляду на виразність ТЕЛА та супутні патології, переважно за індексами тяжкості PESI або його спрощеної форми sPESI, для оцінки ризику в гострій фазі ТЕЛА (ІІа, В) (Aujesky et al., 2011; Aujesky et al., 2005; Jimenez et al., 2010).
Оцінку ПШ за допомогою методів візуалізації, як-то трансторакальна ЕхоКГ та КТ-ангіографія легеневих артерій, або лабораторних біомаркерів (серцевих тропонінів, натрійуретичних пептидів тощо) слід враховувати навіть за наявності низького показника PESI або негативного – sPESI (ІІа, В) (Barco et al., 2019). У пацієнтів без гемодинамічної нестабільності можна розглянути використання валідованої оцінки, що поєднує клінічні, візуалізувальні та лабораторні прогностичні фактори, пов’язані з ТЕЛА, для наступної стратифікації тяжкості гострого епізоду ТЕЛА (ІІb, С) (Jimenez et al., 2016; Hobohm et al., 2016; Fernandez et al., 2015; Bova et al., 2014; Dellas et al., 2014; Lankeit et al., 2013).
Стратегії лікування осіб із ТЕЛА
Гемодинамічна й респіраторна підтримка пацієнтів
Гіпоксемія є однією з ознак тяжкої ТЕЛА і переважно асоційована з невідповідністю між вентиляцією та перфузією. Використання додаткового кисню показане пацієнтам із ТЕЛА та SaO2 <90%. Необхідно також розглянути подальші методи оксигенації, зокрема подання кисню з високим рівнем потоку та штучну вентиляцію легень у разі, приміром, зупинки серця, з огляду на те, що корекція гіпоксемії неможлива без одночасної реперфузії легенів (Messika et al., 2017; Lacroix et al., 2017). Тимчасове використання механічної кардіопульмональної підтримки, переважно за допомогою екстракомпоральної мембранної оксигенації, може бути корисним для пацієнтів із ТЕЛА високого ризику та порушенням кровообігу або зупинкою серця. Невідкладна допомога у разі зупинки серця передбачає застосування розширеного комплексу реанімаційних заходів. Насамперед доцільно розглянути використання тромболітичної терапії. Після приймання тромболітичного препарату слід проводити серцево-легеневу реанімацію принаймні 60‑90 хв, перш ніж припинити спроби (Truhlar et al., 2015).
Гостра правошлуночкова недостатність, що призводить до низького системного кровотоку, є основною причиною летальних наслідків серед пацієнтів із ТЕЛА високого ризику. Якщо центральний венозний тиск низький, можна застосовувати помірне (<500 мл) рідинне навантаження, що сприятиме підвищенню серцевого індексу в осіб із гострою ТЕЛА (Mercat et al., 2012). Мінімальне рідинне навантаження може бути доцільним у разі поєднання низького АТ та відсутності підвищення тиску наповнення ПШ. Оцінка центрального венозного тиску за допомогою його моніторингу чи ультразвукової візуалізації положення кава-фільтра може допомогти визначити об’ємне навантаження.
Часто необхідно використовувати вазопресори супутньо або під час очікування фармакологічного, хірургічного чи інтервенційного реперфузійного лікування. Вазодилататори знижують тиск у легеневій артерії та легеневий судинний опір, але можуть погіршити гіпотензію та системну гіпоперфузію через недостатню специфічність після системного внутрішньовенного введення щодо легеневої судинної системи.
Антикоагулянтна та реперфузійна терапія
Пацієнтам із середньою чи високою клінічною ймовірністю ТЕЛА під час діагностичного обстеження рекомендована негайна антикоагулянтна терапія (І, С). Якщо антикоагуляцію розпочато парентерально, більшості хворих доцільно призначати низькомолекулярний гепарин (НМГ) або фондапаринукс (а не НФГ) (І, А) (Cossette et al., 2010; Buller et al., 2003, 2004; Robertson, Jones, 2017). При ініціації пероральної антикоагулянтної терапії, за відсутності у пацієнта з ТЕЛА протипоказань для використання нових оральних антикоагулянтів (НОАК), як-от апіксабан, дабігатран, едоксабан або ривароксабан, рекомендовано надавати перевагу цим препаратам перед антагоністами вітаміну К (АВК) (І, А). Дабігатран не слід застосовувати пацієнтам із кліренсом креатиніну (КК) <30 мл/хв. Едоксабан потрібно призначати у дозі 30 мг/добу при КК 15‑50 мл/хв і не рекомендовано у разі КК <15 мл/хв. Ривароксабан та апіксабан варто використовувати з обережністю хворим із КК 15‑29 мл/хв та не рекомендовано при цьому показнику <15 мл/хв. НОАК не слід призначати особам із тяжким порушенням функції нирок, під час вагітності та лактації, а також пацієнтам із синдромом антифосфоліпідних антитіл (ІІІ, С) (Agnelli et al., 2013; Buller et al., 2012; Schulman et al., 2009, 2014; Buller et al., 2013). Якщо ж хворі отримують АВК, доцільне сумісне застосування парентерального антикоагулянту до досягнення міжнародного нормалізованого відношення 2,5 при діапазоні 2,0‑3,0 (І, А) (Brandjes et al., 1992; Hull et al., 1990).
Тромболітична терапія рекомендована пацієнтам із погіршенням гемодинамічних параметрів при застосуванні антикоагулянтів (І, В) (Marti et al., 2015). Реперфузійна терапія, здебільшого системний тромболізис, є методом вибору в осіб із ТЕЛА високого ризику. Альтернативою може бути хірургічна емболектомія або черезшкірне катетерне втручання в осіб із протипоказанням до зазначеної вище процедури (ІІа, С). Хворим на ТЕЛА із низьким чи середнім ризиком не варто призначати рутинне використання системного тромболізису (ІІІ, В) (Meyer et al., 2014). Співвідношення ризику та користі хірургічної емболектомії або катетерних процедур при ТЕЛА низького чи середнього ризику ще не встановлено.
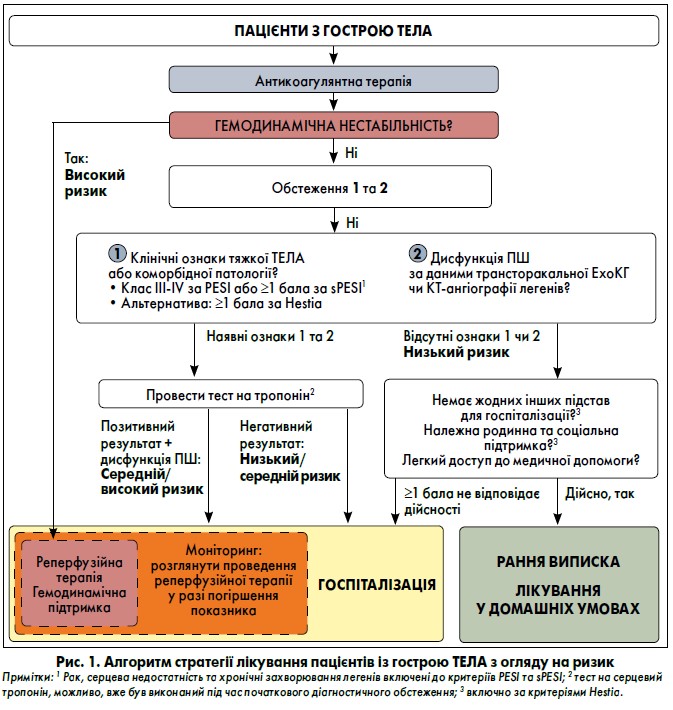
Алгоритм терапевтичного підходу з огляду на ризик гострої ТЕЛА показаний на рисунку 1. Після реперфузійної терапії та стабілізації гемодинаміки пацієнтів із ТЕЛА високого ризику можна переводити з парентерального на пероральне антикоагулянтне лікування. Необхідно дотримуватися вимог щодо вищої початкової дози апіксабану чи ривароксабану (протягом 1 та 3 тижнів після встановлення діагнозу ТЕЛА відповідно) або мінімального загального періоду (п’ять днів) антикоагулянтної терапії гепарином до переходу на дабігатран чи едоксабан.
Необхідно розглянути створення мультидисциплінарної команди та програми з контролю ТЕЛА високого та, в окремих випадках, середнього ризику залежно від медичних ресурсів та клінічного досвіду, наявних у кожній лікарні (ІІа, С).
Рекомендації стосовно лікування осіб із ТЕЛА низького ризику. При прийнятті рішення щодо раннього виписки та продовження лікування у домашніх умовах пацієнтів із ТЕЛА низького ризику необхідно провести ретельне діагностичне обстеження (Aujesky et al., 2011; Agterof et al., 2010; Zondag et al., 2011; Barco et al., 2020). При цьому варто враховувати наступні критерії:
- наявний низький ризик ранньої смерті, пов’язаної з ТЕЛА, або серйозних ускладнень;
- відсутнє тяжке коморбідне захворювання або обтяжливі обставини, що можуть призвести до госпіталізації;
- буде забезпечено належну амбулаторну допомогу й антикоагулянтне лікування з огляду на дотримання пацієнтом режиму терапії та доступні клінічні можливості в межах системи охорони здоров’я.
У домашніх умовах корисним є застосування критеріїв виключення Hestia, що передбачають простий збір даних біля ліжка хворого. Вони включають аспекти тяжкості ТЕЛА, коморбідності та можливості домашнього лікування. Індекси тяжкості PESI та sPESI шляхом фіксування клінічних параметрів щодо виразності ТЕЛА та супутніх станів дозволяють оцінити загальну 30-денну смертність.
Рекомендації щодо лікування пацієнтів із ТЕЛА середнього ризику. У більшості випадків гострої ТЕЛА без гемодинамічного компромісу оптимальним вибором є парентеральна або пероральна антикоагулянтна терапія (без реперфузії). Як показано на рисунку 1, нормотензивні пацієнти, що мають принаймні один показник підвищеного ризику, пов’язаного з ТЕЛА, обтяжливий стан або супутню хворобу, повинні бути госпіталізовані. Цю групу хворих із ознаками дисфункції ПШ на ЕхоКГ або КТ-ангіографії легень, що супроводжуються позитивним тестом на тропонін, слід контролювати протягом перших годин чи днів через ризик ранньої гемодинамічної декомпенсації та порушення кровообігу (Meyer et al., 2014).
Звичайна реперфузійна терапія, зокрема системний тромболіз із повною дозою, не рекомендована, оскільки ризик виникнення небезпечних для життя ускладнень кровотечі є надто високим при зіставленні з очікуваною користю від лікування (Righini et al., 2009). Пацієнтам з ознаками гемодинамічної нестабільності необхідно призначити тромболітичну терапію чи, як альтернативу, – хірургічну емболектомію або черезшкірне катетерне втручання. Можливою доцільною тактикою для осіб із ТЕЛА середнього та високого ризику є продовження антикоагулянтної терапії НМГ протягом перших 2‑3 днів для стабілізування стану перед переведенням на пероральні антикоагулянти.
Рекомендації щодо терапії хворих на ТЕЛА високого ризику. У пацієнтів із ТЕЛА групи високого ризику рекомендовано негайно починати антикоагулянтну терапію НФГ, зокрема болюсну ін’єкцію з коригуванням за вагою (І, С). Також доцільно проводити системну тромболітичну терапію (І, В) (Marti et al., 2015). Хворим на ТЕЛА групи високого ризику слід призначати хірургічну легеневу емболектомію (І, С) або черезшкірне катетерне втручання (ІІа, С), яким тромболіз протипоказаний чи виявився неефективним (Meneveau et al., 2006). Крім того, у даній популяції пацієнтів варто розглянути застосування норадреналіну та/або добутаміну (ІІа, С). Використання екстракомпоральної мембранної оксигенації можливе у поєднанні з хірургічною емболектомією або черезшкірним катетерним втручанням в осіб із ТЕЛА та рефрактерною серцевою недостатністю або зупинкою серця (ІІb, С).
Встановлення кава-фільтрів
Встановлення кава-фільтра у просвіт нижньої порожнистої вени слід розглянути у пацієнтів із гострою ТЕЛА та абсолютними протипоказаннями до антикоагулянтної терапії (IIa, С). Також застосування даних пристроїв може бути доцільним у разі розвитку рецидиву ТЕЛА незважаючи на антикоагулянтне лікування (IIa, С). Рутинне використання кава-фільтрів не рекомендоване (ІІІ, А) (Mismetti et al., 2015; PREPIC Study Group, 2005; Decousus et al., 1998).
Тривале лікування та профілактика рецидивів
Метою тривалої (рутинної) антикоагулянтної терапії є завершення лікування гострого епізоду ТЕЛА та профілактика рецидиву ВТЕ. Частота рецидивів ВТЕ не залежить від клінічного прояву першої події. Однак у хворих на ТЕЛА ВТЕ частіше рецидивує як ТЕЛА, тоді як у тих, хто мав ТГВ, – знов як ТГВ (Murin et al., 2002). Частота летальних наслідків рецидивувальної ВТЕ у пацієнтів із наявним раніше ТЕЛА вдвічі перевищує випадки повторної ВТЕ після ТГВ (Carrier et al., 2010; Douketis et al., 2007).
Продовження антикоагулянтної терапії у пацієнтів із ТЕЛА без онкозахворювань
Для всіх пацієнтів із ТЕЛА рекомендовано проводити антикоагулянтну терапію протягом ≥3 місяців (І, А) (Boutitie et al., 2011). Припинити приймання пероральних антикоагулянтів через три місяці доцільно хворим із першим епізодом ТЕЛА/ВТЕ, яка є вторинною щодо основного тимчасового/зворотного фактора ризику (I, В) (Agnelli et al., 2003; Baglin et al., 2003; Iorio et al., 2010). Особам із рецидивувальною ВТЕ (принаймні одним попереднім епізодом ТЕЛА чи ТГВ), що не пов’язана з основним тимчасовим/зворотним фактором ризику, слід продовжувати антикоагулянтну терапію на невизначений термін, але >3 місяців (I, В) (Schulman et al., 1997). Пацієнтам із синдромом антифосфоліпідних антитіл рекомендоване пероральне застосування антикоагулянтів та АВК протягом невизначеного періоду (I, В) (Schulman et al., 1998). У хворих із першим епізодом ТЕЛА за відсутності встановленого фактора ризику необхідно розглянути довгострокову пероральну антикоагулянтну терапію невизначеної тривалості (IIa, A) (Couturaud et al., 2015; Agnelli et al., 2003; Boutitie et al., 2011; Bauersachs et al., 2010; Weitz et al., 2017; Agnelli et al., 2013).
У пацієнтів із першим епізодом ТЕЛА, що пов’язана зі стійким фактором ризику, відмінним від синдрому антифосфоліпідних антитіл, доречним може виявитися довгострокове використання пероральних антикоагулянтів невизначеної тривалості (IIa, C) (Couturaud et al., 2015; Weitz et al., 2017; Agnelli et al., 2003). Крім того, таке лікування, ймовірно, буде доцільним в осіб із першим епізодом ТЕЛА, що асоційована з незначним тимчасовим або зворотним фактором ризику (IIa, C) (Couturaud et al., 2015; Agnelli et al., 2003; Weitz et al., 2017). Варто зауважити, що у пацієнтів необхідно оцінити ризик кровотечі для виявлення та лікування модифікованих факторів ризику, що може вплинути на прийняття рішення щодо тривалості та режиму/дозування антикоагулянтів.
У разі продовження пероральної антикоагулянтної терапії після епізоду ТЕЛА у пацієнта без онкозахворювання, через шість місяців слід розглянути зниження дози апіксабану (2,5 мг двічі на день) або ривароксабану (10 мг/добу) (ІІа, А) (Weitz et al., 2017; Agnelli et al., 2013). Якщо для тривалого антикоагулянтного лікування обрано дабігатран чи едоксабан, доза має лишатися незмінною, оскільки терапевтичні схеми при зменшеній дозі у спеціальних розширених випробуваннях не вивчали.
У пацієнтів, які відмовляються приймати або не переносять пероральні антикоагулянти, в межах тривалого профілактичного лікування ВТЕ можна розглянути застосування ацетилсаліцилової кислоти (АСК) або сулодексиду (IIb, B) (Brighton et al., 2012; Becattini et al., 2012; Andreozzi et al., 2015). У хворих, які продовжують приймати антикоагулянти, рекомендовано проводити регулярну оцінку толерантності та прихильності до терапії, функції печінки та нирок (особливо у тих, хто отримує НОАК), ризику кровотечі тощо (І, С) (Andreozzi et al., 2018).
Продовження антикоагулянтної терапії після ТЕЛА у пацієнтів з онкопатологією
У хворих на рак після епізоду ТЕЛА слід розглянути застосування НМГ підшкірно з урахуванням ваги протягом перших шести місяців (IIa, A) (Lee et al., 2015; Deitcher et al., 2006; Lee et al., 2003; Meyer et al., 2002). Едоксабан (ІІа, В) та ривароксабан (ІІа, С) потрібно розглянути як альтернативу підшкірному введенню НМГ з корегуванням за вагою в осіб без раку шлунково-кишкового тракту (Raskob et al., 2018; Young et al., 2018). У пацієнтів із ТЕЛА та онкологічним захворюванням доречною може стати довгострокова антикоагулянтна терапія (після перших шести місяців) невизначеної тривалості, або ж поки рак не буде вилікований (IIa, B) (Napolitano et al., 2014). У хворих на онкопатологію рекомендовано розглянути лікування несистемної ТЕЛА, що є зіставним із таким симптомної ТЕЛА, якщо вона уражає сегментарні або більш проксимальні гілки, кілька підсегментарних судин або підтверджено односудинний ТГВ у підсегментнарній частині (ІІа, В) (den Exter et al., 2011; Dentali et al., 2010).
Лікування ТЕЛА у вагітних
Діагностика. У разі підозри на розвиток ТЕЛА під час вагітності або в післяпологовий період рекомендовано виконати діагностичну оцінку за допомогою валідованих методів (I, В) (Righini et al., 2018; van der Pol et al., 2019). Для виключення ТЕЛА у цій популяції хворих слід враховувати показники вимірювання D-димеру та критерії клінічного прогнозування (IIa, B) (Righini et al., 2018; van der Pol et al., 2019). У вагітних пацієнток при підозрюваній ТЕЛА (особливо за наявності симптомів ТГВ) потрібно розглянути можливість проведення КУСГ для уникнення зайвого опромінення (ІІа, В) (Righini et al., 2018). Перфузійну сцинтиграфію або КТ-ангіографію легень (за низької дози радіації) можна застосовувати для виключення підозрюваної ТЕЛА (ІІа, С) (Sheen et al., 2018; van Mens et al., 2017).
Лікування. У більшості жінок із ТЕЛА без гемодинамічної нестабільності на ранніх термінах вагітності рекомендовано призначити терапію НМГ у фіксованій дозі з урахуванням ваги (І, В) (Romualdi et al., 2013; Greer, Nelson-Piercy, 2005). У вагітних із ТЕЛА високого ризику слід розглянути проведення тромболізу або хірургічної емболектомії (IIa, C) (Martillotti et al., 2017).
Введення спинальної або епідуральної голки не рекомендоване, якщо не минуло ≥24 год із моменту використання останньої дози НМГ (III, С). Не варто застосовувати НМГ протягом 4 год після видалення епідурального катетера (III, С). Не слід призначати НОАК під час вагітності або годування грудьми (III, С). Амніотичну емболію доцільно розглянути у вагітної або жінки після пологів із зупинкою серця нез’ясованої природи, стійкою гіпотензією або дихальною недостатністю, особливо якщо вона супроводжується дисемінованою внутрішньосудинною коагуляцією (ІІа, С) (Fitzpatrick et al., 2016; Fong et al., 2015; McDonnell et al., 2015).
Подальше спостереження за хворими після гострої ТЕЛА
У пацієнтів, що перенесли гострий ТЕЛА, рекомендовано проводити регулярну клінічну оцінку через 3‑6 місяців після епізоду (І, В) (Konstantinides et al., 2017; Weitz et al., 2017; Agnelli et al., 2013; Albaghdadi et al., 2018). При цьому лікар має відстежувати симптоми, що можуть свідчити про розвиток рецидивів, кровотеч, злоякісних новоутворень або постійні/нові обмеження фізичної активності, а також прийняти рішення щодо продовження антикоагулянтної терапії. Для забезпечення оптимального переходу від стаціонарної допомоги до піклування в домашніх умовах слід застосовувати інтегровану модель догляду за пацієнтами після ТЕЛА із залученням клініцистів, медичних сестер відповідної кваліфікації та лікарів первинної ланки (I, С).
Симптоматичних пацієнтів із невідповідними дефектами перфузії, що зберігаються при проведенні V/Q-сканування через три місяці після гострої ТЕЛА, потрібно направити до спеціалізованого медичного центру, беручи до уваги результати ЕхоКГ, вимірювання рівня натрійуретичного пептиду та/або кардіопульмонального навантажувального тесту (КНТ) (I, С) (Kim et al., 2013). В осіб зі стійким/новим випадком диспное та/або обмеженням фізичної активності після ТЕЛА, а також у безсимптомних пацієнтів із факторами ризику хронічної тромбоемболічної легеневої гіпертензії (ХТЕЛГ) слід розглянути проведення подальшого діагностичного обстеження (IIa, C) (Pepke-Zaba et al., 2011; Lang et al., 2013; Bonderman et al., 2009; Barco et al., 2018).
Стратегія ведення пацієнтів та діагностичне обстеження щодо довгострокових наслідків ТЕЛА схематично представлені на рисунку 2. Важливо визначити оптимальний підхід щодо подальшого спостереження за хворими з використанням спектра діагностичних процедур, які можуть бути корисними для осіб зі збереженими симптомами та функціональними порушеннями після гострої ТЕЛА. Навіть за відсутності стійких симптомів або обмеження функціональної активності ризик розвитку ХТЕЛГ у таких пацієнтів може бути досить високим. Тож для виявлення та вивчення даної популяції хворих необхідне проведення подальших проспективних когортних досліджень.
Підготувала Олена Коробка
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (71) 2020 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....