Сучасні принципи діагностики та раціональної антибактеріальної терапії інфекційних захворювань органів сечовивідної системи*
На початку року в Києві відбулася професійна колегія лікарів акушерів-гінекологів та урологів «Сучасна мікробіологія у практиці лікаря», яка була організована медичною лабораторією «ДІЛА». У центрі уваги колегії були новітні діагностичні розробки для вирішення клінічних питань, практичні рекомендації щодо їх застосування, можливості сучасної лабораторної діагностики, що турбують не лише практикуючих лікарів, а й усіх пересічних жінок та чоловіків. На колегії було розглянуто актуальні питання лабораторної діагностики та застосування раціональної етіотропної терапії, проблеми антибіотикорезистентності при лікуванні запальних захворювань органів малого таза та сечовивідної системи в акушерській, гінекологічній та урологічній практиці.
Згідно з даними Американського центру контролю і профілактики захворювань (Centers for Disease Control and Prevention, CDC), частота інфекцій, стійких до антибіотиків, з 2013 р. зросла на 30% – з 2 до 2,6 млн випадків, – як і захворювань, що передаються статевим шляхом. Щороку реєструється понад 1 млн уперше виявлених випадків захворювання на гонорею, половина з яких є резистентними до антибіотиків.
.jpg) Із доповіддю «Антибактеріальна терапія інфекцій сечовивідних шляхів в умовах обмеженого застосування фторхінолонів» виступив завідувач кафедри урології Національного медичного університету ім. О. О. Богомольця, завідувач відділу запальних захворювань ДУ «Інститут урології НАМН України», доктор медичних наук, професор Сергій Петрович Пасєчніков.
Із доповіддю «Антибактеріальна терапія інфекцій сечовивідних шляхів в умовах обмеженого застосування фторхінолонів» виступив завідувач кафедри урології Національного медичного університету ім. О. О. Богомольця, завідувач відділу запальних захворювань ДУ «Інститут урології НАМН України», доктор медичних наук, професор Сергій Петрович Пасєчніков.
Проблема інфекцій сечовивідних шляхів (ІСШ) є досить актуальною і широко обговорюваною темою. Її актуальність зумовлена тим, що загальне число хворих на ІСШ у світі протягом багатьох років залишається досить великим та ще й постійно збільшується, поступаючись лише кількості хворих на респіраторні захворювання. Відомо, що на це захворювання найбільш часто страждають жінки починаючи з дитячого віку. Вважається, що в середньому віці кожна друга жінка у світі хоча б раз у житті мала клінічний епізод, викликаний ІСШ, зазвичай циститом. І лише в похилому і старечому віці співвідношення хворих на ІСШ серед чоловіків і жінок дещо вирівнюється.
Хворі на ІСШ умовно розподіляються на дві великі групи – з неускладненим та ускладненим перебігом захворювання. Практичний інтерес становлять неускладнені ІСШ, передусім – найбільш поширений неускладнений цистит. Перший епізод цього захворювання зазвичай доволі легко купірується. Лікують таких хворих не лише (та й не насамперед) урологи, а й лікарі загальної практики (сімейної медицини), акушери-гінекологи, нефрологи та інші наші колеги. Така практика існує у країнах Європи, США та в багатьох інших країнах світу. Цей факт, відповідно, вимагає міждисциплінарного підходу до вирішення проблеми ефективності лікування неускладненого циститу. Адже до 30% жінок, які хоча б один раз перенесли ІСШ, надалі, на жаль, страждають від рецидивуючої інфекції.
Отже, за поширеністю неускладнений гострий цистит посідає перше місце серед усієї урологічної патології. Незважаючи на виражені скарги, це захворювання ніколи не призводить до смерті або незворотних змін в органах сечовидільної системи. Водночас гострий неускладнений цистит за частотою призначень антибіотиків також превалює над усіма урологічними захворюваннями. На жаль, у повсякденній практиці різні фахівці для лікування циститу використовують антибіотики різних груп, дуже часто не дотримуючись принципових положень антибіотикотерапії та доказової медицини. А це є одним із факторів, що спричиняють розвиток стійкості збудників до протимікробних препаратів – глобальної проблеми сучасності.
Як відомо, промислове виробництво першого антибіотика – пеніциліну почалося у 1943 р. За вісім десятиліть, що минули з того часу, кількість антибіотиків та їх виробників збільшилася до грандіозних масштабів. Проте і стійкість збудників до антибіотиків зросла неймовірно, її масштаби сьогодні вже становлять загрозу.
З огляду на важливість і масштабність цієї проблеми, Всесвітня організація охорони здоров’я (ВООЗ) у 2015 р. ухвалила Глобальний план дій щодо боротьби зі стійкістю до антимікробних препаратів. З моменту першої публікації О. Флемінгом інформації про пеніцилін (1929) до прийняття ВООЗ цього документа ще не пройшло й століття. У чому ж причини подібного, фактично зворотного, результату від застосування антибіотикотерапії? Головними з них є швидка відтворюваність бактерій, помножена на кілька мільярдів років неперевершеного досвіду їх виживання в екстремальних умовах.
Тепер звернімося до короткої історії фторхінолонів. Дозволені для клінічного застосування ще у 80-х роках минулого століття, вони посіли особливе, практично домінуюче, місце серед препаратів для лікування інфекцій як відносно малотоксичні, із широким спектром антимікробної активності та пролонгованою дією засоби. Цьому також сприяли оптимальна для лікування урологічних інфекцій фармакокінетика з переважною нирковою екскрецією та висока ефективність при пероральному прийомі, що вкрай важливо для амбулаторної практики.
До 2015 р. включно рекомендаціями Європейської асоціації урології (ЄАУ) такі представники групи фторхінолонів, як офлоксацин, ципрофлоксацин та левофлоксацин, входили до схем терапії гострих і хронічних як неускладнених, так й ускладнених інфекцій нижніх і верхніх сечовивідних шляхів. Якщо додати до цього, що деяким фторхінолонам властива найкраща серед антибіотиків здатність проникати у тканини простати та яєчок, стають зрозумілими причини небаченої популярності цих препаратів серед урологів і лікарів інших спеціальностей у всьому світі протягом кількох десятиліть.
Проте останніми роками саме до фторхінолонів відзначається найактивніше збільшення числа резистентних збудників, включаючи кишкову паличку, клебсієлу та ентеробактер – тобто збудників ІСШ. Внаслідок цього починаючи з 2017 р. фторхінолони, як і амінопеніциліни, експертами ЄАУ вже не рекомендуються для лікування неускладненого циститу із формулюванням: «…через негативний екологічний вплив і селекцію резистентних штамів». Ципрофлоксацин та левофлоксацин залишили тільки для емпіричної терапії неускладненого гострого пієлонефриту та ускладнених ІСШ лише за умов локальної резистентності патогенів <10%.
Разом із тим слід зауважити, що на фармацевтичному ринку України фторхінолони з’явились на 10‑15 років пізніше, ніж у Європі та США, тому у вітчизняній практиці зазначені препарати до цього часу ще зберігають достатню клінічну ефективність і, відповідно, антимікробну активність.
Однак останнім часом дедалі більш застережливою є інформація щодо побічної дії фторхінолонів. Як відомо, деякі з несприятливих ефектів лікарських засобів виявляються не на етапах експериментального або клінічного вивчення, а уже в ході широкого практичного застосування.
Саме це сталося із групою фторхінолонів. Через надшироке постмаркетингове застосування цих антибактеріальних препаратів виявлено цілу низку побічних ефектів. До їх числа входять кардіо- та нефротоксичність, ризик відшарування сітківки, тендиніт, депресія, тяжка діарея тощо. У ґрунтовному огляді літератури H. H. Liu (2010), що охоплює публікації з 1980 по 2009 р., тобто тридцятирічний період, зазначено, що небажані явища, які пов’язані з використанням фторхінолонів, включають шлунково-кишкові розлади, токсичний вплив на центральну нервову систему, аномалії ЕКГ (наприклад, подовження інтервалу QT), порушення метаболізму глюкози, фототоксичність, сухожильні та суглобові розлади.
Доведено, що ципрофлоксацин може спричиняти кристалурію та пов’язаний із цим інтерстиціальний нефрит (Khan M. et al., 2015). Кристали ципрофлоксацину, які утворюються в лужному середовищі, створюваному сечовиною, формують внутрішньоканальцевий преципітат, що призводить до ниркової недостатності.
У дослідженні F. Raguideau et al. (2016) за участю 27,5 тис. дорослих пацієнтів було показано статистично достовірне підвищення ризику відшарування сітківки в 10-денний період із моменту призначення фторхінолонів.
Управлінням із контролю за якістю харчових продуктів і лікарських засобів США (FDA) наведено цілий перелік побічних ефектів із боку скелетно-м’язової та периферичної нервової систем, виникнення яких є можливим при використанні фторхінолонів. Йдеться про тендиніт, розрив сухожилка, відчуття оніміння, поколювання в руках і ногах, м’язову слабкість, біль у м’язах, біль та набряк суглобів. Відповідно до рекомендацій FDA, попередження про ці та інші побічні ефекти внесено до інструкцій з медичного застосування відповідних фторхінолонів.
B. Pasternak, M. Inghammar, H. Svanstrom у 2018 р. опублікували результати ретроспективного когортного дослідження, що підтверджують наявність у фторхінолонів маловідомої побічної дії, яка виявляється у підвищенні ризику розвитку тяжких захворювань аорти. Прийом фторхінолонів був пов’язаний із підвищенням ризику виникнення аневризми/розшарування аорти на 66%. На думку авторів дослідження, подібний ефект зумовлений здатністю препаратів цієї групи підвищувати активність матриксних металопротеїназ, які можуть розщеплювати компоненти позаклітинного матриксу сполучних тканин.
В умовах поширеності туберкульозу в Україні важливим є ще один негативний аспект широкого застосування фторхінолонів. Воно не лише призводить до зростання резистентності мікобактерій, а й перешкоджає своєчасній диференціальній діагностиці, збільшуючи епідеміологічну напруженість. До того ж фторхінолони, діючи системно, викликають колатеральний ефект: змінюється склад нормальної мікрофлори кишечника, яка може перетворюватися зі сприятливої на вірулентну. До речі, це небажане явище завжди потрібно враховувати при виборі антибіотика для лікування ІСШ.
Беручи до уваги всі наведені факти, FDA рекомендує клініцистам при неускладнених урологічних інфекціях не призначати системні фторхінолони тим пацієнтам, у яких існують інші варіанти вибору антибактеріальної терапії, оскільки ризик серйозних побічних ефектів може перевищити потенціальну користь для таких хворих. Також надається рекомендація негайно припинити лікування фторхінолонами, якщо пацієнти повідомляють про серйозні побічні ефекти. Таких хворих для завершення курсу лікування слід переводити на антибіотики іншої групи. Відповідно до методичних рекомендацій Американської урологічної асоціації, застосування фторхінолонів не показане при неускладнених ІСШ, окрім випадків резистентності до інших препаратів.
Станом на 2019 р. для лікування гострого неускладненого циститу ЄАУ також не рекомендує фторхінолони. Як препарати першої лінії слід використовувати фосфоміцину трометамол одноразово, макрокристали нітрофурантоїну протягом 5 днів або півмецилінам протягом 3‑5 днів. Відразу слід зауважити, що два останні із зазначених препаратів в Україні не зареєстровані. Разове ж призначення фосфоміцину трометамолу ще досить часто невиправдано ігнорується лікарями як таке, що, на їхню думку, не забезпечує стійкого ефекту.
Отже, як правильно лікувати ІСШ в сучасних умовах? Які препарати доцільно призначати, а які й чому не варто? З огляду на вищезгадані обставини вітчизняні лікарі у широкій амбулаторній та клінічній практиці мають шукати альтернативу фторхінолонам. Такою альтернативою сьогодні насамперед можна вважати цефалоспорини 3-го покоління. Відомо, що вони застосовуються переважно для парентерального лікування ІСШ у стаціонарах. Проте натепер в Україні зареєстровано й пероральну форму антибактеріальних препаратів цього класу, зокрема цефадроксил та цефіксим, які мають високу ефективність у лікуванні ІСШ, у тому числі неускладненого гострого циститу.
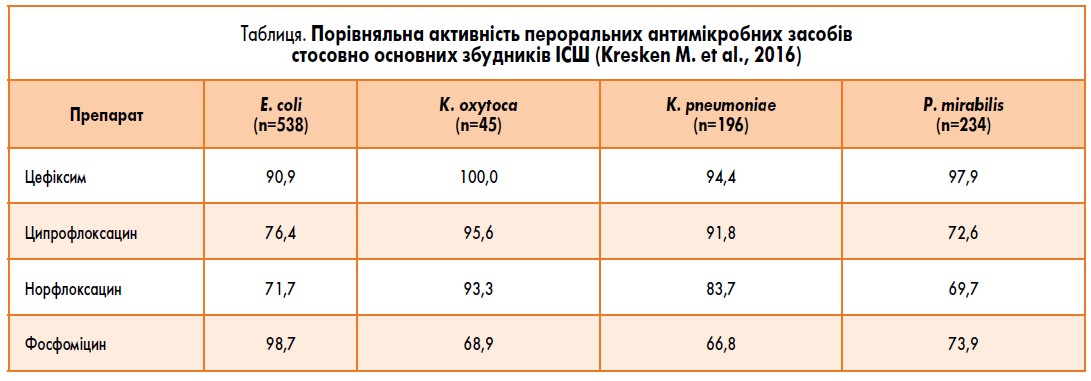
У таблиці наведено порівняльні дані щодо активності найбільш уживаних пероральних антибіотиків проти основних уропатогенів. Чутливість чотирьох основних збудників циститу (Escherichia coli, Klebsiella oxytoca, Klebsiella pneumoniae, Proteus mirabilis) до цефіксиму, наприклад, становить 91‑100%.
Зазначені таблетовані цефалоспорини 3-го покоління мають високу активність щодо позалікарняних штамів кишкової палички та низький потенціал селекції резистентних штамів. При їх застосуванні створюються високі концентрації у сечі та нирковій паренхімі, що робить можливим їх використання при інфекції як нижніх, так і верхніх сечовивідних шляхів. Беручи до уваги той факт, що фосфоміцину трометамол не накопичується в нирковій паренхімі, саме пероральні цефалоспорини 3-го покоління можна вважати адекватною альтернативою фторхінолонам для емпіричної амбулаторної антибактеріальної терапії неускладнених ІСШ – гострого пієлонефриту та гострого циститу.
Серйозну проблему в урологічній практиці становить рецидивуюча інфекція. Приблизно у 30% жінок виникають епізоди циститу понад 2‑3 рази протягом року. Це може бути як результатом реінфекції, так і бактеріальної персистенції, якщо інфекція залишається в сечовивідних шляхах після лікування. На сьогодні в якості неантибактеріальних профілактичних заходів лікарі традиційно призначають імунопрофілактику пероральним препаратом ОМ‑89, замісну гормональну терапію, пробіотики, рослинні препарати, зокрема на основі журавлини, D-манозу та внутрішньоміхурові інстиляції. Разом із тим ЄАУ на даному етапі ефективними щодо запобігання рецидивам ІСШ у жінок постменопаузального віку визнає лише імуноактивну профілактику препаратом ОМ‑89 та вагінальну естрогенотерапію (місцеву, але не пероральну). Не рекомендовано застосовувати для зниження частоти рецидивів пробіотики, журавлину, D-манозу і внутрішньоміхурові інстиляції з огляду на суперечливі дані або недостатню кількість досліджень.
Лікування неускладнених ІСШ може відбуватись амбулаторно під наглядом уролога, нефролога, сімейного лікаря або терапевта. За потреби стаціонарного лікування його можна проводити в умовах урологічного, нефрологічного або терапевтичного відділення.
Щоб допомогти практикуючим лікарям різного фаху визначити межі своєї компетенції в лікуванні хворих на ІСШ, доцільно нагадати наступне. Неускладнені ІСШ – це епізоди гострого циститу або пієлонефриту в невагітних жінок репродуктивного віку, які не мають анатомічних і функціональних порушень та супутніх захворювань сечовивідних шляхів. Усі інші ІСШ фактично відносяться до ускладнених, адже пов’язані зі станами, що підвищують ризик інфікування або неуспішного лікування.
До факторів, що ускладнюють перебіг ІСШ, відносять:
- вагітність;
- літній вік;
- чоловічу стать;
- тривалість симптомів до 7 днів;
- недавній курс протимікробних препаратів;
- госпітальні інфекції;
- цукровий діабет;
- знижений імунітет;
- патологію органів сечовидільної системи;
- катетеризацію сечового міхура;
- недавні урологічні втручання.
Лікарям будь-якої спеціальності дуже важливо усвідомлювати, що ускладнені ІСШ, особливо обструктивний пієлонефрит та гнійні його форми, потребують обов’язкової госпіталізації до урологічного стаціонару через потенційну потребу у дренуванні порожнистої системи нирки або гнійних вогнищ, а також через підвищений ризик розвитку уросепсису. Окрім усунення факторів, що ускладнюють ІСШ, для лікування таких хворих показані внутрішньовенні інфузії цефалоспорину 3-го покоління або комбіноване застосування аміноглікозиду з амінопеніциліном чи цефалоспорином 2-го покоління. Фторхінолони можуть призначатися тільки в регіонах із резистентністю збудників до них <10% – виключно в разі алергії на β-лактами та аміноглікозиди, за винятком хворих урологічних стаціонарів та осіб, які проходили лікування фторхінолонами протягом останніх 6 місяців. Усі згадані обставини позбавляють можливості лікування пацієнтів із ускладненими ІСШ у будь-яких інших умовах, окрім урологічного стаціонару. У компетенції лікарів неурологічного профілю залишається тільки лікування хворих на неускладнений цистит та пієлонефрит.
На завершення констатуємо, що у реаліях нашої країни забезпечення раціональної антибіотикотерапії ускладнюється через цілу низку факторів. Зокрема, в Україні до цього часу не проводиться системний моніторинг антибіотикорезистентності ані позалікарняної мікрофлори, ані госпітальної інфекції. Що це означає? Це означає, що наші лікарі не можуть виконати рекомендації ЄАУ відносно призначення фторхінолонів «тільки в регіонах із резистентністю збудників <10%». Адже інформація про регіональну чутливість мікрофлори в нашій країні відсутня. Крім того, деякі із препаратів, що рекомендовані експертами ЄАУ (наприклад, макрокристали нітрофурантоїну та півмецилінам), взагалі відсутні на українському фармацевтичному ринку.
То що ж необхідно для покращення ситуації? Налагодження ретельного контролю за використанням антибактеріальних препаратів, а саме: чітке дотримання показань до їх призначення та термінів лікування, уникнення недоцільного емпіричного застосування, забезпечення моніторингу випадків резистентності збудників, за можливості – застосування альтернативних антибактеріальних та інших лікарських засобів, зокрема імуно- та фітотерапевтичних.
Усе це потребує безперервного спостереження за процесом, постійного прогнозування стану резистентності мікрофлори та запобігання критичним ситуаціям, а також підвищення рівня підготовки лікарів з усіх зазначених аспектів діяльності. Це нагальні завдання, які ще тільки чекають належного вирішення. Але є й хороша новина – Україна тепер також у тренді протидії антибіотикорезистентності: у березні минулого року Кабінет Міністрів України ухвалив Національний план дій щодо боротьби зі стійкістю до протимікробних препаратів.
* Тематичний номер «Урологія. Нефрологія. Андрологія» № 1, 2020 р.
Підготувала Марія Грицуля
Тематичний номер «Акушерство, Гінекологія, Репродуктологія» № 3 (39) 2020 р.
СТАТТІ ЗА ТЕМОЮ Інфекційні захворювання
Світ не бачив нового класу диво-ліків уже 40 років...
Рекомендації щодо антибіотиків першого і другого вибору для емпіричної терапії негоспітальної пневмонії, середнього отиту та загострення ХОЗЛ...
SARS-CoV‑2 виявився непересічним респіраторним вірусом і спричинив пандемію, яка тривала із 2019 по 2023 рік. Проте вплив цієї інфекції на імунну систему (ІС) людини не обмежується активацією фізіологічних механізмів противірусного захисту. Вірус здатний надмірно активувати ІС, зумовлюючи загрозливе ускладнення – т. зв. цитокіновий шторм, спричинити тяжку вірусну пневмонію, розвиток автоімунного синдрому, впливати на систему коагуляції тощо....
Риносинусит (РС) є одним із найчастіших захворювань у первинній медичній практиці. Трьома найбільш чутливими й специфічними симптомами гострого РС є виділення з носа, закладеність носа, лицевий і головний біль. Неконтрольований гострий біль значно погіршує якість життя пацієнтів із РС: спричиняє психоемоційні розлади, знижує працездатність і соціальну активність, сприяє хронізації больового синдрому і збільшує вартість лікування. Отже, полегшення болю при РС є найпершим завданням лікаря....