Сучасні стратегії лікування кашлю в терапевтичній практиці
 Кашель є найпоширенішим симптомом бронхолегеневих захворювань і найчастішою причиною звернення пацієнтів по медичну допомогу на амбулаторному етапі. Зазвичай від 10 до 38% звернень до пульмонолога зумовлені наявністю хронічного кашлю. Кашель являє собою мультидисциплінарну проблему, пов’язану не лише із захворюваннями дихальних шляхів. На сьогодні відомо >50 причин кашлю, тому розібратися, що саме спричинило його розвиток буває досить складно. Лікування кашлю є актуальною загальнотерапевтичною проблемою, що потребує раціонального та диференційованого підходу.
Кашель є найпоширенішим симптомом бронхолегеневих захворювань і найчастішою причиною звернення пацієнтів по медичну допомогу на амбулаторному етапі. Зазвичай від 10 до 38% звернень до пульмонолога зумовлені наявністю хронічного кашлю. Кашель являє собою мультидисциплінарну проблему, пов’язану не лише із захворюваннями дихальних шляхів. На сьогодні відомо >50 причин кашлю, тому розібратися, що саме спричинило його розвиток буває досить складно. Лікування кашлю є актуальною загальнотерапевтичною проблемою, що потребує раціонального та диференційованого підходу.
Кашель – це складна багатокомпонентна рефлекторна захисно-пристосувальна реакція організму, спрямована на виведення з дихальних шляхів сторонніх тіл та/або патологічного трахеобронхіального секрету, що забезпечує збереження ефективного проведення повітряного струменя дихальним трактом.
Нейрорефлекторна дуга кашльового рефлексу складається з периферичних кашльових рецепторів, аферентних волокон блукаючого та верхнього гортанного нервів, «кашльового» центру, який локалізується в довгастому мозку, еферентних пучків блукаючого і діафрагмального нервів, що проводять імпульси до мускулатури грудної клітки, діафрагми, а також черевного пресу.
Основними подразниками кашльових рецепторів є:
- коливання температури та вологості повітря;
- аерополютанти;
- сигаретний дим;
- мокротиння;
- назальний слиз;
- алергени;
- запалення слизових дихальних шляхів;
- механічна дія (стороннє тіло, тиск пухлини);
- гіпервентиляція;
- гастроезофагеальний рефлюкс;
- ліки (іАПФ, β-блокатори).
В разі тривалого подразнення кашльових рецепторів може розвиватися хронічний виснажливий кашель, що втрачає свою захисну функцію та здатен зумовлювати розвиток низки небезпечних ускладнень. Зокрема, можуть спостерігатися синкопальні стани, спонтанний пневмоторакс, кровохаркання, розриви стінок трахеї та бронхів, крововиливи (в мозок, склеру, сітківку), аритмії, грижі (передньої черевної стінки, пахові, діафрагмальні).
Розглянемо детальніше найпоширеніші причини тривалого кашлю та підходи до його лікування.
Поствірусний кашель
Безперечно, однією з найчастіших причин кашлю є гострі респіраторні інфекції (ГРІ), які в більшості випадків спричиняються вірусами. В перші дні захворювання зазвичай спостерігається сухий непродуктивний кашель, який впродовж 2-5 днів переходить у вологий.
Нерідко на тлі розрішення загальних і місцевих симптомів ГРІ кашель зберігається триваліший час, втрачаючи свою захисну функцію. Такий кашель називають поствірусним (ПК). Частота розвитку ПК після перенесеної ГРІ коливається в межах 11-25%, а його тривалість за відсутності лікування може сягати 8 тиж.
Патогенетичною основою ПК є поєднання тривалого запалення дихальних шляхів і зниження порогу чутливості кашльових рецепторів, які реагують на незначну іритацію холодним повітрям, бронхіальним секретом, пилом тощо. Лікування ПК можна розпочинати з іпратропіуму броміду (докази помірної сили). В разі тяжкого нападоподібного кашлю можна призначати 30-40 мг/добу преднізолону впродовж нетривалого періоду, поки виключатимуть інші причини кашлю (слабкі докази). При неефективності такого лікування експерти рекомендують призначення протикашльових препаратів центральної дії (Irwin R. S. et al. 2006).
Оскільки гострі вірусні інфекції спричиняють віруси, призначення антибактеріальних препаратів з метою лікування кашлю та інших симптомів захворювання є помилкою. Показання до призначення антибактеріальних засобів – документована бактеріальна чи передбачувана бактеріальна інфекція. На користь бактеріальної інфекції свідчать підвищення рівня прокальцитоніну >0,5 нг/л (високоспецифічний маркер) або С-реактивного протеїну >24 мг/л (високоспецифічний маркер). Окрім того, бактеріальну інфекцію слід запідозрити при наявності таких лабораторних ознак, як лейкоцитоз, зсув уліво чи нейтрофілія, лімфопенія.
В пацієнтів, котрі не курять та не мають патологічних змін на рентгенограмі органів грудної клітки, більшість випадків сухого хронічного кашлю зумовлені 3 основними причинами, об’єднаними терміном «патогенетична тріада хронічного кашлю», до якого належать кашльовий синдром верхніх дихальних шляхів (більше відомий як синдром постназального затікання (СПЗ); від 41 до 58% випадків), кашльовий варіант бронхіальної астми (БА) (від 24 до 59% випадків), гастроезофагеальна рефлюксна хвороба (ГЕРХ) (від 21 до 41% випадків).
Кашльовий синдром верхніх дихальних шляхів
Досить часто хронічний кашель зумовлений запальним процесом у порожнині носа, навколоносових пазухах, носоглотці. Причина кашлю в такому випадку – носові виділення, які стікають задньою стінкою глотки та подразнюють кашльові рецептори. Кашльовий синдром верхніх дихальних шляхів може розвиватися при таких захворюваннях, як алергічний (персистуючий), вазомоторний, медикаментозний, постінфекційний риніти, бактеріальний синусит. Зазвичай такі пацієнти скаржаться на відчуття накопичення слизу в задніх відділах порожнини носа, стікання її задньою стінкою глотки, частого відходження слизових згустків. Симптоми посилюються зранку (хворі просинаються з дискомфортом у глотці), а також за тривалого перебування в положенні лежачи на спині. При огляді глотки відсутні ознаки запалення, але можна побачити слизові тяжі, які тягнуться з носоглотки за м’яким піднебінням.
Лікування кашлю в таких випадках має включати терапію основного захворювання (санація носоглотки, деконгестанти, назальні кортикостероїди, антигістамінні засоби) та призначення протикашльових засобів.
Кашльовий варіант БА
Діагностувати БА досить просто, якщо кашель супроводжується задишкою, свистячим диханням, відчуттям здавлення грудної клітки, що мають нападоподібний характер. Якщо епізоди кашлю – єдиний прояв захворювань, то запідозрити БА дозволяють варіабельність симптомів протягом доби, напади нічного кашлю, залежність кашлю від холодових або хімічних подразників, контакту з алергенами. Втім, діагностика кашльового варіанту БА може зумовлювати певні труднощі, оскільки дані фізичного огляду та функціональних легеневих тестів можуть бути в межах норми. Золотим стандартом діагностики кашльового варіанту БА є виявлення бронхіальної гіперреактивності шляхом проведення інгаляційного провокаційного тесту з метахоліном або гістаміном (не рекомендується проводити за відсутності умов для надання екстреної допомоги у випадку виникнення нападу задухи). Остаточно підтвердити діагноз дозволяє лише позитивний результат протиастматичної терапії.
Проведення 2-тижневого курсу інгаляційними кортикостероїдами в середніх дозах (еквівалент 400-800 мкг беклометазону) дозволяє мінімізувати кашель або повністю позбутися його. У випадку резистентного до лікування кашлю може знадобитися тривале призначення інгаляційних кортикостероїдів і бронхолітиків. Хороший ефект чинять антагоністи лейкотрієнових рецепторів, які знижують чутливість кашльового рефлексу в хворих з кашльовою астмою.
Кашель при ГЕРХ
Кашель при ГЕРХ зумовлений мікроаспірацією шлункового вмісту та/або реалізацією вагусних рефлекторних механізмів. Зазвичай це сухий кашель, що з’являється через 10-20 хв після прийому їжі (особливо гострої чи кислої) та посилюється в горизонтальному положенні.
В частки пацієнтів спостерігається виражена клінічна картина основного захворювання (печія, біль у стравоході), проте у 50-75% хворих з ГЕРХ кашель не супроводжується диспепсичними розладами чи іншими симптомами, що утруднює діагностичний пошук. Лікування муколітиками, протикашльовими препаратами, бронхолітиками не знижує інтенсивності кашлю.
Об’єктивна діагностика ГЕРХ здійснюється шляхом проведення 24-годинної стравохідної рН-метрії. Черговість і повторюваність епізодів рефлюксу та кашлю свідчить про зв’язок ГЕРХ з появою кашлю. Проведення пробного антирефлюксного лікування з використанням інгібіторів протонної помпи впродовж 2-3 міс спричиняє розрішення кашлю.
Кашель при застосуванні лікарських засобів
Кашель може з’являтися внаслідок прийому інгібіторів ангіотензинперетворювального ферменту‑2 (ІАПФ), рідше – β-блокаторів або аміодарону. Поширеність кашлю при застосуванні ІАПФ становить 5-20%, причому в жінок зустрічається частіше, ніж у чоловіків. Механізм виникнення кашлю при прийомі ІАПФ пов’язують з порушенням метаболізму брадикініну, підвищенням бронхіальної гіперреактивності, збільшенням концентрації місцевих медіаторів запалення.
Кашель може з’явитися в будь-який час – як через декілька годин, так і через декілька тижнів або місяців після початку прийому препарату. Єдиним ефективним методом лікування кашлю, асоційованого із прийомом ІАПФ, є припинення прийому препарату. Зазвичай кашель зникає впродовж тижня після продовження терапії, рідше – в триваліший термін. Тактика ведення хворих із тривалим кашлем невідомої етіології, котрі приймають ІАПФ, пов’язана зі скасуванням прийому препарату.
Хронічний кашель за відсутності вищезазначених супутніх захворювань – показання до проведення фібробронхоскопії, яка дає змогу виявити трахеобронхіальну дискінезію, стороннє тіло в дихальних шляхах, бронхогенну карциному й іншу патологію, а також дослідити матеріали біопсії та бронхоальвеолярного лаважу в різних діагностичних випадках.
Психогенний кашель
Після виключення органічних причин кашлю слід розглянути варіанти психогенного кашлю, що зустрічається переважно в дітей та зазвичай з’являється як реакція на стресові ситуації або їх очікування. В таких пацієнтів кашель припиняється в нічний час, а також при виконанні цікавих завдань. У разі виключення інших причин і підозри на психогенний генез кашлю рекомендується консультація психіатра, на підставі рекомендацій котрого підбирається адекватна терапія (наприклад, седативні засоби). За необхідності призначають нетривалий курс протикашльових препаратів.
Терапевтична тактика в пацієнтів із хронічним кашлем має включати такі кроки:
- виключення впливу респіраторних іритантів (активного та пасивного куріння, промислових полютантів тощо);
- патогенетичне та симптоматичне лікування основного захворювання, усунення причин, що зумовлюють кашель;
- застосування протикашльових засобів.
У зв’язку з тим, що кашель – важливий механізм евакуації мокротиння з дихальних шляхів, підхід до призначення протикашльових засобів має бути зваженим. Не слід пригнічувати кашель у пацієнтів із бронхіальною гіперсекрецією. Зазвичай протикашльові засоби показані у випадках, коли кашель порушує сон і виснажує пацієнта в денний час.
Протикашльові засоби поділяються на препарати центральної та периферичної дії. Препарати периферичної дії зменшують подразнення рецепторів, розташованих у дихальних шляхах, зменшуючи потік імпульсів до кашльового центру. Препарати центральної дії пригнічують сам кашльовий центр. Таким чином, препарати зазначених груп лише пригнічують кашльовий рефлекс, не впливаючи на сам запальний процес у дихальних шляхах, який у більшості випадків є основною причиною виникнення кашлю. Препарат Ренгалін, котрий має додаткові протизапальні властивості, вигідно відрізняється від інших протикашльових засобів.
Ренгалін створений на основі афінно-очищених високорозбавлених розчинів антитіл (АТ) до медіаторів запалення – брадикініну й гістаміну та АТ до морфіну. Ренгалін реалізує свої ефекти за рахунок модифікації лігандрецепторної взаємодії ендогенних регуляторів з відповідними рецепторами.
Так, АТ до брадикініну впливають на запальний процес і формування кашльового рефлексу шляхом пригнічення синтезу й вивільнення брадикініну, а також розслаблення посмугованої мускулатури органів дихання; водночас вони сприяють зниженню больових відчуттів. АТ до гістаміну впливають на гістамін-залежну активацію гістамінових рецепторів 1 типу, зменшують судинну проникність, гіперпродукцію слизу та знижують набряк слизової оболонки. Завдяки зазначеним ефектам Ренгалін забезпечує комплексну протизапальну, протикашльову, протинабрякову та бронхолітичну дію, а також ефективне лікування сухого, вологого й залишкового кашлю на всіх стадіях інфекційно-запального процесу. Ренгалін не є муколітиком і відхаркувальним засобом, але він здатний полегшувати відходження мокротиння, що зумовлено його протинабряковими та спазмолітичними властивостями.
Ренгалін показаний при гострих і хронічних захворюваннях дихальних шляхів, що супроводжуються кашлем і бронхоспазмом; при продуктивному та непродуктивному кашлі при ГРВІ, гострому фарингіті, ларинготрахеїті, гострому обструктивному ларингіті, хронічному бронхіті й інших інфекційно-запальних і алергічних захворюваннях верхніх та нижніх дихальних шляхів.
На сьогодні клінічна ефективність та безпека Ренгаліну продемонстровані результатами численних рандомізованих клінічних досліджень, що довели його зіставну (а в більшості випадків навіть кращу) ефективність порівняно з амброксолом, фенспіридом, комбінацією бутамірату та гвайфенезину, бутамірату цитратом, а також кодеїнвмісними препаратами.
Показовим є дослідження (Игнатова Г. Л., 2016), у якому порівнювали клінічну ефективність Ренгаліну та фенспіриду в лікуванні хворих на гострий бронхіт (ГБ). До випробування залучили дорослих пацієнтів, у яких ГБ з’явився на тлі ГРІ протягом 1-го тижня з моменту захворювання. Ренгалін призначали за такою схемою: в перші 3 доби – по 2 таблетки 3 р/добу, на 4-7-му добу – по 1 таблетці 3 р/добу (всього на курс – 30 таблеток). Фенспірид призначали в перші 3 доби по 1 таблетці (80 мг) 3 р/добу, на 4-7-му добу – по 1 таблетці 2 р/добу (всього на курс – 17 таблеток). План спостереження передбачав проведення 3 візитів. Візит 1 (до початку лікування) здійснювався не пізніше 7 діб від моменту виникнення перших симптомів ГРІ. Наступні 2-й та 3-й візити, що проводилися на 4-й та 7-й день лікування, включали клінічний огляд, фіксацію результатів за даними індивідуальної реєстраційної картки, а також оцінку безпеки проведеної терапії. Додатково на візиті 3 проводилися оцінка прихильності до лікування на основі показників опитувальника CGI-ЕI («Загальне клінічне враження про ефективність і покращення»). Як первинний критерій оцінки була обрана частка пацієнтів, у яких клінічні прояви бронхіту припинялися на момент завершення спостереження.
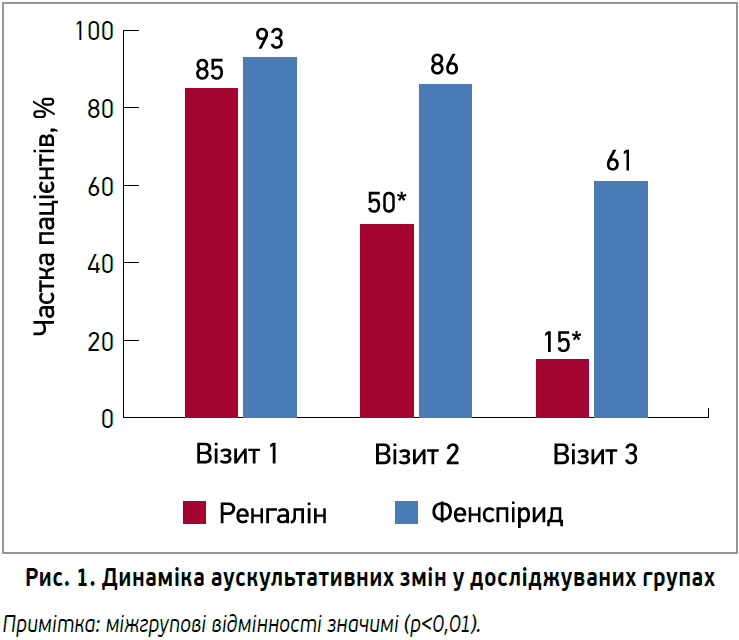
Ренгалін добре себе зарекомендував, продемонструвавши стійкішу тенденцію до повного регресу клінічної симптоматики практично в половини пацієнтів, незважаючи на деякі вихідні відмінності на користь групи порівняння (статистично значимі). Так, на візиті 3 частка пацієнтів, які видужали, в групі Ренгаліну становила 42%, тоді як у групі фенспіриду таких хворих було всього 28,6% (p=0,4). Оцінка динаміки аускультативних даних (наявність жорсткого дихання, хрипів) на тлі початково зіставних результатів фізикального обстеження пацієнтів в обох групах продемонструвала значиму перевагу Ренгаліну (рис. 1). З візиту 2 патологічна аускультативна картина, характерна для ГБ, залишилася лише в 50% пацієнтів групи Ренгаліну, тоді як у групі фенспіриду таких хворих було 86%. До візиту 3 динаміка стала ще переконливішою – жорстке дихання зберігалося лише в 15% пацієнтів групи Ренгаліну проти 61% хворих групи фенспіриду (р<0,01).
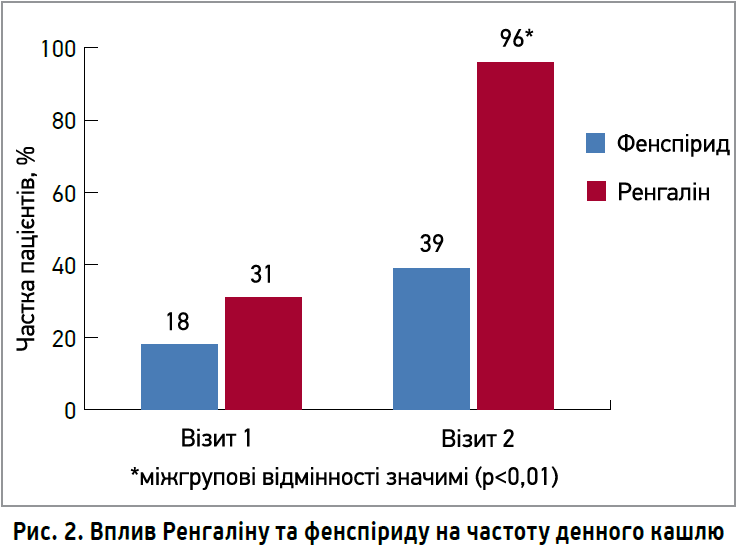
Отримані дані свідчать про наявність у Ренгаліну комбінованої дії, що не залежить від фази ГБ і дає змогу застосовувати цей препарат як при сухому, так і при вологому кашлі. Ренгалін сприяв нормалізації аускультативної картини ГБ у 50% пацієнтів уже на 4-й день; у 85% – на 7-й день лікування. При оцінці тривалості та вираженості денного кашлю на тлі прийому Ренгаліну та фенспіриду було виявлено статистично значимі відмінності між групами (p<0,001). Загалом частка пацієнтів, які видужали повністю чи мали незначні залишкові прояви кашлю (≤2 балів), становила 96% у групі Ренгаліну проти 39% хворих у групі фенспіриду (рис. 2).
Клінічна ефективність Ренгаліну щодо припинення денного кашлю через 7 діб терапії виявилася приблизно в 2,5 разу вищою порівняно із фенспіридом.
Водночас було виявлено чітку тенденцію до швидшого зменшення вираженості нічного кашлю під дією Ренгаліну. До візиту 2 частка пацієнтів без нічного кашлю в групі Ренгаліну збільшилася з 0 до 15%, тоді як у групі фенспіриду цей показник спочатку становив 7%, а до візиту 2 досяг 14%. До візиту 3 у всіх пацієнтів 1-ї групи відзначалося зникнення нічного кашлю (оцінка – 0-1 бал), понад 40% хворих, які отримували Ренгалін, повністю позбулися нічного кашлю (0 балів), а 23% пацієнтів – будь-яких проявів кашлю (як денного, так і нічного). В групі фенспіриду до візиту 3 переважали пацієнти, в яких нічний кашель оцінювався в 2 бали (одноразове пробудження щоночі); їхня частка становила 54%. У 25% хворих не було нічного кашлю, 21% пацієнтів кашляли при засинанні (1 бал), а лише 1 пацієнт (4%) повністю перестав кашляти вдень і вночі. Середня тривалість нічного кашлю в групі Ренгаліну становила 1,72±0,13 дня, тоді як у групі фенспіриду – 1,91±0,14 дня (p>0,2). Водночас при зіставній тривалості нічного кашлю Ренгалін відрізнявся істотнішим впливом на його вираженість, що має важливе значення для забезпечення повноцінного сну. Отже, Ренгалін за впливом на тривалість нічного кашлю зіставний із фенспіридом, але водночас забезпечує меншу вираженість кашлю.
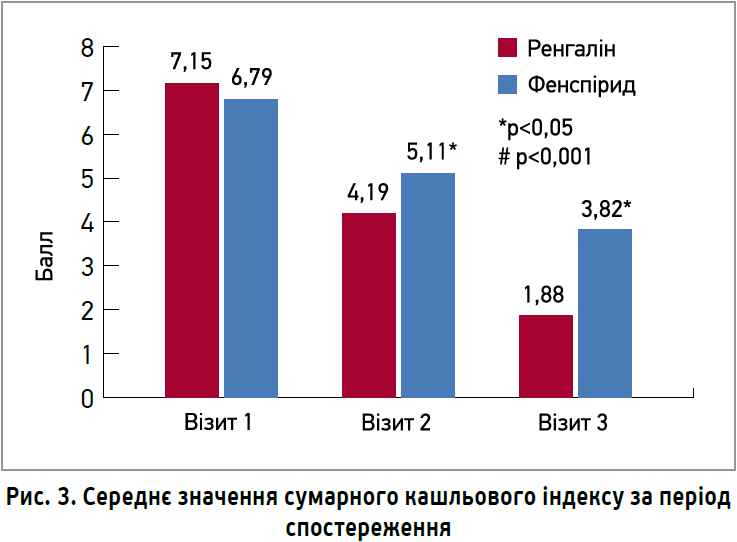
Середні значення показників денного та нічного кашлю на візиті 1 свідчили про більшу вираженість патологічного процесу в групі Ренгаліну. Втім, уже до візиту 2 виявлено статистично значиме переважання терапевтичних ефектів Ренгаліну, а до візиту 3 середні значення сумарного кашльового індексу в порівнюваних групах відрізнялися більше ніж удвічі (рис. 3).
Таким чином, Ренгалін знижує запалення та зменшує набряк слизової дихальних шляхів, вираженість нічного кашлю, інтенсивність і тривалість денного кашлю. Отримані дані свідчать про наявність у Ренгаліну значного терапевтичного потенціалу при ГБ; його застосування сприяє зменшенню вираженості кашлю на будь-якому етапі інфекційно-запального процесу при ГБ завдяки впливу на рефлекторні та запальні механізми кашлю. Отримані дані дають змогу рекомендувати Ренгалін для широкого використання в клінічній практиці при лікуванні кашлю як симптому ГБ.
Ренгалін чинить протизапальну, бронхолітичну, протикашльову дію, впливає на центральні і периферичні ланки кашльового рефлексу.
В іншому дослідженні порівнювали ефективність Ренгаліну в терапії інфекційного та постінфекційного кашлю при ГРІ в дорослих (Вершинина М. В., 2016). Пацієнтів з непродуктивним / малопродуктивним кашлем розподілили на прийом препарату Ренгалін і комбінації бутамірат + гвайфенезин. Здебільшого учасники розпочинали лікування кашлю на 7-8-й день від початку ГРІ.
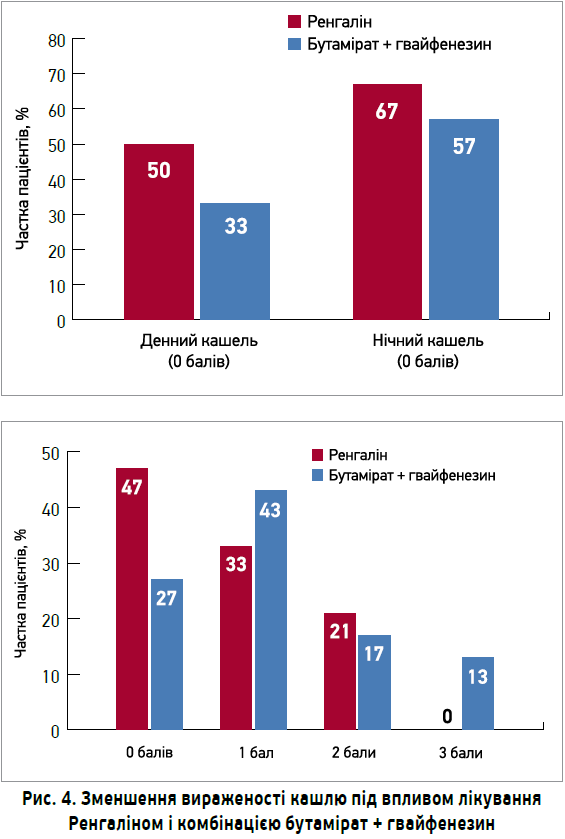
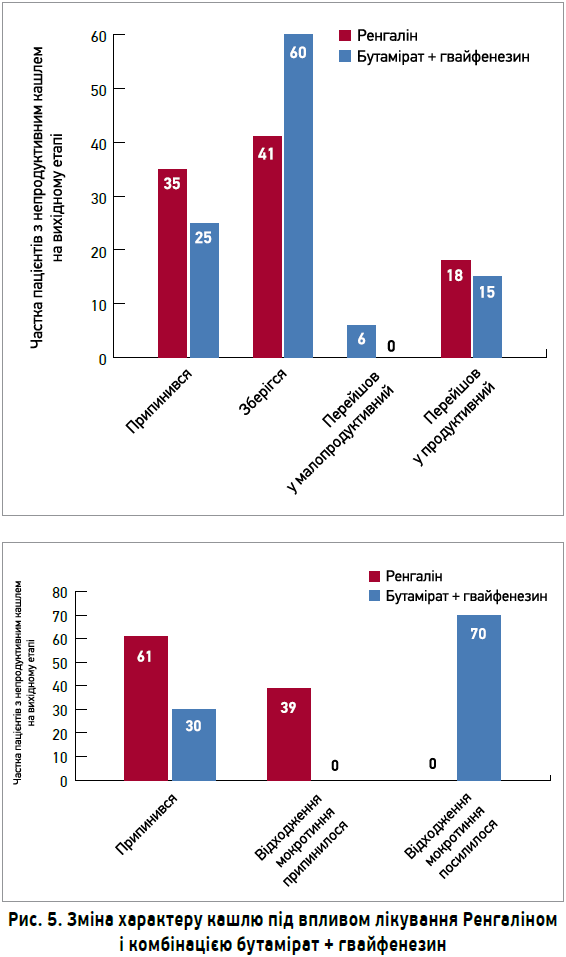
В групі Ренгаліну помітна динаміка зменшення кашлю реєструвалася вже на візиті 2; натомість у пацієнтів, які отримували комбінацію бутамірат + гвайфенезин, аналогічні показники були досягнуті тільки до візиту 3. Зменшення вираженості нічного кашлю та тривалості нападів загалом на візиті 3 в хворих, які отримували Ренгалін, виявилося на 30-50% значимішим (p>0,05) (рис. 4). 80% пацієнтів з постінфекційним кашлем, які приймали Ренгалін протягом 7 днів, не потребували подальшого лікування.
У групі Ренгаліну не було відзначено жодного випадку посилення кашлю, підвищення температури тіла чи інших симптомів, властивих бактеріальним ускладненням (рис. 5).
У 67% пацієнтів із групи лікування комбінацією бутамірат + гвайфенезин, у яких з’явилося мокротиння, незважаючи на зменшення вираженості кашлю, було зареєстровано підвищення температури тіла, що потребувало подальшого застосування антибактеріальної терапії.
Отже, застосування Ренгаліну з метою лікування постінфекційного кашлю дозволяє домогтися вираженіших терапевтичних ефектів у стислі терміни незалежно від характеру кашлю, а також запобігти розвитку бактеріальних ускладнень ГРВІ.
Ренгалін продемонстрував високу ефективність у лікуванні кашлю, зумовленого СПЗ. У порівняльному дослідженні оцінили результати лікування дорослих амбулаторних пацієнтів із клінічно підтвердженим СПЗ, що не потребує хірургічного втручання на лор-органах, а також з непродуктивним кашлем як клінічним проявом СПЗ із тривалістю не менше ніж 12 тиж (Овчинников А. Ю., 2017).
Дослідження складалося з таких етапів: візит 0 (день залучення до випробування, обстеження, призначення лікування), а також послідовних 5 візитів на 5-й, 10-й, 15-й, 21-й та 28-й день терапії.
Лікування в основній групі включало зрошення порожнини носа фізіологічним розчином до 6 р/день, використання топічних кортикостероїдів по 400 мг 2 р/день – 21 день, Ренгалін по 1 таблетці 3 р/день протягом 14 днів.
У контрольній групі призначали зрошення порожнини носа фізіологічним розчином до 6 р/день, використання топічних кортикостероїдів по 400 мг 2 р/день – 21 день, антигістамінний засіб по 1 таблетці в день протягом 14 днів, але без Ренгаліну.
Ефективність лікування оцінювали за шкалою тяжкості денного та нічного кашлю, візуальною аналоговою шкалою якості життя.
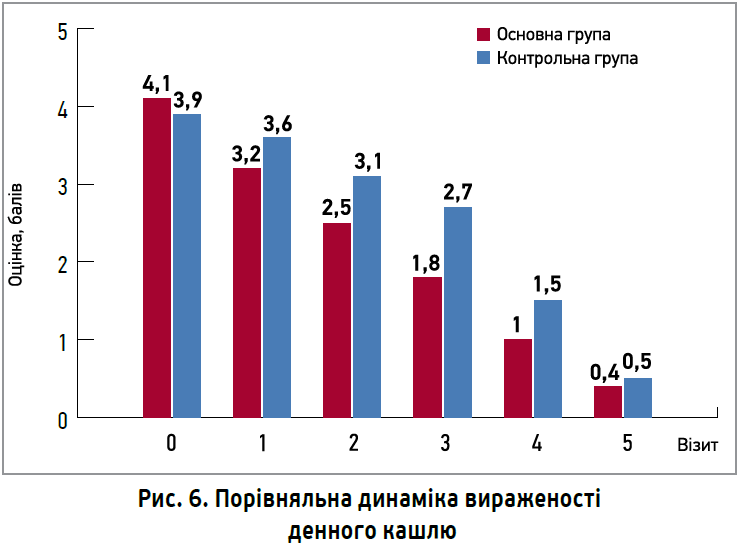
На тлі проведеного лікування позитивна динаміка спостерігалася в обох групах, однак в основній групі вона була вираженішою щодо денного кашлю вже до візиту 1 і зберігалася впродовж подальших візитів (рис. 6).
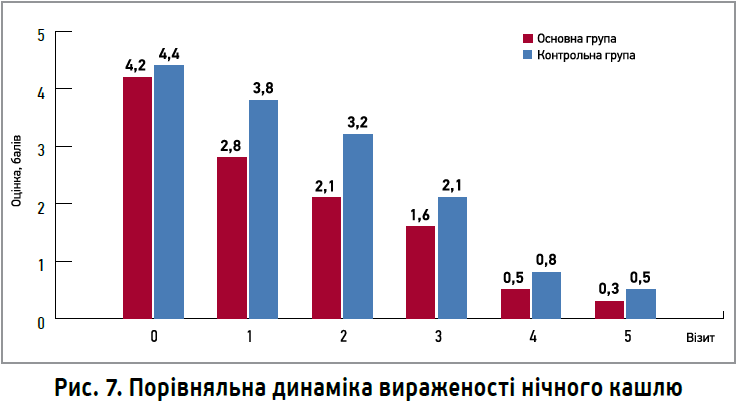
Водночас достовірні відмінності щодо зменшення нічного кашлю між групами були зареєстровані до візиту 1 та зберігалися під час подальших візитів. В основній групі ефект спостерігався раніше – до 5-го дня лікування (рис. 7).
Після закінчення дослідження в основній та контрольній групах відзначено ліквідацію кашлю у 89 і 81% хворих відповідно.
Дослідження продемонструвало, що застосування Ренгаліну в комплексній терапії пацієнтів із СПЗ чинить виражений клінічний ефект уже до 5-го дня від початку лікування, знижує кількість епізодів денного та нічного кашлю і його інтенсивність, підвищує якість життя пацієнтів із хронічним кашлем з перших днів лікування.
Ренгалін здатен забезпечити зручну терапію кашлю для лікаря, позбавляючи його необхідності обрання та заміни препарату залежно від типу кашлю і фази захворювання, а також для пацієнта, прискорюючи одужання, знижуючи ризик ускладнень, підвищуючи прихильність до терапії. Зазначені ефекти дають змогу рекомендувати препарат для широкого застосування в клінічній практиці.
Завдяки протизапальній активності, протикашльовій, протинабряковій і бронхолітичній діям Ренгалін чинить комплексний вплив. Ренгалін показаний при гострих і хронічних захворюваннях дихальних шляхів, які супроводжуються кашлем і бронхоспазмом, продуктивному та непродуктивному кашлі при ГРВІ та грипі, гострому фарингіті, ларинготрахеїті, гострому обструктивному ларингіті, хронічному бронхіті й інших інфекційно-запальних, а також алергічних захворюваннях верхніх і нижніх дихальних шляхів.
Медична газета «Здоров’я України 21 сторіччя» № 10 (503), 2021 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Серед препаратів, які мають велику доказову базу щодо лікування пацієнтів із захворюваннями дихальних шляхів з алергічним компонентом, особливий інтерес становлять антагоністи лейкотрієнових рецепторів (АЛТР). Ці препарати мають хорошу переносимість у дорослих та дітей, а також, на відміну від інгаляційних кортикостероїдів (ІКС), характеризуються високим комплаєнсом, тому посідають чільне місце в лікуванні пацієнтів із респіраторною патологією. У лютому відбувся міждисциплінарний конгрес із міжнародною участю «Життя без алергії International» за участю провідних вітчизняних міжнародних експертів. Слово мав президент Асоціації алергологів України, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Зайков із доповіддю «Місце АЛТР у лікуванні пацієнтів із респіраторною патологією». ...
Розбір клінічного випадку...