Принципи вибору антибіотиків для лікування інфекцій сечовивідних шляхів
Інфекції сечовивідних шляхів є надзвичайно поширеною проблемою в усьому світі. Через широке застосування антибактеріальних препаратів для їх лікування збудники інфекцій стають резистентними до більшості лікарських засобів. Вирішенням цієї глобальної проблеми має бути застосування тих антибіотиків, до яких резистентність збудників є мінімальною. У статті представлено принципи вибору найбільш ефективних антибактеріальних засобів для лікування інфекцій сечовивідних шляхів.
Ключові слова: інфекції сечовивідних шляхів, антибіотикорезистентність, цефалоспорини, цефіксим, Сорцеф.
Сечовидільну систему можна розділити на верхні сечовивідні шляхи, які складаються з нирок (ниркова паренхіма та збиральна система) та сечоводів, та нижні, що включають у себе сечовий міхур, уретру та передміхурову залозу у чоловіків. Збудники інфекцій можуть колонізувати епітелій як верхніх, так і нижніх сечовивідних шляхів, не викликаючи при цьому запалення – такий стан має назву безсимптомної бактеріурії. Інфекціями сечовивідних шляхів (ІСШ) вважається поєднання бактеріальної інвазії та розвитку запального процесу (Kaplan D., 2020). Основними факторами ризику ІСШ є порушення уродинаміки, безсимптомна бактеріурія, розлади обміну речовин, імуносупресія, хронічний алкоголізм, вагітність та атонія кишечника (Єрмоленко В.М., 2012) [2].
Золотим стандартом діагностики ІСШ є виявлення та ідентифікація збудника за наявності клінічних симптомів за допомогою посіву сечі (Franz M., 1999). За більшість ІСШ відповідає обмежена кількість серотипів Escherichia coli. Ці збудники мають підвищену схильність до адгезії, колонізації, інвазії тканин та підвищену стійкість до бактерицидної активності господаря (Kaplan D., 2020) [2]. Кишкова паличка стала ключовим гравцем у пандемії стійкості до антибіотиків завдяки легкості її передачі та здатності мікроорганізму колонізувати кишечник, що дозволяє E. coli знаходитись у тісній взаємодії з безліччю різних бактерій та передавати їм гени стійкості до антибактеріальних препаратів (Galindo-Mendez М., 2020).
Головні принципи емпіричної антибіотикотерапії ІСШ
Емпіричний вибір препарату для лікування пацієнтів із ІСШ традиційно базується на двох основних положеннях:
- структура збудників, які викликають амбулаторні ІСШ, є досить прогнозованою: 65-90% випадків інфекцій викликає E. coli, 5-10% – Staphylococcus saprophyticus та 5-10% – інші збудники;
- друге положення передбачає необхідність враховувати поточну резистентність цих збудників, насамперед E. coli.
Упродовж останніх десятиліть у світі відзначено кілька тенденцій у динаміці антибіотикорезистентності уропатогенної кишкової палички, які змушують переглядати вимоги до антибіотиків для терапії ІСШ (Будник Т.В., 2015). Так, наприклад, було відзначено зростання стійкості кишкової палички до фторхінолонів: у межах Європи стійкість кишкової палички до ципрофлоксацину з 2006 по 2008 рік та за 2014-2016 роки зросла у Великобританії з 0,5 до 15,3%, у Німеччині – з 8,7 до 15,1%, в Іспанії – з 22,9 до 30,8% (Stapleton A.E., 2020). У Київському регіоні відзначається висока резистентність E.coli та Enterococcus spp. до фторхінолонів ІІ-ІІІ покоління (46-55% та 55-77% відповідно), що унеможливлює їх застосування для лікування неускладнених ІСШ (Колесник M.O., 2016). Також відзначається циркуляція великої кількості помірно стійких штамів до нітроксоліну і похідних нітрофурану, тому використання цих засобів не завжди виправдано (Войда Ю.В., 2014). Загалом, дослідження показують, що стійкість до одного або декількох антибіотиків виявляється більше ніж у 14% ізолятів E. coli (Rasheed M.U., 2014).
Цефалоспорини ІІІ покоління у лікуванні ІСШ
Враховуючи зростаючу резистентність до фторхінолонів, обмежене застосування цих препаратів у дітей, вагітних і пацієнтів похилого віку при досить низькій стійкості E. coli до цефалоспоринів ІІІ покоління (до 8%) в Україні, виправданим є застосування для лікування ІСШ саме препаратів цієї групи (Колесник M.O., 2016) [3].
Сорцеф (цефіксим) – цефалоспорин ІІІ покоління – завдяки своєму механізму дії активний проти дуже широкого спектра бактерій, таких як кишкова паличка, золотистий стафілокок, Streptococcus pneumoniae, Streptococcus pyogenes, Haemophilus influenzae, сальмонела, шигела та Neisseria gonorrhoeae (рисунок).
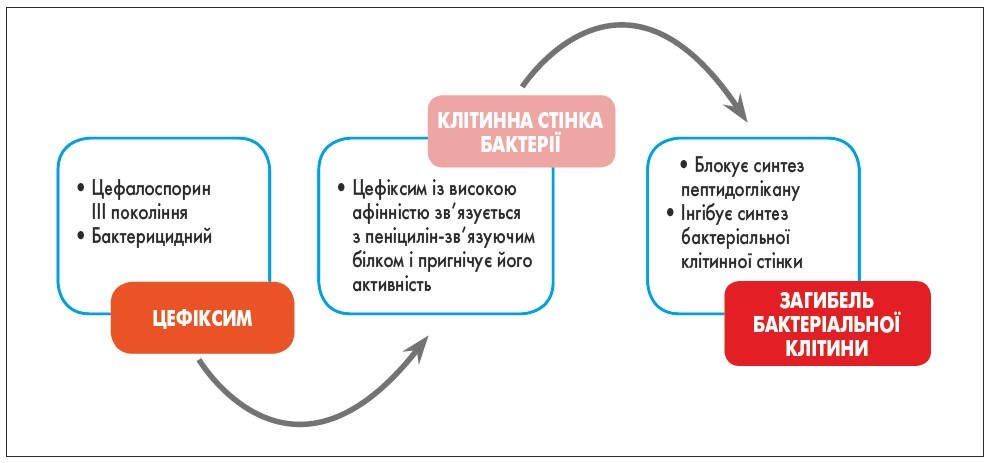 Рис. Механізм дії цефіксиму (Saurabh et al., 2018)
Рис. Механізм дії цефіксиму (Saurabh et al., 2018)
Порівняно з іншими пероральними цефалоспоринами Сорцеф має підвищену активність щодо ентеробактерій, особливо збудників ІСШ, включаючи штами, що продукують β-лактамазу, та штами, стійкі до амоксициліну, цефаклору та цефподоксиму. До того ж він має кращий порівняно з цими препаратами профіль переносимості [4].
Деякі автори рекомендують цефіксим як антибіотик першої лінії при ІСШ (Dreshaj S., 2011), оскільки він виявляє найбільшу активність проти кишкової палички, яка є найбільш часто виділеною бактерією, що спричиняє неускладнені гострі ІСШ. До того ж цефіксим ефективний проти стійких до ципрофлоксацину або продукуючих лактамази розширеного спектра (ЛРС) штамів уропатогенів. Встановлено, що цефіксим інгібує близько 85,7% ізолятів E. coli, що не продукують ЛРС, натомість як ципрофлоксацин інгібує 80,2% цих ізолятів. Також Цефіксим інгібує близько 80-90% резистентних до ципрофлоксацину ізолятів і є активним проти близько 20% ізолятів, що продукують ЛРС [5]. У дослідженні M. Chaudhary (2015) ефективність цефіксиму в лікуванні ІСШ становила 93,85%, і до того ж препарат добре переносився пацієнтами [1].
Цефіксим добре проникає в органи й тканини, а у сечі створює концентрації, що в багато разів перевищують мінімальні інгібуючі концентрації для більшості збудників ІСШ. Режим прийому препарату 1 раз на добу забезпечує високу прихильність пацієнтів до лікування.
Враховуючи високу чутливість основних уропатогенів до Сорцефу та сприятливий профіль його переносимості, цей препарат можна рекомендувати як оптимальний антибактеріальний засіб для терапії ІСШ.
Література
- Chaudhary M. Efficacy of cefixime in the treatment of urinary tract infection. World journal of pharmacy and pharmaceutical sciences 4(04):987-994, January 2015.
- Kaplan D. American Urological Association. Medical Student Curriculum: Adult UTI, 2020.
- Колесник M.O., Степанова Н.М., Кругліков В.Т., Руденко А.В. Етіологічний спектр та десятирічний патерн антибактеріальної резистентності збудників неускладненої інфекції сечової системи (2005-2015) // Український журнал нефрології та діалізу, № 1, (49) 2016. УДК: 616.61/63-022.7-085-035.015.
- Stranieri G. Cefixime for the prophylaxis of urinary tract infections in children with malformative uropathies: an open study. European Review for Medical and Pharmacological Sciences, 2003; 7: 57-64.
- Manthale D., Kadganchi C.D. Cefixime and ofloxacin in the era of antibiotic resistance review of its use in UTI. International journal of scientific research. Microbiology. Volume-6, Issue-1, January 2017, ISSN № 2277 – 8179.
Підготувала Анастасія Романова
Тематичний номер «Урологія. Нефрологія. Андрологія» № 2 (23), 2021 р.
СТАТТІ ЗА ТЕМОЮ Інфекційні захворювання
Світ не бачив нового класу диво-ліків уже 40 років...
Рекомендації щодо антибіотиків першого і другого вибору для емпіричної терапії негоспітальної пневмонії, середнього отиту та загострення ХОЗЛ...
SARS-CoV‑2 виявився непересічним респіраторним вірусом і спричинив пандемію, яка тривала із 2019 по 2023 рік. Проте вплив цієї інфекції на імунну систему (ІС) людини не обмежується активацією фізіологічних механізмів противірусного захисту. Вірус здатний надмірно активувати ІС, зумовлюючи загрозливе ускладнення – т. зв. цитокіновий шторм, спричинити тяжку вірусну пневмонію, розвиток автоімунного синдрому, впливати на систему коагуляції тощо....
Риносинусит (РС) є одним із найчастіших захворювань у первинній медичній практиці. Трьома найбільш чутливими й специфічними симптомами гострого РС є виділення з носа, закладеність носа, лицевий і головний біль. Неконтрольований гострий біль значно погіршує якість життя пацієнтів із РС: спричиняє психоемоційні розлади, знижує працездатність і соціальну активність, сприяє хронізації больового синдрому і збільшує вартість лікування. Отже, полегшення болю при РС є найпершим завданням лікаря....




